直腸癌術前旋轉調強與傳統固定野動態調強放療計劃對比研究
熊 英,周 偉 ,毛 凱,戴甜甜,韓媛媛
(中日友好醫院 放射治療科,北京 100029)
術前同步放化療已經成為局部晚期直腸癌的標準治療[1],近年來多項研究表明采用調強放射治療能有效提高靶區的劑量分布,使盆腔的正常組織得到很好的保護[2]。而快速旋轉調強(intensity-modulated arc therapy,IMAT) 是在動態調強的基礎上加入了旋轉治療的技術,其主要特性為在較短的時間內進行單弧和多弧旋轉照射,在機器旋轉出束的同時改變多葉光柵的位置、射線束的劑量率、機架旋轉速度以調整劑量強度分布,產生高度適形的劑量靶區[3],已有研究表明在鼻咽癌的治療中IMAT技術具有不亞于調強的劑量分布,降低了危及器官的高劑量區受量,縮短了治療時間[4]。本研究通過分析和比較直腸癌術前IMAT技術和固定野動態調強適形放療(IMRT)治療計劃的劑量學差異,旨在探討IMAT技術在直腸癌術前放療中的應用。
1 資料與方法
1.1 臨床資料
選取2012年8月~2013年10月本院的Ⅱ、Ⅲ期直腸癌術前患者22例。男12例、女10例;中位年齡58歲(42~71歲)。病理類型為低分化腺癌4例、中分化腺癌9例、高分化腺癌8例;另有乳頭狀腺癌1例,臨床分期采用AJCC第7版,其中T2有8例,其余 14例為T3。患者均為仰臥位,盆膜固定,CT定位掃描前1h排空膀胱,并口服500ml清水,使掃描時膀胱充盈。在Philip Brilliance CT機上行增強CT掃描,掃描范圍包括整個盆腔,從腰4上緣至會陰下,層厚0.5mm。
1.2 靶區及危及器官的勾畫
由放療醫生勾畫靶區和危及器官,治療靶區由原發病灶(GTV)和區域淋巴引流區(CTV)構成。GTV包括所有影像學可見的癌變組織。CTV包括整個直腸及系膜,骶前區、髂內淋巴結、部分髂總及髂外血管周圍淋巴結、部分閉孔區域,其上界通常為L5下緣,下界為閉孔下緣,側界為真骨盆內緣,前界充盈膀胱后壁1/4~1/3,后界包括骶骨厚度一半(S3上緣以上)和骶骨皮質后緣(s3上緣以下)。計劃靶體積(PTV)由CTV均勻外放0.5 cm而成。勾畫的危及器官為膀胱、小腸、雙側股骨頭[5]。
1.3 計劃設計
采用瓦里安Eclipse 10.0計劃系統為Trilogy加速器制定2種治療計劃方案,IMAT計劃和IMRT治療計劃。IMAT計劃采用單弧照射,起始角度170°,逆時針旋轉到190°。IMRT為五野共面射野, 入射角度分別為: 0°、72°、144°、216°和 288°,所有計劃要求95%的PTV達到50Gy,限定小腸30%的體積受照劑量 D30%<30Gy,Dmax≤45Gy;膀胱 D50%<40Gy;股骨頭 D5%<45Gy[5]。歸一方式為以等中心處劑量歸一。
1 .4 評估及統計學方法
1.4.1 提取IMAT與IMRT的機器跳數及治療時間進行對比。
1.4.2 適形指數(conformity index,CI)[6]
評估等劑量曲線與靶區適形性,定義為VPTV95%/VPTV×VPTV95%/VT, 其中 VPTV95%是95%的等劑量線所覆蓋的PTV體積,VPTV是總的PTV體積,VT是95%等劑量線所覆蓋的全部受照射體積。CI值越接近1,表示計劃的適形性越好。
1.4.3 均勻指數(homogeneity index,HI)[7]
定義為D5/D95,反映靶區內劑量分布的均勻性,D5是指受到高劑量照射的5%靶體積所接受的最低劑量,D95指95%靶體積所接受的最低劑量,HI值越接近1表示均勻性越好。
1.4.4 通過劑量-體積直方圖 (dose-volume histogram,DVH)
分別計算每例患者在2種計劃中膀胱、小腸和雙側股骨頭受照劑量體積參數,比較膀胱、小腸、股骨頭的最大和平均受照劑量及接受30、40和50Gy照射體積占總體積的百分比,以及受照射區域的平均劑量[7]。
統計學分析應用SPSS16.0軟件,采用配對t檢驗比較2種計劃中各參數的差異。
2 結果
IMAT 計劃的機器跳數平均為(622±53)MU,IMRT 為(1078±155)MU,IMAT 計劃較 IMAT 機器跳數減少了42%,差異有統計學意義 (P<0.05)。IMAT 計劃的平均治療時間為 (75±6)s,IMRT 為(366±26)s,平均治療時間節省了 79%,差異有統計學意義(P<0.05)。
IMAT與傳統IMRT計劃的適形性和均勻性及劑量均值都能夠很好滿足靶區分布,其差異無統計學意義(P>0.05),見表1。危及器官的受照射劑量顯示出 IMAT計劃中膀胱 V30、V40和V50低于IMRT計劃中相應的指標,差異有統計學意義 (P<0.05);小腸、股骨頭的關鍵參數如V20、V30、V40、V50,Dmean,Dmax 與傳 統 IMRT 計劃差異無統計學意義(P>0.05),見表 2。
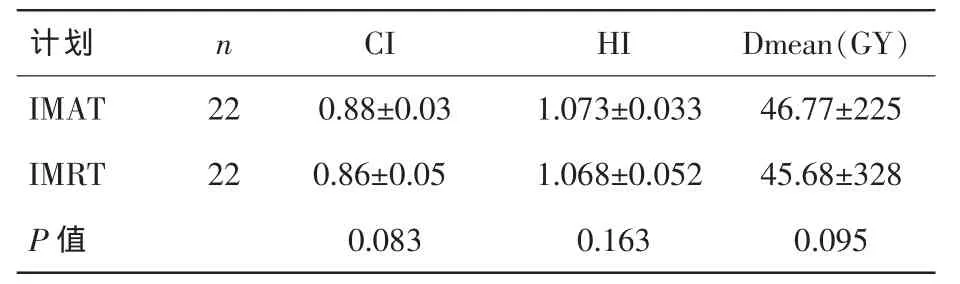
表1 IMAT與IMRT計劃靶區評價參數對比(x-±s)
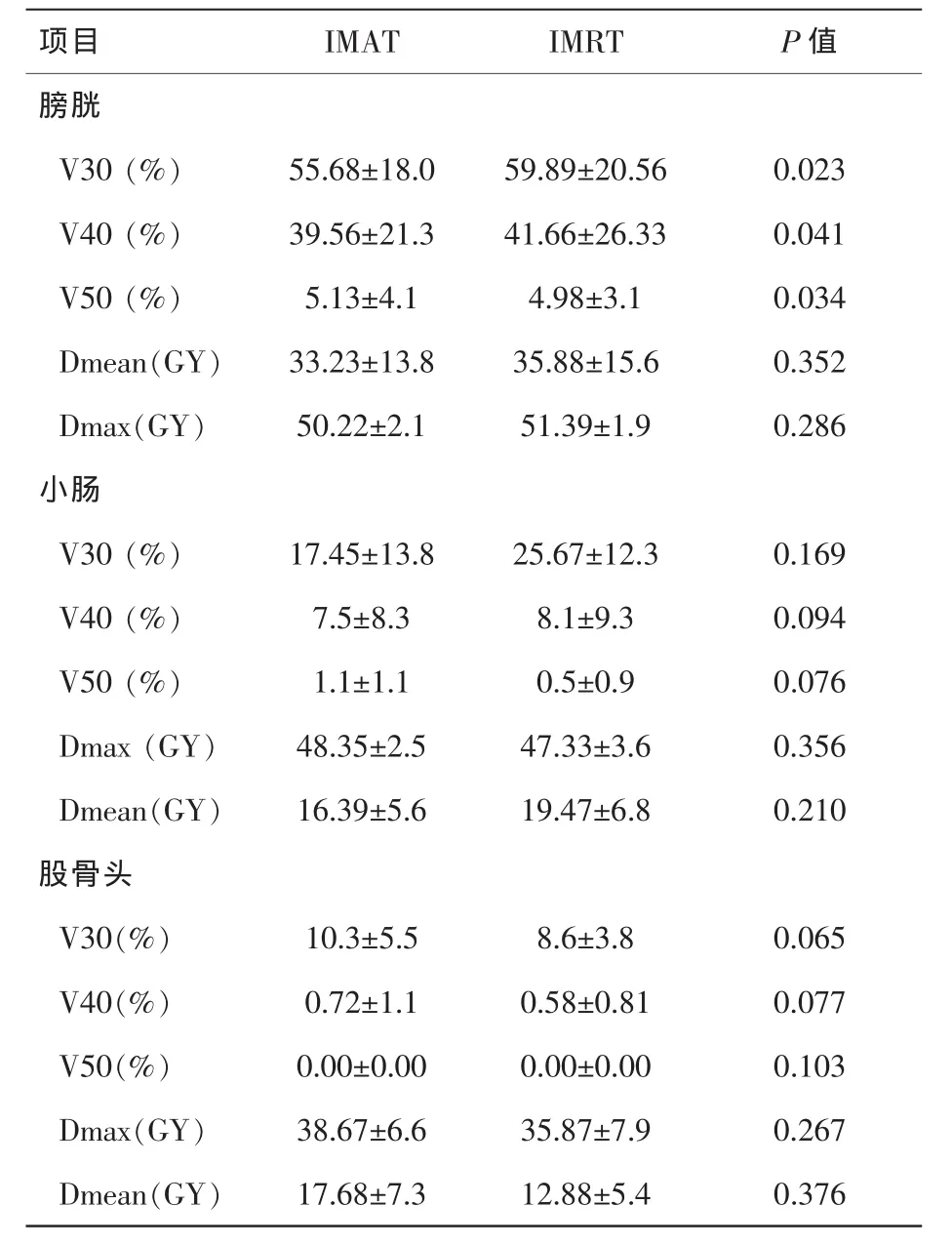
表2 IMAT與IMRT危及器官參數對比(x-±s)
3 討論
直腸癌術前放療最重要的意義在于可使腫瘤細胞產生不同程度的退行性變,纖維組織增生,癌周浸潤消失,能縮小腫瘤體積,使部分原不能手術切除病例的腸壁及腫瘤周圍組織的浸潤減輕,從而提高手術切除率,并能減少手術操作時可能引起的血道、淋巴道轉移。此外,直腸癌開展術前同步放化療技術后相對單純手術能明顯降低局部復發率,提高總生存率,而且手術能夠將接受過照射的直腸大部分甚至全部切除,從而避免了放射性直腸炎對患者生活質量的影響[8]。
放射治療從普通放療時代發展到三維適形,靶區及其周圍組織的劑量分布適形度有了很大飛躍,發展到固定野調強放療得到進一步改善,并可以實施同步加量照射,但由于野數增加導致治療時間增加[9]。近幾年來,隨著快速容積旋轉調強技術的出現,在保證靶區劑量的同時,它可以縮短治療時間,減少患者移動帶來的擺位誤差。直腸癌的放療靶區沿淋巴引流區的形狀較固定,用來做劑量學對比研究有較大的價值[10]。
快速旋轉調強作為我科開展的放療新技術,加速器機架在連續旋轉過程中實施照射,機器跳數及治療時間與傳統IMRT相應減少了42%和79%。同時達到與IMRT一樣理想的靶區適型度及均勻度,顯示出該技術高效、快捷的特點。放射線誘導的繼發腫瘤如淋巴瘤,白血病等,越來越受到關注,減少治療所需跳數對降低發生有重要意義[11],傳統IMRT放療由于跳數較高,散射線也增加,增大了射線泄露概率。全身受到照射總劑量和正常組織受到的低劑量照射區也相應增大。IMAT由于只有傳統IMRT一半的總治療跳數,降低了相應的的風險。此外,如果放射治療時間過長,患者體位移動、器官體積變化和運動等不確定因素,將導致治療位置精度降低。因此,降低治療時間對提高治療精度、減輕患者不適感,增加治療依從性有重要意義。此外還減少了治療過程中患者改變體位的概率,從而降低移動帶來的擺位誤差。
在針對危及器官的常見評價指標中,IMAT治療中膀胱高劑量區受照射體積顯著減少,從而降低了放射性膀胱炎的發生。放射線誘導的膀胱炎為治療過程中較常見的并發癥,其臨床表現主要是出現難以控制的肉眼血尿,甚至出現血凝塊,不能自解小便,膀胱痙攣,尿頻、尿急,少部分患者出現尿痛,一般的止血治療效果不是很好。其產生的原因是放射線促使組織內電離,產生羥自由基從而使末梢血管內膜損傷、小血管閉塞、粘膜充血水腫以致形成潰瘍,周圍有明顯水腫,常合并感染、出血,慢性反應為膀胱纖維化及攣縮[12],治療起來十分困難,因此預防其發生有很重要意義。急慢性放射性腸炎在放療患者中亦較為常見,劇烈的腹瀉常中斷治療影響療效,嚴重時穿孔[13],對于小腸及股骨頭的保護傳統調強時已經能夠達到較好的劑量限制,容積旋轉調強效果與其相似。
[1]Hofheinz RD,Wenz F,Post S,et al.Chemoradiotherapy with capecitabine versus fluorouracil for locally advanced rectal cancer:a randomised, multicenter,non-inferiority,phase Ⅲtrial[J].Lancet Oncol,2012,13(6):579-588.
[2]張玉海,李月敏,夏火生,等.直腸癌術后調強放療和三維適形放療的劑量學比較研究 [J].腫瘤研究與臨床,2009,21:450-452.
[3]Otto K.Volumetric modulated ale therapy:IMRT in a single gantry arc[J].Med Phys,2008,35(1):310-317.
[4]劉同海,尹勇,陳進琥,等.鼻咽癌旋轉調強與固定野調強同步加量計劃比較研究[J].中華放射腫瘤學雜志,2010,19(6):486-492.
[5]Viani GA,stefano EJ,Soares FV,et al.Evaluation of biologic effective dose and schedule of fractionation for preoperative radiotherapy for rectal cancer:meta-analyses and meta-regression[J].Int J Radiat 0ncol Biol Phys,201l,80:985-991.
[6]Yin Y,Chen J,Xing L,et al.Applications of IMAT in cervical esophageal cancer radiotherapy:A comparison with fixed field IMRT in dosimetry and implementation[J].Appl Clin Med Phys,2011,12(2):48-57.
[7]Vivekanandan N,Sriram P,Kumar SA,et al.Volumetric modulated arc radiotherapy for esophageal cancer[J].Med Dosim,2012,37(1):108-113.
[8]Sauer R,Becker H,Hohenberger W,et al.Preoperative versus postoperative chemoradiotherapy for rectal cancer[J].N Engl J Med,2004,351:1731-1740.
[9]姚波,鄭明民,王平,等.直腸癌五野調強放療與傳統適形放療劑量學研究[J].臨床腫瘤學雜志,2009,14(5):446-449.
[10]Ling CC,Zhang P,Archambault Y,et al.Commissioning and quality assurance of IMAT radiotherapy delivery system[J].Int J Radiat Oncol Biol Phys,2008,72(2):575-581.
[11]HallEj,PhilD.Intensive-modulated therapy,protons,and the risk of second cancers[J].Int J Radiat Oncl Boil Phys,2006,65:1-7
[12]Oliai C,Fisher B,Jani A,et al.Hyperbaric oxygen therapy forradiation-induced cystitis and proctitis[J].Int J Radiat Oncol Biol Phys,2012,84:733-740.
[13]Guerrero Urbano MT,Henrys AJ,Adams EJ,et al.Intensity modulated radiotherapy in patients with locally advanced rectal cancer reduces volume of bowel treated to high dose levels[J].Int J Radiat Oncol Biol Phys,2006,65:907-916.
[14]VerbakelWFAR,Senans,LagerwardFJ,etal.IMAT VS IMRT planning:a comparative study with dosimetric validation for head and neck,glioma and pancreas cancer[J].Int J Radiat Oncol boil phys,2008,72(Supple):S596-597.

