晚期非小細胞肺癌患者吉非替尼治療前后血清癌胚抗原水平變化及意義
曹津津,戴瓊艷,段滿林
(1.南京大學醫學院,江蘇 南京,210093; 2.徐州醫學院 麻醉學院,江蘇 徐州,221004;3.南京軍區南京總醫院 麻醉科; 江蘇 南京,210002)
在惡性腫瘤中,肺癌占據首位,其中非小細胞肺癌(NSCLC)的主要治療方法是傳統的系統化療。雖然這類方法在一定程度上緩解了患者的生存時間,但對中晚期非小細胞肺癌療效較差。近年來不少研究[1-2]發現,分子靶向藥物治療治療非小細胞肺癌能收到較好療效。作為分子靶向藥物之一和表皮生長因子受體絡氨酸激酶受體抑制劑(EGFR-TKI),吉非替尼在進展以及復發性非小細胞肺癌中具有較好的抗腫瘤作用[3-4]。本研究通過檢測晚期非小細胞肺癌患者接受吉非替尼治療前后血清癌胚抗原(CEA)水平的變化,探討其在吉非替尼療效評價中的作用。
1 資料與方法
1.1 一般資料
選擇本院2009年1月—2012年2月收治的晚期非小細胞肺癌患者40例為研究對象,均為Ⅲ~Ⅳ期非小細胞肺癌患者。其中男20例,女20例;年齡34~77歲,平均(63.5±5.1)歲。根據組織學世界衛生組織(WHO)分類標準,40例患者中包括腺癌28例,非腺癌12例。臨床分期采用2009年國際抗癌聯盟所制定的肺癌國際分期法:ⅢA期3例,ⅢB期5例,Ⅳ期32例。入組患者均經支氣管鏡活檢并進行病理確診,進行常規頭部、胸腹部CT檢查及全身骨掃描檢查。排除接受1周及以上手術、放療及化療者;以及有嚴重心電圖、血常規、肝腎功能異常者。治療前以50 ng/mL作為血清CEA水平的分界線,將40例患者分為>50 ng/mL組(高CEA組)和≤50 ng/mL組(低CEA組)。
1.2 方法
1.2.1 治療方法:本臨床研究患者采用吉非替尼治療,250 mg/d,直到難以耐受或腫瘤進展時停藥。同時給予常規局部放療。每月進行腦及胸部CT檢查、腹部B超并記錄轉移灶范圍及大小,并對患者隨訪至2013年12月。
1.2.2 血清CEA檢測:所有患者治療前、接受化療2療程后均清晨空腹抽取外周血行血清CEA檢測。CEA的試劑盒全部采用德國羅氏公司腫瘤相關抗原定量測定試劑盒(電化學發光法),測定儀器為德國羅氏公司的ELECYS 2010型全自動電化學發光免疫分析測定儀。
1.3 觀察指標
觀察患者治療前后血清CEA水平、不良反應發生情況、無進展生存時間(PFS)。
1.4 療效評價
參照頭部CT和磁共振、胸腹部CT掃描以及骨掃描,并按照WHO實體瘤的標準,評價患者服用吉非替尼后的療效,將療效分為完全緩解(CR)、部分緩解(PR)、穩定(SD)、進展(PD)。控制組包括CR、PR、SD的患者,非控制組包括PD的患者。
2 結 果
2.1 臨床療效及2組患者一般資料比較
40例患者治療后CR 0例,PR 20例,SD 5例,PD 15例;控制組25例,非控制組15例。2組患者一般資料無顯著差異(P>0.05),具有可比性,見表1。

表1 2組患者一般資料比較
2.2 2組治療前后血清CEA水平比較
由表2可見,治療前,控制組和非控制組血清CEA水平無顯著差異(P>0.05); 治療后,2組血清CEA水平較治療前明顯降低(P<0.01)。控制組治療后血清CEA水平明顯低于非控制組(P<0.01)。
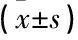
表2 2組治療前后血清CEA水平比較
2.3 患者不良反應
高CEA組(26例)與低CEA組(14例)不良反應發生情況見表3。2組不良反應主要有瘙癢、皮疹、腹瀉、惡心、便秘、發熱等。高CEA組不良反應發生率均高于低CEA組,但2組不良反應發生率無顯著差異(P>0.05)。

表3 2組不良反應發生情況[n(%)]
2.4 患者PFS分析
本研究比較了高CEA組、低CEA組的PFS進展情況。由表4可見,CEA高水平患者在9和12個月的生存率顯著高于CEA低水平患者(P<0.05),3個月、12個月以上的生存率無顯著差異(P>0.05)。

表4 患者PFS進展比較[n(%)]
3 討 論
遺傳標志物、腫瘤血管及細胞受體等是肺癌分子靶向治療的常用靶點,而表皮生長因子(EGFR)受體是現階段研究中的主要靶點[5]。隨著人體免疫學和分子生物學的發展,人們對腫瘤標志物和靶向分子治療有了新的深刻認識,并取得了不少顯著成就。所謂腫瘤標志物,是由機體對腫瘤反應或腫瘤細胞合成分泌的異常物質,不僅可用于診斷,還可用評價療效及預后。不少研究[6]證明,靶向藥物的出現和靶向治療的發展對NSCLC患者的臨床治療極其有益。EGFR是跨膜的酪氨酸激酶受體的一種,其信號轉導通路與腫瘤細胞增殖、侵襲、轉移、血管生成及凋亡密切相關。以往研究表明,EGFR是ErbB家族的主要成員之一,主要含有3個結構:細胞內區、細胞外區及跨膜區。一旦結合配體,EGFR將在細胞表面形成受體同源二聚體或異源二聚體,阻斷肺癌的發生發展。有學者對EGFR的研究[7]表明,其在上皮來源的腫瘤細胞中表達,如:乳腺癌以及非小細胞肺癌等,EGFR不但為細胞增殖有一定的調控作用,而且其對腫瘤的進展、血管的生成以及癌細胞的轉移擴散等均有關鍵性作用,而過度表達的EGFR對化療以及放療均不敏感,從而容易發生遠處轉移,繼而導致其預后不良。也有研究[8]結果顯示,40%~80%的NSCLC患者EGFR水平過高表達,且此類NSCLC患者通常預后較差,但通過靶向治療選擇性抑制酪氨酸激酶的活性,可有效抑制表皮生長因子手提被激活,從而達到抑制腫瘤細胞增殖、浸潤和轉移及增強化療效果的目的。
目前,吉非替尼是經美國FDV注冊和批準使用的第一個用于治療NSCLC的靶向藥物,在臨床上使用較多,對NSCLC的療效值得肯定。其主要作用機制是競爭性結合三磷酸腺苷,抑制EGFR受體磷酸化,阻斷下游信號,從而促進腫瘤細胞的凋亡。CEA當前在臨床上使用最廣泛的腫瘤標志物之一,可由肺癌細胞直接產生,與腫瘤的復發和轉移關系密切。CEA由癌細胞基因表達而合成分泌,可以早期診斷肺癌,評估患者療效及監測病情進展。有學者研究[9]發現,吉非替尼對晚期肺癌的緩解率高達10%~19%,表明其對非小細胞肺癌的治療中的療效,同時可顯著提高患者的生活質量。有學者研究[10]發現,血清CEA水平可作為晚期非小細胞肺癌服用EGFR-TKI治療療效的預測指標。而血清CEA的檢測具有方法簡單、技術成熟以及快捷、定量以及可重復等優點,并可通過在治療期間對患者進行觀測血清中CEA水平進行評估療效。
本研究結果表明,晚期非小細胞肺癌患者治療結束后外周血CEA水平顯著低于治療前,且治療結束后,病情得到控制的患者外周血CEA濃度值明顯低于未控制者。這與其他學者的研究結果一致,提示作為肺癌的靶向藥物,吉非替尼可明顯降低晚期NSCLC患者外周血CEA的表達水平,而后者在療效較好的患者中變化更明顯。在本臨床研究中,作者發現CEA表達高的患者其PFS較表達低的患者有明顯差異性,故作者認為對于CEA表達較高的患者采用吉非替尼進行治療,其預后優于低表達的患者。在對患者不良反應的研究中,作者發現其常見的不良反應為皮膚瘙癢、腹
瀉、惡心以及皮疹,但程度較輕,耐受性很好,不影響治療效果。
[1]Al Zobair A A,Al Obeidy B F,Yang L,et al.Concomitant overexpression of EGFR and CXCR4 is associated with worse prognosis in a new molecular subtype of non-small cell lung cancer[J].Oncology reports,2013,29(4): 1524.
[2]Acunzo M,Romano G,Palmieri D,et al.Cross-talk between MET and EGFR in non-small cell lung cancer involves miR-27a and Sprouty2[J].Proceedings of the National Academy of Sciences,2013,110(21): 8573.
[3]Aydiner A,Yildiz I,Seyidova A.Clinical Outcomes and Prognostic Factors Associated with the Response to Erlotinib in Non-Small-Cell Lung Cancer Patients with Unknown EGFR Mutational Status[J].Asian Pacific Journal of Cancer Prevention,2013,14(5): 3255.
[4]Araki T,Yashima H,Shimizu K,et al.Review of the treatment of non-small cell lung cancer with gefitinib[J].Clin Med Insights Oncol,2012,6: 407.
[5]Al Dayel F.EGFR mutation testing in non-small cell lung cancer (NSCLC)[J].Journal of infection and public health,2012,5: S31.
[6]Chen G,Kronenberger P,Teugels E,et al.Effect of siRNAs targeting the EGFR T790M mutation in a non-small cell lung cancer cell line resistant to EGFR tyrosine kinase inhibitors and combination with various agents[J].Biochemical and biophysical research communications,2013,431(3): 623.
[7]Lee E,Keam B,Kim D W,et al.Erlotinib versus gefitinib for control of leptomeningeal carcinomatosis in non-small-cell lung cancer[J].Journal of Thoracic Oncology,2013,8(8): 1069.
[8]Jeon W I,Ryu P D,Lee S Y.Effects of voltage-gated K+ channel blockers in gefitinib-resistant H460 non-small cell lung cancer cells[J].Anticancer research,2012,32(12): 5279.
[9]Lopez-Rios F,Angulo B,Gomez B,et al.Comparison of molecular testing methods for the detection of EGFR mutations in formalin-fixed paraffin-embedded tissue specimens of non-small cell lung cancer[J].Journal of clinical pathology,2013,66(5): 381.
[10]Karachaliou N,Costa C,Gimenez-Capitan A,et al.BRCA1,LMO4,and CtIP mRNA Expression in Erlotinib-Treated Non-Small-Cell Lung Cancer Patients with EGFR Mutations[J].Journal of Thoracic Oncology,2013,8(3): 295.

