髓過氧化物酶在老年慢性心力衰竭患者中的臨床意義
胡 堅 陳發秀 邱元芝 尹 絹 曹平良 張志勇
(江西省人民醫院一部,江西 南昌 330006)
慢性心力衰竭(CHF)是大多數原發性心血管疾病的嚴重或終末階段。炎癥細胞因子在慢性心力衰竭的發生發展過程中的作用及其分子機制尚不十分清楚。髓過氧化物酶(MPO)是一新近發現的炎癥因子。本研究測定老年CHF患者的血清MPO、腦鈉肽(BNP)、超敏C反應蛋白(hs-CRP)的水平,同時分析CHF組血清MPO、與血清BNP、hs-CRP、左心室參數之間的相關性,探討CHF患者血清MPO濃度變化及其與心力衰竭嚴重程度的關系。
1 對象與方法
1.1對象 2010年1月至2011年5月在我院住院60歲以上的患者141例,分CHF組和對照組。CHF組為111例,男69例,女42例,年齡60~99〔平均(80.5±11.4)〕歲,CHF診斷參照《ACC/AHA成人慢性心力衰竭的診斷和治療指南》(2005修訂版),心功能按NYHA分級:心功能Ⅱ級33例,Ⅲ級35例,Ⅳ級43例。對照組為同期住院無心臟病及心衰的患者30例,男19例,女11例,年齡62~96〔平均(82.1±9.8)〕歲。所有入選病例均除外結締組織病,急、慢性感染,腦血管病,周圍血管病,近期手術,惡性腫瘤,肝腎功能異常,急性冠脈綜合征。兩組性別、年齡、吸煙史、白細胞總數、中性粒細胞計數、高密度脂蛋白膽固醇(HDL-C)水平及他汀類藥物使用、高血壓、冠心病和糖尿病的患病率無顯著差異。而兩組間低密度脂蛋白膽固醇(LDL-C)水平差異有顯著意義(P<0.05)。見表1。

表1 兩組患者臨床資料的比較(%)〕
1.2方法
1.2.1一般資料的收集 包括病史(吸煙史、高血壓、糖尿病、冠心病等)、血常規、肝腎功能、血脂。
1.2.2左心室參數測定 當天采用惠普5500超聲心動圖診斷儀,測定左心室收縮末徑(LVESD)、舒張末徑(LVEDD)、左心室射血分數(LVEF)。
1.2.3血清MPO的檢測 入院后第2日清晨空腹采集肘靜脈血5 ml室溫下靜置后,1 500 r/min離心10 min,分離血清置于-80℃低溫冰箱中保存,待同批所有標本收集齊全后進行檢測分析。標本收集后采用酶聯免疫吸附試驗(ELISA)測定MPO水平,選用德國歐蒙醫學實驗診斷股份公司原裝配套試劑盒,使用美國BIO-TEK酶標儀Elx800,按照試劑盒說明書操作。
1.2.4血清BNP測定 入院后第2天清晨空腹采集肘靜脈血3 ml送檢,采用美國雅培公司原裝配套試劑盒及AXSYM化學發光免疫分析儀,采用化學發光微粒子酶免定量法測定血清BNP水平。
1.2.5血清hs-CRP測定 入院后第2天清晨空腹采集肘靜脈血3 ml送檢,采用德國西門子公司原裝配套試劑盒及德靈BNProspec生化分析儀,采用散色比濁法測定血清hs-CRP的水平。
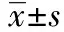
2 結 果
2.1不同組別患者血清MPO、BNP、hs-CRP水平的比較 CHF患者血清MPO水平顯著高于對照組,CHF患者血清BNP水平顯著高于對照組,CHF患者血清hs-CRP水平高于對照組,差異均有統計學意義(均P<0.01),見表1。
2.2不同組別患者血清MPO、BNP、hs-CRP水平的比較 CHF組患者血清MPO、BNP、hs-CRP水平隨NYHA分級增高而明顯遞增,血清MPO、BNP、hs-CRP水平NYHAⅡ、Ⅲ、Ⅳ級與對照組相比,NYHAⅢ、Ⅳ級與Ⅱ級相比,Ⅳ級與Ⅲ級相比差異均有統計學意義(均P<0.01) ,見表2。
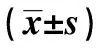
表2 不同組別患者血清MPO、BNP、hs-CRP水平的比較
2.3不同組別超聲心動圖左室功能參數LVEDD、LVEF的比較 CHF組LVEDD比對照組高(P<0.05),CHF組LVEF比對照組低(P<0.05);LVEDD隨著NYHA分級增高而增高(P<0.05),LVEF隨著NYHA分級增高而降低(P<0.05),見表3。
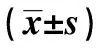
表3 不同組別LVEDD、LVEF的比較
2.4血清MPO水平與NYHA分級之間的關系 以MPO為應變量,年齡、性別、吸煙、冠心病、糖尿病、高血壓、他汀類藥物使用、抗血小板聚集的藥物使用、血清BNP水平、心功能NYHA分級作自變量,入選和剔除變量的F界值分別為F≥3.86和F≤2.74,進行多元線性逐步回歸分析,最后吸煙、冠心病、他汀類藥物使用、抗血小板聚集的藥物使用、NYHA分級被選入方程,確定系數r=0.69,F=32.7,P=0.007 7,而校正了吸煙、冠心病、他汀類藥物使用、抗血小板聚集的藥物使用等影響因素后,不同NYHA分級之間的MPO水平差異仍具統計學意義(P<0.05),且CHF患者血清MPO水平與NYHA分級呈正相關(r=0.4,P<0.01)。
2.5血清MPO、BNP水平與左心室功能的相關性 CHF患者中,血清MPO、BNP水平與心臟結構、功能指標行直線相關分析顯示,血清MPO與LVEF呈負相關(r=-0.677,P<0.05),BNP與LVEF呈負相關(r=-0.598,P<0.01);血清MPO與LVEDD呈正相關(r=0.679,P<0.01) ,血清BNP與LVEDD呈正相關(r=0.632,P<0.01)。
2.6血清MPO、BNP、hs-CRP水平之間的相關性 血清MPO與hs-CRP水平呈現正相關關系(r=0.32,P<0.05);與BNP水平呈正相關關系(r=0.17,P<0.01)。
3 討 論
MPO作為一種新的炎癥標記物,成為新的反映心肌損傷、治療及預后的指標。大量研究表明MPO參與動脈粥樣硬化、冠心病、急性冠脈綜合征等心血管疾病的發生、發展,并可作為判斷病情及預后的指標〔1~3〕。
本研究中血清MPO水平與NYHA分級之間的關系結果與國外的文獻相似〔4〕。Tang等〔5〕采用前瞻性研究方法發現血漿MPO水平能夠預測健康老年人發生心力衰竭的風險。且有研究表明〔6〕,血清MPO水平可長期預測CHF患者不良心臟事件發生。其主要機制可能是由于MPO能直接或間接減少內皮細胞釋放NO和緩激肽等舒張血管物質,使內皮功能受損,冠狀動脈痙攣;其產生的HOCl能活化基質金屬蛋白蛋白酶,抑制金屬蛋白酶組織抑制因子-1的活性,加劇細胞外基質的降解,促使心肌纖維化、心室的擴張與收縮性喪失、心室的重構;HOCl還可導致內皮細胞凋亡,從而導致基質溶解、損傷血管內膜,促進血栓形成;另外MPO還能誘導血管內皮細胞P選擇素和組織因子的表達,促使血小板聚集;MPO在體內能產生一系列可擴散的強氧化劑,氧化LDL和HDL,導致LDL更易被巨噬細胞吞噬,使之成為永久的泡沫細胞沉積在血管內膜下,而氧化的HDL可抑制巨噬細胞內膽固醇的外流,進而促進膽固醇沉積、泡沫細胞形成,促進了動脈粥樣硬化斑塊的形成;這些病理生理過程均可導致HF的發生和加重〔7~9〕。Vasilyev等〔10〕進行動物研究分析急性心肌梗死小鼠的心肌組織,在缺血再灌注24 d后,發現MPO基因敲除小鼠與野生型小鼠比較,左心室擴張程度降低35.1% (P<0.001),且左心室功能升高52.2% (P<0.000 1)。說明MPO產生的氧化劑對MI后左心室重構和功能產生不良影響。La Rocca等〔11〕對行心臟移植的CHF的病人研究發現,無論是體內或體外,心內膜內皮細胞經氧化應激后均能顯著表達MPO,MPO的表達是由于氧化應激的終末產物3-氯-L-酪氨酸的累積所致。研究還發現,心肌梗死后部位的心內膜同樣有MPO的顯著表達。
BNP是反映心力衰竭的血清標志物,其在心力衰竭診斷、狀況評估、判斷預后和指導治療方面具有重要的臨床價值。本研究表明MPO與BNP可能是通過不同的病理機制參與CHF的發生、發展,MPO主要是通過炎癥、內皮功能損傷及氧化應激的途徑參與CHF的發生、發展,而BNP是通過神經激素激活的病理途徑,反應心室室壁壓力。Tang等〔12〕檢測140名慢性心力衰竭患者血漿MPO水平,隨訪4年內發生不良心臟事件(死亡、心臟移植及因心力衰竭住院)的情況。用ROC特征曲線分析,發現聯合使用MPO和BNP對4年內發生不良心臟事件的預測價值(曲線下面積為0.70)比單用BNP(曲線下面積為0.66)的價值大。提示在CHF患者中聯合測定血清MPO與BNP的水平,在心力衰竭診斷、狀況評估、判斷預后和指導治療方面可起到補充作用。
Tang等〔6〕對136例收縮性心力衰竭的患者平均隨訪(34±17)個月后則發現,hs-CRP水平與MPO水平無明顯相關性。在較低hs-CRP水平(<5.34 mg/L)組的病人中,MPO水平高于平均值的病人其嚴重臨床事件的發生升高了2.9倍,而在較低MPO水平(<303 pmol/L)的病人中,hs-CRP水平升高的病人其嚴重臨床事件的發生僅升高了1.9倍,兩者均升高的病人其嚴重臨床事件的發生則升高了6倍。提示兩者可能是通過不同的病理機制參與CHF的發生、發展,MPO是獨立于hs-CRP的炎性指標。兩者結合對CHF的預后價值有相互補充加強作用。
本研究表明MPO、BNP、hs-CRP在CHF發病和病程進展中起到了一定的作用,并在CHF的診斷、病情判斷等方面具有較高的臨床應用價值,且聯合應用更有助于提高準確性及臨床應用價值,但其作用機制有待于更深入的研究。
4 參考文獻
1Nagesh CM,Roy A.Role of biomarkers in risk stratification of acute coronary syndrome〔J〕.Indian J Med Res,2010;132(5):627-33.
2Chan D,Ng LL.Biomarkers in acute myocardial infarction〔J〕.BMC Med,2010;8:34.
3Ferrante G,Nakano M,Franti F,etal.High levels of systemic myeloperoxidase are associated with coronary plaque erosion in patients with acute coronary syndromes:a clinicopathological study〔J〕.Circulation,2010;122(24):2505-13.
4Yoav Michowitz MD,Sarina Kisil MD,Hanan Guzner-Gur MD,etal.Usefulness of serum myeloperoxidase in prediction of mortality in patients with severe heart failure 〔J〕.Isr Med Assoc J,2008;10 (12):884-8.
5Tang WH,Katz R,Breman ML,etal.Usefulness of myeloperoxidase levels in healthy elderly subjects to predict risk of developing heart failure〔J〕.Am J Cardiol,2009;103(9):1269-74.
6Tang WH,Shrestha K,Troughton RW,etal.Integrating plasma high-sensitivity C-reactive protein and myeloperoxidase for risk prediction in chronic systolic heart failure〔J〕.Congest Heart Fail,2011;17(3):105-9.
7Davies MJ.Myeloperoxidase-derived oxidation:mechanisms of biological damage and its prevention〔J〕.J Clin Biochem Nutr,2011;48(1):8-19.
8Shao B,Oda MN,Oram JF,etal.Myeloperoxidase:an oxidative pathway for generating dysfunctional high-density lipoprotein〔J〕.Chem Res Toxicol,2010;23 (3):447-54.
9Veen BS,Winther MP,Heeringa P.Myeloperoxidase:molecular mechanisms of action and their relevance to human health and disease〔J〕.Antioxid Redox Signal,2009;11 (11):2899 -937.
10Vasilyev N,Williams T,Brennan ML,etal.Myeloperoxidase- generated oxidants modulate left ventricular remodeling but not infarct size after myocardial infarction〔J〕.Circulation,2005;112 (18):2812-20.
11La Rocca G,Di Stefano A,Eleuteri E,etal.Oxidative stress induces myeloperoxidase expression in endocardial endothelial cells from patients with chronic heart failure〔J〕.Basic Res Cardiol,2009;104(3):307-20.
12Tang W,Tong W,Troughton RW,etal.Prognostic value and echo-cardiographic determinants of plasma myeloperoxidase levels in chronic heart failure 〔J〕.J Am Coll Cardiol,2007;49(24):2364.

