復元膠囊對大鼠膝骨關節炎模型軟骨細胞凋亡及增殖的影響
周小莉 茍曉燕 李榮亨
(重慶市中醫院風濕病科,重慶 400021)
研究發現一氧化氮(NO)參與介導的軟骨細胞凋亡在關節軟骨退行性改變過程中起著重要作用〔1,2〕。復元膠囊是臨床上長期用于治療骨關節炎(OA)療效有明顯的中藥復方實驗制劑,本實驗觀察復元膠囊對OA模型大鼠軟骨細胞凋亡、關節液中NO及軟骨細胞核增殖抗原(PCNA)mRNA表達的影響。
1 材料與方法
1.1實驗藥物 復元膠囊由人參、淫羊藿、鹿茸、黃芪、川芎、當歸、枸杞子等組成,委托重慶希爾安藥業有限責任公司制成膠囊,僅供實驗使用(醫院制劑批號:[2005]12號B-55);壯骨關節丸,由深圳三九醫藥業股份有限公司生產,批號:Z44023377。
1.2實驗動物 雄性成年SD大鼠48只200~250 g,由重慶醫科大學實驗動物中心提供,實驗動物生產許可證號:SYXK(渝)2002007。
1.3實驗試劑 TUNEL試劑盒購自美國Roche公司;硝酸還原酶法NO檢測試劑盒購自南京建成生物工程研究所;蛋白酶K購自美國Sigma公司;DAB顯色試劑盒購自北京金橋中衫生物技術有限責任公司;RNA提取試劑Trizol購自Invitrogen公司;兩步法RT-PCR試劑盒購自TaKaRa公司;PCNA及內參GAPDH引物購自上海Sangon公司引物序列為:DL2000型DNA Maker購自TaKaRa公司;DEPC水購自sigma公司;瓊脂糖粉購自北京金橋中衫生物技術有限責任公司;GoldViewTM核酸染料購自北京賽百盛公司。
1.4實驗儀器 RD2000型X線機:美國長青公司;BX-50行生物顯微鏡:日本Olympus公司;HITACHI-7500型透射電鏡:日本HITACHI公司;BX40型光學顯微鏡:日本OLYMPUS公司;ELX-800型酶標儀: 德國Eppendorf公司;PCR 儀:德國EPPENDORF公司;Bio-RAD電泳儀及凝膠成像儀:美國BioRad公司。PCNA(290 bp)正向:5' TTGGAATCCCAGAACAGG3';反向5'AGACAGTGGAGTGGCTTT3';GAPDH(492 bp)正向:5'ATCACTGCCACCCAGAAGACT3';反向5'CATGCCAGAGGTCGGTTCGTTTT3'。
1.5方法
1.5.1動物分組 48只SD大鼠隨機分成四組,分別為正常組、模型組、壯骨關節丸組以及復元膠囊組,每組12只。
1.5.2建立動物模型 除正常組外,其余各組參照Hulth造模型方法〔3〕。0.5%的水合氯醛按0.35 g/100 g腹腔注射麻醉大鼠,在無菌條件下切斷右膝內側副韌帶、切除內側半月板以及剪斷前交叉韌帶,逐層縫合,無菌包扎。術后每天肌注青霉素2×104U/kg,共3 d。1 w后,每天驅趕大鼠跑步30 min。
1.5.3給藥 根據Meeh-Rubner公式〔4〕計算大鼠的給藥劑量。手術后第4周,復元膠囊組給予復元膠囊0.72 g·kg-1·d-1(相當生藥5.76 g·kg-1·d-1)、壯骨關節丸組給予壯骨關節丸1.14 g·kg-1·d-1配制成3 ml溶液,正常組、模型組分別給予生理鹽水3 ml,每天灌胃1次,共8 w。
1.6觀察指標
1.6.1大體肉眼觀察 大鼠抽取血液及關節炎液后處死,肉眼觀察膝關節有無滑膜腫脹,并于解剖顯微鏡下觀察股骨內髁、內側脛骨平臺關節面的病理改變。
1.6.2光鏡觀察軟骨細胞及基質 取股骨內髁全層軟骨標本置于4%中性緩沖甲醛溶液中固定,常規石蠟包埋、切片,HE染色。觀察軟骨組織的結構、細胞數量和潮線的完整性,根據Mankin法進行評分。
1.6.3電鏡觀察軟骨細胞及基質 銳利刀片切取1 cm3大小股骨內髁損傷部位全層軟骨,立即放人4 ℃的2.5%戊二醛中固定2 h。10%EDTA脫鈣3 w,1%鋨酸固定2 h,4 ℃冰箱內用乙醇逐級脫水,環氧樹脂包埋,超薄切片50~60 μm,電子染色,并在HITACHI-7500型透射電鏡下觀察。
1.6.4TUNEL法檢測軟骨細胞凋亡 參照Roche公司TUNEL試劑說明書操作,并設立陰性對照。陽性判定:細胞核中有棕黃色顆粒者為TUNEL陽性細胞,即凋亡細胞。每張切片任取5個視野,高倍鏡下計數陽性細胞和總細胞數,細胞凋亡指數(AI) =TUNEL標記陽性細胞數/軟骨細胞數×100%。
1.6.5硝酸還原酶法檢測關節液中NO活性 按照NO測定試劑盒說明書要求設置標準管和空白管,空白管調零,紫外分光光度計在530 nm波長下測定吸光度值(A)。
1.6.6RT-PCR法檢測PCNA mRNA表達 用Trizol提取各組軟骨的總RNA。各組取1 μl總RNA,逆轉錄合成cDNA,逆轉錄反應體系總體積10 μl(含MgC 12 2 μl、10×RT緩沖液1 μl、 RNase Free dH2O 3.75 μl、dNTP混合物1 μl、RNase抑制劑0.25 μl、轉錄酶0.5 μl、Oligo酶0.5 μl)。取逆轉錄產物3 μl進行PCR循環(94 ℃變性30 s,56 ℃退火30 s,72 ℃延伸1 min,共32個循環,末次延伸10 min,4 ℃保存)。反應完畢,取反應產物10 μl于1.5%含50 μl/L GoldViewTM核酸染料瓊脂糖凝膠中進行電泳,BIO-RAD凝膠成像儀中紫外光下觀察拍照,用Quantity One凝膠圖像分析軟件檢測各組目的基因及其GAPDH基因的光密度值,計算二者的比值,作為各組mRNA的相對表達量。
1.7統計學處理 應用SPSS10.0統計軟件進行方差分析及SNK-q檢驗。
2 結 果
2.1大體形態觀察 正常組大鼠關節軟骨外觀呈藍白色,表面光滑,色澤明亮潤澤,無裂紋及軟化,滑膜未充血增生,關節液清亮。模型組軟骨表面極不光滑,色澤晦暗,局部軟骨有缺損,甚至有潰瘍出現,深者可達骨質,軟骨下骨暴露,軟骨邊緣有較多骨贅形成,滑膜充血增生,關節液渾濁。復元膠囊組和壯骨關節丸組滑膜有明顯增生,脛骨平臺變淺,軟骨表面不太規則,部分軟骨有裂紋,甚至有細小潰瘍出現,壯骨關節丸組出現上述改變的程度大于復元膠囊組。
2.2各組大鼠膝關節軟骨組織形態觀察 軟骨表面連續性好,層次清晰,潮線完整,細胞排列整齊,分布均勻。模型組軟骨表層有明顯凹陷,結構難以分辨,嚴重的表層消失,部分區域呈絨毛狀,可見較多裂隙從表層軟骨延伸向下深達輻射層,裂隙中可見稀疏結締組織及松散的網狀連接,有纖維充填,潮線消失。壯骨關節丸組軟骨裂隙深達軟骨下骨,細胞排列紊亂,表層細胞數量減少,中深層可見細胞簇集成團,潮線消失。復元膠囊組軟骨4層界限欠清楚,在表層的凹陷中有軟骨細胞充填,周圍細胞有簇集現象,潮線多數不完整。模型組軟骨Mankin評分明顯高于正常組,復元膠囊組軟骨Mankin評分明顯低于模型組(P<0.01),復元膠囊組軟骨Mankin評分比壯骨關節丸組低(P< 0.05)。見表1。
2.3透射電鏡下觀察軟骨細胞超微結構 正常組軟骨細胞核完整,核膜清晰,核內染色體均勻分布,粗面內質網呈層狀排列,線粒體散在分布、細胞表面有許多微絨毛突起。凋亡細胞體積明顯縮小,突起消失。細胞從周圍軟骨基質退縮,核膜發生皺褶,染色體濃集,胞質密度增高,有典型的凋亡小體,內有細胞器,細胞周圍可見脫落的凋亡小體。
2.4TUNEL法檢測軟骨細胞凋亡情況 凋亡的軟骨細胞核呈棕黃色,主要分布在軟骨的淺層和中層。正常軟骨中有弱陽性表達,主要位于軟骨表層;模型組軟骨的移行層和深層有陽性細胞表達,AI明顯高于正常組。壯骨關節丸組和復元膠囊組在表層和移行層也有陽性細胞表達,但AI明顯低于模型組(P< 0.05),而復元膠囊組和壯骨關節丸組比較差異顯著(P< 0.05),見表1。
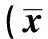
表1 復元膠囊對膝OA軟骨Mankin評分及AI的影響±s,n=12)
2.5復元膠囊對大鼠膝骨關節炎關節液中NO的影響 模型組、壯骨關節丸組和復元膠囊組關節液中NO濃度較正常組升高(P<0.01),而壯骨關節丸組和復元膠囊組比模型組明顯降低(P<0.01),復元膠囊組關節液中NO水平低于壯骨關節丸組(P<0.05)。見表2。
2.6復元膠囊對關節軟骨PCNA mRNA表達的影響 各組軟骨提取的RNA經逆轉錄并PCNA序列擴增后,電泳顯示不同的熒光強度。造模后各組軟骨節軟骨PCNA mRNA表達代償性增加,復元膠囊組與壯關節丸組PCNA mRNA增加高于模型組(P<0.05);復元膠囊組與壯骨關節丸組PCNA mRNA表達比較差異顯著(P<0.05)。見表2。
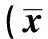
表2 復元膠囊對膝OA關節液中NO、軟骨細胞PCNA mRNA的影響±s,n=12)
3 討 論
研究發現,復元膠囊能促進離體軟骨細胞DNA及Ⅱ型膠原的合成〔5〕,同時,降低大鼠OA模型血清中軟骨代謝標志物COMP水平,從而延緩骨關節炎軟骨退變過程〔6〕。本研究從NO介導的凋亡及增殖角度研究復元膠囊治療OA的作用機制。
關節軟骨退行性改變是OA發病的中心環節,共同的病理學特征是關節軟骨進行性變性、破壞,軟骨下骨硬化,關節邊緣和軟骨下骨反應性增生,骨贅形成〔7〕。通過比較復元膠囊組與模型組軟骨外觀大體觀察、組織學評分,我們可以看出復元膠囊對膝OA模型的軟骨退變有明顯的保護作用,延緩OA病程。
軟骨細胞過度凋亡在軟骨退行性改變過程中起著重要作用。本實驗結果顯示,透射電鏡下可觀察到典型的凋亡形態,包括細胞體積縮小、染色質凝聚、核碎片、細胞皺縮、凋亡小體等;細胞凋亡末端原位檢測(TUNEL)發現,經Hulth法建立的OA動物模型關節軟骨有凋亡細胞陽性表達,主要位于淺層和中層,移行層和深層也有陽性細胞表達明顯,高于正常組,再次證明軟骨細胞凋亡參與了OA的病理改變。
軟骨細胞凋亡的誘導有兩個獨立通路,一是NO依賴通路,二是Fas介導的非NO依賴通路,在OA中NO依賴通路更重要〔2〕,所以通過抑制NO的活性從而抑制細胞過度凋亡可能是一條治療OA的途徑。本實驗結果提示,造模后關節液中NO濃度顯著升高,復元膠囊能降低OA模型膝關節液中的NO濃度。而NO又是誘導凋亡的主要途徑之一,降低NO活性,抑制軟骨細胞凋亡,從而保護了軟骨。因此復元膠囊能通過抑制NO途徑,從而抑制軟骨細胞的凋亡。
軟骨細胞因過度凋亡,導致軟骨破壞,但同時也啟動了機體的增殖,軟骨細胞通過增殖來代償,維持平衡狀態〔8〕。PCNA是從G1期后半至S期前半過程中細胞核內急劇增多的一種核蛋白質,目前認為它的表達是衡量細胞增殖的重要標記物〔9〕。OA患者損傷關節軟骨及負重區軟骨中的軟骨細胞數少于正常人關節軟骨細胞數,凋亡引起軟骨細胞數量減少伴有細胞代償性的增殖〔10〕。本研究發現,造OA模型后軟骨細胞凋亡伴有軟骨PCNA mRNA表達代償性增加,體現了OA的發病是損傷與抗損傷相互作用的結果。復元膠囊能促進軟骨PCNA mRNA的表達,提示復元膠囊可通過促進軟骨細胞增殖而對OA軟骨起保護作用。
綜上,復元膠囊可以減輕骨關節炎關節軟骨的病理改變,降低軟骨細胞凋亡指數及關節液中NO水平,增加軟骨PCNA mRNA的表達,從而減緩骨關節炎病變的發展。
4 參考文獻
1Yan Q,Feng Q,Beier F.Reduced chondrocyte proliferation,earlier cell cycle exit and increased apoptosis in neuronal nitric oxide synthase-deficient mice〔J〕.Osteoarthritis Cartilage,2012;20(2):144-51.
2Calamia V,de Andrés MC,Oreiro N,etal.Hsp90β inhibition modulates nitric oxide production and nitric oxide-induced apoptosis in human chondrocytes〔J〕.BMC Musculoskelet Disord,2011;17(12):237.
3Hulth A,Lindberg L,Telhag H.Experimental osteoarthritis in rabbits preliminary report〔J〕.Acta Orthop Scand,1970;41(5):522-30.
4徐菽云.藥理學實驗方法〔M〕.北京:人民衛生出版社,2002:203-4.
5胡文興,周小莉,李榮亨.復元膠囊含藥血清對軟骨細胞增殖與合成代謝的影響〔J〕.中國中醫基礎醫學雜志,2008;14(4):275-7.
6周小莉,李榮亨.復元膠囊對膝骨關節炎模型血清軟骨寡聚基質蛋白的影響〔J〕.中國老年學雜志,2009;29(2):178-80.
7Goldring MB.Chondrogenesis,chondrocyte differentiation,and articular cartilage metabolism in health and osteoarthritis〔J〕.Ther Adv Musculoskelet Dis,2012;4(4):269-85.
8Pfander D,Swoboda B,Kirsch T.Expression of early and late differentiation markers (proliferating cell nuclear antigen,syndecan-3,annexin VI,and alkaline phosphatase) by human osteoarthritic chondrocytes〔J〕.Am J Pathol,2001;159(5):1777-83.
9Hall PA,Levison DA,Woods HL,etal.Proliferating cell nuclear antigen (PCNA) immunol ocalization in paraffin sections:index of cell prolifer- ation with evidence of deregulated expression in some neoplasms〔J〕.J Pathol,1990;162(2):285-94.
10Tchetina E,Kobayashi M,Yasuda T,etal.Chondrocyte hypertrophy can be induced by a cryptic sequence of type Ⅱ collagen and is accompanied by the induction of MMP-13 and collagenase activity:implications for development and arthritis〔J〕.Matrix Biol,2007;26(4):247-58.

