Delta4在容積弧形調強放療驗證中的應用
劉 磊 吳愛東 閆 冰
(安徽醫科大學附屬省立醫院 放療科,安徽 合肥 230001)
容積弧形調強放射治療 (volumetric modulated arc therapy,VMAT)現已成功地應用于臨床,相對于適形調強放射治療(intensity modulated radiation therapy,IMRT)來說,VMAT計劃在設計和執行的時候更為復雜,它需要精確而又快速運動的多葉準直器,需要能精確運轉的機架,需要加速器理想的劑量率的時間響應[1]。顯然,VMAT技術的出現對放療過程中的質量保證(quality assurance,QA)工作提出了更高的要求,必須進行嚴格的劑量學驗證[2]。自2013年12月到2014年3月,共有50多名患者在我科接受了VMAT治療,筆者隨機抽取10例鼻咽癌和10例宮頸癌患者的VMAT計劃,利用Delta4劑量驗證系統進行劑量驗證,并就其測量結果進行對比分析,旨在為臨床實踐提供借鑒經驗。現將我科的VMAT計劃驗證方法總結報告如下。
1 材料與方法
1.1 病例資料
從安徽省立醫院放療科自2013年12月至2014年3月共50例患者的VMAT計劃中,隨機抽取10例鼻咽癌和10例宮頸癌的VMAT計劃。計劃由飛利浦Pinnacle計劃系統(Version 9.6)利用SmartArc優化模塊優化產生,每個治療方案均有2個治療弧,第1個為179°開始沿逆時針方向旋轉359°照射,第2個為181°順時針方向旋轉359°照射,控制點間隔為4°,為避免葉片間漏射對計劃的影響,小機頭collimator角度均設為10°。
1.2 加速器及治療網絡
瑞典Elekta公司容積旋轉調強(VMAT)醫用直線加速器,劑量率為400MU/min,該加速器內置40對多葉準直器,葉片在等中心的投影寬度為 1cm。 另外,使用 Elekta 公司的 Mosaiq(Version2.20.08E6)網絡驅動加速器治療模體。
1.3 Delta4 劑量驗證系統
瑞典ScandiDos公司生產的Delta4劑量驗證系統是由一個22cm×40cm圓柱型模體、校準模體、一塊探測器主板、兩塊翼板、連接盒、分析軟件及輔助擺位小推車組成。主板和翼板共有1069個P型圓柱形半導體探測器,電離室靈敏度5 nC/Gy,中心6cm×6cm探頭間隔5mm,中心以外的區域間隔10mm。探測器陣列正交插入圓柱型模體中,最大探測面積38cm×20cm。Delta4具有各向同性的特性,能收集任意入射角度的粒子信息,最高分辨率達l×0.05mm2,可完成任意角度的測量[3]。使用Delta4前需在常規加速器對其進行相對劑量校準、絕對劑量校準和方向性校準。
1.4 研究方法
(1)在Pinnacle計劃系統上,將患者的VMAT計劃移植給Delta4模體,治療中心對準圓柱模體等中心,重新計算治療計劃在Delta4模體中的劑量分布,驗證計劃不需要對原計劃做任何改變,包括治療機器跳數,然后通過網絡把原計劃中的RT Structures及驗證計劃的RT Plan導出到Delta4的軟件中等待驗證。
(2)把Delta4模體擺放在直線加速治療床上,激光燈對準模體表面的中心線,Delta4通過信號線與直線加速器的同步信號連接,通過網線與裝有Delta4軟件的電腦連接。打開Delta4電源開關,預熱15分鐘。開始計劃驗證前,先做一個10cm×10cm盒式野計劃的測量,與參考盒式野校準計劃進行比較,校準當次測量中因加速器絕對輸出量不穩定而造成的誤差。
(3)從Mosaiq網絡上調出患者的治療計劃,通過加速器治療Delta4模體。整個流程要仔細檢查每個步驟,盡量減少誤差。Delta4可記錄每個射野的數據和每個段控點測量數據。
(4)測量完畢后,ScandiDos軟件自動合成整個計劃的測量數據,并將Delta4探測器陣列測量得到的劑量分布與治療計劃計算所得的劑量分布進行比較。如圖1所示,得出三種分析比較法的結果,劑量偏差 DD(Dose Deviation)、滿意距離 DTA(Distance to agreement)分析法和γ分析法。按照文獻所建議的QA計劃接受標準并參照大多數醫院使用的標準[4],位移偏差標準(Δdm)為 3mm,劑量偏差標準(ΔDm)為 3%時,Gamma值小于1的測量點百分比(即通過率)>90%,則認為該劑量分布符合臨床治療要求,治療計劃可以用于臨床治療。
1.5 統計方法
計算結果以均數±標準差(x±s)表示,利用 SPSS 19.0 統計軟件對鼻咽癌和宮頸癌2組測量數據進行配對設計t檢驗,P<0.05認為差異有統計學意義。
2 結果
20例患者的VMAT計劃的3mm3%的γ通過率全部大于90%,平均通過率為 96.7%。其中 10例鼻咽癌 VMAT計劃的 DD、DTA、3mm3%γ 的平均通過率分別為 67.35%、94.05%和 94.85%(表 1),10例宮頸癌 VMAT計劃的 DD、DTA、3mm3%γ的平均通過率分別為89.59%、99.19%和 98.54%(表 2)。 二種不同部位患者的 γ 平均通過率結果及比較見表3。
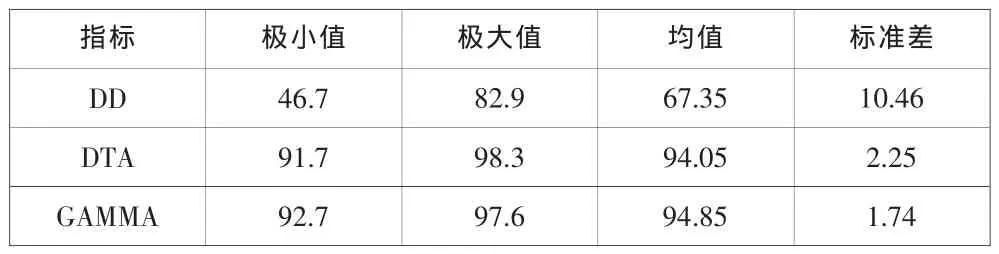
表1 10例鼻咽癌VMAT計劃各評價指標比較
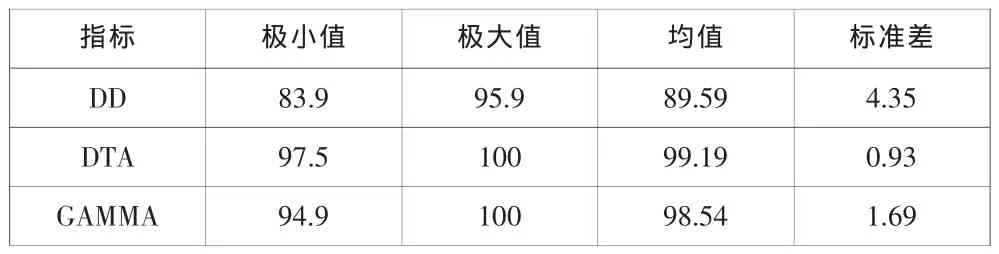
表2 10例宮頸癌VMAT計劃各評價指標比較
3 討論
容積旋轉調強放療技術作為調強放射治療在技術實現上的一種延伸,這一新技術的出現使得放療越來越復雜,復雜的治療計劃必須經過嚴格的驗證。Delta4劑量驗證系統具有簡單、快捷、準確的特點,是理想的容積旋轉調強放療的劑量學驗證工具[5]。本研究應用Delta4劑量驗證系統對20例VMAT計劃進行劑量驗證,結果顯示3mm3%的γ平均通過率為96.7%±1.71,每一例計劃的驗證通過率均大于90%的,符合臨床劑量驗證要求。
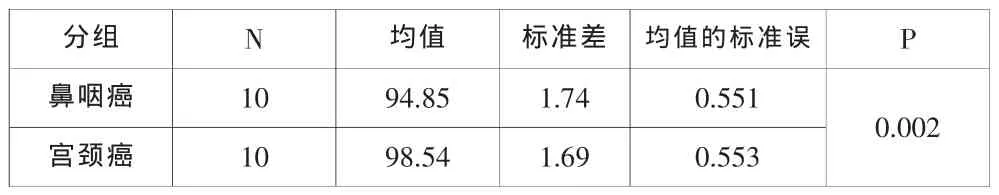
表3 鼻咽癌與宮頸癌VMAT計劃的γ通過率比較
由表1和表2對比DD、DTA和γ這三種分析方法的驗證結果可見,DD在劑量分布梯度大的區域對位置偏移敏感,微小的位置偏移會造成較大誤差,對于劑量分布相對平緩的區域計算結果較好;DTA適用于劑量分布梯度相對較大區域,在劑量分布平緩的區域會造成較大誤差,微小的劑量差異也會造成較大的距離,計算結果偏高;γ分析法則結合了DD與DTA的優點[9],不管對于劑量梯度較大區域還是平緩的區域,其計算值不會過大,誤差較小,能更好地用于臨床劑量驗證。
為研究由于VMAT計劃復雜程度不同引起治療計劃系統計算誤差及加速器輸出誤差對驗證結果的影響,筆者對比了10例鼻咽癌的γ 通過率(94.85%±1.74)和 10例宮頸癌的 γ通過率(98.54%±1.69)的分析結果,發現腫瘤部位及計劃的復雜度是影響驗證通過率結果的主要因素,直接影響計劃的通過率,而加速器狀態、Delta4狀態及人為因素對驗證結果的影響也不能忽略,都需盡量避免,這也是臨床計劃進行驗證測量的目的。在使用Delta4進行VMAT劑量驗證時,要盡可能精確的擺放模體,并定期保養執行VMAT功能的加速器,必要時需對Delta4驗證矩陣校正因子做修正。
綜上所述,筆者利用Delta4劑量驗證系統等已有的設備條件,建立了患者VMAT計劃的劑量學驗證方法,并取得了值得信賴的結果。隨著設備條件的改善和經驗的積累,VMAT計劃的劑量學驗證方法還會得到進一步完善。
[1]Wang C,Luan S,Tang G,et al.Arc-modulated radiation therapy (AMRT):a single-arc form of intensity-modulated arc therapy[J].Physics in medicine and biology,2008,53(22):6291.
[2]Bedford J L,Warrington A P.Commissioning of volumetric modulated arc therapy (VMAT)[J].International Journal of Radiation Oncology*Biology*Physics,2009,73(2):537-545.
[3]Bedford J L,Lee Y K,Wai P,et al.Evaluation of the Delta4 phantom for IMRT and VMAT verification[J].Physics in medicine and biology,2009,54(9):N167.
[4]Low D A,Harms W B,Mutic S,et al.A technique for the quantitative evaluation of dose distributions[J].Medical physics,1998,25(5):656-661.
[5]張偉,馬照,邵鵬,等.Delta4的臨床應用研究[J].中華放射腫瘤學雜志,2010(1):48-51.

