高效液相色譜法測定板藍根注射液中(R,S)-告依春的含量
韓 立,班付國,周紅霞,王 林,劉素梅,張躍京
(1.河南省獸藥監察所,鄭州450008;2.河南省康星藥業股份有限公司,鄭州451464)
板藍根注射液為十字花科植物菘藍(Isatis Indigotica Fort.)的干燥根,以水提醇沉法提取后制成的滅菌水溶液。作為一種清熱解毒、涼血利咽的中獸藥注射液,它具有抗菌、抗病毒、抗內毒素、增強免疫的作用,尤其在抗病毒方面療效確切[1-2],用于治療家畜流感、仔豬白痢、肺炎及某些發熱性疾病。板藍根注射液的成分復雜多樣,主要有靛藍、靛玉紅、(R,S)-告依春、多種有機酸、核苷、氨基酸等多種成分[3-4]。以往報道的含量測定方法多為測定板藍根注射液中靛藍、靛玉紅、有機酸、氨基酸的含量[5-7],但該制劑為水煎提取液,靛藍、靛玉紅為脂溶性,在水提液中溶解性小,因此難以作為含量控制指標。(R,S)-告依春為主要抗病毒活性成分,又為水溶性,因此有必要建立板藍根注射液中(R,S)-告依春的含量測定方法,用以控制板藍根注射液的含量。
1 儀器與試劑
Waters超高效液相色譜儀(美國Waters公司)配置TUV紫外檢測器檢測器,Empower2色譜工作站采集數據。電子天平(BP211D),德國Sartorius公司。超純水裝置,Milli-Q Advantage A10,美國密理博公司。
甲醇(色譜純),磷酸(分析純),中性氧化鋁(層析用),純化水,(R,S)-告依春對照品(含量99.9%,批號110713-200911,中國藥品生物制品檢定所)。板藍根注射液樣品6批(批號分別為20130701, 20130702, 20130703, 20130501,20130502,20130503,均由 1家獸藥生產企業提供)。
2 方法與結果
2.1 色譜條件與系統適用性試驗 流動相為甲醇-0.02%磷酸溶液(7:93);色譜柱:Waters XBridge C18,150 mm ×4.6 mm,5 μm;檢測波長 245 nm;流速1.0 mL/min;進樣量:10 μL;柱溫30 ℃。理論板數按R,S-告依春峰計算不低于2400,主峰的保留時間約為12 min。結果見圖1、圖2。結果表明在上述色譜條件下板藍根注射液分離效果好,R,S-告依春和其他組分達到基線分離。
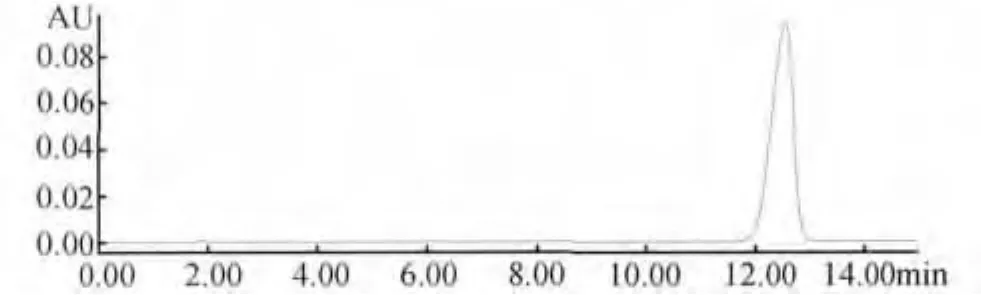
圖1 對照品色譜圖
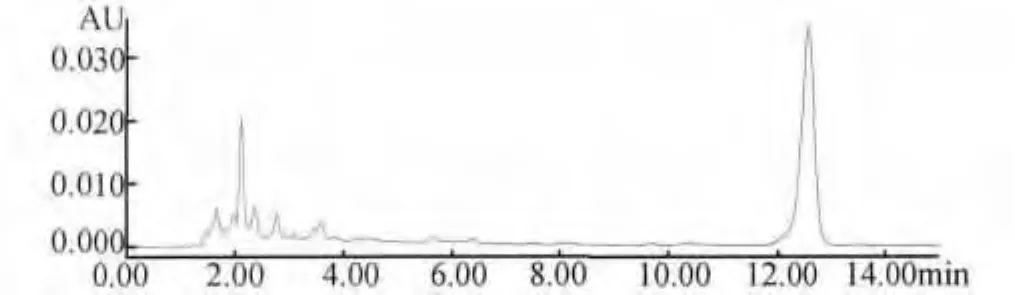
圖2 板藍根注射液色譜圖
2.2 對照品溶液的制備 精密稱取(R,S)-告依春對照品10.36 mg,置250 mL量瓶中,加甲醇制成每 mL 含41.4 μg 的溶液,過 0.45 μm 微孔濾膜,即得。
2.3 供試品溶液的制備 精密量取板藍根注射液5 mL,過中性氧化鋁柱(內徑為1.5 cm,5 g),收集流出液,再用15 mL水洗脫,流出液和洗脫液合并至25 mL容量瓶中,加水稀釋至刻度,作為供試品溶液。
2.4 線性關系考察 取R,S-告依春對照品溶液,分別稀釋成 1、5、10、20、40 μg/mL,精密量取10 μL,注入高效液相色譜儀,記錄色譜圖。以濃度為橫坐標,峰面積為縱坐標,進行線性回歸,回歸方程為:y = 77327x+519.2,相關系數 r= 0.9998,在1~40μg/mL的濃度范圍內,對照品具有良好的線性關系(圖3)。
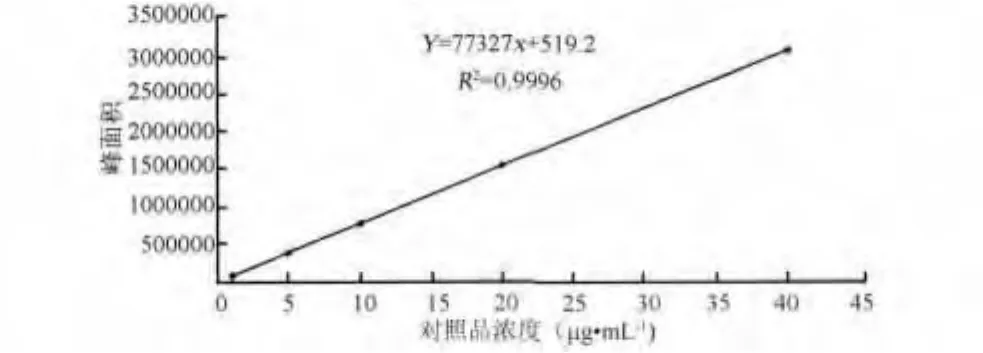
圖3 R,S-告依春標準曲線圖
2.5 精密度試驗 精密吸取(R,S)-告依春對照溶液10 μL注入色譜儀,記錄色譜圖,連續進樣6次測定峰面積。結果相對標準偏差(RSD)為0.31%,表明系統精密度符合要求。
2.6 穩定性試驗 取同一批供試品溶液,分別在樣品處理后的 0,1,2,8,12 h 進樣,測定峰面積,考察樣品穩定性。結果在12 h內含量下降率僅為0.13%,表明供試品溶液在12 h內穩定。
2.7 重復性試驗 取批號為20130701的板藍根注射液,精密量取5 mL,共6份,分別按2.3項下方法制備供試品溶液,按2.1項下條件進樣測定,計算含量及RSD。結果樣品中(R,S)-告依春的含量為 37.8 μg/mL,RSD 為 0.03%,表明該方法重復性良好。
2.8 回收率試驗 取批號為20130701的板藍根注射液,精密量取2.5 mL,共6份,用移液槍分別加入0.4 mg/mL標準貯備液0.236 mL(相當于約94.5 μg的(R,S)-告依春),按照 2.3 項下方法制備供試品溶液,按2.1項下條件測定,計算平均回收率及RSD,結果見表1。結果表明,該方法平均回收率為98.6%,RSD為0.36%,說明方法的回收率較高,重復性良好。
2.9 樣品的測定 取同一公司5批板藍根注射液樣品,每批量取兩份,按供試品處理方法處理。取10 μL樣品溶液注入色譜儀,記錄色譜圖,平行進樣兩次,計算平均含量。各批次樣品的含量見表2。結果表明5批板藍根注射液含板藍根以(R,S)-告依春計,在36.2 ~42.5 μg/mL 之間。
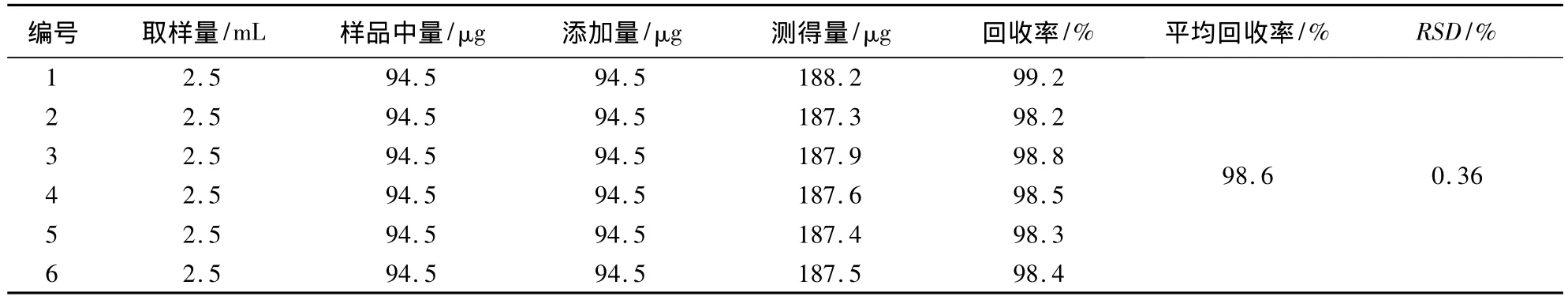
表1 (R,S)-告依春回收率試驗結果
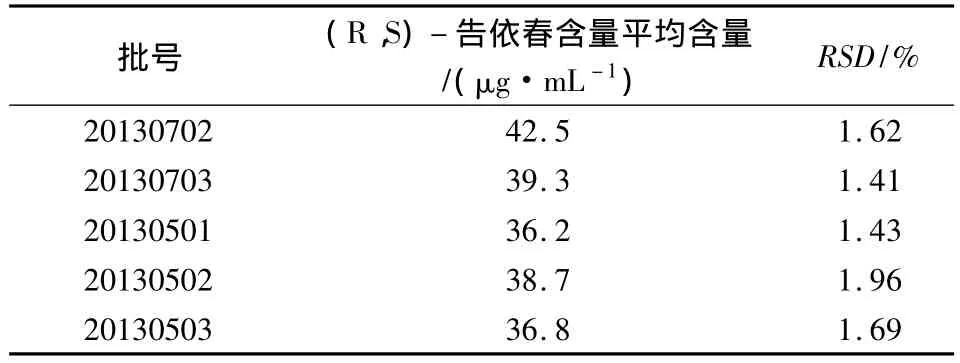
表2 樣品測定結果
3 討論與小結
3.1 樣品提取方法的選擇 板藍根注射液為板藍根水浸出物的滅菌水溶液,主要工藝為加水煎煮,濃縮,醇沉之后加水定容,每1 mL相當于0.5 g原生藥。(R,S)-告依春溶于三氯甲烷、乙醇、甲醇,也能溶于沸水,不溶于冷水。試驗分別比較了甲醇、70%甲醇、30%甲醇、純水作為溶劑進行稀釋提取。結果發現室溫條件下(20~25℃)用純水提取的回收率最高,而用10℃以下的冷水提取時回收率有明顯下降,這與石燕紅[8]的結論相符。因此,試驗選用純水在室溫條件下提取。考慮到(R,S)-告依春在冷水中溶解度很小,應盡量避免使用冷水提取。
3.2 樣品的凈化 試驗比較了樣品過中性氧化鋁柱和不過中性氧化鋁柱的效果。發現不過中性氧化鋁柱時,供試品溶液顏色較深,進樣后雜質峰較多,很難與目的峰分離。當樣品過中性氧化鋁柱后,供試品溶液顏色變淺,雜質峰明顯減少,樣品的含量幾乎沒有變化。可以推斷,色素等雜質被中性氧化鋁吸附,但(R,S)-告依春基本都被洗脫下來。
3.3 樣品的含量 試驗考察了同一公司6批樣品,(R,S)- 告依春含量范圍為 36.2 ~42.5 μg/mL。由于藥材來源不同,不同公司的生產工藝存在差異,板藍根注射液中(R,S)-告依春含量相差可能較大[9]。參照《中華人民共和國藥典》板藍根和《獸藥國家標準》(化學藥品、中藥卷)板藍根注射液有關標準[10-11],有必要對板藍根注射液成品中(R,S)-告依春的收率以及不同來源的板藍根注射液中(R,S)-告依春含量進行進一步的測定和考察,以制定出合理的含量限度。
3.4 方法的評價 現有文獻報道了幾種不同的高效液相色譜流動相條件對(R,S)-告依春進行含量測定,主要包括乙腈-磷酸水系統[12]、乙腈-冰乙酸水系統[13]等流動相系統,試驗對這幾種方法分別進行了考察,發現采用甲醇-0.02%磷酸水溶液(7∶93)流動相系統效果最好,方法學考察均符合要求。
3.5 小結 試驗建立了板藍根注射液中(R,S)-告依春含量測定的高效液相色譜方法。該方法簡單快速,靈敏度高,重復性好,可以有效控制板藍根注射液中(R,S)-告依春的含量,并為板藍根注射液的質量標準修訂提供參考。
[1]趙 軍.板藍根的藥理作用及其臨床應用[J].時珍國醫國藥,2003,14(4):241 -242.
[2]徐 晗,方建國,劉云海.板藍根最新研究進展[J].中草藥,2003,34(4):10 -11.
[3]彭少平,顧振綸.板藍根化學成分、藥理作用研究進展[J].中國野生植物資源,2005,24(5):4 -6.
[4]肖珊珊,金 郁,孫毓慶,等.板藍根化學成分、藥理及質量控制研究進展[J].沈陽醫科大學學報,2003,20(6):455 -459.
[5]王燕恒,劉國瑞,需 方,等.RP-HPLC法測定板藍根中靛藍和靛玉紅的含量[J].河北大學學報:自然科學版,2005,25(5)507-508.
[6]楊元娟,夏之寧,楊元梅.板藍根注射液中有機酸成分的毛細管電泳分析[J].激光雜志,2009,30(6):94 -95.
[7]王 欣,孟憲杰,張 懿.高效液相色譜測定板藍根注射液中三種核苷的含量[J].現代中西醫結合雜志,2012,21(6):646 -647.
[8]石燕紅,謝志勇,吳迎春,等.RP-HPLC測定板藍根制劑中R,S-告以春[J].中國實驗方劑學雜志,2011,17(8):128 -130.
[9]張曉靜,張俊義,胡海聰,等.RP-HPLC法同時測定清開靈注射液、板藍根藥材中尿苷、鳥苷、(R,S)-告依春和腺苷的含量[J].遼寧中醫藥大學學報,2013,15(11):53 -55.
[10]國家藥典委員會.中華人民共和國藥典2010年版一部[S].
[11]中國獸藥典委員會.獸藥國家標準(化學藥品、中藥卷)第一冊[S].
[12]鄒耀華,劉宇文.HPLC測定感冒退熱顆粒中R,S-告以春含量[J].中國現代應用藥學,2011,28(11):1035-1037.
[13]張 葉,張 蕾,王 玉.RP-HPLC法測定板藍根藥材中腺苷和表告以春的含量[J].藥物分析雜志,2008,28(11):1948-1950.

