紫銅在海洋微生物作用下的電化學腐蝕行為
陳海燕,林振龍,陳丕茂,秦傳新,唐振朝,余 景
(1廣東工業大學 材料與能源學院,廣州510006;2中國水產科學研究院 南海水產研究所,廣州510300)
銅及其合金具有良好導電導熱、耐磨、易于加工成型和耐腐蝕性能好等優點,被廣泛應用于海洋開發領域,如船舶的海水管路、濱海電廠的海水熱交換和人工魚礁等[1-3]。然而由于海水是一個極端復雜的環境,除了含有大量的腐蝕性氯離子,還有多種微生物和宏觀生物。事實證明,銅及其合金雖然短期的實驗中表現良好的耐腐蝕性[4-6],但在實際使用時往往出現早期失效的現象,雖然銅和其合金由于表面可形成有毒溶液的薄層,使得銅和銅合金材料有一定的防止海洋生物污損能力,但銅和銅合金本身對微生物腐蝕仍然是敏感的,在核電站的冷卻水等系統中,曾遇到一些由于微生物活動影響而發生的銅合金的孔蝕、和應力腐蝕破裂的事例[7,8]。
與碳鋼和不銹鋼相比[9-12],目前有關銅和銅合金的微生物腐蝕的文獻報道較少[13]。本工作在實驗室中對海洋微生物進行培養,采用紫銅的開路電位分析、極化曲線和交流阻抗技術等電化學方法,研究了在海洋微生物作用下銅的腐蝕行為和腐蝕機制,為建立合理有效的防治微生物腐蝕的系統方法提供科學依據。
1 實驗
1.1 實驗材料
退火態紫銅T2,其主要成分見表1。鹽度為30.26的海水(取自廣東惠州大亞灣,含氧量為0.4%,體積分數,下同)、鹽度為18.43的咸淡水(取自廣東柘林灣,含氧量為2%)。
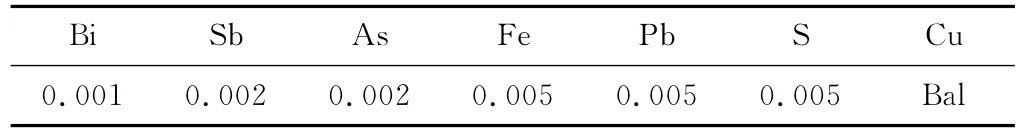
表1 紫銅T2的化學成分(質量分數/%)Table 1 Chemical composition of T2type copper(mass fractiom/%)
1.2 實驗方法
1.2.1 試樣制備
銅板切割成尺寸為10mm×10mm的片狀試樣,為了消除加工組織對腐蝕行為的影響,試樣均經退火處理(550℃保溫1h,水冷,再在200℃回火30min,爐冷)。采用800號以上的砂紙打磨,酒精除油,蒸餾水清洗后吹干。
1.2.2 菌種培養
培養基按如下組成配置:胰蛋白胨10g/L;蛋白胨5g/L;酵母粉1g/L,用氫氧化鈉溶液調節pH值為7.0±0.2。將配置好的培養基倒入錐形瓶中,用醫用紗布包扎好瓶口,在120℃高壓蒸汽殺菌器滅菌,有菌培養是將海水菌種和滅菌培養基以1∶10(體積比)混合,無菌培養是將滅菌海水和滅菌培養基以1∶10(體積比)混合,有菌培養則放入恒溫振蕩器中進行培養,每隔4h取樣,用分光光度計測量有菌培養溶液的吸光度,以測出細菌的生長曲線。對裝有細菌的培養液進行觀察實驗中的所有玻璃儀器經高溫、高壓滅菌,在無菌操作實驗臺操作,確保實驗中無雜菌干擾。
1.2.3 附著生物形貌
將試樣打磨拋光,丙酮除除,75%酒精消毒并用紫外燈滅菌后浸泡入有細菌的培養液中,待各個菌落數量達到高峰期后取出用戊二醛固定生物膜,干燥后用AMRAY-100B電子顯微鏡對附著金屬表面上的微生物的形態和分布進行觀察。
1.2.4 電化學測試
將腐蝕介質(包括海水和咸淡水)分成兩組進行電化學實驗,一組在恒溫振蕩器中培養了30h后的有菌介質中;另一組在紫外燈殺菌后的無菌介質。(1)開路電位:采用UJ25型直流高電勢電位差計測量材料的開路電位,參比電極為飽和甘汞電極,測得的電極電位值均為相對飽和甘汞電極電位(SCE)(下同)。(2)陽極極化曲線和交流阻抗:為研究試樣在不同的腐蝕介質的腐蝕行為,用穩態恒電位法測定陽極極化曲線。實驗儀器為德國產的電化學工作站IM6,參比電極用飽和甘汞電極,輔助電極用鉑電極,掃描速率為40mV/min。
1.2.5 腐蝕率
在室溫下將各種材料分別放入各腐蝕介質中泡浸100天后取出試樣清除腐蝕產物,干燥后稱重,其中有菌介質采用間歇式培養方式。
2 實驗結果與分析
2.1 微生物生長規律和附著形貌
細菌的生長規律分為4個周期:遲緩期、對數生長期、穩定生長期和衰亡期。圖1為大亞灣海水和柘林灣咸淡水的細菌生長曲線,從圖1中可看出,曲線1為海水中的細菌生長規律,海水中的細菌在0~8h內處于生長遲緩期;8~16h細菌數量激增,幾乎成對數增長,這就是細菌的對數生長區;在16~30h,因為細菌的大量繁殖,細菌基本達到一個平衡狀態,細菌死亡率跟出生率基本一樣,細菌的數量從開始培養到30h后細菌數量達到最大值;35h后,由于培養基中營養不足,死亡的細菌多于新增的細菌,所以細菌總數急劇下降,這段時間叫衰亡期。曲線2為咸淡水中的細菌生長曲線,與海水中的細菌相比,緩慢區域內細菌數量增長速率較為緩慢,13~23h后,增長速度激增,細菌大量繁殖,但是大量繁殖會造成培養基成分不足以提供細菌增長的環境,所以在24h后出現增長速率減緩的趨勢,28h后細菌數量基本不變,42h后咸淡水細菌進入衰亡期。

圖1 海水和咸淡水中細菌生長曲線Fig.1 Growth curves of the bacteria in seawater and estuary water
圖2為分別浸泡在海水帶菌和咸淡水帶菌體系中30h后,紫銅微生物的附著微觀形貌。從圖2(a)看出,有少量的半透桿狀細菌附在銅板表面,材料表面分布著大量桿狀的微小凹坑,這是由于紫銅表面形成生物膜疏松且不連續,造成細菌脫落后留在膜層表面形成了坑洞。圖2(b)中可觀察到銅板表面形成了連續均勻的生物膜,膜層表面能觀察到明顯的微彎桿狀微生物菌落,各種桿菌的大小、長短、彎度、粗細差異較小,大多數桿菌大小為長2~5μm,寬0.3~1μm。

圖2 銅板上的附著的微生物形貌 (a)海水;(b)咸淡水Fig.2 SEM of the microbe adhesions on the copper (a)seawater;(b)estuary water
2.2 開路電位
將紫銅試樣分別放入海水有菌培養基、無菌培養基和咸淡水有菌培養基、無菌培養基四種介質中,開路電位曲線如圖3所示,圖中4種介質條件下銅電極的自腐蝕電位隨著時間的增加呈現負移趨勢,表明紫銅在富集氯離子的海水或咸淡水介質中不能形成致密的鈍化膜。對比曲線1和曲線3可以看出,在無菌條件下,銅電極在海水的開路電位比咸淡水低,說明隨著介質海水鹽度的提高,紫銅發生電化學腐蝕的可能性增大。但在有菌條件下,在咸淡水的開路電位遠遠小于海水的路電位,這是因為在咸淡水環境中,大量細菌吸附在試樣表面,由于新陳代謝等復雜的生命活動形成的某些特殊物質,使得紫銅在鹽度較小的情況發生腐蝕傾向增大。
2.3 陽極極化曲線

圖3 銅電極開路電位隨時間變化曲線Fig.3 Open circuit potential curves of copper
紫銅電極在有菌和無菌介質中的陽極極化曲線如圖4所示,可見電極在4種介質中的極化曲線形狀基本一致:都經過活化區、活化鈍化過渡區、鈍化區和過鈍化區。由圖4(a)中的海水極化曲線中可以看出紫銅在有菌海水的開路電位較負,腐蝕電流密度較大,反映了微生物的存在對紫銅的腐蝕起到了促進作用。對比圖4(b)中的兩條曲線,可看出,紫銅在有菌的咸淡水中自腐蝕電位很小,表明紫銅在有菌的咸淡水中發生腐蝕的可能性較大,這與開路電位結果一致。這表明不管是海水還是咸淡水,微生物附著和繁殖加速了紫銅的腐蝕,降低了其在海洋環境中的耐蝕性。
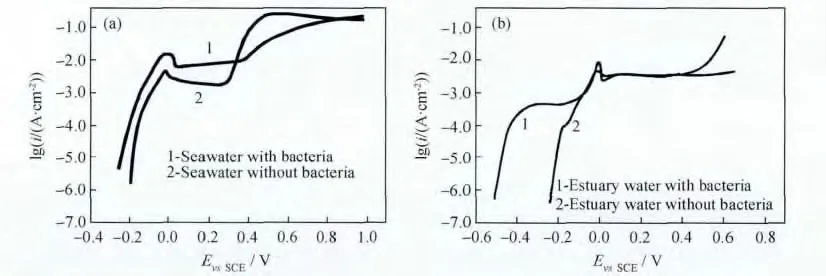
圖4 紫銅電極在介質中的陽極極化曲線 (a)海水;(b)咸淡水Fig.4 Anode polarization curves of the copper (a)seawater;(b)estuary water
2.4 自然腐蝕
紫銅分別在不同鹽度的有菌介質和無菌介質中自然腐蝕100天后,腐蝕率結果如表2所示。

表2 紫銅在各介質的腐蝕率Table 2 Corrosion rate of the copper sample in different mediums
從表2可看出無菌條件下,紫銅在鹽度為18.43的咸淡水的腐蝕率較小,隨著介質鹽度的增加,紫銅的腐蝕率也會增加,因此無菌海水的侵蝕性比無菌咸淡水的大。相同鹽度的條件下,細菌明顯加劇紫銅的腐蝕。但紫銅在有菌海水和有菌咸淡水中的腐蝕率非常接近,這是可能是因為在咸淡水中銅板表面吸附著較多的微生物菌落造成的。
2.5 電化學阻抗譜
EIS的測量進一步揭示紫銅微生物腐蝕的電化學機制[13],輸入的正弦波電流擾動信號頻率范圍為3×10-2~1×105Hz,振幅設為5mV,測試溫度為25℃。紫銅在無菌和有菌的介質(包括海水和咸淡水)中浸泡30h后的阻抗圖如圖5所示。

圖5 紫銅浸泡在各介質中30h后的電化學阻抗譜(a)海水 Nyquist;(b)無菌海水Bode;(c)有菌海水Bode;(d)咸淡水 Nyquist;(e)無菌咸淡水Bode;(f)有菌咸淡水BodeFig.5 EIS diagrams of copper after 30hof immersion in different mediums (a)Nyquist diagrams in seawater;(b)Bode diagrams in seawater without bacteria;(c)Bode diagrams in seawater with bacteria;(d)Nyquist diagrams in estuary water(e)Bode diagrams in estuary water without bacteria;(f)Bode diagrams in estuary water with bacteria
采用ZSIMPWIN軟件對紫銅體系的阻抗譜進行擬合,可得出最佳等效電路如圖6,圖中Rs是從參比電極的魯金毛細管口到被研究電極之間的溶液電阻;Rt為銅表面膜層的電阻;Qt為銅表面膜層的常相位角元件;Ct為銅表面膜層電容;Rp為極化電阻;Cp為雙電層電容;Qp為雙電層的常相位角元件;Zw為由擴散過程引起的法拉第阻抗。圖6中所示的等效電路各參數的擬合值如表3所示。
圖5(a)~(c)為紫銅分別在無菌海水和有菌海水中浸泡30h后的阻抗譜。從圖5(a)可看出紫銅有菌海水中的容抗弧半徑小于在無菌海水的,說明細菌的存在降低紫銅在海水的阻抗模值;而且有菌海水的紫銅極在低頻段呈現典型的Warburg阻抗特征,表明在有菌海水中的紫銅腐蝕行為同時受電化學和濃差極化控制。由圖5(b)和圖5(c)的波特圖中的相位角ψ-頻率f曲線可知,紫銅在有菌海水和無菌海水浸泡30h都只有一個時間常數。在鹽度較高的海水中的無菌條件下,從表3的元件參數可知紫銅極表面膜的Rt電阻很大(4412Ω/cm2),說明試樣表面形成了較為完整的阻擋膜,對基體起到了保護作用;同時極化電阻Rp也較大(6188Ω/cm2),表明在腐蝕過程中銅發生溶解反應受到的阻滯也較大。當海水中富集細菌時,由于細菌生命活動造成銅極表面膜發生局部溶解或破裂,使得表面膜的形成了局部的缺陷,表面孔隙率上升,導致銅極表面膜電阻Rt急劇變小;活化極化電阻Rp也由于細菌作用而變小,加快了腐蝕反應速率;從表面氧化膜層的常相位角元件參數Qt值來看,由于材料表面附著疏松不均勻生物膜,導致銅極表面形成許多微小凹坑,從而使得銅極表面的比面積增大,故細菌導致銅表面的介電常數Qt增大。由于細菌導致腐蝕加速,生物膜的形成導致銅電極表面附近的反應物的濃度與溶液本體的濃度有明顯的差別,形成了濃差極化,因此說明在低頻部分,擴散控制將超過電化學活化控制,出現Warburg阻抗這個擴散過程。

圖6 紫銅浸泡30h后電極的等效電路 (a)無菌海水;(b)有菌海水;(c)無菌咸淡水;(d)有菌咸淡水Fig.6 Equivalent circuit models for electrodes in different mediums (a)seawater without bacteria;(b)seawater with bacteria;(c)estuary water without bacteria;(d)estuary water with bacteria
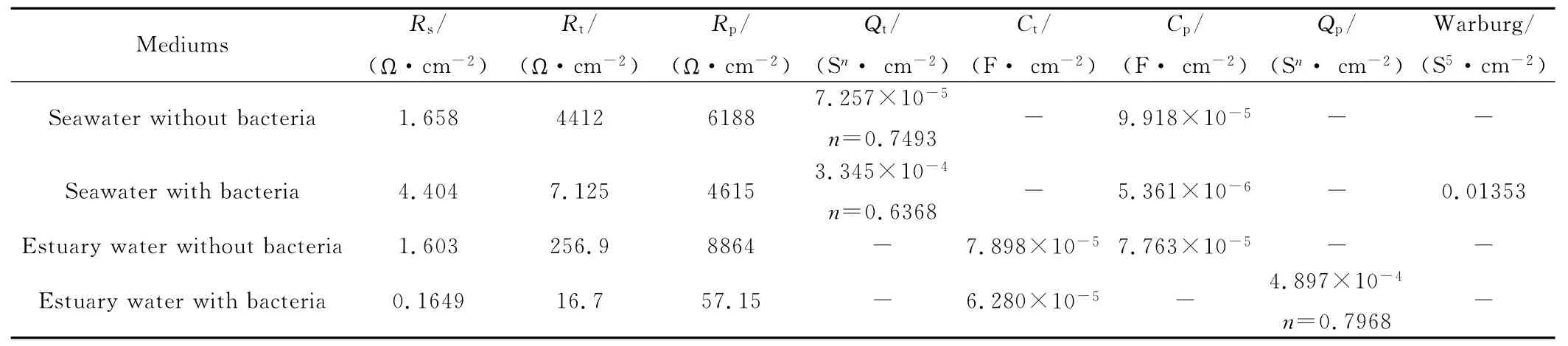
表3 等效電路中各參數擬合值Table 3 Fitted values of the parameter in the equivalent circuit models
圖5(d)為紫銅在無菌咸淡水的Nyquist,在復平面上都呈單一的容抗弧特征,紫銅在帶菌咸淡水中的容抗弧半徑遠遠小于在無菌咸淡水的容抗弧半徑。其中圖5(e)的波特圖的相位角ψ-頻率f曲線出現了雙峰,表明在無菌咸淡水中浸泡30h時有兩個時間常數,這兩個時間常數,一個與銅極氧化膜的電阻、電容有關,另一個與低頻端紫銅的腐蝕性反應電阻及雙電層電容有關,其等效電路如圖6(c)。圖5(f)為紫銅在有菌咸淡水的波特圖,在Nyquist和Bode圖中可知具有一個時間常數的單一容抗弧,而且這段圓弧的圓心在第4象限,因此電極與溶液之間界面的雙電層并非純電容,而是具有“彌散效應”的常相位角元件Qp,其等效電路如圖6(d)。在咸淡水中,紫銅在無菌介質下的阻抗模值遠遠大于有菌介質,擬合后可得各個元件參數如表3所示,其中在咸淡水中由于微生物在材料表面活動消耗氧,產生酶、硫化物[16]等物質,促進了紫銅表面局部溶解,顯著降低Rt值。由于在咸淡水體系中沒有出現Warburg阻抗特征,可忽略擴散阻抗,因此極化電阻Rp主要是受控于銅的腐蝕反應速率,從表3可看出,由于細菌的生命活動使Rp變小,表明銅在細菌作用下的發生腐蝕反應速率較快。
3 結論
(1)在海水和咸淡水中,微生物的存在改變了紫銅的電化學過程,降低了紫銅的開路電位,提高了腐蝕電流密度,使得紫銅的熱力學穩定性變差,腐蝕速率加快。
(2)紫銅板上附著的微生物以微彎桿狀菌為主,由于咸淡水中的紫銅板上吸附的微生物較多,使得在鹽度較低的咸淡水中,紫銅耐蝕性變差。
(3)在鹽度不同的海水和咸淡水中,微生物的存在降低了紫銅的極化電阻和表面膜的電阻,從而加速了紫銅的腐蝕進程。在有菌海水中,紫銅腐蝕過程受電化學極化和濃差極化混合控制。
[1]NAKAYAMA S.Mechanistic study by electrochemical impedance spectroscopy on reduction of copper oxides in neutral solutions[J].SEI Technical Review,2009,1343-4349:62-68.
[2]TSAI T H,WU Y F,YEN S C.A study of copper chemical mechanical polishing in urea-hydrogen peroxide slurry by electrochemical impedance spectroscopy [J].Applied Surface Science,2003,214(1-4):120-135.
[3]王宏智,陳君,周建奇,等.紫銅海水管焊接部位在海水中的腐蝕特征[J].中國有色金屬學報,2006,16(4):645-650.WANG Hong-zhi,CHEN Jun,ZHOU Jian-qi,etal.Corrosion characteristics of welded joints of copper pipe in seawater[J].The Chinese Journal of Nonferrous Metals,2006,16(4):645-650.
[4]CLAYTOR R .Investigation to the Susceptibility of Corrosion Resistant Alloys to Biocorrosion[M].USA:Naval Research Laboratory,2004:36-48.
[5]SZAKALOS P.Corrosion of copper by water[J].Electrochemical and Solid-State Letters,2007,10(11):63-67.
[6]SANDBERG J.Corrosion-induced copper runoff from naturally and pre-patinated copper in a marine environment[J].Corrosion Science,2006,48(12):4316-4338.
[7]范工業.防止銅合金熱交換器腐蝕的技術改進[J].全面腐蝕控制,2006,20(5):42-44.FAN Gong-ye.The technical improvement to prevent copper alloy heat exchanger corrosion[J].Total Corrosion Control,2006,20(5):42-44.
[8]姜英,王衛國,郭紅.同步改善黃銅H68晶界腐蝕行為和力學性能[J].中國有色金屬學報,2011,21(2):377-383.JIANG Ying,WANG Wei-guo,GUO Hong.Improvements of intergranular corrosion resistance and mechanical properties of brass[J].The Chinese Journal of Nonferrous Metals,2011,21(2):377-383.
[9]段冶,李松梅,杜娟,等.Q235鋼在假單胞菌和鐵細菌混合作用下的腐蝕行為[J].物理化學學報,2010,26(12):3203-3211.DUAN Ye,LI Song-mei,DU Juan,etal.Corrosion behavior of Q235steel in the presence of pseudomonas and iron bacteria[J].Acta Phys-Chim Sin,2010,26(12):3203-3211.
[10]SHENG Xiao-xia.Evaluation of an organic corrosion inhibitor on abiotic corrosion and microbiologically influenced corrosion of mild steel[J].Industrial and Engineering Chemistry Research,2007,46(22):7117-7125.
[11]LEE A K,BUEHLER M G,NEWMAN D K.Influence of a dual-species biofilm on the corrosion of mild steel[J].Corros Sci,2006,48:165-178.
[12]YUAN S J,PEHKONEN S O.Microbiologically influenced corrosion of 304stainless steel by aerobic pseudomonas NCIMB2021bacteria:AFM and XPS study[J].Collids and Surfaces B:Bionterfaces,2007,59(1):87-99.
[13]ABRAHAM G J,KAIN V,DEY G K.MIC failure of cupronickel condenser tube in fresh water application[J].Engineering Failure Analysis,2009,16(3):934-943.
[14]孫秋霞.材料腐蝕與防護[M].北京:冶金工業出版社,2001.34-59.
[15]曹楚南,張鑒清.電化學阻抗譜導論[M].北京:科學出版社,2002.7.
[16]IWONA B B,Corrosion of technical materials in the presence of biofilms-current understanding and state-of-the-art methods of study[J].Intern Biodeter Biodegrad,2004,53:177-183.

