5株發酵劑對熏馬腸成熟過程中內源菌的影響*
李蕊婷,盧士玲,李開雄,馬宇霞,鄧紅梅
(石河子大學食品學院,新疆石河子,832000)
目前,肉制品的發酵劑研究在我國屬于一個比較熱門的領域。在肉制品成熟的過程中添加合適的發酵劑,對實現發酵肉工業化生產,縮短產品成熟期,對使產品特征標準化和安全化將起重要的作用[1]。但是隨著肉制品的發酵和成熟,其內源菌群不斷變化,加入不同的發酵劑可能對內源菌群產生一定影響(拮抗或協同)。本研究在不采取化學添加物的前提下,在熏馬腸生產過程中添加有抑菌作用并可產生物胺氧化酶的菌株作發酵劑,以不同的添加組合,采用PCR-DGGE技術研究發酵劑對內源微生物在熏馬腸發酵和成熟過程中動態變化的影響,為熏馬腸安全生產提供技術支持。
1 材料與主要試劑
1.1 試驗材料
馬肉及其他輔料均購自石河子愛家超市。
發酵劑:本實驗室分離提取到的4株葡萄球菌和1株植物乳桿菌(Staphylococcus epidermidis;Staphylococcussimulans.001;Staphylococcussimulans.002;Staphylococcus simulans.003;Lactobacillus plantarum)注:Staphylococcus simulans有3個不同種,分別編號為 001、002、003。
1.2 主要儀器和試劑
恒溫恒濕培養箱,德國 BINDER公司;灌腸機(MM12型絞肉機);海爾冰箱;電子天平;高速離心機;小型離心機(Anke TLG-16G);超凈工作臺(SWCF-1F);PCR儀,美國 Bio-Rad公司;DGGE電泳儀,美國Bio-Rad公司;凝膠成像儀(GelDoc 2000 system Bio-Rad,美國);微型振蕩器;海爾控溫冰箱;Eppendorf移液槍(1 ~10μL、1 ~20 μL、20 ~ 200 μL、10 ~1 000 μL)。
細菌總DNA提取試劑盒(天根);溶菌酶(sigma);PCR相關試劑盒,MarkⅢ,去離子水,丙烯酰胺,甲叉雙丙烯酰胺(Sigma),尿素(Sigma),TRIS(Sigma),EDTA-2Na(Sigma),TE(Sigma),過硫酸銨(Sigma),SYBR Green I(Bio-V)。
2 試驗內容及方法
2.1 熏馬腸基本加工工藝
原料肉進行處理,將肥膘(20%)切丁進行漂洗(40℃),瘦肉(80%)絞肉,混合腌制接種發酵劑;灌入腸衣發酵2 d,(發酵條件:18 ±0.5℃,RH 90% ~95%);成熟過程控制不同條件3~4 d[(14±0.5)℃,RH 80% ~85%],5 ~7 d[(12 ± 0.5)℃,RH 75% ~80%],8 ~28 d[(10 ± 0.5)℃,RH 70% ~75%]。
2.2 試驗設計
按照熏馬腸的加工工藝,利用分離純化得到的4株葡萄球菌及1株植物乳桿菌,制作9種不同類型熏馬腸(見表1),其中發酵劑的接種量為107CFU/g,復合發酵劑以1∶1添加。在熏馬腸的發酵和成熟的過程中,分別對 9 組熏馬腸 A、B、C、D、E、F、G、H、I于0、2、7、14、28 d 進行無菌取樣并冷凍保藏,分別對其進行菌相測定。

表1 接種不同發酵劑類型的熏馬腸Table 1 The smoked horsemeat sausage of inoculating with different starter culture
2.3 實驗方法
2.3.1 細菌總DNA的提取
取待測樣品20g于180 mL生理鹽水中,搖床振蕩30 min;4 000重力加速度的條件下4℃離心10 min;再取上清液1 mL于1.5 mL離心管在10 000重力加速度條件下4℃離心10 min,棄去上清液,反復幾次。參照DNA提取試劑盒(天根)的說明,提取樣品總細菌的DNA。所提取的DNA溶于TE緩沖液,經1.0%的瓊脂糖凝膠電泳檢測后,于-20℃條件下貯藏以備PCR擴增使用。
2.3.2 PCR擴增
所選用的引物為[2]:上游引物為帶GC夾子的U968(5'-CGC CCG GGG CGC GCC CCG GGC GGG GCG GGG GCA CGG GGG GAA CGC GAA GAA CCT TAC-3'),下游引物為 L1401(5'-CGG TGT GTA CAA GAC CC-3')。對細菌的16S rDNA的 V6-V8區段進行PCR擴增,擴增出的片段為400bp。
PCR 反應為25 μL體系:包括1μL模板DNA,上游引物和下游引物各0.5μL,HS MIX(東盛)12.5μL,無菌水10.5μL。
PCR反應程序:95℃預變性10 min,35個循環(95℃變性30s;56℃退火30s;72℃延伸30s),最終72℃延伸5 min。PCR產物經1.0%瓊脂糖凝膠電泳檢測后,-20℃冰箱保存以備DGGE使用。
2.3.3 變性梯度凝膠電泳(DGGE)
DGGE采用Bio-rad電泳儀,聚丙烯酰胺凝膠濃度為8%(丙烯酰胺:甲叉雙丙烯酰胺37.5:1)。變性梯度為40%~60%(40%變性劑凝膠溶液:9.6 mL 0%變性劑+14.4 mL 100%變性劑 +50μL 20%APS溶液+5μL TEMED;60%變性劑凝膠溶液:14.4 mL 0%變性劑 +9.6 mL 100%變性劑 +50μL 20%APS溶液 +5μL TEMED),濃縮膠為:6 mL 0%變性劑 +30μL 20%APS溶液 +6μL TEMED。在 pH 為7.4的1×TAE緩沖液中,將PCR產物加入膠孔,溫度設定為60℃,然后開始電泳,電泳條件為:200V電壓預跑10 min,之后85V電壓16 h。
2.3.4 SYBR Green I染色
待電泳結束后,小心取下膠片,放入50 mL pH為7.0~8.5的1×TAE(含5μL SYBR Green I)中室溫避光振蕩染色30 min,之后再將膠片放入超純水中漂洗幾次。
2.3.5 凝膠成像及DNA的回收
待染色后,小心地將DGGE膠片轉移到凝膠成像系統下拍照并割膠(要盡快操作,否則在紫外光的作用下,很快圖像的效果就會降低),圖像分析采用Quantity one軟件。割膠回收是用無菌手術刀切下DGGE膠上相應位置的條帶,分別放入已經滅菌的1.5 mL離心管里,加入20μL無菌的TE溶液,置于4℃條件下過夜以備DNA測序的使用。
2.3.6 DNA的測序
取2μL回收的DNA為模板進行16S rDNA的V6-V8區域擴增,細菌上游引物為U968(5'-AAC GCG AAG AAC CTT AC-3'),下游引物 L1401(5'-CGG TGT GTA CAA GAC CC-3'),PCR 擴增程序同2.3.2。擴增后的PCR產物經1.0%瓊脂糖凝膠電泳檢驗,條帶的位置在400bp就可以證明該回收DNA的存在,之后將剩余PCR產物送到華大基因測序,登錄NCBI將所得序列與數據庫中已知序列進行相似性比對[3]。
3 結果與分析
3.1 細菌總DNA提取結果
選取9組不同處理的樣品,分別在其成熟過程中第0,2,7,14,28天的取樣。用細菌總 DNA 提取試劑盒,對樣品進行無菌操作并提取樣品中的總DNA,之后將溶于TE緩沖液的DNA經1.0%瓊脂糖電泳檢測,得到明顯的條帶,說明在實驗過程中對樣品的細菌總DNA提取效果很好,提取方法合適,所得到總DNA適合后續PCR擴增實驗。
3.2 細菌的16S rDNA PCR擴增
以不同處理的熏馬腸細菌總DNA為模板,用引物GC-U968和L1401對16S rDNA的V6-V8可變區進行PCR擴增,擴增產物經1.0%瓊脂糖電泳檢測,獲得約400bp的特異性片段,所有樣品均有較亮的擴增條帶,說明本實驗的PCR擴增條件是適合的,可以滿足后續DGGE電泳分析實驗的條件。
3.3 熏馬腸成熟過程中細菌DGGE圖譜主要條帶的DNA序列相似性比較
由圖1和圖2可看出,因2張圖中均有對照組A,將2張圖片進行位置比對后,發現圖2中條帶在圖1中有相互對應的條帶。DGGE指紋圖上的1個條帶就代表1個微生物類群,因此,圖2中部分條帶割膠后沒有進行測序。經比對后,對應的位置為:m1→M1,m2→M2,m3→M3,m4→M6,m6→M8,m7→M9,m8→M10,m10→M11,m11→M13,m12→M14,m13→M15。其他 M4,M5,M7,M12,m5,m9 沒有相對應的條帶。
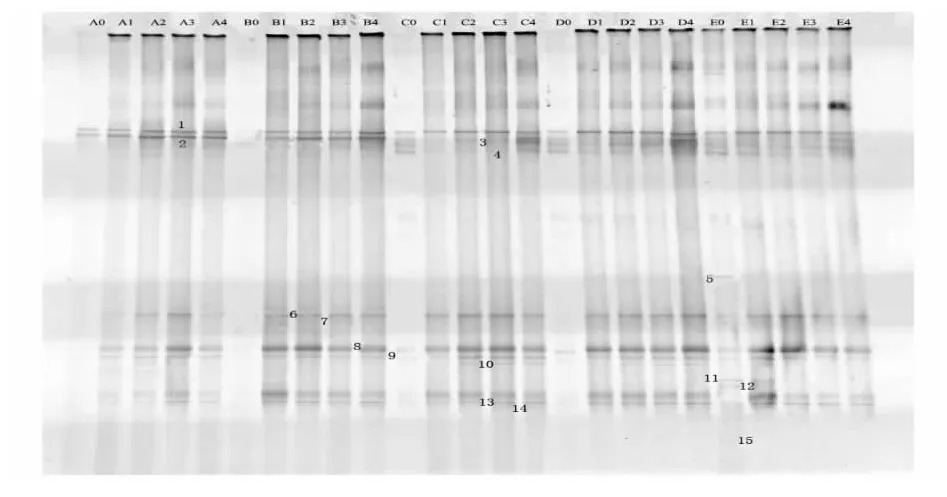
圖1 熏馬腸成熟過程中細菌PCR-DGGE圖譜Fig.1 DGGE fingerprinting of PCR products of smoked horsemeat sausage during ripening
3.4 細菌DGGE圖譜主要條帶的DNA序列分析
通過PCR-DGGE電泳照相后,把條帶割膠用不帶GC夾子的引物擴增序列(同2.3.6)后,其中m9和M12于條帶太弱,菌活力弱,菌液中濃度過低,沒有測出相應的序列,其余可進行后續分析。將測序結果與Gene bank數據庫中序列進行比對,確定結果(見表2)。

圖2 熏馬腸成熟過程中細菌PCR-DGGE圖譜Fig.2 DGGE fingerprinting of PCR products of smoked horsemeat sausage during ripening
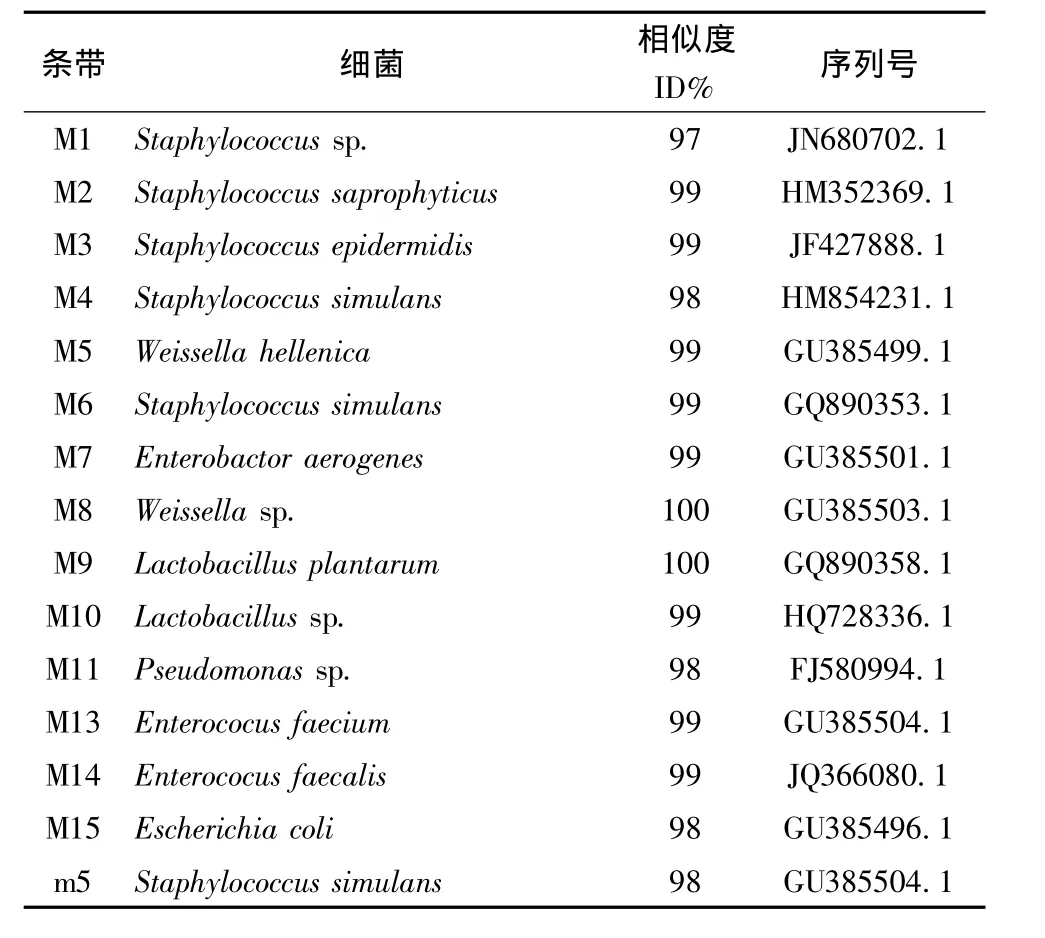
表2 熏馬腸成熟過程中細菌PCR-DGGE圖譜上條帶系列分析(圖1中的條帶)Table 2 Identities of bands obtained from DGGE analysis of bactrial communities in smoked horsemeat sausage during ripening(bands obtained from Fig.1)
4 討論
如圖1、圖2可看出,空白組第14天的菌相最豐富,且數量最大,第0天使M1、M2數量多,其他的菌濃度都低。第2天時,隨著發酵時間的增長,菌相開始豐富,M6、M7、M8、M9、M10 均出現。第 7 天時,種類基本無變化,數量增多。第14天時,M10消失,出現M13、M14。第28天時,菌數量減少,菌群達到動態穩定狀態,M1、M2為自然發酵劑,且一直是優勢菌種,幾乎不受添加發酵劑的影響。M9為植物乳桿菌,在C、E、G、I四組復合添加植物乳桿菌中,數量比不復合的相應組數量要多,同時其他條帶的亮度也都降低,說明此株植物乳桿菌能夠在一定程度上抑制內源菌的生長。
B組和C組中,M3、M9為發酵劑,B組中M3隨著發酵時間的增加越來越少,C組中M3增強,2組中的M9數量越來越大。與空白組對照,增加了內源菌的生長;D組和E組中,M4、M9為加入的發酵劑,D組中M4一直未變,M9逐步增多,內源菌增多。E組中M4越來越少,M9到第2天時增多后又下降。E組的發酵劑的內源菌的數量減少,種類變多;F組和G組中,m4、m7為發酵劑,2組的M7都逐漸增多,F組中的m4增大到28 d時降低且穩定,G組的m4持續增多。內源菌的種類和數量都降低;H組和I組中,m5、m7為發酵劑,m5在0 d時出現,后被抑制。m7越來越多,發酵結束后并沒有明顯影響內源菌的種類和數量。
在熏馬腸中,實際菌相可能比檢測到的更加復雜,存在一些在本研究過程中沒有檢測到的其他屬菌或乳酸菌、腸細菌、微球菌和假單胞菌屬中的其他種類。在很多相關的報道中,對主要腐敗菌進行初步分離和鑒定,發現假單胞菌(Pseudomonas sp.)是主要的腐敗優勢菌之一[4-5]。有研究表明,當該種微生物占整個微生物種群數小于1%時,DGGE將檢測不到該種微生物的存在[6]。
研究表明,糞腸球菌、屎腸球菌、陰溝腸桿菌、大腸埃希氏菌和產氣腸桿菌可產生大量的生物胺[7],一些乳酸菌也可產生生物胺[8],控制它們的生長能夠更好的保障發酵香腸的品質。Cocolin等人[9]將DGGE用于自然發酵意大利香腸成熟過程中菌相的分析,實驗結果表明乳酸菌是其香腸發酵過程中的優勢菌,其中 Lactobacillus sake和 Lactobacillus curvatus對產品的酸化和蛋白質的水解有重要作用,決定了發酵香腸的感官質量。在本研究中,Weissella sp.是優勢菌,但Weissella sp.不產生物胺已經得到證實[10];微球菌屬中的一些菌也能產生生物胺,但產生物胺的能力極其有限[11],它們的存在對香腸的品質影響不明顯。
5 結論
本研究采用傳統PCR-DGGE的方法揭示了熏馬腸成熟過程中優勢菌相的變化。結果表明,添加不同發酵劑的熏馬腸菌相分布呈現不同變化,但是隨著成熟時間的變化,優勢菌趨于明顯。添加發酵劑所有組合對內源菌Escherichia coli有較強的抑制作用;腐敗菌條帶 M8,M10,M13,M14從成熟初期到結束一直存在,添加發酵劑所有組合對內源菌Escherichia coli有較強的抑制作用;其中C,D,E組中細菌種類在發酵初期較多,但到發酵結束時,其菌含量下降,尤其對內源菌 Pseudomonas sp.,Staphylococcus carnosus和Staphylococcus xylosus有較強抑制作用;G組中內源的Pseudomonas sp.一直存在;與E組對應的添加單一發酵劑的D組在發酵初期并沒有E組的微生物種類多,但其抑菌效果較好;內源的Weissella sp.和Staphylococcus sp.在成熟過程中一直存在,不受發酵劑的抑制,但Weissella sp.不產生物胺。F組在28 d發酵結束時,菌群的種類和數量為最低,抑菌效果最好。
[1] 賈士芳,陳美玲,鐘瑾,等.肉制品發酵劑木糖葡萄球菌I2的研究[J].食品與發酵工業,2006,32(8):72-74.
[2] Ercolini D.PCR-DGGE fingerprinting:novel strategies for detection of microbes in food[J].Journal of Microbiological Methods,2004,56(3):297-314.
[3] Altschul S F,Madden T L,Schaffer A A,et al.Gapped BLAST and PSIBLAST:a new generation of protein database search programs [J].Nucleic Acidas Research,1997,25(17):3 389-3 402.
[4] Ols son C,Ahrné S,Pettersson B,et al.The bacterial flora of fresh and chill-stored pork:analysis by cloning and sequencing of 16S rRNA genes[J].International Journal of Food Microbiology,2003,83(3):245-252.
[5] Gill C O,Dus sault F,Holley R A A,et al.Evaluation of the hygienic perform ances of the processes for cleaning,dressing and cooling pig carcasses at eight packing plants[J].International Journal of Food Microbiology,2000,58(1-2):65-72.
[6] Muyzer G,E C de Waa,Uitterlinden A G.Profiling of comples microbial population by denaturing gradient gel electrophoresis analysis of polymerase chain reaction-amplified genes coding for 16S rDNA[J].Appl Environ Microbial,1993,59(3):695-700.
[7] 盧士玲,樊慶魯,李開雄.豬肉自然發酵香腸中細菌和乳酸菌對生物胺積累的作用[J].食品研究與開發,2006,27(2):37-40.
[8] Montel M C,F.M,R.T.Comparison of biogenic amine content in traditional and industrial French dry sausages[J].Sciences des Aliments,1999,19(2):247-254.
[9] Cocolin L,Manzano M,Cantoni C,et al.Denaturing gradient gel electrophoresis analysis of the 16S rRNA gene V1 region to Monitor dynamic changes in the bacterial population during fermentation of Italian sausages[J].Appl Environ Microbiol,2001,67(11):5 113-5 121.
[10] Bover-Cid S,Holzapfel W H.Improved screening procedure for biogenic amines production by lactic acid bacteria[J].International Journal of Food Microbiology,1999,53(1):33-41.
[11] Martuscelli M,Gardini F,Torriani S,et al.Production of biogenic amines during the ripening of Pecorino Abruzzese cheese[J].International Dairy Journal,2005,15(6-9):571-578.

