藻藍蛋白分離純化技術及其影響因素分析*
趙靜,祁巖,王月華,馮敘橋
1(渤海大學食品科學研究院,遼寧省食品安全重點實驗室,遼寧錦州,121013)
2(美國加州大學戴維斯分校環境毒理系,美國加州戴維斯市,95616)
3(美國伊利諾伊理工大學食品安全與健康學院,美國伊利諾伊州芝加哥市,60616)
4(沈陽農業大學食品學院,遼寧 沈陽,110866)
藻膽蛋白是藻類特有的捕光色素蛋白,主要可以分為藻紅蛋白、藻藍蛋白、別藻藍蛋白和藻紅藍蛋白。藻藍蛋白(phycocyanin,PC)是一種深藍色粉末,它既是蛋白質又是良好的天然食用色素,多見于螺旋藻[1]、魚腥藻[2]、地木耳[3]中,其中螺旋藻細胞中的蛋白質含量豐富,PC占總蛋白質的7%左右[4]。
PC具有抗癌、抗氧化、治療腦缺血損傷、提高機體免疫力等多種生理功能,有關PC的研究已經成為天然海洋藥物的研究熱點[5]。PC的提取分離技術也成為時下人們所關注的問題之一。本文對近年來涌現出的PC提取和分離技術以及影響其分離純化的因素加以整合,并進行了論述。
1 PC的分離純化技術
傳統的PC分離提純技術一般通過超聲、反復凍融、酶解和高壓均質等方法使細胞裂解獲得PC粗提液,之后將(NH4)2SO4沉淀法與多種色譜層析法結合使用[6],從而達到分離純化的目的。此類方法存在步驟繁瑣、蛋白質損失量較大、難以規模化推廣,且高于50%的生產成本用在純化的過程中[7]等缺點。為解決PC純度問題,近幾十年來出現了一系列分離純化PC的技術,其主要目標是為了改善PC的品質,它們的分離提純工藝大致相同,但卻在分離提純時間、成本、回收率、純度等方面各有所長。目前,PC常用的分離純化技術有鹽析、雙水相萃取、反膠團萃取、柱層析等幾種,下面分別對每種方法的特點進行介紹。
1.1 多步鹽析
鹽析(salting out)是現今蛋白質分離純化中較常用的方法,主要通過向蛋白質溶液中加入濃的無機鹽溶液[如(NH4)2SO4或Na2SO4溶液],進而使蛋白質凝聚而析出。鹽析是一個可逆的過程,不會影響蛋白質本身特有的性質。隨著蛋白質分離技術的不斷發展,研究人員對鹽析方法有了新的改良,使之成為更適用于PC提純的方法。
王巍杰等[8]以鈍頂螺旋藻為材料,對多步鹽析分離純化進行了研究。他們采用反復凍融的方法將藻體細胞破碎,并將獲得的PC粗體液依次進行兩步鹽析、四步鹽析、六步鹽析和多步鹽析,進而分析鹽析次數對PC回收率和純度的影響。兩步鹽析即將PC粗體液分別置于 15%、20%、25%、30%的 4個(NH4)2SO4飽和梯度組中,4℃靜置12 h后離心,取上清液,各組飽和度分別追加至45%、50%、55%、60%,在 4℃溫度下靜置 12 h,離心,沉淀用 PBS(0.01 mol/L 磷酸鹽緩沖液,pH=7,含 0.002 mol/L EDTA,簡稱PBS)溶解后測其吸光度,計算兩步鹽析后PC回收率和純度。四步鹽析即將二步鹽析得到的粗體液分別置于 5%、10%、15% 的 3個(NH4)2SO4飽和梯度組中,4℃下靜置12 h,離心,取上清,各組飽和度分別追加至33%、35%、37%,4℃靜置12 h,離心,沉淀用PBS溶解后測其吸光度,計算四步鹽析后PC的回收率和純度。六步鹽析即將四步鹽析得到的粗體液分別置于20%、23%、25%、27% 的4個(NH4)2SO4飽和梯度組中,4℃靜置12 h,離心,取上清液,各組飽和度分別追加至30%、35%、40%、45%,4℃靜置12 h,離心,沉淀用PBS溶解后測其吸光度,計算六步鹽析后PC的回收率和純度。多次鹽析即將六步鹽析得到的上清液,加入(NH4)2SO4使其飽和度達到23%,4℃靜置12 h,離心,上清液飽和度追加至35%,4℃靜置12 h,離心,沉淀用PBS溶解后測其吸光度,如此反復多次。通過對比二步鹽析、四步鹽析、六步鹽析以及多次鹽析(NH4)2SO4飽和度對PC純度和回收率的影響,可分析得知多次分段鹽析的回收率雖然僅有9.66%,但PC 純度高達3.92。
一般的鹽析方法主要是先用(NH4)2SO4等鹽類使PC析出,而后再利用層析等方法分離提純蛋白質,步驟繁瑣,而多步鹽析法通過多次的分離而達到提純目的,更加簡易方便。
1.2 雙水相萃取法
雙水相萃取技術(aqueous two-phase extraction,ATPE),又稱水溶液兩相分配技術(partion of two aqueous phase extraction)[9],其原理主要是:在一定濃度下,2種水溶性不同的聚合物或者一種聚合物和無機鹽的混合溶液體系會自然分成互不相容的兩相,形成雙水相體系,被分離物質進入雙水相體系后,在表面性質、電荷間作用和各種作用力(疏水鍵、氫鍵和離子鍵)等因素的影響下,兩相間的分配系數不同,導致上下相的濃度不同而達到分離的目的[10]。雙水相萃取是一種新型的生物分離技術[11],可用于PC的分離提純。
劉楊等[12]采用反復凍融的方法將鈍頂螺旋藻藻體破碎后,將獲得的PC粗提液加入一定量的聚乙二醇(polyethylene glycol,PEG)和無機鹽中,充分振蕩使成相物質溶解,完成了PC在雙水相系統中的分配過程。此雙水相系統靜置一定時間,當兩相達到相分離后,分別抽取上下相的溶液,在波長280、620、650 nm下測吸光度,計算PC的質量濃度和純度。結果發現,試驗中雙水相萃取分離得到的PC純度為2.1,比采用鹽析沉淀與層析分離相結合方法分離出的PC純度低 3.4,但其操作簡便[13]。
對比鹽析的過程,雙水相萃取法不僅節省了分離提純的時間,簡化了操作步驟,而且處理條件較為溫和,可較好地保持蛋白質的活性[14-15]。然而,相比只考慮鹽溶液的鹽析過程來說,雙水相萃取提純PC需要考慮聚合物的濃度、種類、平均分子質量等因素,對于環境的要求較為苛刻。
1.3 鹽析結合雙水相萃取提取純化法
鹽析結合雙水相萃取法(salting out combined two-aqueous phase extraction)是劉清新等[16]研究出的一種采用鹽析和雙水相萃取相結合的新型方法。此方法先用飽和度為35% ~75%的(NH4)2SO4溶液沉淀PC,再用飽和度為10% ~30%的(NH4)2SO4除去螺旋藻雜蛋白,而后在雙水相系統中采用8%PEG 4000、16%檸檬酸鈉和4%KCl分離純化鹽析后的PC。即先進行(NH4)2SO4的反復梯度鹽析,而后將反復鹽析后的PC溶液置于雙水相系統中,達到分離提純的目的。結果證明,經鹽析結合雙水相萃取提取純化后的PC純度可達4.0。
此方法結合了2種分離提純PC的方法,雖然步驟較為繁雜,耗時較長,同時要兼顧影響2種方法的因子,但它大大提高了蛋白質的純度,同時也為運用多種方法分離蛋白質提供了一個先例。
1.4 反膠團萃取法
反膠團萃取(reversed micellar extraction)是近年來一種新型的蛋白質分離提純方法,它是利用表面活性劑在有機相中形成的反膠團(reversed micelles)形成分散的親水微環境,從而使生物分子在有機相(萃取相)內存在于反膠團親水微環境中,解決了蛋白質類生物活性物質難溶解于有機相中或在有機相中發生不可逆變性的問題。由于此方法選擇性高、萃取過程簡單[17],可有效保護蛋白質大分子,因此成為提取PC的新型方法之一。
甘林火等[3]將地木耳細胞分離獲PC粗提液,同時將配制好的陽離子十六烷基三甲基溴化銨(cetyl trimethyl ammonium bromide,CTAB)反膠團溶液與粗提液充分混合、靜置分層,將油水兩相分離(油相為反膠團萃取液),抽取上相(油相)溶液并測定其PC含量,向油相中加入不同pH值的無機鹽KBr溶液,使兩相充分混合,PC達到分配平衡。再次靜置分層,將油水兩相分離,水相為反膠團反萃取液,抽取下相(水相)溶液并測定其PC含量。最終得到了最佳分離條件為0.05 mol/L CTAB/正己醇-正辛烷(體積比1∶4)的反膠團體系用于萃取pH=7.0的地木耳細胞破碎液,PC萃取率可達98.1%,分配系數達到50.7;采用 pH=4.0、3 mol/L KBr反萃液反萃取 PC,反萃率可達98.5%,其純度可達16.8。
劉楊等[18]將加入磷酸緩沖液的螺旋藻粉采用反復凍融技術破碎藻體細胞,獲得藻膽蛋白粗提液,并與CTAB反膠團溶液混合后離心,反復提取水相溶液,在568、620和650 nm下測吸光度,計算PC的含量。此外,劉楊等還分析了鹽離子種類和濃度等對萃取效果的影響。
利用反膠團萃取法提純PC可以有效地防止其變性,蛋白質的純度也遠遠超過4.0,純度大幅度提高,此類方法可適用于對蛋白質純度要求較高的醫療行業。
1.5 殼聚糖親和沉淀-活性炭吸附-DEAE Sephadex A-25柱層析法
針對傳統PC純化能耗高、損失大、耗時長等缺點,廖曉霞[6]等探究出了殼聚糖親和沉淀-活性炭吸附-DEAE Sephadex A-25柱層析(chitosan affinity precipitation-activated carbon adsorption-DEAE Sephadex A-25 column chromatography)三步法分離純化PC方法(圖1)。通過分析殼聚糖親和沉淀條件,活性炭吸附,DEAE Sephadex A-25凝膠層析洗脫曲線以及PC的光譜特性,得出向PC粗提液中加入0.29%殼聚糖,調節pH值至6.9,攪拌5 min后,離心棄沉淀,向上清液中加入80 g/L活性炭吸附5 min,離心、超濾濃縮上清液,采用DEAE Sephadex A-25柱層析法,用10 mmol/L 磷酸鉀緩沖液(pH 6.8)+0.1 ~0.3 mol/L NaCl梯度洗脫得純度達到4.3的PC。
此方法所需材料成本低、考慮因素較少、條件溫和、不易使蛋白質變性,可適用于工業化大生產,然而相比反膠團萃取法提純蛋白質,其蛋白質純度較低。
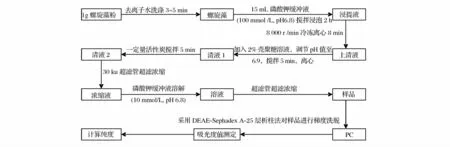
圖1 殼聚糖親和沉淀-活性炭吸附-DEAE Sephadex A-25柱層析法提純PC工藝流程Fig.1 Process of phycocyanin purification by chitosan affinity precipitation-activated carbon adsorption-DEAE Sephadex A-25column chromatography
1.6 離子交換色譜與疏水間相互作用色譜結合法
離子交換色譜與疏水間相互作用色譜結合法(combined ion exchange chromatography and hydrophobic interaction chromatography)是將提取后的PC先后經過離子交換色譜法、疏水間相互作用色譜法來進一步純化PC。Santiago-Santos等[19]將從稻田中分離的絲狀藍藻,經一定條件培養后離心分離,沉淀懸浮于10 mL 0.1 mol/L、pH=7 磷酸鹽緩沖液中(含有 13.6 mmol/L的EDTA和2 mg單位濕重為2 mg/g溶解酶),懸浮液靜置24.5 h使細胞破碎,經再次離心后獲PC粗提物。粗提物用50 mmol/L pH=7.5 Tris-HCl緩沖液(經過PD10柱)平衡,使其可以在相同的條件下進行離子交換。進行離子交換色譜時,首先將樣品裝入經50 mmol/L、pH=7.5的Tris-HCl緩沖液平衡后的Q-Sepharose 4快速流動柱中,用14 mL相同的緩沖液洗脫,吸附的蛋白質被10 mL具有線性梯度(0 ~0.6 mol/L)的 NaCl緩沖液(50 mmol/L、pH=7.5的Tris-HCl)洗脫,收集 A620/280檢測后大于1.5的組分與1.3 mol/L的(NH4)2SO4混合,隨后將其裝入用pH=7.5 Tris-HCl緩沖液平衡后的且含有 1.3 mol/L的(NH4)2SO4甲基宏觀準備柱,用30 mmol/L平衡緩沖液洗脫,蛋白質用25 mL含有線性梯度(0 ~1.3 mol/L)的(NH4)2SO4洗脫,收集 A620/280檢測后大于3.5的組分。
此方法在預處理過程中未采用反復凍融法,而是通過生化手段使細胞破碎,通過增加細胞的破碎程度來提高回收率。然而,此方法在預處理方面所需時間較長,純化步驟也較為繁瑣,不適用于工業化大生產。
上述主要介紹了近年來研究的6種PC的分離純化方法,這些方法各有優勢,也各有不足之處(表1)。在考慮實際應用時,需要根據實際情況,例如是否可以工業化生產、純化率、回收率等,選用適當的分離提純方法。
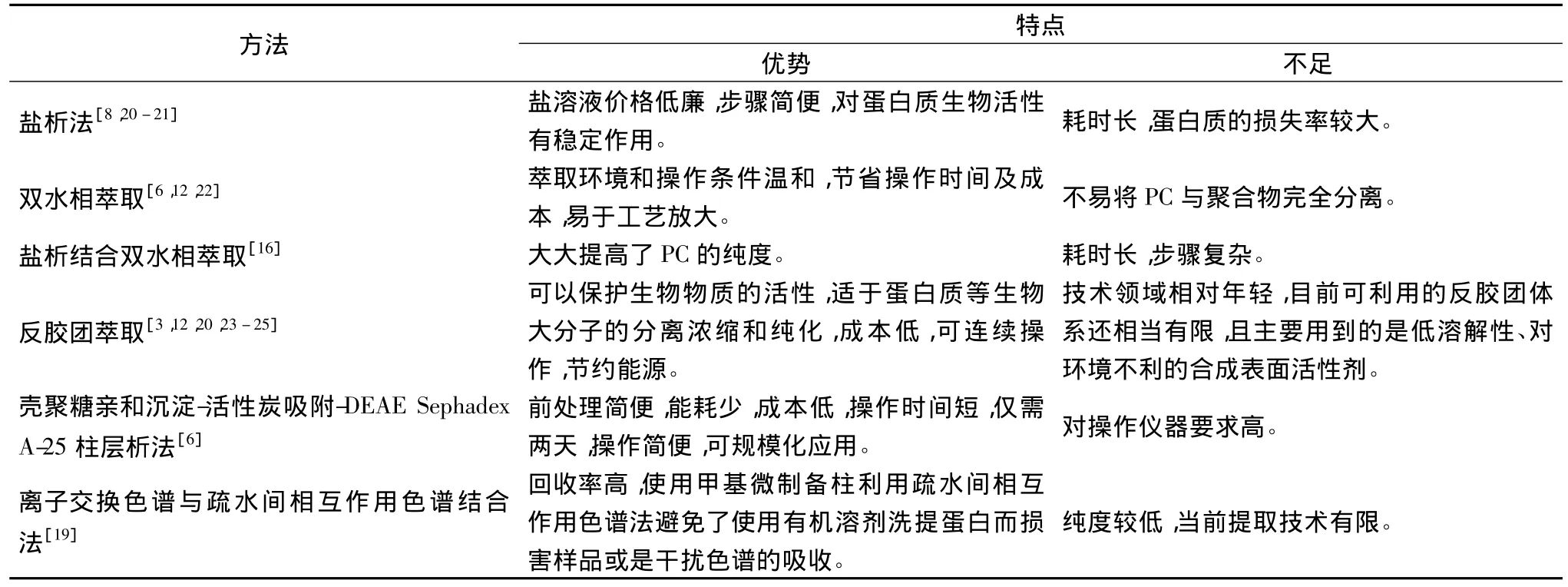
表1 PC分離純化技術方法對比Table 1 Comparison on advantages and disadvantages of phycocyanin separation and purification technologies
2 影響PC分離提純的因素
當選用適當的PC分離提取方法時,為達到盡可能大的回收率、純化率,節省時間,需要考慮各種影響因子(表2),對每個因子的適用條件加以分析,使其達到最優化的程度,進而達到更好的提純效果。
2.1 鹽析次數
此因素主要影響與鹽析過程有關的方法,例如多步鹽析法[8]和鹽析結合雙水相萃取法[16]。王巍杰等[8]在提取PC時進行了多次分段鹽析,分析了鹽析次數對PC回收率和純度的影響。在4次鹽析實驗結果中得出,隨著鹽析次數的增多,PC的回收率降低,但PC的純度呈現出先升后降的趨勢,純度在第3次的鹽析操作中(23%除雜,35%沉淀PC)最高,為3.92,表明增加鹽析次數可在一定程度上提高蛋白質的純度,然而過多次數的鹽析則會適得其反,因此需要經多次試驗找出最適的鹽析次數,使PC純度的達到峰值。
2.2 聚合物平均分子質量
此因素主要影響與雙水相萃取過程有關的方法,例如雙水相萃取法[12]和鹽酸結合雙水相萃取法[16]。PEG的平均分子質量極大程度地影響著雙水相體系的平衡。劉楊等[12]選用了平均分子質量分別為600、1 000、2 000、4 000、6 000,質量分數為 10% 的PEG,觀察溶液的分層情況。結果發現,在PEG分子質量為4 000時,溶液開始出現分層現象。因此,在相同的聚合物和無機鹽濃度下,PEG平均分子質量低的溶液不能形成雙水相體系,PEG分子質量越大,越容易形成雙水相體系,但PEG分子質量過大,不會對PC純度有明顯的提高作用。
2.3 表面活性劑的濃度
此因素主要影響反膠團萃取法的提純效率。劉楊等[18]采用濃度分別為 0.02、0.03、0.04、0.05、0.06 mol/L的CATB陽離子表面活性劑,從PC的萃取現象、萃取率、分配系數、分離因數方面分析表面活性劑濃度對反膠團萃取PC的影響。通過實驗可知,隨著CATB濃度的增加,油水液面變得逐漸清晰,PC的萃取率和分配系數都在逐漸增加,CATB濃度在0.04 mol/L最好,然而分離因數的變化卻不顯著。而且,當CTAB濃度增加到一定程度(高于0.05 mol/L)時,有機相黏度增大的程度會影響油水兩相的分層速度,因此在利用反膠團萃取法萃取PC時,0.04 mol/L為較適合的陽離子活性劑濃度。
2.4 活性炭加入量
該因素主要針對殼聚糖親和沉淀-活性炭吸附-DEAE Sephadex A-25柱層析法對PC的提純效果。廖曉霞等[6]的研究表明,活性炭可用來純化PC。實驗表明,用活性炭處理PC粗提液5 min,即可達到純化PC的目的,但處理時間的過度延長,不但不能進一步提高PC的純度,反而較大程度地影響了PC的得率。為進一步研究出活性炭加入量對藍藻蛋白提純效果的影響,他們采用濃度分別為20、40、60、80、100 g/L的活性炭,分析PC的得率和純度。結果表明,隨著活性炭濃度的增加,PC的得率逐漸降低,純度則呈現一個峰值。因此,在考慮了PC的得率和純度因素后,活性炭的最適濃度選擇為出現純度峰值時所對應的活性炭濃度(80 g/L)。

表2 PC分離提取方法及其主要影響因素Table 2 Main influencing factors of phycocyanin separation and purification technologies
3 現有問題與建議
盡管人們對于PC有了一定的關注,研究人員也研制出了多種提純方法來滿足人們對于PC的需要,但目前我國對PC分離提取方法的研究還不夠完善,主要表現在以下幾點:
(1)現有PC分離提純技術在產品安全方面有待完善。近年來,由于工業廢水造成的環境重金屬污染,例如鉻污染以及水體富營養化造成的有毒藻類污染、微囊藻毒素污染,使藻類原料面臨著重金屬和藍藻毒素污染的風險[27-30],對PC的質量造成威脅。然而,在PC的分離提純中,鮮有去除重金屬、藻類毒素的考量和相關檢驗等工序,這給PC的使用安全性,特別是醫療保健和化妝品等行業,無法提供完全的保障。因此,在將來的PC分離純化技術研究中,要這種解決重金屬和藍藻毒素污染去除的問題。
(2)提取PC時所用的化學試劑得不到較好處理,造成了嚴重的環境污染。例如,在PC的提純過程中研究人員可能用到(NH4)2SO4試劑,如處理不當排入水中,會造成氨氮污染。2009年《中國環境統計年報》顯示,我國廢水中的氨氮排放總量已達122.6萬t,相當于受納水體環境容量的4倍左右。其中化工等以高濃度氨氮廢水為主的8個行業的氨氮排放量占全國工業氨氮排放總量的85.9%。水中氨氮在一定條件下可轉化為亞硝酸鹽,如果長期飲用,水中的亞硝酸鹽將和蛋白質結合成亞硝胺,亞硝胺是一種強致癌物質,嚴重影響人體健康[31]。因此,要特別注意提取技術的應用,不能造成環境水體污染。
(3)現有PC分離純化技術的產品品質不理想。例如,現在常用的多步鹽析法,雖節省操作成本,但回收率卻較低;雙水相萃取法雖然萃取條件溫和,但不易與聚合物分離。由此可見,每一種方法都有其優勢,同時存在不足之處,進而影響提純PC的品質。
針對上述3個方面問題,建議從下述3個途徑加以解決:
(1)研究人員應該注重改善水體中氮、磷的營養結構,抑制有毒藻類的生長方法的研究[31],研究對諸如重金屬和藍藻毒素等易摻入PC中的有害物質的特殊有效的檢測方法,例如高效液相色譜檢測或酶聯免疫吸附檢測[33],以進一步提高PC的純度,保證PC質量安全性。同時,要讓人們正確認識PC的成本與價格的關系,對價格低廉的PC,人們應注意其純度和添加物。
(2)加大對相關化學藥品的回收處理力度,加強對回收化學藥品有效處理方法的研究,嚴禁私自將化學試劑傾倒入河流湖泊,對于工業用或化學用藥品要預先做好方案規劃,進行多部門的綜合監督和多學科參與的研究,避免環境污染和資源浪費[34]。
(3)研究開發新技術,鼓勵研究人員對蛋白質提純方法的創新。可將不同的蛋白質技術提純方法組合,彌補相互缺陷,達到更大地提高蛋白質純度的目的。例如王巍杰等[8]采用多步鹽析法獲得的PC的純度為3.92,而劉清新等[16]采用鹽析結合雙水相萃取法純度可達4.0。
4 展望
PC有著多重作用,它可以作為天然色素,應用于食用工業和化妝品行業中;可以作為醫藥保健用品,起到抗氧化、消炎等功效;也可以因其熒光特性而作為生物學、細胞學等學科的研究試劑,應用前景十分廣闊。此外,我國幅員遼闊,淡水藻類資源豐富,PC生產有著充足的原料來源。然而,僅僅有豐富的資源還不夠,一方面,市場內高純度的PC已被國外壟斷,其售價極高,例如食品級的PC(純度高于0.7)售價達到0.13 US$/mg,分析級的PC(純度高于4.0)售價達到15 US$/mg;另一方面,我國對于PC的研究開發大都處于實驗室水平,其成熟的工藝技術還需要一段時間的研究探索[35-37]。因此,還需要加大分離提純方法的研究力度,從提純技術方法組合、儀器設備使用、環境保護、PC質量安全和PC質量保證[38]等方面盡快研究出既可以提高純度、加大回收率、節省時間,又可以節約成本、適合于工廠化生產的最優化方法。
[1] 尹興娟,唐愛國,劉繼憲,等.藻藍素的提取及其光學性質的研究[J].應用化工,2010,39(4):484-490.
[2] 蘇明星,廖智,劉少華,等.魚腥藻藻藍蛋白的提取·分離純化和抑菌研究[J].安徽農業科學,2012,40(8):4 866-4 918.
[3] 甘林火,翁連進.反膠團萃取分離地木耳中藻藍蛋白[J].化工進展,2010,29(12):2362-2367.
[4] 王勇,錢凱先,董強,等.高純度藻藍蛋白分離純化及光譜特性研究[J].生物化學與生物物理進展,1999,26(5):457-459.
[5] 趙艷景,胡虹,王穎.藻藍蛋白生理活性及作用機制研究進展[J].安徽農業科學,2011,39(11):6 332-6 490.
[6] 廖曉霞,張學武.高效分離純化藻藍蛋白新法[J].食品工業科技,2011,32(6):273-280.
[7] Patil G,Raghavarao K S M S.Aqueous two phase extraction for purification of C-phycocyanin[J].Biochemical Engineering Journal,2007,34:156-164.
[8] 王巍杰,徐長波,程紅燕.鹽析法分離藻藍蛋白的研究[J].食品科技,2010,35(5):238-241.
[9] 郭憲厚.雙水相萃取技術研究進展[J].廣州化工,2008,36(5):17-20.
[10] 戈延茹,曹恒杰.雙水相萃取技術及其在藥物提取分離中的應用近況[J].中國現代應用藥學雜志,2009,26(8):623-627.
[11] 謝藍華,杜冰,張嘉怡,等.雙水相萃取技術在食品工業中的應用研究進展[J].食品與機械,2012,28(5):234-238.
[12] 劉楊,王雪青,龐廣昌,等.雙水相萃取法富集分離螺旋藻藻藍蛋白的研究[J].海洋科學,2008,32(7):30-32,37.
[13] 王廣策,周百成,曾呈奎.鈍頂螺旋藻C-藻藍蛋白和多管藻R-藻紅蛋白的分離及其摩爾消光系數的測定[J].海洋科學,1996,20(1):52-55.
[14] 趙新穎,屈鋒,董敏,等.雙水相萃取結合液相色譜法分離蛋白質[J].分析化學,2012,40(1):38-42.
[15] 于淑坤,岳思軍,田露,等.聚乙二醇-硫酸銨雙水相體系萃取螺旋藻藻藍蛋白的研究[J].食品科技,2012,37(11):249-252.
[16] 劉清新,郭衛芹,王巍杰.鹽析結合雙水相萃取法提取純化藻藍蛋白[J].農業機械,2011,9:122-125.
[17] 李宏,王崇均.蛋白質的反膠團萃取機制及動力學模型研究進展[J].天然產物研究與開發,2011,23:379-383.
[18] 劉楊,王雪青,龐廣昌.反膠團萃取分離螺旋藻藻藍蛋白[J].天津科技大學學報,2008,23(2):30-33.
[19] Santiago-Santos M C,Ponce-Noyola T,Olvera-Ram'?rez R,et al.Extraction and purification of phycocyanin from Calothrix sp.[J].Process Biochemistry,2004,39:2 047-2 052.
[20] 呂微,蔣劍春,徐俊明.蛋白質提取及分離純化研究進展[J].精細石油化工進展,2010,11(11):52-58.
[21] 張唐偉,李天才.藻膽蛋白質的提取純化與生物活性研究進展[J].生物技術通報,2010(1):9-13.
[22] 江詠,李曉璽,李琳,等.雙水相萃取技術的研究進展及應用[J].食品工業科技,2007,28(10):235-238.
[23] 郭珍,陳復生,李彥磊,等.反膠束萃取技術及其在植物蛋白質提取中的應用研究進展[J].食品與機械,2013,29(1):240-242.
[24] Peng X,Yuan X,Zeng G,et al.Extraction and purification of laccase by employing a novel rhamnolipid reversed micellar system [J].Process Biochemistry,2012,47:742-748.
[25] 徐寶財,王媛,肖陽,等.反膠團萃取分離技術研究進展[J].日用化學工業,2004,34(6):390-393.
[26] 張莉麗,張蘭威,杜明,等.凝膠層析和離子交換層析結合法純化高鹽發酵液中谷氨酰胺轉胺酶[J].分析化學,2012,40(8):1 225-1 230.
[27] 胡梁斌,王淼焱,李紅波,等.藻藍蛋白的純化及功能飲料的開發[J].河南科技學院學報,2011(6):19-22.
[28] 張少斌,穆楊,劉慧,等.重金屬離子鉻(Ⅵ)對螺旋藻生長的影響[J].江西農業學報,2012,24(2):145-146.
[29] 胡碧洋,趙蕾,周文靜,等.我國水華藍藻資源化研究現狀、問題與對策[J].水生態學雜志,2012,33(3):138-143.
[30] 楊濤,陳華.微囊藻毒素污染現狀及其生殖發育危害[J].海峽預防醫學雜志,2011,17(2):23-25.
[31] 謝建華,劉海靜,王愛武.淺析氨氮、總氮、三氮轉化及氨氮在水污染評價和控制中的作用[J].內蒙古水利,2011(5):34-36.
[32] 朱旭宇,江志兵,杜萍.氮磷營養鹽結構對有害藻類的影響[J].江西農業學報,2011,23(1):152-156.
[33] 夏商周,楊朝暉.微囊藻毒素的檢測及危害研究進展[J].四川環境,2012,31(3):90-93.
[34] 吳新民,鄭向榮,郗艷娟,等.水產品質量安全與控制對策[J].河北漁業,2011(5):56-57.
[35] 韓士群,李輝東,嚴少華,等.太湖藍藻藻藍蛋白的提取及純化[J].江蘇農業學報,2012,28(4):777-782.
[36] Chaiklahan R,Chirasuwan N,Loha V,et al.Separation and purification of phycocyanin from Spirulina sp.using a membrane process [J].Bioresource Technology,2011,102:7 159-7 164.
[37] 陳志桃,王立興,林維欽,等.螺旋藻藻藍蛋白的研究進展[J].海峽藥學,2003,15(6):1-5.
[38] Chaiklahan R,Chirasuwan N,Bunnag B.Stability of phycocyanin extracted from Spirulina sp.:Influence of temperature,pH and preservatives[J].Process Biochemistry,2012,47:659-664.

