冷藏對藍莓果實細胞壁組分及其降解酶活性的影響*
紀淑娟,卜鳳雅,周倩,張春蕾,程順昌
(沈陽農業大學食品學院,遼寧沈陽,110866)
藍莓又名越橘,為杜鵑花科(Ericaceae)越橘屬(Vaccinium spp.),小漿果類,果實呈藍色,色澤明亮,果肉細膩,種子極小,香氣獨特,富含花色苷、黃酮、SOD等多種生理活性成分,具有極強的抗氧化性和保健功能,是國際糧農組織列出的人類五大健康食品之一,被譽為“漿果之王”[1-2]。藍莓果實成熟于6~8月份的高溫多濕季節,田間熱和呼吸熱較高,采后的生理代謝旺盛,導致藍莓果實采后品質下降,主要表現為果實嚴重失水、硬度下降快、果肉變軟、易腐爛,極不耐貯藏。因此,如何控制藍莓果實采后軟化成為其在貯藏和銷售過程中亟待解決的重要問題。
冷藏是目前應用最有效廣泛的物理保鮮技術之一,可有效緩解采后藍莓果實的腐爛變質,但在冷藏藍莓出庫后的常溫貨架期間,果實軟化加快,蒂痕部出現凹陷,品質變劣,降低了其食用品質和商品價值,所以,研究藍莓果實軟化機理,對控制其果實的后熟軟化進程,延長貯藏期和提高商品價值都具有重要的意義。前人研究表明,果實軟化主要是由細胞中膠層結構的改變造成的細胞壁降解及組分變化而引起的[3],其中果膠物質的變化最為顯著,在貯藏過程中不溶性的原果膠降解成可溶性的果膠和果膠酸,最終導致果實軟化。果實軟化與細胞壁降解酶的活性也密切相關,PE、PG、Cx和β-Gal是導致果實成熟軟化的主要細胞壁降解酶[4]。研究發現,果實種類的不同導致其在成熟軟化過程中細胞壁組分的變化和細胞壁降解酶活性的改變方面存在著很大的差異[5-7]。目前關于藍莓果實細胞壁代謝的研究鮮有報道,本文以“藍豐”藍莓果實為試材,在細胞壁組分及其降解酶活性與果實硬度相關性分析的基礎上,研究了冷藏過程及冷藏后常溫貨架期間藍莓果實細胞壁組分及其降解酶活性的變化,以期了解冷藏對藍莓果實細胞壁代謝的影響,為藍莓果實的貯藏保鮮提供理論依據。
1 材料與方法
1.1 材料與處理
供試藍莓品種為“藍豐”,于2013年7月22日采自遼寧省農科院藍莓基地,采收當日選取成熟度為8~9成熟、大小均勻一致和無病、蟲、傷的果實立即運回實驗室,并在0~1℃下預冷18 h后裝入厚度為0.02 mm的聚乙烯薄膜袋中,每袋盛果200 g,一部分藍莓果實經預冷后置于常溫下(20±3)℃進行貯藏,每隔1天測定各項指標;另一部分藍莓果實經預冷后置于(0±0.5)℃下貯藏,分別在貯藏的30、60 d取出進行常溫貨架期的觀察與測定,每隔1天測定各項指標。設3次重復。
1.2 儀器與設備
BSA224S分析天平,北京賽多利斯科學儀器有限公司;TU-1810紫外可見分光光度計,北京普析通用儀器有限責任公司;TA.XT Plus型質構儀,英國SMSTA公司。
1.3 指標的測定
1.3.1 硬度
用英國產TA.XT Plus型質構儀進行測定,探頭直徑為8 mm,穿越距離為7 mm,測定速度為0.5 mm/s。
1.3.2 細胞壁物質的提取、分離及含量測定
參考 Yun Deng等和茅林春等的方法略加改進[8-9],分別提取水溶性果膠(WSP),離子結合型果膠(ISP)和共價結合型果膠(CSP),果膠含量測定采用咔唑比色法。
1.3.3 PE活性
已有研究認為植被、覆蓋物(凋落物積雪)都會對土壤理化性質產生影響,從而影響溫室氣體的排放。低溫生態系統的溫室氣體排放是一個多因素影響的綜合效應過程。但是某生態因子的改變對生態系統非生長季溫室氣體排放的影響大小,在不同的研究中存在差異[11,34]。因而,今后研究也應運用更多現代分析手段,如同位素、PLFA、DGGE等,對非生長季土壤理化性質、微生物功能群的多樣性及其動態變化等進行分析[11]。這也將是今后研究工作的一個方面。
參照Hagerman等的方法[10]。以每克鮮樣每分鐘吸光度變化0.01為1個過氧化物酶活性單位,單位U為0.01 OD620/(g·min)。
1.3.4 PG活性
參照Figueroa等的方法[11]。以每分鐘每克鮮樣在37℃分解多聚半乳糖醛酸產生1 μmol的半乳糖醛酸的質量表示,即 μg/(g·min)。
1.3.5 Cx活性
參照王亞楠等的方法[12]。以每分鐘每克鮮樣在40℃分解羧甲基纖維素鈉產生1 μg葡萄糖為1個Cx活性單位,即μg/(g·min)。
1.3.6 β-Gal活性
參照Brummell等的方法[13]。以每分鐘每克鮮樣產生 1 μmol的對硝基苯酚物質的量表示,即μmol/(g·min)。
1.4 數據處理
采用Excel和SPSS軟件進行數據統計分析。
2 結果與分析
2.1 常溫自然后熟的藍莓果實硬度、細胞壁組分及其降解酶活性之間的關系
由表1可知,在常溫自然后熟的藍莓果實細胞壁組分中,果實硬度與ISP呈顯著負相關,而與CSP呈極顯著正相關,與WSP相關性不大;在藍莓果實細胞壁酶中,果實硬度與Cx和β-Gal呈極顯著負相關,與PG呈顯著負相關;由表1亦可知,細胞壁組分及其相關降解酶之間也存在著密切的關系,WSP與PE、PG呈顯著正相關;ISP與PG、Cx呈極顯著正相關,與β-Gal呈顯著正相關;而CSP與PG、Cx呈顯著負相關,與β-Gal呈極顯著負相關,與PE相關性不大。
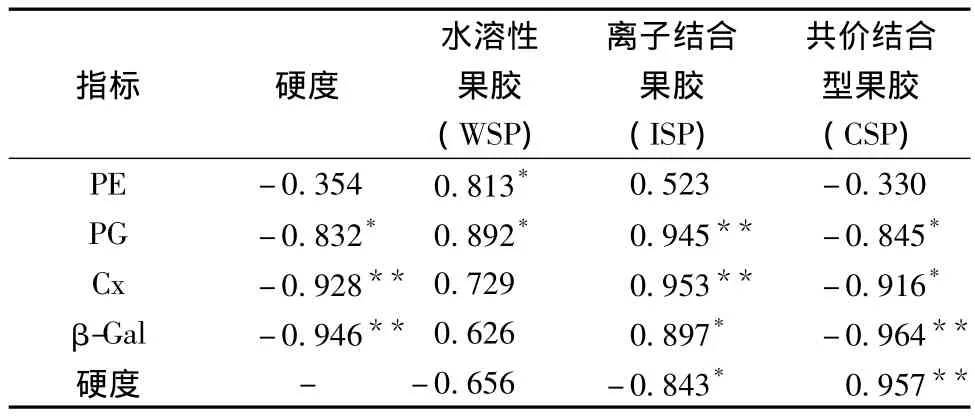
表1 常溫自然后熟的藍莓果實硬度、細胞壁組分及其降解酶活性之間的相關性Table1 The correlation of blueberry firmness,cell wall compositions and their metabolizing enzyme activity at room temperature
2.2 冷藏過程中藍莓果實硬度、細胞壁組分及其降解酶活性的變化
2.2.1 果實硬度變化
由圖1可知,藍莓果實的硬度隨冷藏時間的延長而逐漸降低,冷藏的前30天硬度下降緩慢,幅度小,冷藏30 d果實硬度僅下降5.2%;在冷藏的后期,藍莓果實硬度急速下降,冷藏60 d時下降了22.21%,與入庫時相比差異達顯著水平(P<0.05)。

圖1 冷藏期間藍莓果實硬度的變化Fig.1 Changes in firmness of blueberries during cold storage
2.2.2 果實細胞壁組分的變化

圖2 冷藏期間藍莓果實細胞壁組分的變化Fig.2 Changes in cell wall components of blueberries during cold storage
由圖2可知,隨著冷藏時間的延長藍莓果實的WSP含量呈逐漸上升趨勢,尤其是在冷藏的后期WSP快速上升;與WSP相反,藍莓果實CSP含量隨冷藏時間的延長而逐漸降低,在冷藏的后期急速下降;與WSP和CSP相比,藍莓果實中ISP含量較低,在冷藏過程中變化幅度小。
2.2.3 細胞壁降解酶活性的變化
由圖3可知,在冷藏期間PE、PG和β-Gal三種酶活性均呈現逐漸上升趨勢,其中PG和β-Gal兩種酶的活性在冷藏的前30 d上升緩慢,后期出現突躍性變化,活性上升幅度大;Cx活性則隨著冷藏那個時間的延長呈先緩慢下降后急劇上升的變化趨勢。
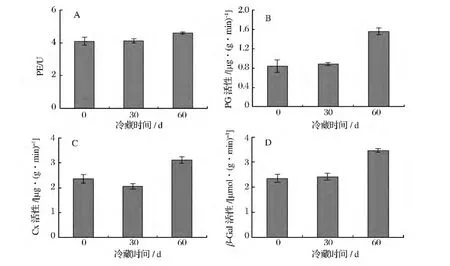
圖3 冷藏期間藍莓果實細胞壁降解酶活性的變化Fig.3 Changes in cell wall-degrading enzyme activity of blueberries during cold storage
2.3 冷藏對藍莓果實常溫貨架期果實硬度、細胞壁組分及其降解酶活性的影響
2.3.1 果實硬度變化
由圖4可見,經過冷藏的藍莓果實在常溫貨架期硬度的變化趨勢與采后常溫自然后熟果實略有不同。采后常溫自然后熟果實硬度呈勻速下降趨勢;冷藏30 d的藍莓果實在常溫貨架期的前6 d,硬度下降緩慢,之后快速下降,由此可見,冷藏30 d的藍莓果實貨架期較長;冷藏60 d的藍莓果實出庫后果實硬度迅速下降,在整個常溫貨架期間硬度均顯著低于其他處理,由此可見,冷藏60 d的藍莓果實不宜在常溫下放置。

圖4 常溫貨架期藍莓果實硬度的變化Fig.4 Changes in firmness of blueberries during shelf life at room temperature
2.3.2 細胞壁組分的變化
由圖5-A可知,冷藏30 d的藍莓果實在常溫貨架期WSP含量的變化趨勢與常溫自然后熟果實相似,均呈先上升后下降的趨勢,在第6天達到最大值,整個常溫貨架期間,2個處理之間差異不顯著(P>0.05);冷藏60d的藍莓果實在常溫貨架的前4 d,WSP含量上升速度快,在第4天時,與采后自然后熟的果實差異達到極顯著水平(P<0.01),之后上升速度趨緩,在貨架期第8天之后急速下降。由圖5-B看出,冷藏30 d的藍莓果實和采后常溫自然后熟的果實ISP含量均在常溫貨架的第2天和第8天分別出現最低峰和最高峰,但是,冷藏30 d果實的低峰值和高峰值均略低于采后常溫自然后熟的果實;冷藏60 d的藍莓果實在出庫時ISP含量較高,在整個常溫貨架期變化幅度小。圖5-C表明,采后自然后熟的藍莓果實從貨架期第2天開始,CSP含量持續下降;而冷藏30 d的果實在常溫貨架期的前4天變化幅度很小,之后CSP含量快速下降,而且30天冷藏的果實CSP下降幅度小于常溫自然后熟的果實,由此可見,中期冷藏可在一定程度上抑制CSP的下降;冷藏60天的藍莓果實自出庫開始,CSP含量便開始迅速下降,且在整個常溫貨架期間均顯著低于其他2個處理(P<0.05)。

圖5 常溫貨架期藍莓果實細胞壁組分的變化Fig.5 Changes in cell wall components of blueberries during shelf life at room temperature
2.3.3 細胞壁降解酶的變化
由圖6-A可知,采后常溫自然后熟的藍莓果實PE活性呈先上升后下降的趨勢,并在貨架第4天出現高峰;冷藏30 d的果實PE活性極顯著受到抑制(P<0.01),在整個常溫貨架期變化幅度小,而且未出現活性高峰;冷藏60 d的果實PE活性的整體變化趨勢與采后自然后熟的果實相似,二者無顯著差異(P>0.05)。圖6-B表明,冷藏30 d的藍莓果實與采后常溫自然后熟果實的PG活性均呈先上升后下降的趨勢,但是,冷藏30 d的果實PG活性高峰的出現推遲了2 d;冷藏60 d的藍莓果實在整個常溫貨架期間,PG活性均極顯著高于其他處理(P<0.01)。由6-C看出,冷藏30 d的藍莓果實與采后自然后熟的果實Cx活性均在貨架期前8天持續升高,至第8天時出現高峰,但是,冷藏30 d的藍莓果實Cx活性高峰值極顯著低于采后自然后熟的果實(P<0.01);冷藏60 d的藍莓果實在常溫貨架期間Cx活性高峰提前,而且,整個貨架期間極顯著的高于采后自然后熟的果實(P<0.01)。由此可見,適當冷藏可有效抑制藍莓果實在常溫貨架期間Cx的活性;由圖6-D可知,3個處理的藍莓果實均呈波動上升趨勢,但是,冷藏30 d的果實在整個常溫貨架期間β-Gal活性變化幅度小,且活性始終處于較低的水平,冷藏60 d的果實β-Gal活性始終極顯著高于其他2個處理(P<0.01)。

圖6 常溫貨架期藍莓果實細胞壁降解酶活性的變化Fig.6 Changes in cell wall-degrading enzyme activity of blueberries during shelf life at room temperature
3 結論與討論
果實軟化是果實成熟的重要特征之一,果實質地變軟與果實細胞壁組分及其降解酶活性的變化有著密切的關系。研究結果表明,藍莓果實硬度與ISP含量呈顯著負相關,與CSP含量呈極顯著正相關,這與魏建梅等在京白梨的研究中結果相似[7],貯藏期間,ISP含量升高,CSP含量急速下降引起藍莓果實細胞中膠層結構改變,細胞壁結構喪失以及細胞壁物質大量分解導致了其硬度快速下降;果實硬度與PG活性呈顯著負相關,與Cx活性和β-Gal活性呈顯著負相關,本試驗結果中PE、PG活性均呈先上升后下降趨勢,且PG活性高峰出現時間較PE晚2 d,這與趙云峰等在茄子的研究中結果相似[14],這可能是由于PE的作用是去除果膠分子鏈上的半乳糖醛酸羧基上的酯化基團,為PG提供合適的作用底物,進而 使PG沿多聚半乳糖醛酸主鏈水解果膠酸,導致果膠降解,PE并沒有直接參與果膠分子的降解過程,Cx活性的上升引起纖維素的解聚從而導致細胞壁解體,果實硬度下降,β-Gal可以降解果膠中的半乳聚糖,使細胞壁組分不穩定[15],導致果實軟化,Cross等在西紅柿的研究中發現,β-Gal在果實成熟的早期先于PG出現[16],本研究結果表明,β-Gal活性在藍莓果實采后自然后熟的前4天,上升速度快,幅度大,由此推測,β-Gal可能在藍莓果實軟化的初期起重要作用。由此可知,藍莓果實的軟化與ISP含量、CSP含量、PG活性、Cx活性和β-Gal活性關系密切。
冷藏期間,隨著藍莓果實硬度的下降,CSP含量逐漸上升,尤其是在貯藏后期上升速度快,而ISP含量低,變化幅度較小;PG活性和β-Gal活性在冷藏期間均呈現逐漸上升趨勢,Cx活性呈現先下降后上升的趨勢,3種酶的活性均在冷藏的后期急劇上升,可能由于三者的協同作用加劇了冷藏后期藍莓果實的軟化現象。冷藏的前30天,果實細胞壁降解酶活性變化緩慢,果實硬度保持良好;隨著冷藏時間的延長,細胞壁降解酶活性突躍性上升,CSP含量大幅下降,WSP含量快速增加,藍莓果實的硬度快速下降。冷藏30 d的藍莓果實在常溫貨架期間CSP含量變化幅度較小,PE、PG、Cx、β-Gal活性變化幅度小,且始終處于較低水平,尤其是PE和Cx活性極顯著降低,PE未出現活性高峰。由此可見,冷藏30 d可一定程度抑制藍莓果實細胞壁組分含量及其相關酶活性的變化,較好地保持果實的商品性。
[1] 朱麟,凌建剛.國內外藍莓保鮮技術研究進展[J].食品與發酵工業,2011,37(11):173-176.
[2] 亦菲.藍莓,漿果之王的傳奇[J].食品與藥品,2010,12(8):10-11.
[3] Luis F Goulao,Cristina M Oliveira.Cell wall modifications during fruit ripening:when a fruit is not the fruit[J].Trends in Food Science&Technology,2008,1(19):4-25.
[4] 程杰山,沈火林,孫秀波,等.果實成熟軟化過程中主要相關酶作用的研究進展[J].北方園藝,2008(1):49-52.
[5] Brummell D A,Cin V D,Crisosto C H,et al.Cell wall metabolism during the development of chillg injury in coldstored peach fruit:assocition of mealiness with arrested disassembly of cell wall pectins[J].Journal of Experimental Botany,2004,55(405):2 041-2 052.
[6] HU Lan-Ying,HU Shu-Li,WU Jun,et al.Hydrogen sulfide prolongs postharvest shelf Life of strawberry and play an antioxidative role in fruit[J].Journal of Agricultural and Food Chemistry,2012,60(35):8 684-8 693.
[7] 魏建梅,馬鋒旺,關軍鋒,等.京白梨果實后熟軟化過程中細胞壁代謝及其調控[J].中國農業科學,2009,42(8):2 987-2 996.
[8] DENG Yun,WU Ying,LI Yunfei.Changes in firmness,cell wall composition and cell wall hydrolases of grapes stored in high oxygen atmospheres[J].Food Research International,2005,38(7):769-776.
[9] 茅林春,張上隆.間歇低溫脅迫對桃果實細胞壁代謝的影響[J].植物生理學報,2001,27(2):151-155.
[10] Hagerman A E,Austin P J.Continuous spectrophotometric assay for plant pectin methyl esterase[J].Journal of Agricultural and Food Chemistry,1986,34(3):440-444.
[11] Figueroa Carlos R,Rosli Hernan G,Civello Pedro M.Changes in cell wall polysaccharides and cell wall degrading enzymes during ripening of Fragaria chiloensis and Fragaria ananassa fruits[J].Scientia Horticulturae,2010,124(4):454-462.
[12] 王亞楠,胡花麗,張璇,等.氣調貯藏對‘紅陽'獼猴桃果膠含量及相關酶的影響[J].食品與發酵工業,2013,8(39):207-211.
[13] 金昌海,水野雅史,汪志君,等.蘋果β-半乳糖苷酶對細胞壁多糖降解特性的研究[J].揚州大學學報(農業與生命科學版),2002,23(4):71-74.
[14] 趙云峰,林瑜,吳玲艷.茄子果實采后軟化過程中細胞壁組分及其降解酶活性的變化[J].食品與發酵工業,2012,38(10):212-216.
[15] 魏建梅,馬鋒旺.蘋果果實β-Gal和LOX活性變化特性及其與果實軟化的關系[J].園藝學報,2009,36(5):631-638.
[16] Cross K C,Wallner S J.Degradation of cell wall polysaccharides during tomato fruit ripening[J].Plant Physiology,1979,63(1):117-120.

