苦丁冬青苦丁茶中咖啡酰奎尼酸類物質與牛血清白蛋白的相互作用
徐冬蘭,周 莉,胡 冰,孫 怡,曾曉雄
苦丁冬青苦丁茶中咖啡酰奎尼酸類物質與牛血清白蛋白的相互作用
徐冬蘭,周 莉,胡 冰,孫 怡*,曾曉雄
(南京農業大學食品科技學院,江蘇 南京 210095)
從苦丁冬青苦丁茶中分離純化得到了4種咖啡酰奎尼酸(caffeoylquinic acids,CQA):5-CQA、3,4-diCQA、3,5-diCQA和4,5-diCQA,并在模擬人體生理條件(pH 7.4,310 K)下,利用熒光光譜法分析4種CQA與牛血清白蛋白(bovine serum albumin,BSA)的相互作用,使用修正后的Stern-Volmer方程與van’t Hoff方程探討CQA-BSA之間的結合常數、結合位點數及熱力學參數。結果表明:4種CQA均能與BSA結合,從而導致BSA分子內部熒光發生猝滅,結合能力的大小順序為3,4-diCQA>3,5-diCQA>4,5-diCQA>5-CQA,說明咖啡酰基的增多提高了結合能力。熱力學參數ΔH>0、ΔS>0和ΔG<0,表明CQA與BSA主要靠疏水作用力結合,反應自發進行。此外,CQA的結合引起BSA 3D熒光光譜和同步熒光光譜的變化,表明兩者之間的結合主要是通過與BSA中色氨酸和酪氨酸的作用而實現的。
苦丁茶;咖啡酰奎尼酸;牛血清白蛋白;熒光光譜;相互作用
血清白蛋白是血漿中最豐富的蛋白質,具有貯運內源代謝產物和外源性小分子等重要生理功能。當藥物進入人體后,首先通過血漿的貯存與運輸達到受體部位,進而發揮藥理作用。因此,研究藥物小分子和血清白蛋白的結合對于確定藥物的藥代動力學和藥效方面的性質有著非常重要的作用[1]。近年來,茶多酚的多種藥理作用已被廣泛證明,探討茶多酚與蛋白質之間的相互結合機理也成為了一個熱點[2]。例如,張海蓉等[3]利用光譜學方法研究了兒茶素與牛血清白蛋白(bovine serum albumin,BSA)之間的相互作用,確定了兩者結合的結合常數、結合位置和結合類型等參數。柳全文等[4]的研究表明咖啡酸能與BSA發生結合,從而導致其內部的熒光發生猝滅。Nozaki等[5]采用圓二色譜法研究了表沒食子兒茶素沒食子酸酯((-)-epigallocatechin gallate,EGCG)對BSA構象的影響,探討了EGCG在BSA分子中的具體結合位點。
苦丁茶是由冬青科或木犀科等植物的葉加工而成的一種代用茶,在我國有著2 000多年的飲用歷史[6-8]。苦丁茶主要分為兩大類:冬青科苦丁茶和木犀科苦丁茶。目前用于加工苦丁茶的主要原料為冬青科的苦丁茶冬青、大葉冬青和枸骨[9-10]。苦丁茶富含三萜、酚酸類、黃酮以及氨基酸等多種活性物質,具有抗氧化、抗炎癥、抗腫瘤以及降脂減肥等功效[11-12]。在前期的研究中,Liu Lixiang等[13]發現苦丁冬青苦丁茶中的主要多酚類物質為咖啡酰奎尼酸(caffeoylquinic acids,CQA)類物質,并表明其具有較強的體外抗氧化活性。王晴川等[14]以苦丁冬青苦丁茶為材料,通過柱層析和半制備色譜分離純化得到了6種CQA類物質,包括3-CQA、4-CQA、5-CQA、3,4-diCQA、3,5-diCQA、4,5-diCQA,其結構式見圖1。CQA被證明具有多種藥理功能,如抗氧化活性、抑制消化酶作用、降低血糖以及抑制腫瘤發生等[15-18]。然而,關于CQA與血清白蛋白的相互作用卻鮮有報道。因此,在前期的研究基礎上,本實驗采用熒光光譜法研究并比較4種CQA(5-CQA、3,4-diCQA、3,5-diCQA和4,5-diCQA)與BSA的結合作用,為闡明CQA在體內的運輸、吸收和代謝提供重要信息。
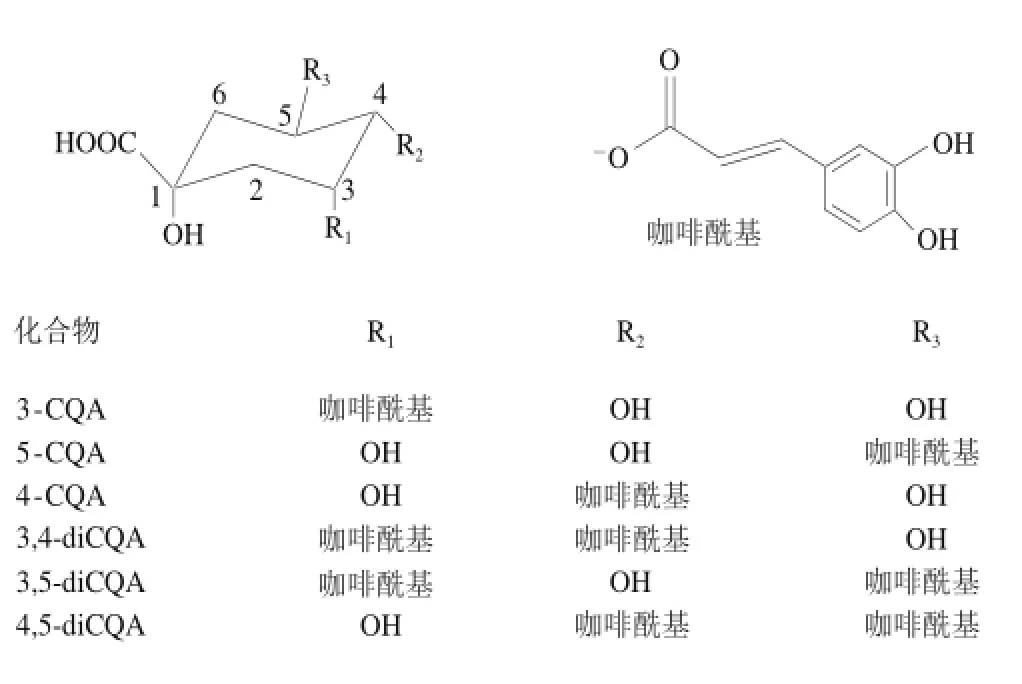
圖1 苦丁茶中CQA類物質結構Fig.1 General structures of caffeoylquinic acid derivatives (CQAs) from Kudingcha
1 材料與方法
1.1 材料與試劑
苦丁冬青苦丁茶海南椰仙生物科技有限公司;大孔樹脂HP-20日本三菱公司。
四種咖啡酰奎尼酸:5-CQA、3,4-diCQA、3,5-diCQA、4,5-diCQA實驗室自制,純度均>95%;牛血清白蛋白(相對分子質量為66 210)、Tris-HCl緩沖溶液(pH 7.4,0.05 mol/L,含0.1 mol/L NaCl)、甲醇(色譜純)美國Sigma公司;其他試劑均為分析純,實驗用水為二次蒸餾水。
1.2儀器與設備
F-7000型熒光分光光度計日本Hitachi公司;BL-220H分析天平日本Shimadzu公司;HH-4數顯恒溫水浴鍋江蘇國華電器有限公司;Heidolph Laborota 4000真空旋轉蒸發儀德國Heidolph公司;LyoQuest-55真空冷凍干燥機西班牙Telstar公司;Agilent 1100高效液相色譜儀美國Agilent公司;?KTA Purifier蛋白純化系統美國通用電氣公司。
1.3方法
1.3.1 5-CQA、3,4-diCQA、3,5-diCQA和4,5-diCQA的制備
采用本實驗室建立的方法[14,19]并稍作修改。稱取適量粉碎過篩的苦丁冬青苦丁茶粉末,以1∶10(m/V)的料液比加入沸水并于95℃水浴中浸提45 min,5 000×g離心15 min,取上清液,將剩余殘渣重復抽提兩次,合并上清液,濃縮、冷凍干燥得到苦丁茶多酚粗提物。將粗提物用去離子水配制成溶液,上樣于HP-20大孔樹脂層析柱(5 cm×30 cm),之后分別用3個柱床體積的純水與體積分數70%的乙醇洗脫,高效液相色譜法(high performance liquid chromatography,HPLC)在線檢測,收集相應的洗脫液,并濃縮、冷凍干燥,經Folin-Ciocalteu法測定初步純化產物總多酚含量為78.4%。以初步純化產物為原料,采用?KTA純化系統制備4種CQA單體,純化流程使用YMC-PACK ODS-A色譜柱(10 cm×250 mm,5μm),檢測波長為280 nm,每次進樣500μL,流速為2 mL/min,先后用體積分數為20%和40%的甲醇洗脫。根據HPLC檢測結果將出峰時間相同的物質富集起來,對照各CQA的標準品,合并相同的組分,經濃縮、凍干,得到5-CQA、3,4-diCQA、3,5-diCQA和4,5-diCQA。經過HPLC分析,4種CQA峰形清晰、單一,純度均在95%以上。
1.3.2 CQA與BSA相互作用的熒光光譜分析
熒光光譜測定:BSA和CQA均用Tris-HCl緩沖溶液(pH 7.4)溶解。在5 mL離心管中準確移入3.0 mL 1.0×10-6mol/L的BSA溶液,用移液槍分別加入不同濃度(2.5×10-6、5.0×10-6、7.5×10-6、1.0×10-5、1.25×10-5、1.5×10-5、1.75×10-5mol/L)的4種CQA(5-CQA、3,4-diCQA、3,5-diCQA或4,5-diCQA)溶液。使用1.0 cm的石英比色皿,設定激發光柵和發射光柵的狹縫寬度為5.0 nm,激發波長(λex)為280 nm,恒溫掃描BSA及反應混合物在290~450 nm波長范圍內的熒光發射光譜。并以280 nm/340 nm為激發波長/發射波長(λex/λem),測定不同溫度(293、310 K)條件下體系的熒光強度,所得實驗數據用于猝滅常數和結合常數等的計算。
3D熒光光譜分析:設定激發波長與發射波長的掃描范圍均為200~600 nm,狹縫寬度為5 nm,得到BSA及CQA-BSA反應混合物的3D圖譜。
同步熒光光譜測定:在310 K的溫度條件下,采用同步掃描模式,將激發和發射波長之間的差值分別固定在15 nm和60 nm(Δλ=15、60 nm),狹縫寬度為5.0 nm,掃描速率為1 200 nm/min,同時掃描激發光譜和發射光譜,記錄BSA及反應混合溶液的同步熒光光譜。
2 結果與分析
2.1 CQA對BSA熒光光譜的猝滅效應
熒光光譜通常用來研究藥物及其他小分子與蛋白質之間的相互作用[20]。小分子的結合可能導致蛋白質內部熒光發生猝滅。BSA分子中含有色氨酸、酪氨酸等氨基酸殘基使其具有內源性熒光,并在激發波長和發射波長分別為280 nm和340 nm處有最大熒光峰[21]。由圖2可知,保持BSA的濃度不變,當加入不同濃度的CQA后,BSA的熒光光譜發生了猝滅。隨著CQA濃度的不斷增大,BSA的熒光強度明顯降低。3種二取代咖啡酰奎尼酸(3,4-diCQA、3,5-diCQA和4,5-diCQA)的猝滅效果大于單取代咖啡酰奎尼酸(5-CQA),表明CQA和BSA之間發生了結合作用,并且分子中咖啡酰基的增多提高了CQA的結合能力。此外,BSA的最大發射波長發生微弱紅移(5-CQA從340 nm移至344 nm;3,4-diCQA從340 nm移至348 nm;3,5-diCQA從340 nm移至345 nm;4,5-diCQA從340 nm移至344 nm),表明CQA的結合導致了BSA發色團疏水環境的改變。
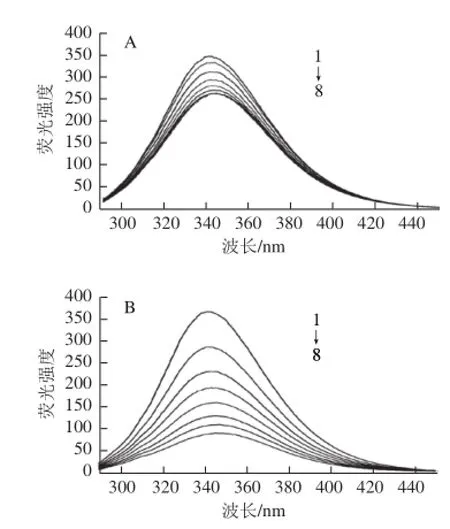
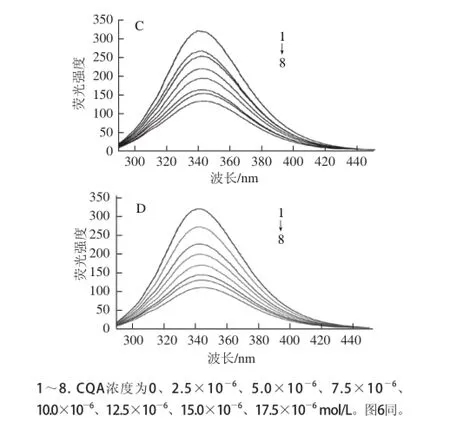
圖2 310 K溫度條件下5-CQA(A)、3,4-diCQA(B)、3,5-diCQA(C)和4,5-diCQA(D)對BSA熒光圖譜的猝滅效應Fig.2 Fluorescence quenching effects of 5-CQA (A), 3,4-diCQA (B), 3,5-diCQA (C) and 4,5-diCQA (D) on fluorescence spectra of BSA at 310 K
2.2 CQA對BSA的熒光猝滅機理及猝滅常數分析
熒光猝滅的機理主要分為動態猝滅和靜態猝滅。動態猝滅是由處于激發態的熒光分子與猝滅劑發生碰撞接觸而產生的,而靜態猝滅則是由處于基態的熒光分子與猝滅劑生成了不發熒光的復合物引起的[22]。為了確定CQA對BSA的猝滅機理,采用Stern-Volmer方程[23]分析熒光猝滅數據:
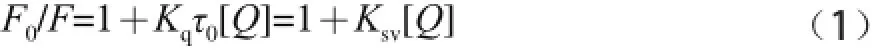
式中:F0、F分別表示猝滅劑不存在和存在時蛋白質的熒光強度;[Q]為猝滅劑濃度;Kq為雙分子表觀猝滅速率常數;τ0為無猝滅劑存在時熒光分子的平均壽命,大部分生物大分子的熒光壽命為10-8s;Ksv為猝滅常數。
根據式(1),以F0/F對CQA濃度[Q]作圖,得到Stern-Volmer猝滅曲線,結果如圖3所示。根據曲線斜率計算得到CQA和BSA之間相互作用的表觀猝滅速率常數Kq及猝滅常數Ksv,結果見表1。對于動態猝滅,各類猝滅劑對生物大分子的最大Kq約為2×1010L/(mol·s)[24]。此外,動態和靜態猝滅可根據猝滅常數Ksv隨溫度的變化關系加以判斷。對于動態猝滅,由于其依賴于擴散,因此溫度的升高將增加有效碰撞和加劇電子轉移過程,使Ksv隨溫度升高而增大,而靜態猝滅則正好相反[22]。根據表1數據可知,隨著溫度的升高,4種CQA類物質對BSA的熒光猝滅常數Ksv均呈減小趨勢,并且反應的Kq遠大于各類猝滅劑對生物大分子的最大猝滅常數2×1010L/(mol·s),表明反應形成了BSA-CQA基態復合體,猝滅機理為靜態猝滅。另外,3,4-diCQA、3,5-diCQA和4,5-diCQA的猝滅常數均大于5-CQA,說明diCQA與BSA更易形成穩定的復合物,與猝滅效應分析的結果一致。

圖3 不同溫度條件下5-CQA(A)、3,4-diCQA(B)、3,5-diCCQQAA(C)和4,5-diCQA(D)猝滅BSA的Stern-Volmer圖Fig.3 Stern-Volmer plots of BSA quenched by 5-CQA (A), 3,4-diCQA (B), 3,5-diCQA (C) and 4,5-diCQA (D) at different temperatures
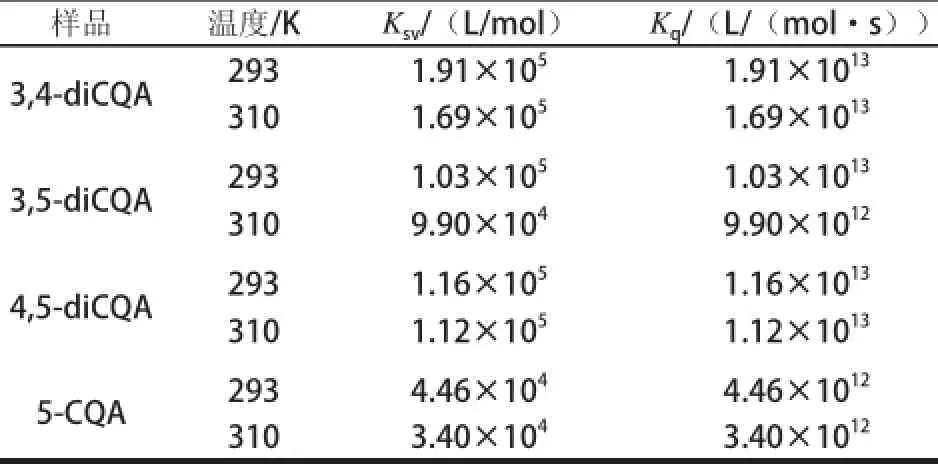
表1 不同溫度條件下CQA對BSA的猝滅常數Table 1 Stern-Volmer quenching constants for the interactions of CQAs with BSA at different temperatures
2.3 結合常數及結合位點數的確定
對于靜態猝滅過程,當小分子與大分子結合時,熒光猝滅強度與猝滅劑濃度之間的關系可用修正后的Stern-Volmer方程描述:
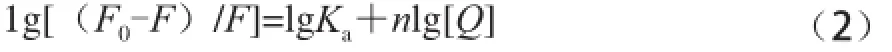
式中:Ka為CQA與BSA的結合常數;n為結合位點數。
以lg[(F0-F)/F]對lg[Q]作圖可得一組直線(圖4),由直線的斜率和截距可以求出不同CQA與BSA 相互作用的結合常數Ka和結合位點數n(表2)。
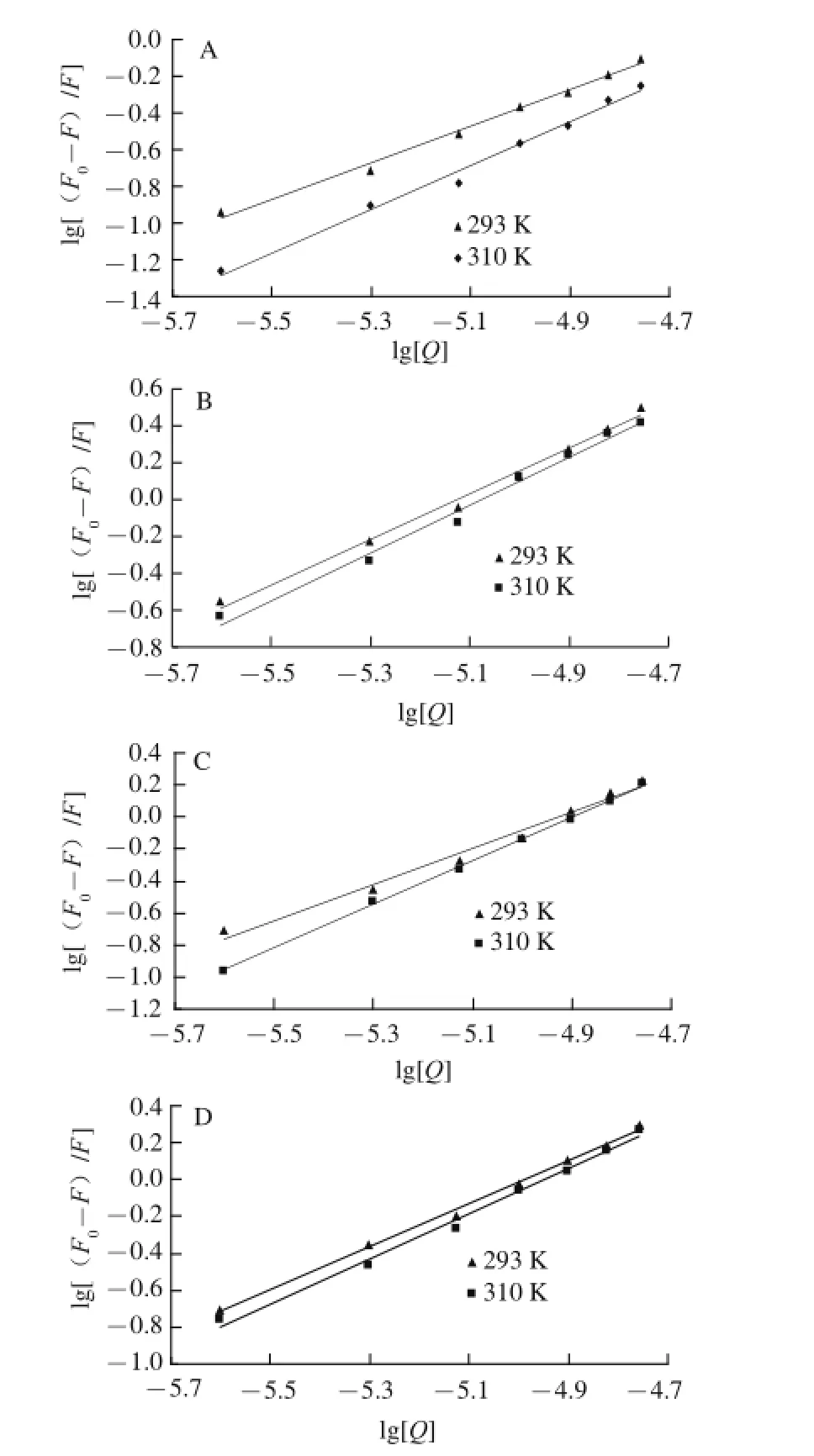
圖4 不同溫度條件下5-CQA(A)、3,4-diCQA(B)、3,5-diCQA(CC)和4,5-diCQA(D)對BSA熒光猝滅的雙對數圖Fig.4 Double logarithmic curves for the quenching of BSA fluorescence by 5-CQA (A), 3,4-diCQA (B), 3,5-diCQA (C) and 4,5-diCQA (D) at different temperatures
小分子與大分子之間的相互作用力包括氫鍵、范德華力、靜電作用及疏水作用力[25]。在溫度變化不大時,反應的焓變ΔH可以看作一個常量,根據van’t Hoff方程,可計算出ΔH和ΔS。
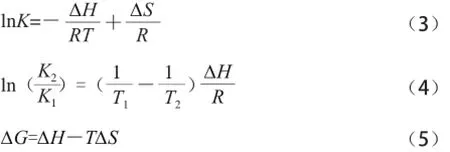
式中:K為相應溫度下(293、310 K)反應體系的結合常數;R為氣體常數。
根據公式(3)、(4)計算得到ΔH和ΔS,再由式(5)計算得到ΔG,結果列于表2。
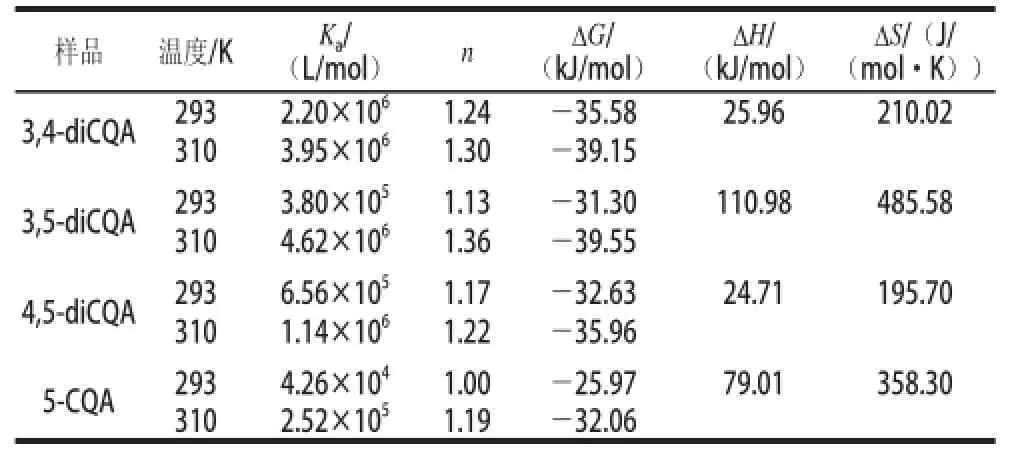
表2 不同溫度條件下CQA與BSA的結合常數及相關熱力學參數Table 2 Binding parameters and relative thermodynamic variables forCQAs binding to BSA at different temperatures
圖4和表2的結果表明,CQA和BSA之間存在強大的結合力,并且diCQA的結合能力強于5-CQA。所有CQA的結合常數均隨著溫度升高而增大,這表明溫度升高后,CQA與BSA的結合能力略有增強,從而導致BSA-CQA復合體的穩定性增加。n值約為1,表明CQA與BSA具有一個結合位點。
2.4 CQA與BSA相互作用的熱力學參數及結合類型的確定
由表2可知,4種CQA與BSA反應的ΔG<0,表明反應是自發進行。Ross等[26]根據大量實驗總結了水相中小分子與生物大分子結合的熱力學參數與主要作用力之間的關系,1)若ΔH>0、ΔS>0,則為疏水作用力;2)若ΔH<0、ΔS<0,則為氫鍵和范德華力;3)若ΔH≈0,ΔS>0,則為靜電引力。根據表2計算結果,CQA與BSA結合反應的ΔH和ΔS均>0,表明反應的主要作用力為疏水相互作用。
2.5 CQA對BSA的3D熒光猝滅效應
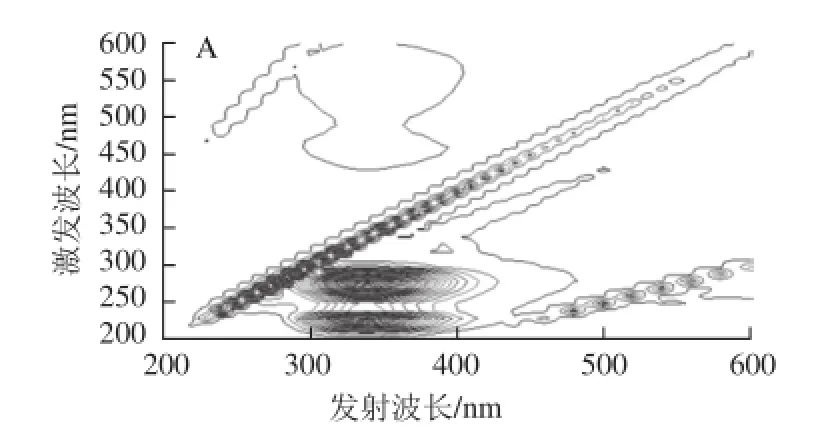
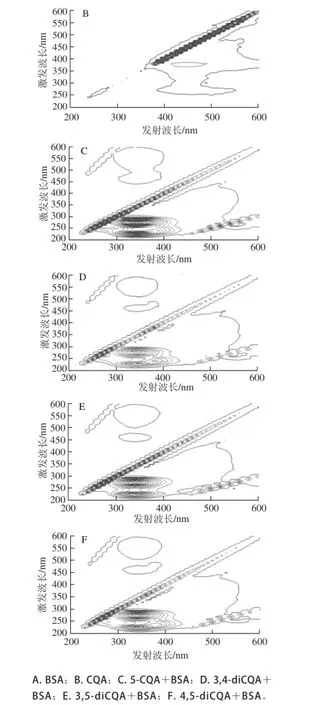
圖5 BSA及CQA-BSA復合體的3D熒光光譜Fig.5 Three dimensional spectral contour maps of BSA and BSA-CQA system
近年來,蛋白質的3D熒光圖譜經常被用來研究小分子對蛋白分子結構的影響[27]。如圖5所示,4種CQA與BSA結合后,對BSA的熒光特征吸收峰產生了影響。CQA在檢測波長內無熒光峰,BSA在激發波長為230 nm和280 nm,發射波長為340 nm處分別有一個最大吸收峰。其中230 nm/340 nm(λex/λem)處的特征光譜峰是由于蛋白質肽鏈結構中π-π*和n-π*電子轉移引起的,而280 nm/340 nm(λex/λem)處的吸收峰表現的是蛋白結構中酪氨酸和色氨酸殘基的光譜特性[22]。當加入CQA后,BSA的兩個特征峰均被不同程度地猝滅,表明CQA與BSA發生了結合,從而導致蛋白肽鏈的伸展,分子內部的熒光發色基團所處的微環境發生變化。
2.6 CQA對BSA構象的影響
蛋白質的同步熒光光譜常被用來判斷蛋白質的構象變化,得到關于生色團分子周圍環境的信息[28]。當固定激發波長和發射波長的掃描差值為15 nm(Δλ=15 nm)時,只顯示酪氨酸殘基的熒光特征光譜,當固定Δλ=60 nm時,只顯示色氨酸殘基的特征熒光,因此由熒光波長的改變可判斷蛋白質中酪氨酸和色氨酸殘基所處微環境的變化[29]。牛血清白蛋白含有色氨酸和酪氨酸殘基,當加入不同CQA后,其在Δλ為15 nm和60 nm處的同步熒光光譜均發生了改變(圖6)。當蛋白質濃度固定時,隨著CQA濃度的增加,BSA中色氨酸殘基和酪氨酸殘基的熒光強度都不斷降低,表明CQA可以猝滅BSA內部熒光,并且3種diCQA的猝滅效果大于5-CQA。從圖中還可以看出,CQA使BSA中色氨酸殘基的最大激發波長發生了紅移,而酪氨酸殘基的最大激發波長則發生了微弱的藍移,表明兩者的結合影響了BSA的構象,改變了兩個殘基所處微環境的疏水性。由此可以判斷CQA與BSA的相互作用可能是通過CQA與色氨酸和酪氨酸的結合而實現的。
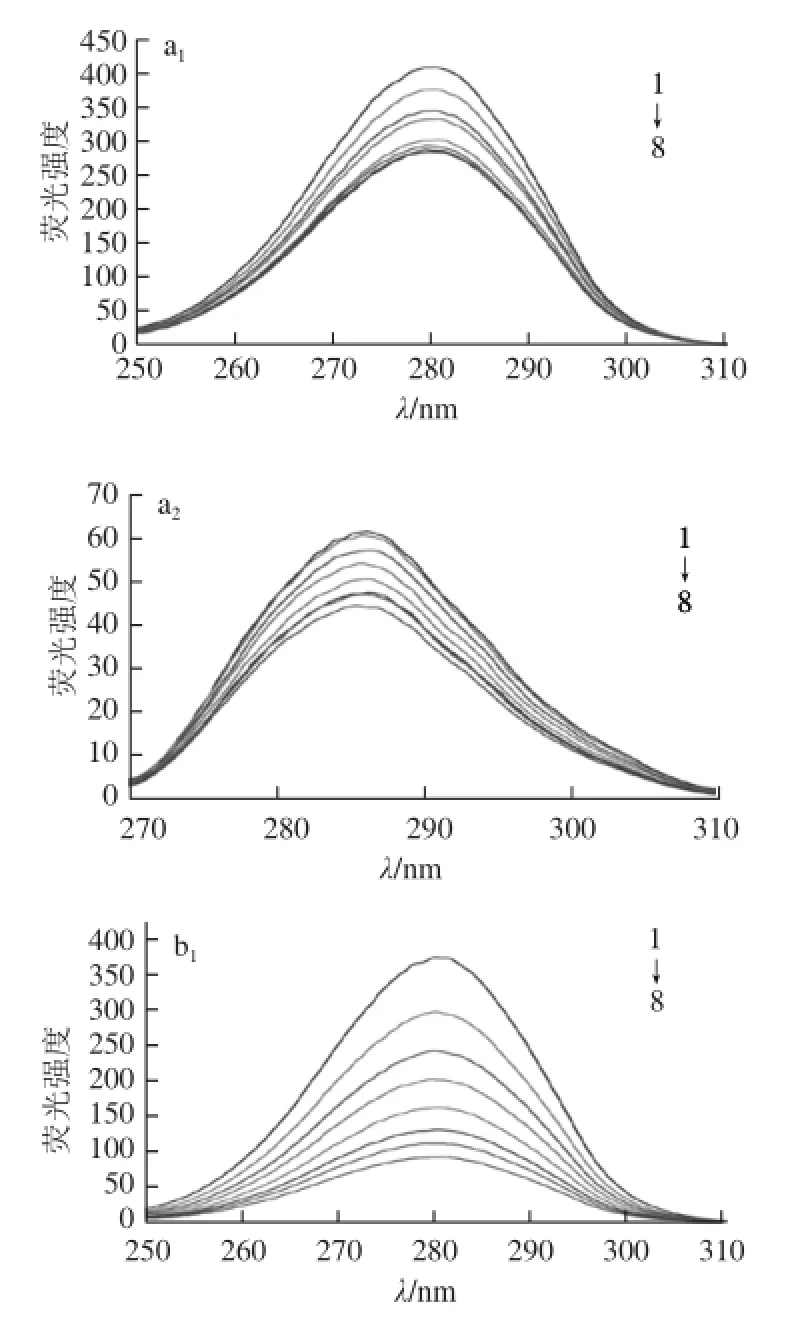
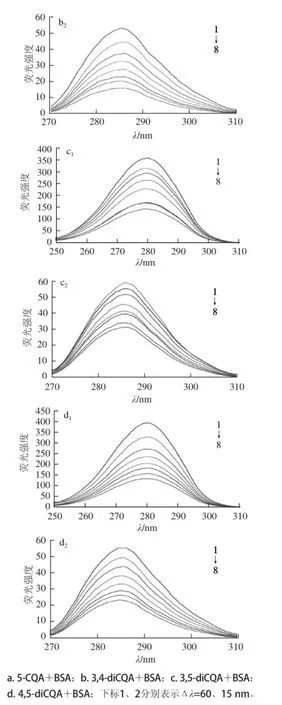
圖6 CQA與BSA相互作用的同步熒光光譜Fig.6 Synchronous fluorescence spectra of CQA-BSA interaction
3 結 論
采用熒光光譜的方法研究與比較了苦丁冬青苦丁茶中5-CQA、3,4-diCQA、3,5-diCQA和4,5-diCQA在不同溫度條件下與BSA的相互作用。研究發現4種CQA均能與BSA發生結合,形成穩定復合物,導致BSA的熒光發生猝滅,并且diCQA的猝滅效果大于5-CQA,表明結構中的咖啡酰基對結合過程貢獻很大。Stern-Volmer方程分析得到兩個溫度下(293、310 K)的猝滅常數,表明猝滅機理為靜態猝滅。采用修正后的Stern-Volmer方程計算了反應的結合常數和結合位點數,說明CQA和BSA之間存在強大的結合力,具有一個結合位點。熱力學參數計算結果表明CQA與BSA之間主要依靠疏水作用力結合,反應自發進行。CQA的結合引起BSA 3D光譜和同步熒光光譜的變化,推測CQA與BSA的作用可能是通過與BSA中色氨酸和酪氨酸殘基的結合而實現的。本實驗為探討咖啡酰基奎尼酸類化合物在生物體內的作用及其機制提供了重要信息。
[1] MULLER W E, WOLLERT U. Human serum albumin as a‘silent receptor’for drugs and endogenous substances[J]. Pharmacology, 1979, 19(2): 59-67.
[2] BANDYOPADHYAY P, GHOSH A K, GHOSH C. Recent developments on polyphenol-protein interactions: effects on tea and coffee taste, antioxidant properties and the digestive system[J]. Food & Function, 2012, 3(6): 592-605.
[3]張海蓉,邊賀東,潘英明,等.光譜法研究兒茶素與牛血清白蛋白的相互作用[J].光譜學與光譜分析, 2009, 29(11): 3052-3056.
[4]柳全文,徐慧,李桂華,等.咖啡酸與牛血清白蛋白相互作用的熒光光譜法研究[J].食品科學, 2010, 31(1): 24-28.
[5] NOZAKI A, HORI M, KIMURA T, et al. Interaction of polyphenols with proteins: binding of (-)-epigallocatechin gallate to serum albumin, estimated by induced circular dichroism[J]. Chemical & Pharmaceutical Bulletin, 2009, 57(2): 224-228.
[6]劉國民,李娟玲,陳榆,等.我國苦丁茶冬青種質資源的形態學研究Ⅰ.莖葉的形態學研究[J].貴州科學, 2004, 22(3): 9-23.
[7]王新,陸慧寧,林少琨.苦丁茶冬青葉化學成分及藥理作用研究進展[J].天然產物研究與開發, 2005, 17(3): 366-370.
[8]劉韶,杜方麓.冬青屬苦丁茶研究進展[J].湖南中醫學院學報, 2001, 21(2): 68-70.
[9]陳杖洲.苦丁茶的開發及其利用[J].中國茶葉加工, 1998(4): 29-31.
[10] 鄢東海.苦丁茶名稱的演變、植物種類及保健價值[J].貴州農業科學, 2007, 35(1): 114-116.
[11] LI L, XU L J, MA G Z, et al. The large-leaved kudingcha (Ilex latifoliaThunb andIlex kudingchaC.J. Tseng): a traditional Chinese tea with plentiful secondary metabolites and potential biological activities[J]. Journal of Natural Medicines, 2013, 67(3): 425-437.
[12]劉瑾,丁平.冬青屬藥用植物資源、化學成分及藥理作用研究進展[J].廣州中醫藥大學學報, 2008, 25(3): 277-280.
[13] LIU Lixiang, SUN Yi, LAURU T, et al. Determination of polyphenolic content and antioxidant activity of kudingcha made fromIlex kudingchaC.J. Tseng[J]. Food Chemistry, 2009, 112(1): 35-41.
[14]王晴川,張鑫,張文芹,等.苦丁冬青苦丁茶中咖啡酰奎尼酸類物質的分離純化和高效液相色譜法分析[J].食品科學, 2013, 34(22): 119-122. doi: 10.7506/spkx1002-6630-201322024.
[15] THUONG P T, SU N D, NGOC T M, et al. Antioxidant activity and principles of Vietnam bitter teaIlex kudingcha[J]. Food Chemistry, 2009, 113(1): 139-145.
[16] SONG Chengwu, XIE Chao, ZHOU Zhiwen, et al. Antidiabetic effect of an active components group fromIlex kudingchaand its chemical composition[J]. Evidence-Based Complementary & Alternative Medicine, 2012. doi: 10.1155/2012/423690.
[17] MURASE T, MISAWA K, MINEGISHI Y, et al. Coffee polyphenols suppress diet-induced body fat accumulation by downregulating SREBP-1c and related molecules in C57BL/6J mice[J]. American Journal of Physiology: Endocrinology and Metabolism, 2011, 300(1): E122-E133.
[18] OOI K L, MUHAMMAD T S T, TAN M L, et al. Cytotoxic, apoptotic and anti-α-glucosidase activities of 3,4-di-O-caffeoyl quinic acid, an antioxidant isolated from the polyphenolic-rich extract ofElephantopus mollisKunth[J]. Journal of Ethnopharmacology, 2011, 135(3): 685-695.
[19]孫怡,張鑫,張文芹,等.苦丁茶冬青苦丁茶中多酚類物質的分離純化與結構解析[J].食品科學, 2011, 32(11): 60-63.
[20] RAWEL H A, MEIDTNER K, KROLL J. Binding of selected phenolic compounds to proteins[J]. Journal of Agricultural and Food Chemistry, 2005, 53(10): 4228-4235.
[21] LI Daojin, WANG Ye, CHEN Jianjun, et al. Characterization of the interaction between farrerol and bovine serum albumin by fluorescence and circular dichroism[J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2011, 79(3): 680-686.
[22] SINGHA R A, PANDEY N K, DASGUPTA S. Preferential binding of fisetin to the native state of bovine serum albumin: spectroscopic and docking studies[J]. Molecular Biology Reports, 2013, 40(4): 3239-3253.
[23] LAKOWICZ J R. Principles of fluorescence spectroscopy[M]. New York: Springer, 2006: 8-12.
[24] BI Shuyun, SONG Daqian, KAN Yuhe, et al. Spectroscopic characterization of effective components anthraquinones in Chinese medicinal herbs binding with serum albumins[J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 2005, 62(1): 203-212.
[25] WU Xuli, WANG Wenpu, ZHU Tian, et al. Phenylpropanoid glycoside inhibition of pepsin, trypsin and α-chymotrypsin enzyme activity in Kudingcha leaves fromLigustrum purpurascens[J]. Food Research International, 2013, 54(2): 1376-1382.
[26] ROSS P D, SUBRAMANIAN S. Thermodynamics of protein association reactions: forces contributing to stability[J]. Biochemistry, 1981, 20(11): 3096-3102.
[27] YUE Yuanyuan, ZHANG Yaheng, QIN Jin, et al. Study of the interaction between esculetin and human serum albumin by multispectroscopic method and molecular modeling[J]. Journal of Molecular Structure, 2008, 888(1/3): 25-32.
[28]陶慧林,黎舒懷,徐銘澤,等.山奈素與牛血清蛋白相互作用: Tachiya模型與Stern-Volmer方程的對比研究[J].分析測試學報, 2013, 32(2): 186-192.
[29] LIU Xiaoli, XIA Wenshui, JIANG Qixing, et al. Binding of a novel bacteriostatic agent-chitosan oligosaccharides-kojic acid graft copolymer to bovine serum albumin: spectroscopic and conformation investigations[J]. European Food Research and Technology, 2015, 240(1): 109-118.
Interaction of Caffeoylquinic Acid Derivatives from Ilex kudingcha C. J. Tseng with Bovine Serum Albumin
XU Donglan, ZHOU Li, HU Bing, SUN Yi*, ZENG Xiaoxiong
(College of Food Science and Technology, Nanjing Agricultural University, Nanjing 210095, China)
In the present study, the interactions between bovine serum albumin (BSA) and four caffeoylquinic acid (CQA) derivatives (5-CQA, 3,4-diCQA, 3,5-diCQA and 4,5-diCQA) isolated from the leaves ofIlex kudingchaC. J. Tseng were investigated by fluorescence spectroscopy under simulated physiological condition (pH 7.4 and 310 K). The binding parameters were calculated according to modified Stern-Volmer equation, and the thermodynamic parameters were determined by the van’t Hoff equation. The results showed that CQA derivatives interacted with BSA, and the binding constants were ranked in the following order: 3,4-diCQA > 3,5-diCQA > 4,5-diCQA > 5-CQA, suggesting that the addition of caffeoyl moiety significantly increased the binding capacity. Thermodynamic analysis showed that the ΔHand ΔSvalues were both positive and the ΔGwas negative, indicating that the interaction process was spontaneous, and hydrophobic force might be primarily responsible for the interaction. In addition, the conformational change of BSA was observed by 3D fluorescence and synchr onous fluorescence spectra, indicating that the interaction between CQA and BSA was achieved through the binding of CQA to the tryptophan and tyrosine residues of BSA.
Kudingcha; caffeoylquinic acid; bovine serum albumin; fluorescence spectroscopy; interaction
TS272;TS201.3
1002-6630(2015)11-0006-07
10.7506/spkx1002-6630-201511002
2015-01-26
國家自然科學基金面上項目(31171666);江蘇高校優勢學科建設工程資助項目(PAPD)
徐冬蘭(1990—),女,碩士研究生,研究方向為食品生物技術。E-mail:2013108031@njau.edu.cn
*通信作者:孫怡(1966—),女,高級實驗師,博士,研究方向為食品營養與化學。E-mail:sunyi01@njau.edu.cn

