抗壞血酸/半胱氨酸體系美拉德反應(yīng)形成風(fēng)味物質(zhì)動(dòng)力學(xué)
唐樂(lè)攀,楊小洪,余愛(ài)農(nóng),*
抗壞血酸/半胱氨酸體系美拉德反應(yīng)形成風(fēng)味物質(zhì)動(dòng)力學(xué)
唐樂(lè)攀1,2,楊小洪2,余愛(ài)農(nóng)1,2,*
(1.生物資源保護(hù)與利用湖北省重點(diǎn)實(shí)驗(yàn)室,湖北 恩施 445000;2.湖北民族學(xué)院化學(xué)與環(huán)境工程學(xué)院,湖北 恩施 445000)
在抗壞血酸/半胱氨酸體系中,應(yīng)用溶劑萃取法對(duì)美拉德反應(yīng)形成的特征風(fēng)味物質(zhì)進(jìn)行富集,通過(guò)氣相色譜-質(zhì)譜聯(lián)用儀(gas chromatography-mass spectrometry,GC-MS)和氣相色譜-氫火焰離子化檢測(cè)器(gas chromatography-flame ionization detector,GC-FID)進(jìn)行定性研究和準(zhǔn)確的定量分析,研究其反應(yīng)動(dòng)力學(xué)。結(jié)果表明:基于抗壞血酸的美拉德反應(yīng)與傳統(tǒng)的美拉德反應(yīng)存在明顯差異,主要表現(xiàn)在起始反應(yīng)溫度和風(fēng)味物質(zhì)的種類(lèi)及動(dòng)力學(xué)上。對(duì)特征風(fēng)味物質(zhì)進(jìn)行動(dòng)力學(xué)分析發(fā)現(xiàn),2-乙酰基噻吩和3-乙酰基噻吩由于結(jié)構(gòu)相似,含量及動(dòng)力學(xué)表現(xiàn)也極為相似;2-丙基四氫噻吩在高溫下濃度會(huì)先升高后降低,最終均穩(wěn)定在0.035 mmol/L左右;2-甲基-4-丙基噻唑和2-乙酰基噻唑含量差別很大,表明兩者生成機(jī)理完全不同;2-甲基四氫噻吩-3-酮和四氫噻吩-3-酮結(jié)構(gòu)相似,但后者會(huì)進(jìn)一步反應(yīng)使得兩者含量差別較大;甲基吡嗪的生成滿(mǎn)足零級(jí)動(dòng)力學(xué),且反應(yīng)溫度高于125 ℃時(shí)其生成速率基本保持不變。
美拉德反應(yīng);風(fēng)味物質(zhì);動(dòng)力學(xué)
美拉德(Maillard)反應(yīng)是食品加工和貯藏過(guò)程中發(fā)生的最主要的非酶褐變反應(yīng)之一,其實(shí)質(zhì)是羰基化合物和氨基化合物在一定溫度下發(fā)生的一系列復(fù)雜反應(yīng)的總稱(chēng)[1]。由于該反應(yīng)可造成食品營(yíng)養(yǎng)價(jià)值的改變,使食品顏色加深,產(chǎn)生特殊的揮發(fā)性產(chǎn)物,賦予或改變食品的風(fēng)味[2],因此在食品工業(yè)中有著特殊的地位。特別是隨著人們更加深入地研究,發(fā)現(xiàn)使用美拉德反應(yīng)制備的香料具有香味更加自然濃厚的特點(diǎn),因此美拉德反應(yīng)形成風(fēng)味物質(zhì)的研究受到廣泛重視。
目前對(duì)于美拉德反應(yīng)形成風(fēng)味物質(zhì)的研究多集中于產(chǎn)物種類(lèi)的分析、反應(yīng)條件的影響和生成機(jī)理的研究上[3-7]。但是由于美拉德反應(yīng)的復(fù)雜性,使得反應(yīng)程度往往難以把握,一般的定性研究并不能對(duì)香味物質(zhì)進(jìn)行控制和預(yù)測(cè),而以定量為基礎(chǔ)的動(dòng)力學(xué)研究并不多見(jiàn)。其次,美拉德反應(yīng)研究體系多以還原糖為主,而抗壞血酸作為一個(gè)在美拉德反應(yīng)中引起廣泛注意且具有潛在羰基組分的化合物[8],廣泛存在于植物性食物及動(dòng)物食品中,但是對(duì)其研究卻并不多見(jiàn)。就抗壞血酸和半胱氨酸體系而言,Adams等[9]研究了在干燥、烘烤、無(wú)溶劑、K2CO3存在等條件下抗壞血酸與半胱氨酸反應(yīng)形成呋喃類(lèi)化合物和噻吩類(lèi)化合物,其他研究工作主要由本課題組完成的,包括pH值、金屬離子、尿素以及肌肽等對(duì)揮發(fā)性物質(zhì)種類(lèi)的影響及其形成機(jī)理[10-13],而有關(guān)抗壞血酸/半胱氨酸體系美拉德反應(yīng)動(dòng)力學(xué)研究均未見(jiàn)文獻(xiàn)報(bào)道。
對(duì)美拉德反應(yīng)進(jìn)行反應(yīng)動(dòng)力學(xué)研究,可預(yù)測(cè)反應(yīng)速率控制點(diǎn)以及對(duì)反應(yīng)的進(jìn)程進(jìn)行最優(yōu)設(shè)計(jì)和最優(yōu)控制。本實(shí)驗(yàn)以抗壞血酸和半胱氨酸美拉德體系為基礎(chǔ),使用溶劑萃取法對(duì)產(chǎn)生的風(fēng)味物質(zhì)進(jìn)行富集、濃縮,應(yīng)用氣相色譜-氫火焰離子化檢測(cè)器(gas chromatography-flame ionization detector,GC-FID)以及氣相色譜-質(zhì)譜聯(lián)用儀(gas chromatography-mass spectrometry,GC-MS)、標(biāo)準(zhǔn)物質(zhì)和線(xiàn)性保留指數(shù)(linear retention index,LRI)對(duì)不同溫度條件下風(fēng)味物質(zhì)進(jìn)行定量以及定性分析。選取分離度、峰型較好,LRI之間誤差較小,GC-MS相似度較高的特征風(fēng)味成分作為研究對(duì)象。通過(guò)GC-FID進(jìn)行準(zhǔn)確定量并找到其含量隨溫度、時(shí)間變化關(guān)系,分析其動(dòng)力學(xué),為今后對(duì)于基于抗壞血酸的風(fēng)味物質(zhì)生成的控制和預(yù)測(cè)提供理論依據(jù)。
1 材料與方法
1.1 材料與試劑
L-抗壞血酸、L-半胱氨酸、磷酸氫二鈉、磷酸二氫鈉、氫氧化鈉、無(wú)水硫酸鈉(均為分析純) 上海國(guó)藥集團(tuán)化學(xué)試劑有限公司;乙醚(分析純) 上海嘉定馬陸化工廠(chǎng)有限公司;正十三烷、C5~C22正構(gòu)烷烴美國(guó)Sigma-Aldrich公司;四氫噻吩-3-酮、3-乙酰基噻吩、2-乙酰基噻吩 比利時(shí)Acros Organics公司;2-甲基-四氫噻吩-3-酮、3-甲基-2-乙酰基噻吩、噻吩(3-2-b)并噻吩 東京Chemical Industry公司;2-乙酰基噻唑、2-甲基吡嗪 中國(guó)百靈威化學(xué)技術(shù)有限公司。
1.2 儀器與設(shè)備
GC-MS 6890N氣相色譜-5975I質(zhì)譜聯(lián)用儀、1260高效液相色譜儀(配有二極管陣列檢測(cè)器)、6890N氣相色譜儀(配有FID檢測(cè)器) 美國(guó)安捷倫科技公司;干浴式氮吹儀 上海安普科學(xué)儀器有限公司;BS-124S電子天平 德國(guó)賽多利斯公司;P160001厚壁耐壓瓶 北京欣維爾玻璃儀器有限公司。
1.3 方法
1.3.1 色譜條件
色譜柱:安捷倫HP-5毛細(xì)管色譜柱(30 m× 0.25 mm,0.25μm);進(jìn)樣量2μL;進(jìn)樣口溫度270 ℃;不分流進(jìn)樣;載氣流量0.9 mL/min;程序升溫:柱溫初始40 ℃,保持5 min,以4 ℃/min上升至260 ℃,然后以15 ℃/min上升至280 ℃,保持1 min。GC-FID和GC-MS采用同樣的色譜條件。
1.3.2 質(zhì)譜條件
電子轟擊離子源;電子能量70 eV;接口溫度280 ℃;離子源溫度230 ℃;四極桿溫度150 ℃;電離電壓70 eV;電子倍增電壓1 753 V;掃描速率1 scan/s;質(zhì)量掃描范圍30~400 amu。
1.3.3 內(nèi)標(biāo)的配制
用微量移液器準(zhǔn)確吸取60 μL正十三烷(0.06 mL,45.6 mg,質(zhì)量濃度為0.76 g/mL)并溶解于20 mL無(wú)水乙醚中。此內(nèi)標(biāo)相當(dāng)于2.28 mg/mL的正十三烷乙醚溶液[14]。現(xiàn)配現(xiàn)用。
1.3.4 反應(yīng)液的制備
[10],用電子天平準(zhǔn)確稱(chēng)取0.880 7 g(0.005 mol)L-抗壞血酸和0.605 8 g(0.005 mol)L-半胱氨酸溶解于50 mL 0.2 mol/L pH 8的Na2HPO4-NaH2PO4緩沖液中,再用適量NaOH調(diào)pH值至8并裝入P160004厚壁耐壓反應(yīng)瓶中密封。在125、135、140、145、155 ℃條件下分別反應(yīng)60、90、120、150、180、210 min,反應(yīng)完成后取出快速冷卻。每份樣品均反應(yīng)3 份作為平行樣。
1.3.5 風(fēng)味物質(zhì)的萃取及濃縮
向50 mL反應(yīng)液中加入100 μL上述內(nèi)標(biāo)溶液(相當(dāng)于0.228 mg正十三烷),分別用20、20、15、15 mL無(wú)水乙醚萃取4 次[15-16],合并萃取液,并加入適量無(wú)水硫酸鈉干燥2 h。待干燥完成,倒出萃取液,使用氮吹儀濃縮至約2 mL,轉(zhuǎn)移至氣相色譜進(jìn)樣瓶準(zhǔn)備進(jìn)樣。
2 結(jié)果與分析
2.1 反應(yīng)溫度對(duì)產(chǎn)物生成的影響
使用GC-FID對(duì)不同溫度下反應(yīng)不同時(shí)間形成的揮發(fā)物進(jìn)行分析,圖1和圖2分別是125 ℃反應(yīng)60 min和140 ℃反應(yīng)60 min樣品的色譜圖。由圖1可知,在125 ℃條件下,反應(yīng)60 min后樣品中除了內(nèi)標(biāo)物質(zhì)外,基本上沒(méi)有檢測(cè)出其他物質(zhì),表明此溫度下美拉德反應(yīng)十分緩慢,幾乎沒(méi)有風(fēng)味物質(zhì)產(chǎn)生。這與經(jīng)典的美拉德反應(yīng)有著較大的差異,傳統(tǒng)的還原糖和氨基酸之間的美拉德反應(yīng)最高溫度一般只有110 ℃,最低在80 ℃下就能夠反應(yīng)[17],說(shuō)明基于抗壞血酸的美拉德反應(yīng)有著特殊的性質(zhì),值得進(jìn)一步深入研究。當(dāng)反應(yīng)溫度上升至140 ℃后,反應(yīng)風(fēng)味物質(zhì)含量及種類(lèi)都有明顯的增加[10],大致上,一般食品加工溫度在160 ℃以?xún)?nèi),否則會(huì)損失營(yíng)養(yǎng)物質(zhì),因此本實(shí)驗(yàn)選擇以140 ℃為中心,研究125~155 ℃條件下溫度對(duì)風(fēng)味物質(zhì)動(dòng)力學(xué)特征的影響。
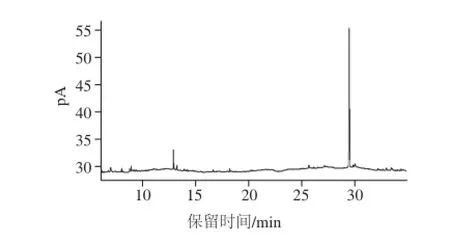
圖1 125 ℃反應(yīng)60 min風(fēng)味物質(zhì)氣相色譜圖Fig.1 GC chromatogram of volatile flavor compounds formed by Maillard reaction at 125 ℃ for 60 min
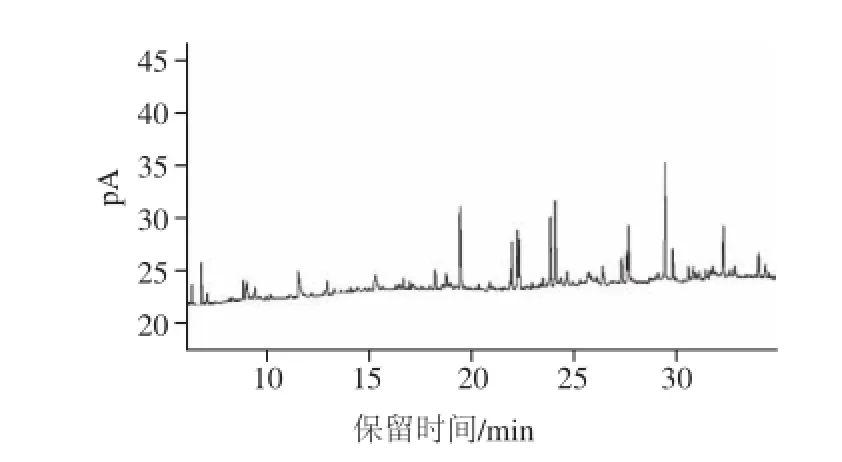
圖2 140 ℃反應(yīng)60 min風(fēng)味物質(zhì)氣相色譜圖Fig.2 GC chromatogram of volatile flavor compounds formed by Maillard reaction at 140 ℃ for 60 min
2.2 樣品中風(fēng)味物質(zhì)的定性分析
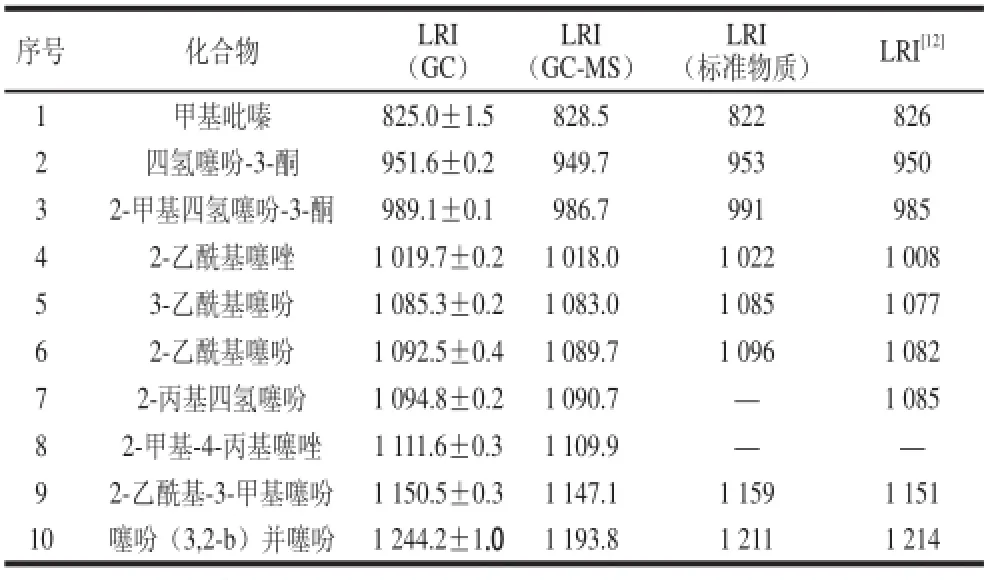
表1 風(fēng)味物質(zhì)線(xiàn)性保留指數(shù)的鑒定Table 1 Identification of volatile favor compounds by LRI
根據(jù)實(shí)驗(yàn)溫度范圍,選取具有代表性的125、140、155 ℃,反應(yīng)時(shí)間為120 min的3 組樣品,在上述GC-MS條件下進(jìn)行分析,并通過(guò)質(zhì)譜數(shù)據(jù)庫(kù)對(duì)各個(gè)峰進(jìn)行初步定性。其次,分別在GC和GC-MS中測(cè)定C5~C22正構(gòu)烷烴,計(jì)算各樣品中所有物質(zhì)的LRI取平均值。之后,挑選標(biāo)準(zhǔn)物質(zhì)分批進(jìn)行GC分析,并根據(jù)C5~C22正構(gòu)烷烴保留時(shí)間計(jì)算標(biāo)準(zhǔn)物質(zhì)的LRI。最后查找相關(guān)文獻(xiàn),確定化合物的LRI[12]。表1為相應(yīng)10 種化合物的LRI。
通過(guò)比較色譜圖,選取分離度、峰型較好,LRI之間誤差較小,GC-MS相似度較高的化合物作為本實(shí)驗(yàn)的研究對(duì)象。
2.3 風(fēng)味物質(zhì)形成的動(dòng)力學(xué)
通過(guò)2.2節(jié)對(duì)化合物的定性分析,根據(jù)GC色譜圖中各物質(zhì)與內(nèi)標(biāo)物的峰面積比,換算出各化合物的濃度隨時(shí)間的變化關(guān)系。
2.3.1 噻吩類(lèi)
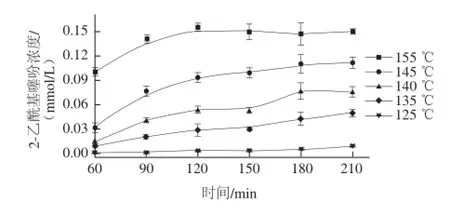
圖3 不同溫度條件下2-乙酰基噻吩濃度隨時(shí)間的變化Fig. 3 2-Acetylthiophene production at a function of reaction time at different temperatures
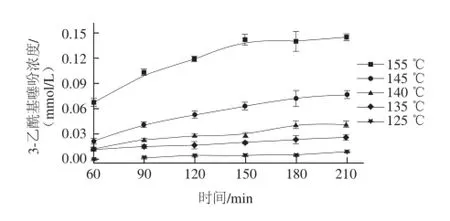
圖4 不同溫度條件下3-乙酰基噻吩濃度隨時(shí)間的變化Fig.4 3-Acetylthiophene production as a function of reaction time atdifferent temperatures
圖3、4分別是不同溫度條件下2-乙酰基噻吩和3-乙酰基噻吩濃度隨時(shí)間變化關(guān)系。兩種物質(zhì)結(jié)構(gòu)相似,只是取代基的位置不同,故其含量及動(dòng)力學(xué)表現(xiàn)也極為相似。兩種物質(zhì)的含量均隨著溫度的升高及加熱時(shí)間的延長(zhǎng)而增加,并在155 ℃條件下穩(wěn)定在0.15 mmol/L左右。當(dāng)反應(yīng)溫度由145 ℃升高到155 ℃時(shí),60 min時(shí)兩種物質(zhì)含量均變化明顯,增加了近3 倍。2-乙酰基噻吩由0.034 1 mmol/L升高至0.099 9 mmol/L,3-乙酰基噻吩由0.021 5 mmol/L升高至0.067 4 mmol/L。
考察兩種物質(zhì)濃度隨時(shí)間的變化關(guān)系,發(fā)現(xiàn)其變化滿(mǎn)足零級(jí)動(dòng)力學(xué)方程。分別對(duì)其擬合得到相應(yīng)的表觀速率常數(shù)(k),見(jiàn)表2。
在低溫125 ℃條件下,兩種物質(zhì)的表觀速率常數(shù)基本相同,這是由于低溫條件下兩種物質(zhì)生成都較慢,故差別不大。但是隨著溫度的升高,2-乙酰基噻吩的表觀速率常數(shù)增加更快,表明高溫更有利于 其生成。
圖5為2-丙基四氫噻吩濃度隨時(shí)間的變化關(guān)系,其與上述兩種化合物差異較大。當(dāng)溫度達(dá)到140 ℃以上時(shí),2-丙基四氫噻吩濃度會(huì)先增加至約0.055 mmol/L,之后隨著反應(yīng)時(shí)間的增加,濃度會(huì)逐漸減小,最終穩(wěn)定在0.035 mmol/L左右。可能原因是較高溫度條件下,2-丙基四氫噻吩會(huì)繼續(xù)發(fā)生其他反應(yīng)而被消耗。
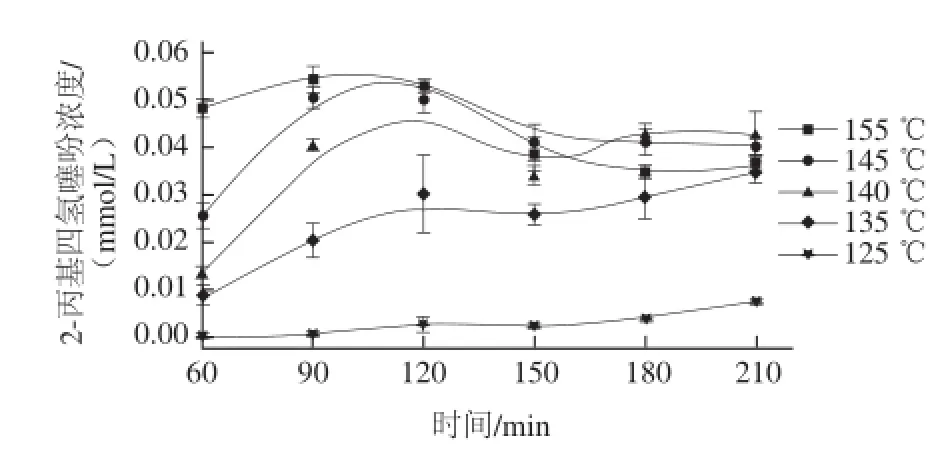
圖5 不同溫度條件下2-丙基四氫噻吩濃度隨時(shí)間變化Fig.5 2-Propyltetrahydrothiophene production as a function ofreaction time at different temperatures
2.3.2 噻吩酮類(lèi)
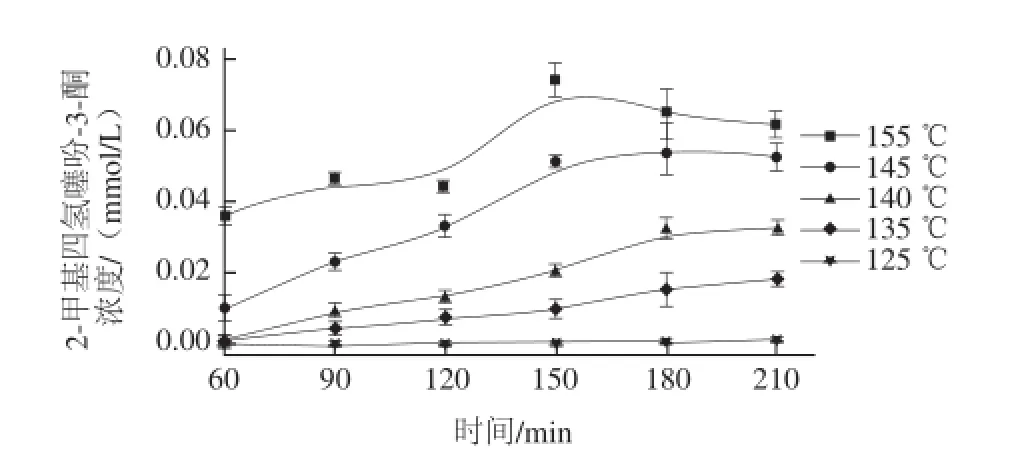
圖6 2-甲基四氫噻吩-3-酮濃度隨時(shí)間變化Fig.6 2-Methyltetrahydrothiophen-3-one production as a function of reaction time at different temperatures
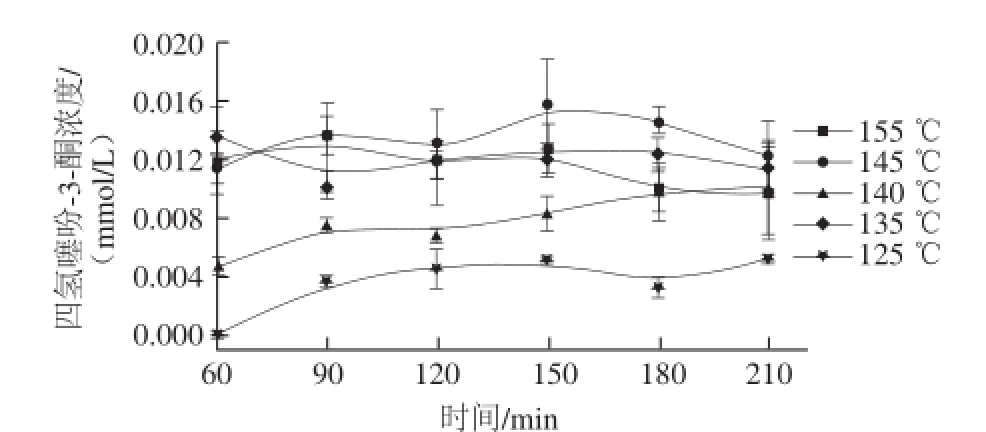
圖7 四氫噻吩-3-酮濃度隨時(shí)間變化Fig.7 Tetrahydrothiophen-3-one production as a function of reaction time at different temperatures
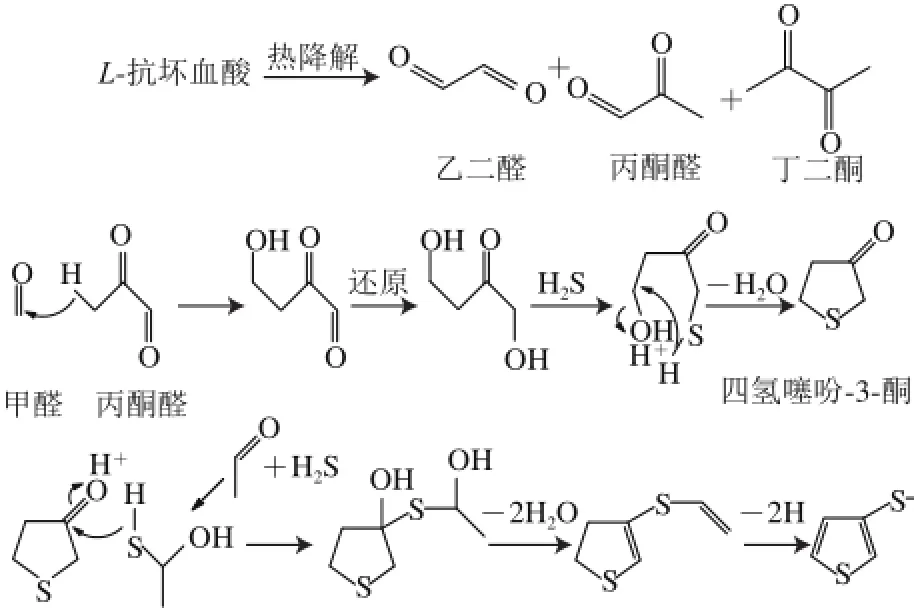
圖8 四氫噻吩-3-酮進(jìn)一步反應(yīng)機(jī)理[133,,1188]]Fig.8 Proposed formation mechanism of tetrahydrothiophen-3-one[13,18]
2-甲基四氫噻吩-3-酮和四氫噻吩-3-酮的濃度隨時(shí)間變化的關(guān)系分別見(jiàn)圖6和圖7。雖然兩種物質(zhì)結(jié)構(gòu)類(lèi)似,但是濃度變化趨勢(shì)都完全不同,表明其生成機(jī)理也完全不同。據(jù)文獻(xiàn)[13,18]報(bào)道,抗壞血酸會(huì)按照?qǐng)D8所示的途徑發(fā)生自身熱解反應(yīng),之后進(jìn)一步反應(yīng)生成噻吩酮類(lèi)。由圖8可知,抗壞血酸分解后生成的四氫噻吩-3-酮會(huì)進(jìn)一步與巰基加成,生成新的化合物,導(dǎo)致其含量比2-甲基四氫噻吩-3-酮低。
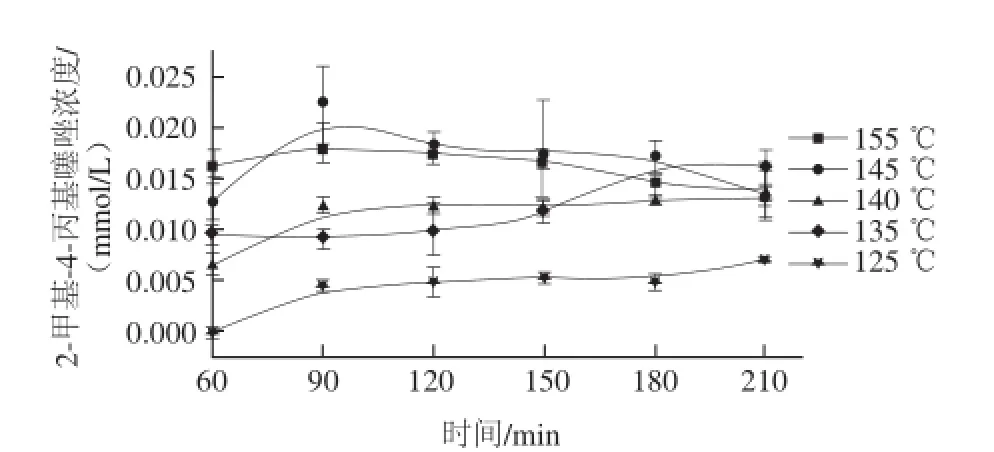
圖9 2-甲基-4-丙基噻唑濃度隨時(shí)間的變化Fig.9 2-Methyl-4-propylthiazole production as a function of reaction time at different temperatures
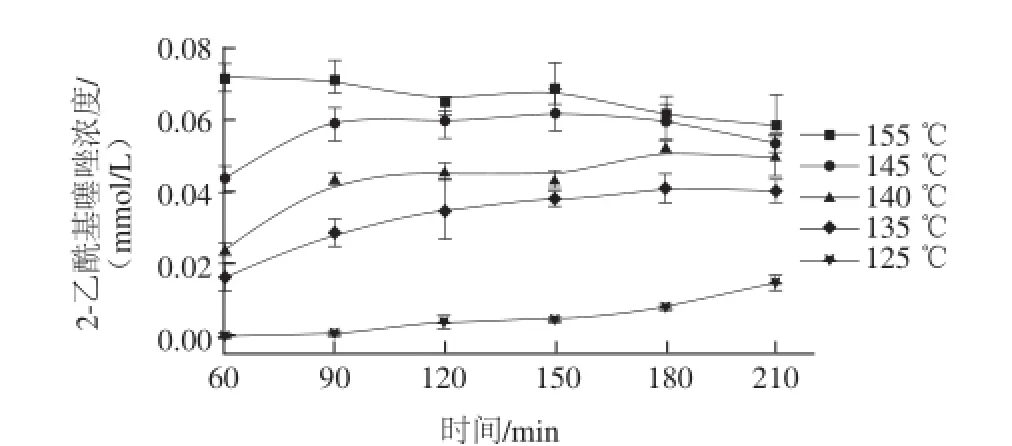
圖10 2-乙酰基噻唑濃度隨時(shí)間的變化Fig.10 2-Acetylthiazole production as a function of reaction time at different temperatures
2.3.3 噻唑類(lèi)
由圖9、10可知,兩種噻唑濃度差別很大,2-甲基-4-丙基噻唑濃度最高只有0.02 mmol/L,且溫度繼續(xù)升高,其含量基本保持不變。相同溫度條件下,2-乙酰基噻唑的濃度更高,且其濃度隨時(shí)間變化較明顯。當(dāng)溫度從145 ℃升高到155 ℃時(shí),反應(yīng)60 min后其濃度由0.043 mmol/L升高到了0.073 mmol/L,但之后濃度開(kāi)始下降,最后穩(wěn)定在0.06 mmol/L。
2.3.4 吡嗪類(lèi)
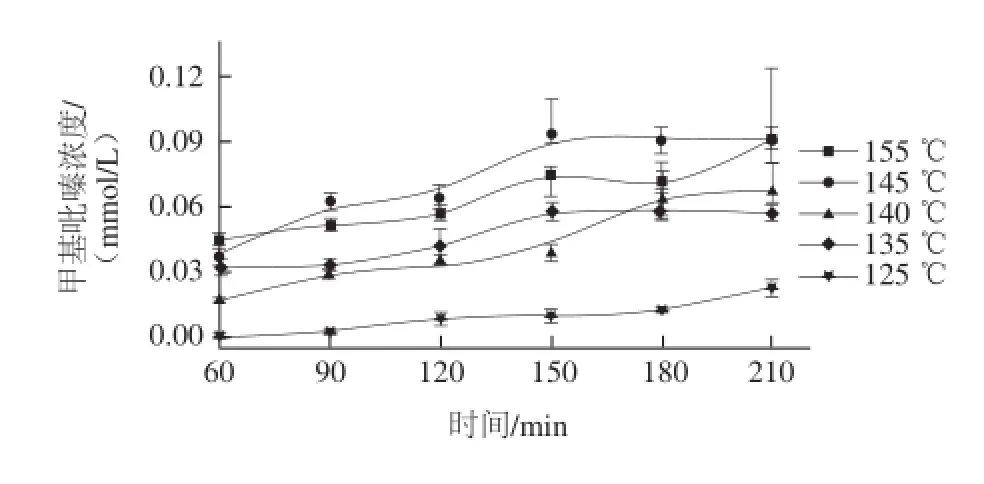
圖11 甲基吡嗪濃度隨時(shí)間的變化Fig.11 Methylpyrazine production as a function of reaction time at different temperatures
由圖11可知,反應(yīng)溫度高于125 ℃時(shí),甲基吡嗪的生成濃度顯著高于125 ℃時(shí)的生成濃度,即使在125 ℃條件下,反應(yīng)210 min也只有少量甲基吡嗪生成,說(shuō)明在本實(shí)驗(yàn)體系中,只有在135 ℃以上時(shí)才能形成具有燒烤風(fēng)味的甲基吡嗪。
根據(jù)實(shí)驗(yàn)數(shù)據(jù),分別與零、一、二級(jí)動(dòng)力學(xué)模型進(jìn)行擬合,結(jié)果發(fā)現(xiàn)甲基吡嗪的生成滿(mǎn)足零級(jí)動(dòng)力學(xué),與文獻(xiàn)[19]報(bào)道相一致,并計(jì)算得到相應(yīng)的表觀速率常數(shù),見(jiàn)表3。

表3 不同溫度下甲基吡嗪的表觀速率常數(shù)Table 3 Apparent rate constants of methylpyrazine at different temperatures
由表3可知,除了最低溫度125 ℃之外,其他所有溫度條件下甲基吡嗪的表觀速率常數(shù)基本相同,表明當(dāng)溫度升高到一定程度時(shí),其生成速率與溫度的關(guān)系不再明顯,與文獻(xiàn)[19]報(bào)道結(jié)果相一致。其原因可能是受反應(yīng)機(jī)理的影響,據(jù)相關(guān)文獻(xiàn)報(bào)道[20],吡嗪類(lèi)化合物的生成與氨基酸的降解有關(guān),當(dāng)溫度高于125 ℃時(shí),半胱氨酸很快會(huì)分解完全,導(dǎo)致吡嗪類(lèi)化合物前體物迅速積累,故繼續(xù)升溫并不會(huì)繼續(xù)影響其反應(yīng)速率。
3 結(jié) 論
本實(shí)驗(yàn)使用溶劑萃取法,通過(guò)GC-MS和GC-FID對(duì)噻吩、噻唑、吡嗪等特征風(fēng)味物質(zhì)進(jìn)行了定性定量分析。結(jié)果發(fā)現(xiàn)在低溫條件下(125 ℃)基本上沒(méi)有檢測(cè)出除了內(nèi)標(biāo)物質(zhì)外的其他物質(zhì),說(shuō)明抗壞血酸/半胱氨酸體系在125 ℃以下美拉德反應(yīng)緩慢,與傳統(tǒng)美拉德反應(yīng)存在較大差異。
對(duì)特征風(fēng)味物質(zhì)進(jìn)行動(dòng)力學(xué)分析發(fā)現(xiàn),不同溫度條件下2-乙酰基噻吩和3-乙酰基噻吩濃度隨時(shí)間變化趨勢(shì)相近,可能原因是兩者結(jié)構(gòu)相似,因此生成機(jī)理相同。低溫條件下兩種物質(zhì)的表觀速率常數(shù)基本相同,但是隨著溫度的升高,2-乙酰基噻吩的生成速率增加更快;較高溫度條件下,2-丙基四氫噻吩濃度隨著反應(yīng)時(shí)間的延長(zhǎng)而增加,但之后逐漸減小,最終穩(wěn)定在0.035 mmol/L左右;2-甲基四氫噻吩-3-酮和四氫噻吩-3-酮兩種物質(zhì)雖然結(jié)構(gòu)類(lèi)似,但是含量卻差別較大,表明其生成機(jī)理完全不同,且四氫噻吩-3-酮會(huì)繼續(xù)參與反應(yīng)生成新的化合物;兩種噻唑類(lèi)物質(zhì)2-甲基-4-丙基噻唑和2-乙酰基噻唑濃度隨時(shí)間變化趨勢(shì)也不盡相同,表明兩種物質(zhì)的生成機(jī)理不同;通過(guò)研究甲基吡嗪濃度變化發(fā)現(xiàn),當(dāng)溫度升高到一定程度時(shí),其生成速率保持不變,與文獻(xiàn)[19]的報(bào)道相一致。
參考文獻(xiàn):
[1] HODGE J E. Dehydrated foods, chemistry of browning reactions in model systems[J]. Journal of Agricultural and Food Chemistry, 1953, 1(15): 928-943.
[2] SILVAN J M, van de LAGEMAAT J, OLANO A, et al. Analysis and biological properties of amino acid derivates formed by Maillard reaction in foods[J]. Journal of Pharmaceutical and Biomedical Analysis, 2006, 41(5): 1543-1551.
[3] UMANO K, HAGI Y, NAKAHARA K, et al. Volatile chemicals formed in the headspace of a heated D-glucose/L-cysteine Maillard model system[J]. Journal of Agricultural and Food Chemistry, 1995, 43(8): 2212-2218.
[4] CERNY C. Origin of carbons in sulfur-containing aroma compounds from the Maillard reaction of xylose, cysteine and thiamine[J]. LWTFood Science and Technology, 2007, 40(8): 1309-1315.
[5] CERNY C, BRIFFOD M. Effect of pH on the Maillard reaction of [13C5] xylose, cysteine, and thiamin[J]. Journal of Agricultural and Food Chemistry, 2007, 55(4): 1552-1556.
[6] AMES J M, GUY R C, KIPPING G J. Effect of pH and temperature on the formation of volatile compounds in cysteine/reducing sugar/starch mixtures during extrusion cooking[J]. Journal of Agricultural and Food Chemistry, 2001, 49(4): 1885-1894.
[7] MOTTRAM D S, NOBREGA I C C. Formation of sulfur aroma compounds in reaction mixtures containing cysteine and three different forms of ribose[J]. Journal of Agricultural and Food Chemistry, 2002, 50(14): 4080-4086.
[8] ROGACHEVA S M, KUNCHEVA M J, PANCHEV I, et al. L-ascorbicacid in nonenzymatic reactions. I. Reaction with glycine[J]. Zeitschrift für Lebensmittel-Untersuchung und-Forschung A, 1995, 200(1): 52-58.
[9] ADAMS A, de KIMPE N. Formation of pyrazines from ascorbic acid and amino acids under dry-roasting conditions[J]. Food Chemistry, 2009, 115(4): 1417-1423.
[10] YU Ainong, ZHANG Aidong. Aroma compounds generated from thermal reaction of L-ascorbic acid with L-cysteine[J]. Food Chemistry, 2010, 121(4): 1060-1065.
[11] YU Ainong, TAN Zhiwei, SHI Boan. Influence of the pH on the formation of pyrazine compounds by the Maillard reaction of L-ascorbic acid with acidic, basic and neutral amino acids[J]. Asia-Pacifi c Journal of Chemical Engineering, 2012, 7(3): 455-462.
[12] 劉應(yīng)煊. 抗壞血酸與半胱氨酸的Maillard反應(yīng)形成香味化合物的研究[D]. 武漢: 中國(guó)地質(zhì)大學(xué), 2010: 17-23.
[13] YU Ainong, TAN Zhiwei, WANG Fasong. Mechanism of formation of sulphur aroma compounds from L-ascorbic acid and L-cysteine during the Maillard reaction[J]. Food Chemistry, 2012, 132(3): 1316-1323.
[14] BAISIER W M, LABUZA P L. Maillard browning kinetics in a liquid model system[J]. Journal of Agricultural and Food Chemistry, 1992, 40(5): 707-713.
[15] CHEN J H, HO C T. Comparison of volatile generation in serine/ threonine/glutamine-ribose/glucose/fructose model systems[J]. Journal of Agricultural and Food Chemistry, 1999, 47(2): 643-647.
[16] CHEN Yong, XING Jinsong, CHIN C K, et al. Effect of urea on volatile generation from Maillard reaction of cysteine and ribose[J]. Journal of Agricultural and Food Chemistry, 2000, 48(8): 3512-3516.
[17] ZHANG Zhouyao, PAWLISZYN J. Headspace solid-phase microextraction[J]. Analytical Chemistry, 1993, 65(14): 1843-1852.
[18] YU Ainong, TAN Zhiwei, WANG Fasong. Mechanistic studies on the formation of pyrazines by Maillard reaction between L-ascorbic acid and L-glutamic acid[J]. LWT-Food Science and Technology, 2013, 50(1): 64-71.
[19] JOUSSE F, JONGEN T, AGTEROF W, et al. Simplified kinetic scheme of flavor formation by the Maillard reaction[J]. Journal of Food Science, 2002, 67(7): 2534-2542.
[20] YU Ainong, ZHANG Aidong. The effect of pH on the formation of aroma compounds produced by heating a model system containing L-ascorbic acid with L-threonine/L-serine[J]. Food Chemistry, 2010, 119(1): 214-219.
Kinetic Study of Volatile Favor Compound Formation in Ascorbic Acid-Cysteine Maillard Reaction System
TANG Lepan1,2, YANG Xiaohong2, YU Ainong1,2,*
(1. Key Laboratory of Biological Resources Protection and Utilization of Hubei Province, Enshi 445000, China; 2. School of Chemistry and Environmental Engineering, Hubei University for Nationalities, Enshi 445000, China)
This study is based on the ascorbic acid-cysteine Maillard reaction system. The volatile favor compounds were enriched by solvent extraction and analyzed qualitatively and quantitatively by GC-MS and GC-FID. The kinetics of their formation was studied. The results indicated that Maillard reaction based on ascorbic acid was quite different from the conventional one. The kinetic changes of 2-acetylthiophene and 3-acetylthiophene were resembled because of their similar structures. At higher temperature, the concentration of 2-propyltetrahydr othiophene increased at fi rst and then decreased to 0.035 mmol/L. The widely varying concentrations of 2-methyl-4-propylthiazole and 2-acetylthiazole were due to different generation mechanisms. Although the molecular structures of 2-methyltetrahydrothiophen-3-one and tetrahydrothiophen-3-one were similar, the latter one could conduct further reaction, thereby leading to a decrease in its concentration. The generation of methylpyrazine was a zero-order reaction and the rate remained the same at a temperature above 125 ℃.
Maillard reaction; volatiles; kinetics
TS201.2
A
10.7506/spkx1002-6630-201511006
2014-08-11
國(guó)家自然科學(xué)基金地區(qū)科學(xué)基金項(xiàng)目(31360408)
唐樂(lè)攀(1989—),男,碩士,研究方向?yàn)槭称坊瘜W(xué)。E-mail:809328707@qq.com
*通信作者:余愛(ài)農(nóng)(1963—),男,教授,博士,研究方向?yàn)槭称坊瘜W(xué)。E-mail:anyufoodchem@hotmail.com

