自體脂肪干細胞移植治療2型糖尿病的安全性及有效性
張新,周玉紅,白云
(遼河油田總醫院內分泌科,遼寧 盤錦 124010)
自體脂肪干細胞移植治療2型糖尿病的安全性及有效性
張新,周玉紅,白云
(遼河油田總醫院內分泌科,遼寧 盤錦 124010)
目的探討自體脂肪干細胞(ADSCs)移植治療2型糖尿病的安全性和有效性。方法培養自體ADSCs,并進行鑒定。將2型糖尿病患者48例分為2組:A組(n=24)行ADSCs移植聯合常規治療,B組(n=24)行常規治療。隨訪觀察15個月,分析2組患者治療時和治療后3、6、12、15個月的空腹血糖(FPG)、餐后2 h血糖(2h-PGh)、糖化血紅蛋白(HbA1c)、空腹C肽(FC-P)、C肽曲線下面積(AUCC)、胰島素劑量、不良反應的情況。結果培養的ADSCs符合自體臨床應用標準。與治療前相比,2組患者FPG、2h-PGh和HbA1c都有明顯降低,且A組降低更顯著;A組在FC-P、AUCC和胰島素用量方面的改善明顯優于B組。在干細胞治療過程中無明顯不良反應。結論采用自體ADSCs移植可以安全有效地治療2型糖尿病。
2型糖尿病;自體脂肪干細胞;移植;安全性和有效性
糖尿病已成為繼心腦血管疾病和腫瘤之后的第三大非傳染性疾病,且其中90%以上為2型糖尿病[1]。目前,臨床上治療2型糖尿病主要是通過飲食、運動、藥物和注射胰島素治療,但常常無法取得滿意的效果。近年來,隨著干細胞研究的不斷深入,成體干細胞尤其是間充質干細胞(mesenchymal stem cells,MSC),因具有取材方便、多向分化和自我更新等特點,被部分研究者用于2型糖尿病的臨床治療,并取得了較好的短期療效,為治愈2型糖尿病帶來了希望[2,3]。本研究將人體儲量大、干細胞獲得率較高的自體脂肪干細胞(autologous adipose-derived stem cells,ADSCs)用于2型糖尿病患者的自體移植,并通過隨訪觀察對其療效和安全性做出初步評價。
1 材料與方法
1.1 一般資料
選擇2011年9月至2013年6月于我院就診的2型糖尿病患者48例,采用單盲實驗設計,按照隨機數字表法分為A組和B組,每組24例。A組行干細胞移植聯合常規治療,B組單純行常規治療,2組常規治療方案一致。本研究經本院倫理委員會討論通過,患者知情同意。本研究符合赫爾辛基宣言和國家衛生計生委關于干細胞臨床研究的管理辦法。
納入標準:符合1999年WHO關于糖尿病的診斷標準和分型標準;年齡16~65歲,性別不限;服用藥物或注射胰島素控制血糖。排除標準:嚴重心、肝、腎功能不全;消耗性疾病;其他內分泌系統疾病;有血液系統疾病或出血傾向;發生嚴重不良事件或不能耐受者。
1.2 ADSCs移植
ADSCs培養:從患者腹部取脂肪組織,用Ⅳ型膠原酶(Sigma公司,美國)消化后,離心。將收集到的有核細胞用無血清培養液(Gibco公司,美國)接種到6孔板中,置于37℃、5%CO2培養箱培養;48 h后,觀察細胞貼壁,此后每隔3 d換液1次,待細胞生長至80%~90%融合時,進行1∶3傳代。
ADSCs鑒定:(1)用倒置顯微鏡觀察記錄ADSCs形態;(2)用MTT方法檢測ADSCs接種后第1、2、3、5、6、7天細胞存活率,并繪制生長曲線;(3)用流式細胞儀檢測ADSCs表面標記CD105、CD90、CD73和CD34、CD45、HLA-DR的表達量;(4)用成骨、成脂誘導液誘導ADSCs向骨和脂肪2個方向分化,并分別用茜素紅和油紅O染液進行染色后在顯微鏡下拍照,以檢測ADSCs多向分化能力;(5)檢測移植前ADSCs存活率和內毒素。
ADSCs移植:培養的ADSCs收獲后用生理鹽水重懸,按1×107/kg體質量進行靜脈回輸,移植后患者留院觀察4 h。
1.3 療效觀察判定方法及安全性評價
記錄患者性別、年齡、病程、煙酒史、身高和治療前后的體質量等一般資料,并計算體重指數(body mass index,BMI)=體質量(kg)/身高2(m2)。實驗室檢查治療前后2組患者的空腹血糖(fasting plasma glucose,FPG),餐后2 h血糖(2 h postprandial blood glucose,2h-PGh),糖化血紅蛋白(glycosylated hemoglobin,HbA1c),空腹C肽(fasting C-peptide,FCP),C肽曲線下面積(area under curve for C-peptide,AUCC)。AUCC=0.5×FC-P0 h+FC-P0.5 h+FC-P1 h+FC-P2 h+0.5×FC-P3 h;胰島素劑量。觀察移植后及隨訪過程中患者的不良反應。
1.4 應急處理
培養過程中,若發現污染則立即廢棄細胞,重新取患者脂肪組織進行培養。若質檢時發現細胞質量不過關,重新復蘇擴增培養,或重新取患者脂肪組織進行培養。ADSCs治療基本無不良反應,細胞回輸后患者出現寒戰、低熱(體溫37.5~38.5℃)的概率很低,可臨床觀察24 h,基本會自行消退。不退熱的情況下,采用酒精擦拭等方法進行降溫即可。
1.5 隨訪
移植治療后每2周由專人對患者進行電話隨訪,詢問每位患者血糖控制和胰島素使用情況,并根據患者血糖控制情況適當調整胰島素劑量。患者在移植后3、6、12、15個月時來院復診,并進行相應的實驗室檢查。
1.6 統計學分析
2 結果
2.1 一般臨床資料
比較2組患者的性別、年齡、煙酒史、BMI、病程,差異均無統計學意義(P>0.05),2組具有可比性。見表1。

表1 一般臨床資料比較Tab.1 Comparison of the basic clinical data of the two groups
2.2 ADSCs鑒定
2.2.1 ADSCs形態:原代培養的細胞接種后24 h即可見部分細胞貼壁,并逐漸伸展成為紡錘狀。經換液后,貼壁細胞主要為ADSCs,呈長梭形成纖維細胞樣。7~10 d時細胞基本貼滿孔板底部,細胞扁平,呈魚群狀、旋渦狀整齊排列。傳代培養的ADSCs生長旺盛,形態與原代相似。見圖1。

圖1 ADSCs細胞形態Fig.1 The morphology of ADSCs
2.2.2 ADSCs生長曲線:將第3代ADSCs種于96孔板,檢測細胞活性,讀取吸光度值(OD值),繪制生長曲線。結果顯示:細胞在接種后最初2 d處于生長潛伏期,第3~6天處于對數生長期,第6天達峰值,之后細胞生長速度減慢,進入生長平臺期,平均5~6 d傳代1次。見圖2。

圖2 ADSCs生長曲線Fig.2 The growth curve of ADSCs
2.2.3 ADSCs多向分化能力:用成骨和成脂誘導培養基分別誘導ADSCs,行茜素紅或油紅O染色,光鏡下觀察并拍照。成骨誘導后,可見部分細胞由長梭形逐漸變為多角形,細胞聚集,表面有一層分泌物,茜素紅染色呈陽性。成脂誘導后,細胞由長梭形逐漸收縮變短,細胞內有脂滴出現,經油紅O染色,可見細胞內有大量的脂質沉積,被染成紅色。觀察發現P3代ADSCs可向中胚層來源的2個以上方向分化。見圖3。

圖3 ADSCs誘導分化Fig.3 The differentiation of ADSCs
2.2.4 ADSCs表面標記檢測:結果顯示,P3代ADSCs呈CD105、CD90和CD73陽性,陽性率>98%;CD45、CD34和HLA-DR陰性,陽性率<2%。見圖4。
2.2.5 移植前ADSCs存活率和內毒素檢測:臺盼藍染色結果顯示,用于移植的ADSCs細胞存活率均>95%。鱟試劑凝膠法內毒素檢測結果顯示內毒素≤5 EU/mL,符合臨床使用標準。
2.3 移植前后各項觀察指標的變化
如表2所示:與治療前相比,B組患者治療后3個月FPG水平明顯改善(P<0.01),A組患者雖有改善但不明顯,2組患者治療后3個月2h-PGh和HbA1c含量均有明顯改善(P<0.05);治療后6、12、15個月,2組患者FPG、2h-PGh和HbA1c含量較治療前均有明顯改善(P<0.01);A組治療后3個月2h-PGh改善效果明顯優于B組(P<0.01),治療后6個月HbA1c改善效果明顯優于B組(P<0.05),治療后12和15個月FPG、2h-PGh、HbA1c改善效果均明顯優于B組(P<0.05)。治療后12個月,B組患者FC-P含量較治療前明顯降低(P<0.05);而A組患者在治療后隨訪的各個時間點FC-P含量均較治療前有明顯提高(P<0.05),且與相應時間點B組患者有統計學差異(P<0.01)。B組患者AUCC在隨訪的各時間點均無明顯變化,而A組患者AUCC在治療后3、12、15個月均有明顯增加(P<0.05),且與相應時間點B組患者AUCC相比有統計學差異(P<0.05)。隨著治療時間的延長,B組患者胰島素用量有增加的趨勢,但差異不明顯,而A組患者胰島素用量逐漸減少,且A組各時間點與治療前及與B組相比均有統計學差異(P<0.01)。

圖4 ADSCs流式檢測Fig.4 The flow cytometric analysis of ADSCs
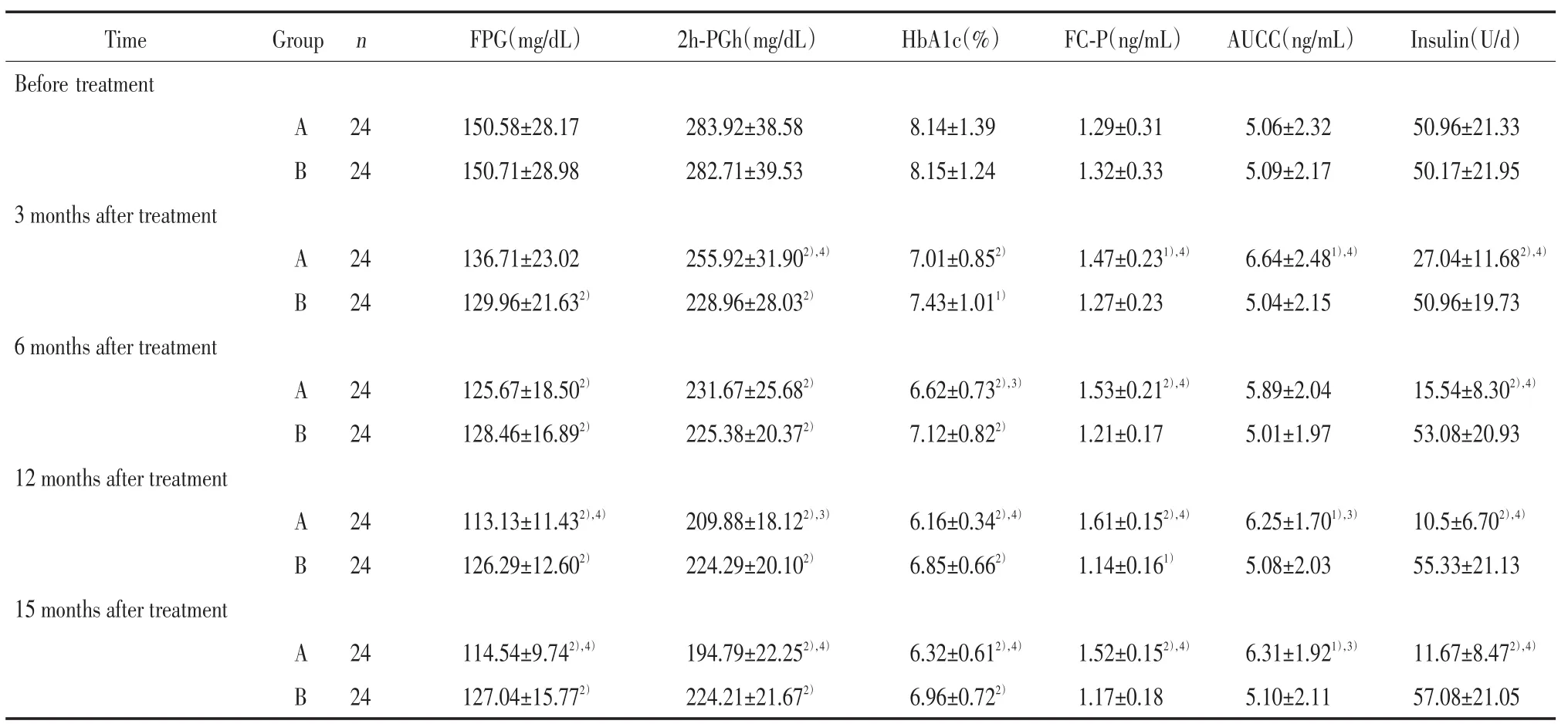
表2 2組各項指標的變化Tab.2 Changes in the clinical data of the two groups
2.4 不良反應
在治療和隨訪過程中,A組患者未出現發熱、皮疹等過敏反應和其他不良反應。
3 討論
近年來,全球2型糖尿病患病率逐年增加,由于其并發癥具有高致殘致死率,嚴重影響人類健康。目前,臨床上治療2型糖尿病仍處于胰島素治療、運動加飲食治療等臨床控制階段,迫切需要有突破臨床控制的治療方式的出現。干細胞移植作為一種新興的治療方式,日益受到人們的關注。國內外學者用臍血干細胞[4,5]、外周血干細胞[6]、骨髓來源的MSC[7~12]、臍帶來源的MSC[13]等治療2型糖尿病,均在控制血糖、修復胰島分泌功能方面取得了更佳效果。到2015年10月10日為止,在互聯網上(http:// www.clinical.gov)能查到91項關于干細胞治療2型糖尿病的臨床研究。本研究采用具有人體儲量大、易于采集培養、分化增殖能力強等優點的ADSCs進行移植,觀察其治療2型糖尿病的安全性和有效性。結果顯示,在ADSCs移植后及隨訪過程中,患者未出現發熱、皮疹等不良反應及其他并發癥,說明ADSCs是治療2型糖尿病的安全的新方法,具有一定的臨床可行性。
本研究結果顯示:培養的ADSCs形態正常、一致性好,具有可向中胚層來源的2個方向分化和增殖能力強等MSCs的特性,且細胞存活率高、無菌、無支原體,符合成體干細胞的臨床應用標準[15]。本研究采用靜脈回輸的方法,利用干細胞的“歸巢”特性,期望能夠獲得如Gitelman等[16]實驗中骨髓干細胞促進胰島β細胞再生和修復胰島分泌功能的結果。結果顯示,在2型糖尿病患者平均血糖控制方面,ADSCs移植聯合常規治療比僅用常規治療有明顯優勢,聯合治療能使胰腺β細胞的分泌功能增強,而僅用常規治療則不能,甚至有可能使胰腺β細胞的分泌功能降低;聯合治療能在很好地控制血糖的基礎上,降低患者胰島素用量,并有7例患者脫離了胰島素,而僅用常規治療則需增加胰島素用量才能維持患者的血糖水平。以上結果提示,ADSCs移植聯合常規治療效果明顯優于單純常規治療,因此,該方法是一種可行性高、安全有效的治療2型糖尿病的方式。
干細胞治療技術是生物治療領域的一種新興項目,目前許多治療作用的確切機制尚不完全清楚,且缺少多中心、大樣本的研究數據和干細胞移植的規范化操作,因此,對于干細胞移植治療2型糖尿病還需進一步深入研究和探討。
[1]Nitzan O,Elias M,Chazan B,et al.Urinary tract infections in patients with type 2 diabetes mellitus:review of prevalence,diagnosis,and management[J].Diabetes Metab Syndr Obes,2015,8:129-136.
[2]Kong D,Zhuang X,Wang D,et al.Umbilical cord mesenchymal stem cell transfusion ameliorated hyperglycemia in patients with type 2 diabetes mellitus[J].Clin Lab,2014,60(12):1969-1976.
[3]Lei L,Zhang X,Mao Y,et al.Statin therapy and bone marrow CD34+cell frequency in type 2 diabetes mellitus:a cross-sectional study[J].Int J Cardiol,2014,175(1):214-216.
[4]Tong Q,Duan L,Xu Z,et al.Improved insulin secretion following intrapancreatic UCB transplantation in patients with T2DM[J].J Clin Endocrinol Metab,2013,98(9):E1501-1504.
[5]徐谷根,楊茵,尹卓娜,等.臍帶血干細胞移植治療2型糖尿病臨床分析[J].中國醫藥科學,2011,1(22):22-25.
[6]丁明超,王意忠,王斌,等.經導管自體外周血干細胞灌注治療2型糖尿病的臨床價值[J].中華臨床醫師雜志(電子版),2012,6(17):5126-5130.
[7]Bhansali A,Upreti V,Walia R,et al.Efficacy and safety of autologous bone marrow derived hematopoietic stem cell transplantation in patients with type 2 DM:a 15 months follow-up study[J].Indian J Endocrinol Metab,2014,18(6):838-845.
[8]Bhansali A,Asokumar P,Walia R,et al.Efficacy and safety of autologous bone marrow-derived stem cell transplantation in patients with type 2 diabetes mellitus:a randomized placebo-controlled study[J].Cell Transplant,2014,23(9):1075-1085.
[9]Bhansali A,Upreti V,Khandelwal N,et al.Efficacy of autologous bone marrow-derived stem cell transplantation in patients with type 2 diabetes mellitus[J].Stem Cells Dev,2009,18(10):1407-1416.
[10]王攀,吳正蓉,田景倫,等.經皮脾動脈自體骨髓細胞移植治療2型糖尿病5例[J].中國組織工程研究與臨床康復,2010,14(23):4355-4358.
[11]姚金萍,段煉,童強,等.自體骨髓干細胞移植治療2型糖尿病的安全性及有效性[J].第三軍醫大學學報,2012,34(1):74-77.
[12]周旋,余衛,陳玲珍,等.自體骨髓間充質干細胞移植治療2型糖尿病的臨床研究[J].當代醫學,2013,19(17):20-21.
[13]Liu X,Zheng P,Wang X,et al.A preliminary evaluation of efficacy and safety of Wharton′s jelly mesenchymal stem cell transplantation in patients with type 2 diabetes mellitus[J].Stem Cell Res Ther,2014,5(2):57.
[14]Jiang R,Han Z,Zhuo G,et al.Transplantation of placenta-derived mesenchymal stem cells in type 2 diabetes:a pilot study[J].Front Med,2011,5(1):94-100.
[15]Tzouvelekis A,Paspaliaris V,Koliakos G,et al.A prospective,nonrandomized,no placebo-controlled,phase Ib clinical trial to study the safety of the adipose derived stromal cells-stromal vascular fraction in idiopathic pulmonary fibrosis[J].J Transl Med,2013,11:171.
[16]Gitelman SE,Gottlieb PA,Rigby MR,et al.Antithymocyte globulin treatment for patients with recent-onset type 1 diabetes:12-month results of a randomised,placebo-controlled,phase 2 trial[J].Lancet Diabetes Endocrinol,2013,1(4):306-316.
(編輯 王又冬)
Efficacy and Safety of Autologous Adipose-derived Stem Cells Transplantation in Patients with Type 2 Diabetes Mellitus
ZHANGXin,ZHOUYu-hong,BAIYun
(Department of Endocrinology,Liaohe Oilfield General Hospital,Panjin 124010,China)
ObjectiveTo evaluate the clinical efficacy and safety of ADSCs infusion in patients with type 2 diabetes mellitus(T2DM).MethodsAutologous ADSCs were cultured and identified.Totally 48 cases of type 2 diabetes patients were divided into two groups:24 cases in A group received ADSCs and conventional treatment,while the other24 cases in B group received conventional treatment.With 15 months′follow-up,FPG,2h-PGh,HbA1c,FC-P,AUCC,insulin medication changes and security on post-treatment3,6,12 and 15 months were calculated.ResultsThe ADSCs which cultured met the clinical application of standards.FPG,2h-PGh and HbA1c in both groups were significantly decreased,and the values in A group were more impressive than B.There were significant improvement in FC-P,AUCC and insulin of A group compared with B group.There was not treatment related adverse events.ConclusionThe clinical data demonstrate that the treatment with ADSCs can improve metabolic control and beta cell function in patients with T2DM.Moreover,the safety oft he treatment method was considerable.
type 2 diabetes mellitus;autologous adipose-derived stem cells;transplantation;efficacy and safety
R5
A
0258-4646(2015)12-1137-05
張新(1979-),女,主治醫師,碩士.
E-mail:xixi_1979@163.com
2015-04-08
網絡出版時間:

