新型耐酸鋼在硫酸鹽酸混合溶液中的腐蝕行為
張 聰,周 成,葉先祥
(北京科技大學 材料科學與工程學院,北京100083)
在冶金、電力、石化等工業領域,以重油或燃煤為主要燃料的煙氣處理系統,如鍋爐低溫部位的空氣預熱器、省煤器、煙道、煙囪以及脫硫裝置等,普遍會遇到燃料中含硫量偏高的情況。重油燃料中通常含有2%~3%的硫及硫化物,燃燒中絕大部分形成二氧化硫。二氧化硫中約有1%~5%在一定條件下與氧化合成三氧化硫。當它與煙氣中水蒸汽(5%~18%)結合形成硫酸蒸汽時,會大幅度提高煙氣的露點。當接觸煙氣的裝置表面溫度低于露點時,即發生酸液的凝結并強烈的腐蝕金屬。這種現象稱之為硫酸露點腐蝕[1-2]。同理,煤燃料中98%以上的氯轉化成HCl留于廢氣中。比較低碳鋼在燃燒廢氣中含HCl與不含HCl時的腐蝕量,當60℃以上時無差異,在60℃以下含有HCl的低碳鋼腐蝕量明顯增加[3]。因為在此溫度下有HCl結露,稱之為鹽酸露點腐蝕。隨著硫含量越來越高,導致燃燒或熱交換系統設備遭受冷卻過程中發生的露點腐蝕。在這種環境中不銹鋼的腐蝕速率比低碳鋼還高,因此也不易使用不銹鋼。為解決這一難題,人們采用提高排煙溫度的方法,或采用玻璃管等非金屬材料管代替鋼管,然而這樣影響了熱效率,也增加了技術上的難度[4]。
出于節能、降耗、減排的國家戰略思路,發電、石化等行業要求排出氣體的低溫化(要求低于130℃)。低溫化后低溫段的硫酸露點腐蝕(60~70℃腐蝕最嚴重)更為嚴重,同時在低溫段還產生鹽酸露點腐蝕(露點溫度60~70℃)。傳統耐硫酸露點腐蝕鋼服役溫度高于130℃,該服役環境下僅需滿足高溫段硫酸露點腐蝕性能,不存在鹽酸露點腐蝕現象[5]。因此傳統的耐硫酸露點腐蝕鋼已不適應于排煙低溫化后的服役環境,因此,開發使用一種能夠在硫酸和鹽酸露點腐蝕環境下長期使用的新型耐酸鋼,對于提高鍋爐、省煤器、空氣預熱器、煙囪等部件的使用壽命,減少能耗和環境保護,都具有重要意義[6]。
本工作以16.9%H2SO4+0.35%HCl的混合溶液為腐蝕介質,在60℃的溫度條件下進行試驗,這是韓國一種煙氣脫硫裝置最具代表性的腐蝕環境[7]。實驗室研制了一種新型耐硫酸鹽酸露點腐蝕鋼,這是一種添加了合金元素的低合金鋼。在鐵碳合金中,為了改進鋼的某一種或幾種性能,特意向鋼中加入一定量的一種或幾種合金元素。鉬能有效地提高鋼的抗大氣腐蝕能力。當鋼中含0.4%~0.5%鉬時,在大氣環境(尤其是工業大氣)條件下鋼的腐蝕速率可能降低1/2以上。鉬的作用在于改善了銹層的性質,并能促使生成非晶態的氧化膜[8]。因此可以模擬在這種硫酸鹽酸混合條件下,研究新型耐酸鋼的耐硫酸鹽酸露點腐蝕性能。
1 試驗
1.1 腐蝕失重試驗
試驗材料為新型耐酸鋼(稱為1號鋼)和Q235鋼,其化學成分見表1。樣品經機械加工后,再用800號到2000號砂紙逐級打磨,最后用丙酮和酒精清洗試樣表面,放入干燥皿24h后稱量,精確度為0.1mg,試樣尺寸為50mm×25mm×4mm,取三個平行試樣。腐蝕溶液為16.9%H2SO4+0.35%HCl的混合溶液,試驗溫度為60℃。在試樣上方打一個φ2mm的孔,將1號試樣和Q235試樣分別懸掛浸泡在1 000mL的腐蝕溶液中6h。對于浸泡腐蝕后的試樣,首先采用500mL鹽酸+500mL去離子水+10g六次甲基四胺去除腐蝕產物,在室溫下進行。疏松的外銹層除去后再用毛刷刷洗殘留的銹層。銹層被除盡后的試樣用蒸餾水沖洗,用酒精清洗,吹干后放入干燥器中,24h后稱量。

表1 1號鋼和Q235鋼的主要化學成分Tab.1 Chemical composition of 1#steel and Q235steelmass fraction/%
腐蝕速率采用下式計算:

式中:v是腐蝕速率,g·(m-2·h-1);W0是試樣原始質量,g;Wt是試樣除去產物后的質量,g;S是試樣表面積,m2;t為浸泡時間,h。
1.2 電化學極化曲線和電化學阻抗譜測試
電化學測試在Princeton VMP3電化學工作站上進行,使用鉑片作為輔助電極,飽和甘汞電極(SCE)作為參比電極,工作電極尺寸10mm×10mm×4mm,用銅導線點焊留出引線,用環氧樹脂封住并留出10mm×10mm的工作面積,用砂紙打磨到2000號。腐蝕介質為16.9%H2SO4+0.35%HCl的混合溶液,由于在高溫下測試開路電位(OCP)難以達到穩定狀態,參考國內外研究方法降低試驗溶液溫度而不改變濃度,在室溫條件下(20℃)進行電化學測試。動電位極化曲線和電化學阻抗譜(EIS)均在開路電位(OCP)達到穩定后進行,極化曲線測試電壓掃描范圍為-0.3~0.3V,掃描速率0.5mV/s。EIS測試頻率范圍為100mHz~10kHz,正弦電壓振幅為10mV。
1.3 銹層微觀形貌分析
將1號鋼和Q235鋼加工成15mm×15mm×4mm尺寸,置于16.9%H2SO4+0.35%HCl的混合溶液中,在60℃條件下全浸6h,取出試樣吹干,置于干燥皿24h。采用ZEISS S-360型掃描電鏡(SEM)觀察試樣表面銹層的致密度和連續性。
2 結果與討論
2.1 腐蝕失重試驗
試樣在60℃的16.9%H2SO4+0.35%HCl的混合溶液中浸泡6h后,按照腐蝕速率計算公式,算出1號鋼的Q235鋼的腐蝕速率如表2所示。

表2 60℃的試樣在16.9%H2SO4+0.35%HCl的混合溶液中的腐蝕速率Tab.2 The corrosion rate for specimens in 16.9%H2SO4+0.35%HCl solution at 60℃
從表2可以看出混合溶液中:1號鋼的腐蝕速率為7.17g·m-2·h-1,Q235鋼的腐蝕速率為225.01g·m-2·h-1,是1號鋼的31倍,說明1號鋼的耐硫酸鹽酸露點腐蝕性能遠優于Q235鋼,含有銅,銻,鉬的低合金鋼適合于硫酸鹽酸腐蝕環境。新型耐酸鋼在Q235成分的基礎上,適當減小碳含量,添加適量的合金元素銅,銻,鉬可以使試樣在腐蝕溶液中表面生成了一層致密的腐蝕產物,它有效地阻礙了腐蝕溶液對金屬基體的進一步侵蝕,提高鋼種的耐硫酸鹽酸露點腐蝕性能。
2.2 動電位極化曲線
可以通過對1號和Q235試樣進行極化曲線測試分析比較兩個鋼種的耐硫酸鹽酸腐蝕性能。圖1顯示出兩種試樣在20℃的16.9%H2SO4+0.35%HCl的混合溶液中測得的極化曲線,極化曲線電化學參數擬合結果見表3。

表3 20℃時試樣在16.9%H2SO4+0.35%HCl的混合溶液極化曲線測試的電化學參數Tab.3 Electrochemical parameters of potentiodynamic polarization measurements for specimens in 16.9%H2SO4+0.35%HCl solution at 20℃
從圖1可以看出,在這種溶液條件下,剛開始時1號鋼和對比鋼Q235鋼的陽極腐蝕電流密度均隨著電位的升高而增大,呈活性溶解狀態,沒有明顯的鈍化區。但是隨著電位的升高,1號鋼的陽極腐蝕電流密度出現減小的趨勢,這可能是由于合金元素銅,銻,鉬的添加使試樣表面生成了一層保護膜,可以抑制金屬陽極活性溶解,同時抑制陰極析氫反應的發生,降低腐蝕電流密度,有效的阻礙腐蝕的進一步發生。而Q235鋼由于沒有添加合金元素,沒有生成致密的保護膜,不能有效抑制金屬陽極的活性溶解和陰極析氫反應的發生,陽極腐蝕電流密度繼續增大,腐蝕更加嚴重。從表3可知1號鋼的自腐蝕電流密度Jcorr比Q235的小很多,進一步說明添加了銅,銻,鉬等合金元素的低合金鋼1號較普通碳鋼Q235具有優異的耐硫酸鹽酸腐蝕性能。
其中年腐蝕速率根據Faraday定律及腐蝕電流密度按照公式推算出[9]:


圖1 20℃時試樣在16.9%H2SO4+0.35%HCl的混合溶液極化曲線Fig.1 Potentiodynamic polarization curves for specimens in 16.9%H2SO4+0.35%HCl solution at 20℃
式中:Jcorr是自腐蝕電流密度(A·cm-2);M是金屬的摩爾質量(g·mol-1);z是每個金屬原子轉移的電子數;F是Faraday常數;ρ是金屬的密度(g·cm-3)。推算出的年腐蝕速率(表3),反映出1號鋼相比Q235鋼具有優異的耐硫酸鹽酸腐蝕性能。
2.3 電化學阻抗譜
電化學阻抗譜測試能反映腐蝕速率的大小,校準溶液的電阻。圖2是兩種試樣在20℃的16.9%H2SO4+0.35%HCl的混合溶液中測得的Nyquist圖,Nyquist圖中的高頻容抗弧與試樣表面生成的銹層相關,低頻容抗弧與電荷轉移過程相關,電化學阻抗譜顯示的是一個半圓弧,如圖3所示。

圖2 20℃時試樣在16.9%H2SO4+0.35%HCl的混合溶液中的Nyquist圖Fig.2 Nyquist plot of specimens in 16.9%H2SO4+0.35%HCl solution at 20℃
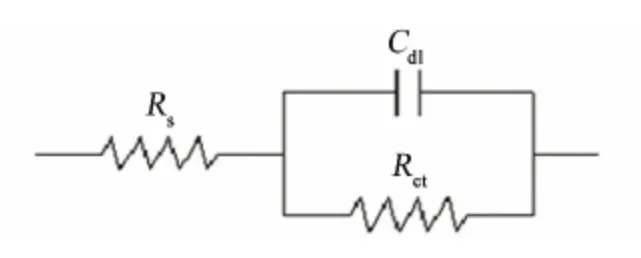
圖3 電化學阻抗譜的等效電路圖Fig.3 Equivalent circuit used to fit EIS data
將試樣在16.9%H2SO4+0.35%HCl的混合溶液中的電化學阻抗譜進行等效電路擬合,如圖3所示,等效電路圖由溶液電阻Rs、雙電層電容Cdl和電荷轉移電阻Rct組成[10]。通過Zsimpwin軟件擬合出電荷轉移電阻Rct如表4所示。

表4 20℃時試樣在16.9%H2SO4+0.35%HCl的混合溶液中的電荷轉移電阻Tab.4 The charge transfer resistance for specimens in 16.9%H2SO4+0.35%HCl solution at 20℃
從電化學阻抗譜測試可以看出1號鋼的電荷轉移電阻為40.35Ω·cm2,Q235鋼為9.62Ω·cm2,這說明在16.9%H2SO4+0.35%HCl的混合溶液中1號鋼具有遠比普通碳鋼Q235優異的耐蝕性。說明合金元素銅,銻,鉬的添加有利于增大金屬的電荷轉移電阻Rct,從而抑制金屬的溶解反應。
2.4 銹層微觀形貌分析
圖4是1號鋼和Q235鋼在16.9%H2SO4+0.35%HCl的混合溶液中浸泡6h后的腐蝕產物微觀形貌。從圖4可以看出經過腐蝕浸泡后,1號鋼發生均勻腐蝕,腐蝕產物很致密,腐蝕產物緊緊的粘附在金屬基體表面,沒有明顯的裂紋和孔洞。進一步放大后發現1號鋼的腐蝕產物由團簇狀細小顆粒組成,這種腐蝕產物比較致密,對基體有更好的保護作用[11],能夠減小腐蝕溶液對金屬基體的腐蝕。而Q235發生溝槽狀腐蝕,腐蝕產物有明顯分層現象,局部腐蝕產物已經脫落,進一步放大后發現蝕孔和大量裂紋,這當然不能有效的抑制溶液對基體的進一步腐蝕。相反當孔洞和裂紋充滿溶液時,會產生較大的腐蝕電流密度,加劇腐蝕的進行。因此添加合金元素銅,銻,鉬可以使金屬表面生成致密的保護膜,這樣就能有效抑制腐蝕溶液對金屬基體的進一步腐蝕,提升鋼種的耐硫酸鹽酸露點腐蝕性能。
3 結論
(1)新型耐酸鋼在Q235成分的基礎上,適當減小碳含量,添加適量的合金元素銅,銻,鉬,可以大幅提高鋼種的耐硫酸鹽酸露點腐蝕性能。
(2)合金元素銅,銻,鉬的添加可以同時抑制金屬的陽極溶解反應和陰極析氫反應,降低腐蝕電流密度,增大金屬的電荷轉移電阻。
(3)合金元素銅,銻,鉬的添加使鋼在浸泡條件下生成了一層致密的保護膜,從而抑制了金屬基體的進一步腐蝕。

圖4 經過6h浸泡后試樣表面的SEMFig.4 SEM images of specimens after 6himmersion(a) 1# (b) Q235
[1]王鈞.耐硫酸露點腐蝕JNS鋼板的研制[J].山東冶金,2007,29(3):31-32.
[2]王維宗.硫酸露點腐蝕機理與防護[J].石油化工腐蝕與防護,1992(4):16-22.
[3]許適群.關于露點腐蝕及用鋼的綜述[J].石油化工腐蝕與防護,2000,17(1):1-6.
[4]朱忠亞.耐硫酸露點腐蝕無縫鋼管用低合金鋼——09CrCuSb(ND鋼):中華人民共和國,CN1490427A[P].2004-04-21.
[5]錢余海,李自剛,楊阿娜.低合金耐硫酸露點腐蝕鋼的性能和應用[J].特殊鋼,2005,26(5):30-34.
[6]RYUJI U,YASUSHI H,TAKUYA H,et al.Steels for energy production and transport[J].Nippon Steel Technical Report,2012(101):68-78.
[7]LE D P,JI W S,KIM J G,et al.Effect of antimony on the corrosion behavior of low-alloy steel for flue gas desulfurization system[J].Corrosion Science,2008,50:1195-1204.
[8]徐增華.金屬耐蝕材料 第三講 耐蝕低合金鋼[J].腐蝕與防護,2001,22(3):135-138.
[9]SUN-AH P,SEUNG-HWAN L,JUNG-GU K.Effect of chromium on the corrosion behavior of low alloy steel in sulfuric acid[J].Met Mater Int,2012,18(6):975-987.
[10]PARK S A,WOO S J,JUNG G K.Effect of chromium on the corrosion behavior of low-alloy steels containing copper in FGD environment[J].Int J Electrochem Sci,2013,8:7498-7509.
[11]CHENG X Q,SUN F L,LüS J,et al.A new steel with good low-temperature sulfuric acid dew point corrosion resistance[J].Materials and Corrosion,2012,63(7):598-606.

