AG490對大鼠腦缺血損傷的保護作用及其機制
高延才,杜愛玲,張林朋,張合鵬,曹少鵬,王振剛,季泰令(濰坊醫學院,山東濰坊6053;濰坊醫學院附屬醫院)
AG490對大鼠腦缺血損傷的保護作用及其機制
高延才1,杜愛玲2,張林朋1,張合鵬1,曹少鵬1,王振剛2,季泰令2(1濰坊醫學院,山東濰坊261053;2濰坊醫學院附屬醫院)
摘要:目的研究JAK激酶/信號轉導和轉錄激活因子(JAK/STAT)信號通路的阻斷劑AG490對大鼠腦缺血損傷的保護作用,并探討其作用機制。方法用健康SD大鼠制作大腦中動脈栓塞(MCAO)模型,隨機分為四組:mCAO組、假手術組、高劑量AG490干預組和低劑量AG490干預組。MCAO組采用左側頸外動脈插栓法造模;假手術組不插栓,結扎并剪斷左側頸外動脈,夾閉左側頸總動脈1 h后撤動脈夾,縫皮;高劑量AG490干預組和低劑量AG490干預組在造模成功后1 h分別給予腹腔注射6、3mg/kg AG490,MCAO組和假手術組給予等量生理鹽水。動物麻醉清醒后6、12、24 h,應用神經功能行為學評分評價腦缺血損傷程度;動物麻醉清醒后24 h用2,3,5-氯化三苯基四氮唑染色技術檢測腦組織梗死范圍,ELISA法檢測腦組織內腫瘤壞死因子α(TNF-α)和白細胞介素1β(IL-1β)水平。結果大鼠麻醉清醒后24 h,與假手術組比較,MCAO組、高劑量AG490干預組和低劑量AG490干預組神經功能行為學評分、TNF-α和IL-1β水平高,腦組織梗死范圍大(P<0.05或<0.01);與MGAO組比較,高劑量AG490干預組、低劑量AG490干預組神經功能行為學評分低,TNF-α、IL-1β水平低,腦組織梗死范圍小(P均<0.01)。結論AG490對大鼠腦缺血損傷具有保護作用,其作用是通過抑制JAK/STAT信號傳導通路、減輕炎癥反應實現的。
關鍵詞:腦缺血; AG490; JAK激酶;信號轉導和轉錄激活因子;大鼠
腦血管病在人類各種疾病死因中一直位于前3位,成為人類死亡的主要原因。其中缺血性腦血管病(ICVD)臨床較多見,約占全部腦血管病患者的85%,最為常見的是大腦中動脈栓塞(MCAO)引起的。由于大鼠的腦血管分布與人腦部血管類似,而且愈合能力強、易于飼養、便于操作,因此本實驗采用了目前常見的大鼠MCAO模型。AG490是一種人工合成的苯亞甲基丙二腈的脂類衍生物,是JAK激酶/信號轉導和轉錄激活因子(JAK/STAT)信號通路的阻斷劑[1]。目前研究表明,JAK/STAT信號轉導途徑參與中樞神經系統的多個生物學分化過程,與腦外傷、腦腫瘤、免疫反應機制等相關[2]。2014年10月~2015年6月,我們就AG490對腦缺血損傷的作用及其作用機制進行了相關探討。現報告如下。
1 材料與方法
1.1材料雄性SD大鼠,體質量250~280 g(北京斯貝福實驗動物科技有限公司),潔凈動物房飼喂,大鼠自由飲水進食,飼喂3d,適應環境后進行試驗; AG490(美國BioLegend公司); 2,3,5-氯化三苯基四氮唑(TTC)(北京化學試劑公司); TNF-α和IL-1β ELISA試劑盒(北京環亞泰克生物醫學技術有限公司)。
1.2動物分組與MCAO模型建立依據隨機數字表將大鼠分為4組:假手術組、MCAO組、低劑量AG490(3mg/kg)干預組和高劑量AG490(6mg/kg)干預組。大鼠均采用腹腔注射麻醉(10%水合氯醛0.3mL/100 g),MCAO組采用頸外動脈插栓法,做頸正中切口,暴露頸總動脈(CCA)、頸外動脈(ECA)及頸內動脈,將0.26mm單絲尼龍魚線頭端0.5 cm用石蠟包被,并于20mm處標記,大鼠均通過左側ECA切口處插入,栓線長度自CCA分叉處18~20mm,根據動物體質量而定,栓塞左側大腦中動脈,然后縫合皮膚,栓線尾端部分固定于皮膚上。缺血達到2 h后小心抽出栓線,即形成再灌注。假手術組只是不插入尼龍魚線,其余步驟同MCAO組。低劑量AG490干預組和高劑量AG490干預組分別于術前24 h給予3mg/kg和6mg/kg的AG490腹腔注射,其余步驟同MCAO組。在缺血期間及再灌注后2 h保持體溫在(37±0.5)℃。以大鼠手術麻醉清醒后出現右側肢體癱瘓,站立不穩,提尾時向一側轉圈為模型成功的判斷標準。
1.3腦缺血損傷程度的評價采用神經行為學評分。參考Ergul等[3]的5分制法,在動物麻醉清醒后6、12、24 h進行評分。0分:無神經損傷癥狀; 1 分:不能完全伸展對側前爪; 2分:向對側轉圈; 3分:向對側傾倒; 4分:不能自發行走,意識喪失。分值越高,說明動物行為障礙越嚴重。
1.4腦組織梗死范圍的檢測采用TTC染色法。動物麻醉清醒后24 h將大鼠斷頭,取出完整的腦組織,迅速置于-20℃的冰箱中,凍存20min。切成5~6片,每隔2mm切一片。第一刀在腦前極與視交叉連線中點處;第二刀在視交叉部位;第三刀在漏斗柄部位;第四刀在漏斗柄與后葉尾極之間[4]。切片應均勻。將切片置于TTC中,常規濃度為2%,用錫箔紙蓋住后,放入37℃恒溫箱15~30min,不時翻動腦片,保證均勻接觸到染色液。最后,數碼相機拍照,計算機計算梗死區域體積所占大腦半球總體積的百分比。
1.5腦組織TNF-α和IL-1β測定動物麻醉清醒后24 h,選取栓塞缺血同側的大鼠腦組織,勻漿處理腦組織,然后離心,取上清液。采用ELISA法,嚴格按照ELISA試劑盒說明書操作測定腦組織TNF-α 和IL-1β水平。
1.6統計學方法采用SPSS13.0統計軟件。計量資料以±s表示,神經行為學評分比較采用秩和檢驗,組間比較采用單因素方差分析。P<0.05為差異有統計學意義。
2 結果
2.1各組不同時間神經行為學評分比較見表1。
表1 各組不同時間神經行為學評分比較(分,)
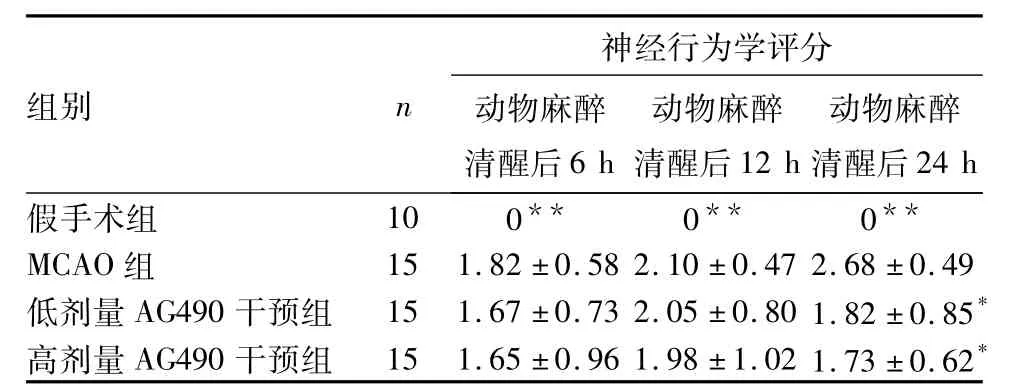
表1 各組不同時間神經行為學評分比較(分,)
注:與MCAO組同期比較,*P<0.05,**P<0.01。
組別 n 24 h神經行為學評分動物麻醉清醒后6 h動物麻醉清醒后12 h動物麻醉清醒后假手術組 10 0** 0** 0**MCAO組 15 1.82±0.58 2.10±0.47 2.68±0.49低劑量AG490干預組 15 1.67±0.73 2.05±0.80 1.82±0.85*高劑量AG490干預組 15 1.65±0.96 1.98±1.02 1.73±0.62*
2.2各組腦組織梗死范圍比較假手術組無腦組織梗死發生,MCAO組腦組織梗死范圍為(16.84± 4.60)%,低劑量AG490干預組為(10.37± 2.60)%,高劑量AG490干預組為(8.26±3.07)%。MCAO組、高劑量AG490干預組和低劑量AG490干預組腦組織梗死范圍均高于假手術組(P均<0.01);高劑量AG490干預組、低劑量AG490干預組和MCAO組腦組織梗死范圍依次增高(P均<0.01)。
2.3各組腦組織TNF-α和IL-1β水平比較見表2。
表2 各組腦組織TNF-α和IL-1β水平比較(mg/g,)
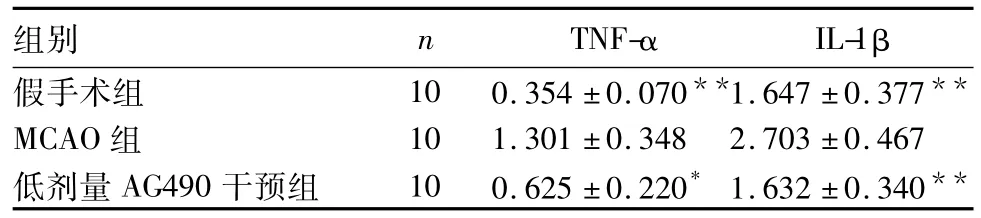
表2 各組腦組織TNF-α和IL-1β水平比較(mg/g,)
注:與MCAO組比較,*P<0.05,**P<0.01。
組別 n TNF-α IL-1β假手術組 10 0.354±0.070**1.647±0.377**MCAO組 10 1.301±0.348 2.703±0.467低劑量AG490干預組 10 0.625±0.220*1.632±0.340**
3 討論
目前,面對日益加重的老齡化問題,心腦血管疾病已經成為危害人們身體健康的主要疾病,其發病率呈現逐年增高的趨勢。腦缺血損傷后的區域主要表現為炎癥反應,包括氧自由基產生、水解酶生成、溶酶體破壞、白細胞聚集以及炎癥介質形成等方面。腦缺血損傷后的一系列炎癥反應,最終會導致血腦屏障受損,內皮細胞的參與會加重腦損害,引起腦水腫。以上的病理生理過程中會有各種各樣的炎性因子參與其中,包括TNF-α和IL-1β。
IL-1β是IL-1在腦組織中主要的活性形式,可由內皮細胞和神經膠質細胞等多種活性細胞合成和分泌。其不僅能協同其他細胞因子促進T、B細胞活化,還能誘導其他炎癥介質產生,增強內皮細胞與白細胞的黏附,調節TNF-α和IL-6的產生[5,6]。目前認為,IL-1β是一種重要的炎性因子,其失控性表達是炎癥反應失控性發生、發展的重要因素,是反映腦缺血急性期損傷程度的標志物[7]。它誘導的炎癥反應與JAK/STAT信號通路密切相關[8]。TNF-α具有觸發和級聯放大炎癥反應的作用,是誘導過度炎癥反應的關鍵性促炎因子,在缺血性腦血管病的發病機制中起重要作用,是腦缺血形成后腦組織梗死的主要原因[9,10]。其可誘導細胞黏附因子表達,增加血管內皮細胞通透性,導致炎癥介質釋放和聚集,在腦缺血損傷后期的炎癥細胞浸潤和組織損傷中發揮很大作用,因此降低TNF-α的表達是對腦缺血損傷后神經功能障礙的一種保護性措施。本研究結果顯示,與假手術組比較,MCAO組、高劑量AG490干預組和低劑量AG490干預組神經功能行為學評分、TNF-α和IL-1β水平高,腦組織梗死范圍大;與MCAO組比較,高劑量AG490干預組、低劑量AG490干預組神經功能行為學評分低,TNF-α、IL-1β水平低,腦組織梗死范圍小。提示AG490可通過降低TNF-α和IL-1β水平,抑制炎癥反應從而起到腦組織保護作用。
研究表明,眾多細胞內的信號轉導需要借助JAK-STAT信號轉導通路,其在缺血性腦血管病中的作用越來越受到關注[11]。本實驗采用的干預藥物AG490是一種選擇性拮抗JAK2酪氨酸磷酸化的抑制劑,能有效地阻斷下游信號轉導和轉錄激活子STAT的活化,特異性地抑制JAK-STAT信號轉導通路,從而有效地阻斷其信號通路的信號轉導過程。結果顯示采用AG490阻斷JAK-STAT信號轉導通路后,大鼠腦缺血損傷后的神經功能損傷程度減輕、腦組織梗死范圍縮小和炎癥反應減輕,因此推斷AG490通過抑制JAK-STAT信號轉導通路保護腦缺血損傷。
參考文獻:
[1]Fenyo IM,Florea IC,Raicum,et al.Tyrphostin AG490 reduces NAPDH oxidase activity and expression in the aorta of hypercholesterolemic apolipoprotein E-deficientmice[J].Vascul Pharmacol,2011,54(3-6): 100-106.
[2]Kondylim,Gatzounis G,Kyritsis A,et al.Immunohistochemicaldetection of phosphorylated JAK-2 and STAT-5 proteins and correlation with erythropoietin receptor(EpoR)expression status in human brain tumors[J].J Neurooncol,2010,100(2): 157-164.
[3]Ergul A,ElgebalymM,MiddlemoremL,et al.Increased hemorrhagic transformation and altered infarct size and localization after experimental stroke in a ratmodel type 2diabetes[J].BMC Neurol,2007,(7): 33.
[4]張均田.現代藥理實驗方法[M].北京:北京醫科大學中國協和醫科大學聯合出版社,1998: 1382,1409-1413.
[5]BenningerdH,Georgiadisd,Kremer C,et al.Mechanism of ischemic infarct in spontaneous carotiddissection[J].Stroke,2004,35(2): 482-485.
[6]Castellanosm,Castillo J,GarcíamM,et al.Inflammation-mediateddamage in progressing lacunar infarctions: a potential therapeutic target[J].Stroke,2002,33(4): 982-987.
[7]Clark WM,Rinker LG,Lessov NS,et al.Lack of interleukin-6 expression is not protective against focal central nervous system ischemia[J].Stroke,2000,31(7): 1715-1720.
[8]Jee SH,Chu CY,Chiu HC,et al.Interleukin-6 induced basic fibroblast growth factor-dependent angiogenesis in basal cell carcinoma cell line via JAK/STAT3 and PI3-kinase/Akt pathways[J].J Investdermatol,2004,123(6): 1169-1175.
[9]Sairanen T,Carpén O,Karjalainen-LindsbergmL,et al.Evolution of cerebral tumor necrosis factor-alpha productionduring human ischemic stroke[J].Stroke,2001,32(8): 1750-1758.
[10]Fenyo IM,Florea IC,Raicum,et al.Tyrphostin AG490 reduces NAPDH oxidase activity and expression in the aorta of hypercholesterolemic apolipoprotein E-deficientmice[J].Vascul Pharmacol,2011,54(3-6): 100-106.
[11]Ke JJ,Wang YL,Li JG,et al.Pretreatment effect of adenosine on activation of NF kappaB and level of TNF-alphaduringmyocardial ischemia and reperfusion in rats[J].Chin J Traumatol,2004,7(1): 25-27.
·臨床研究·
收稿日期:( 2015-07-06)
文章編號:1002-266X(2015)37-0031-03
文獻標志碼:A
中圖分類號:R651.1
doi:10.3969/j.issn.1002-266X.2015.37.010

