超聲引導下射頻消融術(shù)聯(lián)合靶向治療對晚期肝細胞癌患者免疫功能的影響
陳旭蘭,付靖楠,李 穎,屈 波
?
超聲引導下射頻消融術(shù)聯(lián)合靶向治療對晚期肝細胞癌患者免疫功能的影響
陳旭蘭,付靖楠*,李穎,屈波

*共同第一作者
[摘要]目的探討超聲引導下射頻消融術(shù)(RFA)聯(lián)合靶向治療對晚期肝細胞癌患者免疫功能的影響。方法將2011年3月—2014年7月收治的晚期肝細胞癌90例隨機分為觀察組和對照組,每組45例。觀察組入院后行超聲引導下經(jīng)皮腹腔穿刺RFA 1周后給予吉非替尼聯(lián)合卡培他濱靶向治療,對照組給予基礎(chǔ)治療1周行靶向治療。治療前、后均測定兩組免疫細胞及體液免疫功能。結(jié)果觀察組治療后4周血清CD3、CD4、CD4/CD8、CD3+CD56+NK和血清IgG、IgM、IgA濃度均較治療前和對照組升高,CD8較治療前和對照組降低(P<0.05),對照組治療后4周CD3、CD4、CD4/CD8、CD3+CD56+NK和血清IgG、IgM、IgA濃度較治療前降低,CD8較治療前升高(P<0.05)。結(jié)論晚期肝細胞癌患者行超聲引導下RFA聯(lián)合靶向治療能很好地改善免疫功能。
[關(guān)鍵詞]癌,肝細胞;超聲引導;導管消融術(shù);靶向治療;免疫功能
超聲是一種使用簡單方便、無創(chuàng)、價格低廉、無放射性的影像學檢查手段,廣泛應用于臨床輔助性診斷與治療中。超聲引導下行射頻消融術(shù)(radiofrequency ablation, RFA)治療中晚期肺癌、肝癌已在臨床廣泛開展,且取得了很好的治療效果[1-4]。目前超聲引導下經(jīng)腹腔穿刺RFA具有創(chuàng)面小、并發(fā)癥少等優(yōu)點,臨床用于治療病灶體積較小、轉(zhuǎn)移灶較少、復發(fā)性及失去手術(shù)切除機會的肝癌患者的治療[5]。靶向治療是近年來針對惡性腫瘤所采用的一種治療手段,臨床已取得較好效果,但仍不能很好地控制腫瘤的發(fā)展與轉(zhuǎn)移[6],因此需要探尋一種新的治療方案。近年來研究表明,RFA不但可以直接殺死腫瘤細胞、毀壞腫瘤組織、防止腫瘤細胞轉(zhuǎn)移外,還可以提高機體對腫瘤的免疫功能[7],但是目前國內(nèi)外尚無針對超聲引導下治療中晚期肝細胞癌的研究報道。2011年3月—2014年7月我院采用超聲引導下經(jīng)皮腹腔穿刺RFA聯(lián)合藥物靶向治療晚期肝細胞癌45例,取得了較好療效,現(xiàn)報告如下。
1資料與方法
1.1納入和排除標準
1.1.1納入標準:①經(jīng)病理結(jié)合醫(yī)技檢查(典型的影像學表現(xiàn)以及甲胎蛋白≥500 ng/ml)診斷為肝細胞癌;②患者本人及家屬同意后參與且經(jīng)醫(yī)院醫(yī)學倫理委員會批準;③接受靶向治療時間≥3個月;肝功能Child-pluge分級為A級;④至少有1個可以測量的腫瘤且直徑≥1 cm;⑤主要器官無嚴重功能衰竭;⑥中性粒細胞≥1.5×109/L,血紅蛋白≥90 g/L(14 d內(nèi)無輸血史),血小板≥80×109/L。
1.1.2排除標準:①KPS評分<70分;②合并嚴重心腦血管疾病、糖尿病、甲狀腺功能亢進等代謝及內(nèi)分泌系統(tǒng)疾病患者;③混合細胞性肝癌;④合并其他惡性腫瘤;⑤腹部CT檢查結(jié)果提示腹腔內(nèi)有大量積液;⑥治療前1個月內(nèi)有外傷史及大手術(shù)史;⑦出現(xiàn)中樞神經(jīng)系統(tǒng)的廣泛性轉(zhuǎn)移;⑧影像學(CT/MRI)檢查結(jié)果顯示有重要血管及其周圍神經(jīng)的侵蝕且因血管侵蝕而出現(xiàn)出血;⑨病灶直徑>6 cm;⑩既往有煙酒等不良嗜好。
1.2臨床資料本組90例,男49例,女41例;年齡32~73歲;體重指數(shù)23~26 kg/m2。均經(jīng)肝臟穿刺病理組織學證實為晚期(ⅢB~Ⅳ期)肝細胞癌,且經(jīng)CT平掃顯示病灶直徑≤6 cm,肝內(nèi)轉(zhuǎn)移灶較少。按隨機數(shù)字表法分為觀察組和對照組,每組45例。兩組性別、年齡、體重指數(shù)、病情等方面比較差異無統(tǒng)計學意義(P>0.05),具有可比性。見表1。
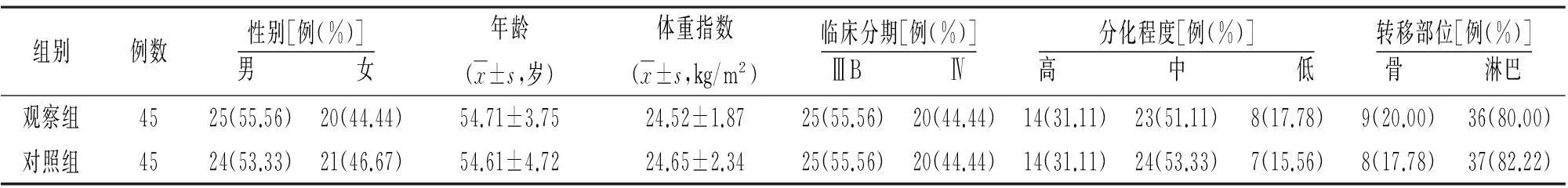
表1 兩組晚期肝細胞癌患者一般資料
注:對照組給予靶向治療,觀察組給予射頻消融聯(lián)合靶向治療
1.3方法
1.3.1藥物及試劑:吉非替尼片(英國阿斯利康制藥有限公司,規(guī)格:250 mg/片,批號:H301173);卡培他濱(瑞士羅氏制藥有限公司,規(guī)格:500 mg/片,批號:H0292);淋巴細胞分離液為天津TBD生物技術(shù)公司產(chǎn)品;CD3、CD4、CD8細胞檢測采用IgGrl-FITC/IgGr2a-PE、CD3-FITC/CD4-PE、CD3-FITC/CD8-PE、FacA Lysing Solution溶血素為美國BD公司產(chǎn)品,IgG、IgM、IgA體液免疫指標檢測采用美國BD公司提供的TriTEST CD3-PE/CD4雙色熒光試劑盒。
1.3.2儀器:LOGQ3型三維彩超儀為美國GE公司產(chǎn)品,探頭頻率為3.00~6.00 MHz;CT引導裝置為SIEMENS SOMATOMSensation 16排螺旋CT;RFA-Ⅱ多極射頻消融儀為北京博萊德光電技術(shù)開發(fā)有限公司提供(微電極展開后直徑2.0~4.0 cm); AxSYM型全自動免疫發(fā)光分度儀為美國雅培公司產(chǎn)品;Calibur型流式細胞儀為美國BD公司產(chǎn)品;AWED-432A型超低溫冰箱由日本三洋公司提供。
1.3.3治療方法:觀察組入院后即開始行RFA治療,術(shù)前禁食水,肌內(nèi)注射鹽酸哌替啶25 mg、鹽酸異丙嗪25 mg,平臥后行彩超檢查,根據(jù)彩超顯示的圖像選取最佳穿刺點及穿刺角度(必要時配以CT),常規(guī)消毒后鋪孔巾,用利多卡因在穿刺點處局部浸潤麻醉,將RFA多導電極穿刺到腫瘤部位,根據(jù)腫瘤的體積打開電極,每次消融采用90~100℃,持續(xù)時間根據(jù)腫瘤大小決定,一般為10~15 min,根據(jù)腫瘤體積及數(shù)量決定射頻消融的次數(shù)(直徑≤15 mm,消融1次;直徑>15 mm者,可以反復多次進針消融,但總次數(shù)應≤5次),退針時需要電凝止血,RFA 1周后給予靶向治療。對照組給予基礎(chǔ)治療1周后行靶向治療。
1.3.4靶向治療方案:兩組均于入院1周后開始口服靶向治療藥物,吉非替尼250 mg/d(治療過程中劑量不做調(diào)整),連續(xù)服用12周,出現(xiàn)以下情況需要終止或暫停口服:①急性消化道出血;②嚴重肝功能衰竭;③高血壓(Ⅲ級以上);④反復蛋白尿(>2 g/d)。卡培他濱按照0.7 g/m2,2/d,d1~14,3周為1個療程,連續(xù)服用4個療程,在治療過程中出現(xiàn)以下情況需要降低劑量20%:①第1次出現(xiàn)血液毒性(Ⅲ級);②第2次出現(xiàn)非血液毒性(Ⅱ級)或者任何時候出現(xiàn)非血液毒性(Ⅲ級)。出現(xiàn)以下情況需要降低劑量40%:①第1次出現(xiàn)血液毒性(Ⅳ級);②第2次出現(xiàn)血液毒性(Ⅲ級);③任何時候出現(xiàn)非血液毒性(Ⅳ級);④第2次出現(xiàn)非血液毒性(Ⅲ級)或者第3次出現(xiàn)非血液毒性(Ⅱ級)。出現(xiàn)以下情況應終止服用:①第2次出現(xiàn)血液毒性(Ⅳ級);②第3次出現(xiàn)血液毒性(Ⅲ級);③第4次出現(xiàn)非血液毒性(Ⅱ級);④第3次出現(xiàn)非血液毒性或者第2次出現(xiàn)非血液毒性(Ⅳ級)。
1.4檢測指標
1.4.1外周血細胞免疫指標檢測:治療前及治療后4周抽取靜脈血,用淋巴細胞分離液密度梯度離心法分離外周血中有核細胞,外周血中有核細胞染色標記30 min,溶血10 min,以3000 r/min離心10 min,棄去上清液,PBS液沖洗2次,隨后上機檢測,并采用Cellquest軟件進行樣本檢測。
1.4.2體液免疫指標檢測:治療前及治療后4周抽取靜脈血5 ml,注入玻璃試管中,靜置10 min,以3000 r/min離心10 min,分離血清在-70℃超低溫冰箱內(nèi)保存待測,用免疫散射比濁法檢測免疫球蛋白(IgG、IgM、IgA),操作過程嚴格按照試劑盒說明進行。

2結(jié)果
2.1細胞免疫指標觀察組治療后4周血清CD3、CD4、CD4/CD8與CD3+CD56+NK較治療前和對照組升高,CD8較治療前和對照組降低(P<0.05),對照組治療后4周CD3、CD4、CD4/CD8與CD3+CD56+NK較治療前降低,CD8較治療前升高(P<0.05),見表2。

±s)
注:對照組給予靶向治療,觀察組給予射頻消融聯(lián)合靶向治療;與同組治療前比較,aP<0.05;與對照組治療后4周比較,cP<0.05
2.2體液免疫指標觀察組治療后4周血清IgG、IgM、IgA濃度較治療前和對照組升高(P<0.05),對照組治療后4周血清IgG、IgM、IgA濃度較治療前降低(P<0.05),見表3。

±s,g/L)
注:對照組給予靶向治療,觀察組給予射頻消融聯(lián)合靶向治療;與治療前比較,aP<0.05;與對照組比較,cP<0.05
3討論
肝細胞癌是全球常見的消化系統(tǒng)惡性腫瘤[8-10],在消化系統(tǒng)惡性腫瘤中發(fā)病率僅次于胃癌,2007年美國癌癥協(xié)會公布的研究數(shù)據(jù)顯示:全球新發(fā)肝癌711 000例,病死率居所有惡性腫瘤的第3位,新發(fā)病例中發(fā)展中國家占80%以上,我國占55%以上[11]。近年來針對晚期肝細胞癌的治療仍局限于手術(shù)、放療和化療,但是這3種方法均不能很好地控制腫瘤細胞的轉(zhuǎn)移,而晚期肝細胞癌一旦確診后生存期為2~4個月,且這3種方法存在毒性作用應大、患者耐受性差等缺點[12]。
RFA治療是利用頻率在400~460 kHz范圍內(nèi)的電磁波作用于腫瘤組織內(nèi)部而殺死腫瘤細胞的方法,早在1990年,就已經(jīng)將RFA用于肝臟局部熱損傷的動物實驗模型[13-14]。2000年由美國學者Dupuy等[15]在國際首次報道,治療時通過彩超或CT引導下的射頻電極針經(jīng)皮穿刺進入腫瘤組織內(nèi),電極針發(fā)出的射頻電磁波可引起腫瘤細胞內(nèi)的極性分子發(fā)生震蕩,震動過程中分子間相互摩擦產(chǎn)生大量熱能,使腫瘤組織內(nèi)部溫度為90~110℃,高溫導致細胞內(nèi)蛋白質(zhì)的變性與DNA斷裂,同時高熱還能導致腫瘤周圍肝組織血管發(fā)生凝固閉合,可以有效防止出血與腫瘤細胞轉(zhuǎn)移。而周圍正常肝組織血流豐富,熱量很容易隨著血液散發(fā),使能量易于集聚,瘤體內(nèi)部壞死徹底,進而避免周圍正常組織的損傷[16-19]。
吉非替尼是一種表皮生長因子受體(epidermal growth factor receptor, EGFR)抑制劑[20],近年來使用最廣泛,應用于肺癌、肝細胞癌等的治療。在肝細胞癌的治療中,吉非替尼能阻斷細胞周期的G1/S期,抑制腫瘤細胞增生,但是針對31例原發(fā)性晚期肝細胞癌患者單獨使用吉非替尼治療的二期臨床試驗結(jié)果顯示,癥狀無明顯緩解,因此需要配合其他化療藥物使用,與其他化療藥物配合使用導致的毒性作用增多,耐受性較差,導致機體免疫力降低[21-22],而近年來研究表明,RFA治療肝細胞癌能使患者的免疫功能得到很好的改善[7],Dromi等[23]研究表明,經(jīng)RFA治療后的小鼠,瘤體內(nèi)可出現(xiàn)大量抗原提呈細胞的浸潤,增強了抗腫瘤免疫力。機體抗腫瘤主要通過細胞和體液免疫兩種方式進行,而細胞免疫是T淋巴細胞及CD3+CD56+NK細胞參與的一種重要免疫反應,而惡性腫瘤患者往往免疫功能受到嚴重的抑制,且經(jīng)放化療、手術(shù)創(chuàng)傷均能加重免疫抑制,表現(xiàn)為外周血中CD3、CD4、CD3+CD56+NK減少,這些均參與機體特異性細胞免疫反應,抑制淋巴細胞亞群CD8增多,CD4/CD8比例降低[24]。B細胞是機體內(nèi)參與體液免疫的一種重要淋巴細胞,其水平高低與血清抗體水平密切相關(guān),銀杏葉提取物能很好地提高機體血清抗體濃度,IgG、IgM是人體內(nèi)重要的免疫球蛋白,在體液免疫過程中發(fā)揮重要作用[25]。本研究結(jié)果顯示,觀察組治療后4周血清CD3、CD4、CD3+CD56+NK、CD4/CD8與IgG、IgM、IgA濃度較治療前升高,CD8較治療前降低,與朱玲燕等[26]研究結(jié)果相同,而對照組治療后4周血清CD3、CD4、CD3+CD56+NK、CD4/CD8與IgG、IgM、IgA濃度較治療前降低,CD8較治療前升高。提示靶向藥物聯(lián)合傳統(tǒng)化療藥物能導致患者機體免疫力降低[12]。治療后觀察組血清CD3、CD4、CD4/CD8、IgG、IgM、IgA濃度明顯高于對照組,CD8較對照組低。提示靶向治療聯(lián)合經(jīng)超聲引導下RFA能很好地糾正因靶向藥物治療導致的機體免疫力低下。
RFA穿刺治療晚期肝細胞癌轉(zhuǎn)移灶較少,治療過程中的注意事項及臨床經(jīng)驗為:①需要嚴格把握適用人群。本研究入選的病例均為彩超檢查示瘤體血供豐富,CT平掃結(jié)果顯示腫瘤轉(zhuǎn)移灶較少,且單個瘤體直徑≤6 cm,因為病灶太大,射頻消融不徹底易導致周圍血管閉合不完全,壞死的血管易導致大出血,目前的臨床經(jīng)驗提示對于直徑<3 cm、病灶數(shù)目<3個的肝細胞癌RFA治療效果已經(jīng)得到了充分肯定,直徑較大的病灶需要反復穿刺,而反復穿刺又易導致腫瘤細胞的轉(zhuǎn)移[27]。②肝臟血供豐富,含有大血管,結(jié)構(gòu)復雜,因此必要時需要配合CT甚至MRI檢查定位。李凱等[28]研究通過CT、MRI,甚至血管造影術(shù)對超聲顯示困難的肝細胞癌進行輔助性檢查。③肝功能Child-pluge分級為B或C級的患者不建議行RFA治療。因RFA前需要肝臟有較強的儲備力。黃伍奎等[14]證實,RFA后5 d肝轉(zhuǎn)氨酶水平升高,說明RFA對肝臟有一定破壞性,因此不建議肝功能較差者應用。④RFA治療前后可以皮下注射白介素-2(IL-2)。有研究報道,RFA聯(lián)合IL-2在小鼠模型實驗中能很好地抑制腫瘤細胞生長[29]。
綜上所述,RFA聯(lián)合靶向治療方案能很好地改善轉(zhuǎn)移灶較少的中晚期肝細胞癌患者的免疫功能,緩解靶向治療或傳統(tǒng)化療導致的免疫力降低,操作簡單安全,但其聯(lián)合免疫細胞靜脈滴注對中晚期肝細胞癌患者免疫功能的影響還需在今后進一步探索。
[參考文獻]
[1]劉麗莉,方勇,王凱峰,等.CT引導射頻消融治療膈頂部肝癌的臨床研究[J].腫瘤,2014,25(1): 4-10.
[2]李凱,劉波,曾慶勁,等.實時虛擬導航系統(tǒng)在肝細胞肝癌患者射頻消融治療中的應用價值[J].中華肝臟外科手術(shù)學電子雜志,2012,1(1):19-23.
[3]張軍,劉會春,周磊,等.原發(fā)性肝癌的射頻治療效果分析[J].肝膽外科雜志,2011,19(1):30-33.
[4]郭放,劉永葉,鄭振東,等.超聲引導下射頻消融治療原發(fā)性肝癌36例[J].解放軍醫(yī)藥雜志,2014,26(4):68-70.
[5]Bruix J, Sherman M. Asherman Association for the Study of Liver Diseases. Management of hepatocellular carcinoma: an update[J].Hepatology, 2011,53(3):1020-1022.
[6]Chakravarti A, Wang M, Robins H I,etal. RTOG 0211: a phase 1/2 study of radiation therapy with concurrent gefitinib for newly diagnosed glioblastoma patients[J].Int J Radiat Oncol Biol Phys, 2013,85(5):1206-1211.
[7]扈彩霞,鄭加生,錢智玲,等.原發(fā)性肝癌患者射頻消融前后外周血T淋巴細胞絕對值變化的臨床意義[J].北京醫(yī)學,2011,33(6):451-453.
[8]王康康,肖興國.肝細胞癌中Survivin、Livin蛋白的表達及其臨床意義[J].中國當代醫(yī)藥,2013,20(10):58-59.
[9]唐大平,林如景,王學健,等.索拉非尼治療中晚期肝細胞癌療效及血清甲胎蛋白水平變化意義分析[J].疑難病雜志,2014,13(5):451-455.
[10]王書長,黃萬里,黃書立,等.肝動脈化療栓塞結(jié)合射頻消融治療中晚期肝癌的臨床療效分析[J].中國醫(yī)藥科學,2015,5(4):7-9,37.
[11]Garcia M, Jemal A, Ward E M,etal. Global cancer facts & figures 2007. American Cancer Society[EB/OL].(2010-07-31)(2014-08-02).http://www.Cancer.org.
[12]Hsu C, Shen Y C, Cheng C C,etal. Geographic difference in survival outcome for advanced hepatocellular carcinoma: implications on future clinical trial design[J].Contemp Clin Trials, 2010,31(1):55-61.
[13]趙峰,鄂亞軍.經(jīng)導管動脈化療栓塞聯(lián)合射頻消融治療原發(fā)性肝癌臨床觀察[J].解放軍醫(yī)藥雜志,2014,26(8):60-63.
[14]黃伍奎,由麗娜,帕哈爾丁·白克熱,等.肝癌多點射頻消融術(shù)后肝功能和并發(fā)癥的研究[J].中國全科醫(yī)學,2012,15(9):3121-3124.
[15]Dupuy D E, Zaqoria R J, Akerley W,etal. Percutaneous radiofrequency ablation of malignancies in the lung[J].AJR Am roentqenol, 2000,174(1):57-59.
[16] Mizukoshi E, Nakamoto Y, Arai K,etal. Enhancement of tumor-specific T-cell responses by transcatheter arterial embolization with dendritic cell infusion for hepatocellular carcinoma[J].Int J Cancer, 2010,126(9):2164-2174.
[17]曾江正,郝新寶,張建輝,等.冷循環(huán)射頻消融治療中晚期肝癌的近期療效評價[J].海南醫(yī)學院學報,2010,16(12):1618-1620.
[18]范瑞芳,柴福錄,李榮梓,等.腹腔鏡射頻消融治療原發(fā)性肝癌的研究[J].西北國防醫(yī)學雜志,2009,30(3):171-173.
[19]范瑞芳,張超,肖毅,等.射頻消融輔助肝切除治療原發(fā)性肝癌的研究[J].西北國防醫(yī)學雜志,2012,33(6):621-623.
[20]Mok T, Wu Y L, Zhang L,etal. A small step towards personalized medicine for non-small-cell lung cancer[J].Discov Med, 2009,8(43):227-231.
[21]O'Dwyer P, Giantonio B, Levy D,etal. Gefinatinib in advanced unreasectable hepatocellular carcinoma: results from the Eastern Cooperative Oncology Group Study E1203[J].J Clin Oncol, 2006,24(18s):4143.
[22]王曉明,趙超塵,岑鈞華,等.吉非替尼聯(lián)合卡培他濱治療晚期肝細胞癌的療效觀察[J].中國現(xiàn)代醫(yī)生,2012,50(10):60-61.
[23]Dromi S A, Walsh M P, Herby S,etal. Radiofrequency ablation induces antigen-presenting cell infiltration and amplification of weak tumor-induced immunity[J].Radiology, 2009,251(1):58-66.
[24]謝天鵬,趙雍凡,劉華英,等.早期腸內(nèi)營養(yǎng)對食管癌術(shù)后全身炎性反應及細胞免疫功能的影響[J].四川醫(yī)學,2005,26(1):18-20.
[25]李曉輝,李軍民,馮秋霞,等.圍手術(shù)期腸內(nèi)營養(yǎng)支持對食管癌患者術(shù)后免疫功能的影響[J].中國醫(yī)學創(chuàng)新,2011,8(8):57-59.
[26]朱玲燕,龐雄昊,周嘉,等.小肝癌患者外周免疫狀態(tài)變化及手術(shù)、射頻消融治療的影響[J].山東醫(yī)藥,2012,52(42):1-3.
[27]Kobayashi M, Ikeda K, Kawamura Y,etal. Randomized controlled trial for the efficacy of hepatic arteria occlusion during radiofrequency ablation for small hepatocellular carcinoma-direct ablative effects and a long-term outcome[J].Liver Int, 2007,27(3):353-359.
[28]李凱,曾慶勁,鄭榮琴,等.導航引導和導航超聲造影輔助消融超聲顯示困難肝癌[J].中山大學學報:醫(yī)學科學版,2012,33(4):549-552.
[29]Fagnoni F F, Zerbini A, Pelosi G,etal. Combination of radiofrequency ablation and immunotherapy [J].Front Biosci, 2008,13(2):369-381.
(收稿時間:2014-12-28修回時間:2015-02-28)
·論著·
Effect of Radiofrequency Ablation Combined with Targeted Therapy under Ultrasound Guide on Immune Function of Patients with Advance Hepatocellular Carcinoma
CHEN Xu-lan1a, FU Jing-nan2b, LI Ying2, QU Bo1c(a. Department of Special Inspection, b. Department of Enterochirurgia, c. Department of Surgical Oncology, 1. Affiliated Hospital of Logistics Academy of the Chinese People's Armed Police Force, Tianjin 300162, China; 2. Department of Special Inspection, General Hospital of Tianjin Armed Police Force, Tianjin 300162, China)
[Abstract]ObjectiveTo investigate the effect of radiofrequency ablation (RFA) combined with targeted therapy under ultrasound guide on immune function of patients with advanced hepatocellular carcinoma. MethodsA total of 90 patients with advanced hepatocellular carcinoma during March 2011 and July 2014 were randomly divided into observation group (n=45) and control group (n=45). The observation group was treated with RFA under ultrasound guided for one week, and then targeted therapy of Gefitinib combined with Capecitabine followed; while the control group was treated with targeted therapy following basic therapy. The immune function indications of cells and body fluids were detected in the two groups before and after the treatment. ResultsIn observation group, the concentrations of CD3, CD4, CD4/CD8, CD3+CD56+NK, IgG, IgM and IgA 4 weeks after the treatment were significantly higher, while the CD8 concentration was significantly lower than those before the treatment in the same group and after the treatment in the control group (P<0.05); in the control group, the concentrations of CD3, CD4, CD4/CD8, CD3+CD56+NK, IgG, IgM and IgA 4 weeks after the treatment were significantly lower, while the CD8 concentration was significantly higher than those before the treatment in the same group (P<0.05). ConclusionRadiofrequency ablation combined with targeted therapy under ultrasound guide may significantly improve the immune function of patients with advanced hepatocellular carcinoma.
[Key words]Carcinoma, hepatocellular; Ultrasonic guidance; Catheter ablation; Targeted therapy; Immune function
[DOI]10.3969/j.issn.2095-140X.2015.05.012
[文獻標志碼][中國圖書資料分類號]R735.7A
[文章編號]2095-140X(2015)05-0041-05
[通訊作者]李穎,E-mail: tianjin2009001@163.com
[基金項目][作者單位]300162 天津,武警后勤學院附屬醫(yī)院特檢科(陳旭蘭),肛腸外科(付靖楠),腫瘤外科(屈波);300162 天津,武警天津市總隊醫(yī)院特檢科(李穎)

