吲哚-2,3-二酮對腫瘤壞死因子α所致大鼠主動脈平滑肌A7r5細胞增殖的影響Δ
劉占濤,楊志宏,趙永娟,冀立霞,郭錫春,岳 旺,尹 磊(青島大學醫學院藥學院,山東青島 266021)
動脈粥樣硬化(Atherosclerosis)是最常見的心血管疾病之一,主要累及大中動脈,并可引起一系列繼發性病變[1]。近年來,人們逐漸認識到動脈粥樣硬化等心血管疾病與炎性反應有著十分密切的關系。血管內皮細胞受損時,釋放大量的炎性因子如腫瘤壞死因子α(TNF-α)、白細胞介素6(IL-6)等,引起平滑肌細胞增殖,最終形成動脈粥樣硬化[2]。通過抑制血管平滑肌細胞移行及增殖的物質,可延緩或抑制動脈粥樣硬化病變的形成[3]。
吲哚-2,3-二酮的化學結構明確,生物活性廣泛。本課題組前期研究表明,其具有抗炎和抗動脈粥樣硬化的作用[4-6]。本研究采用大鼠主動脈平滑肌細胞A7r5,觀察吲哚-2,3-二酮對TNF-α所致A7r5 細胞增殖和細胞周期的影響,初步探討吲哚-2,3-二酮對動脈粥樣硬化炎性反應的作用機制,為其臨床應用提供參考。
1 材料
1.1 儀器
BB5060UV 型CO2培養箱(德國赫利公司);SW-CJ-40 型超凈工作臺(上海蘇凈實業有限公司);CKX41 型倒置顯微鏡(日本Olympus公司);550型酶標儀(瑞典Rosys Anthos公司);流式細胞儀(美國BD公司)。
1.2 藥品與試劑
吲哚-2,3-二酮(青島大學藥物研發基地提供,純度:99.7%);高糖改良馬丁瓊脂(DMEM)培養基、胎牛血清、MTT(美國Sigma 公司);碘化丙啶(PI)染液(南京凱基生物科技發展有限公司);TNF-α(北京天來生物醫學科技有限公司)。
1.3 細胞
大鼠主動脈平滑肌A7r5 細胞,購于中國科學院上海生命科學院細胞庫。
2 方法
2.1 培養基和溶液的組成
10%DMEM 培養基:10%胎牛血清、100 μg/ml 鏈霉素、100 u/ml青霉素、DMEM培養基。20%DMEM培養基:20%胎牛血清、100 μg/ml 鏈霉素、100 u/ml 青霉素、DMEM 培養基。磷酸鹽緩沖液(PBS):氯化鉀0.10 g/L、磷酸氫二鈉1.75 g/L、氯化鈉8.00 g/L、磷酸二氫鉀0.10 g/L,雙蒸水配制。
2.2 細胞的培養
取A7r5 細胞用10% DMEM 培養基培養,在37 ℃下5%CO2的培養箱內傳代培養,取指數生長期的細胞進行試驗。
2.3 吲哚-2,3-二酮試驗質量濃度的確定
收集指數生長期A7r5 細胞,確定細胞濃度為1×105ml-1,接種到96 孔板,每孔100 μl,24 h 細胞貼壁后分為(1)對照組:加入100 μl無血清培養基;(2)試驗組:加入含不同質量濃度吲哚-2,3-二酮的無血清培養基100 μl,最終質量濃度分別為10-11、10-10、10-9、10-8、10-7、10-6、10-5mg/ml。24 h后棄上清液,每孔加入MTT溶液20 μl,37 ℃孵育4 h后棄孔內液體,每孔加入150 μl 二甲基亞砜(DMSO)溶液,振蕩1 min,在570 nm 波長處檢測光密度(OD),用OD值表示細胞存活情況。試驗重復3次。以OD值確定吲哚-2,3-二酮的試驗質量濃度。
2.4 TNF-α造模質量濃度的確定
收集指數生長期A7r5 細胞,確定細胞濃度為1×105ml-1,每孔100 μl,接種到96 孔板內,24 h 細胞貼壁后,將培養基更換為無血清培養基,24 h后使細胞同步化于G0/G1期。將細胞分為(1)空白組:加入20%DMEM 培養基;(2)TNF-α組:加入含不同質量濃度TNF-α的20%DMEM培養基,使其最終質量濃度分別為0.078、0.156、0.625、2.5、5、10、20、40、80 ng/ml。48 h后棄去上清液,每孔加入MTT溶液20 μl,孵育4 h后吸出MTT 溶液,每孔加入DMSO 150 μl,在氣浴振蕩儀中振蕩10 min使結晶物完全溶解,在570 nm波長處檢測OD值。試驗重復3次。以OD值確定TNF-α的造模質量濃度。
2.5 吲哚-2,3-二酮對TNF-α所致A7r5細胞增殖的影響
收集指數生長期A7r5 細胞,確定細胞濃度為1×105ml-1,接種到96孔板內,每孔100 μl,24 h細胞貼壁后,將培養基更換為無血清培養基,24 h后使細胞同步化與G0/G1期。將細胞分為(1)空白對照組:加入20%DMEM培養基;(2)模型組:加入含5 ng/ml TNF-α的20% DMEM 培養基;(3)吲哚-2,3-二酮組:加入含5 ng/ml TNF-α和10-8、10-7、10-6、10-5mg/ml 吲哚-2,3-二酮的DMEM培養基。孵育48 h,棄去上清液,每孔加入20 μl MTT 溶液,孵育4 h 后吸出MTT 溶液,每孔加入DMSO 150 μl,在氣浴振蕩儀中振蕩10 min 使結晶物完全溶解,在570 nm波長處檢測OD值。試驗重復3次。
2.6 吲哚-2,3-二酮對TNF-α所致A7r5細胞增殖周期的影響
收集指數生長期A7r5 細胞,分組和給藥同“2.5”項,孵育48 h,用0.25%的胰蛋白酶溶液消化細胞并收集細胞,以預冷的PBS 溶液洗滌細胞2 次,將細胞重懸于70%的冰乙醇溶液中,-20 ℃固定1 h。再將各組細胞用PBS清洗1次,分別加入500 μl PBS 與5 μl RNA 酶于37 ℃孵育1 h,加入5 μl PI 染液,檢測各組細胞的周期分布。試驗重復3次。
2.7 統計學方法
采用SPSS 17.0 統計軟件對數據進行分析。數值均以表示,組間比較采用方差分析。P<0.05 表示差異具有統計學意義。
3 結果
3.1 吲哚-2,3-二酮試驗質量濃度的確定
結果顯示,與對照組比較,10-11、10-10、10-9、10-8、10-7、10-6、10-5mg/ml 的吲哚-2,3-二酮對A7r5 細胞的存活無明顯影響,差異無統計學意義(P>0.05)。綜合考慮,選擇吲哚-2,3-二酮的試驗質量濃度為10-8、10-7、10-6、10-5mg/ml,結果見表1。
表1 不同質量濃度吲哚-2,3-二酮對A7r5 細胞存活的影響(,n=3)Tab 1 Effects of different concentrations of indol-2,3-dione on A7r5 cell survival(,n=3)
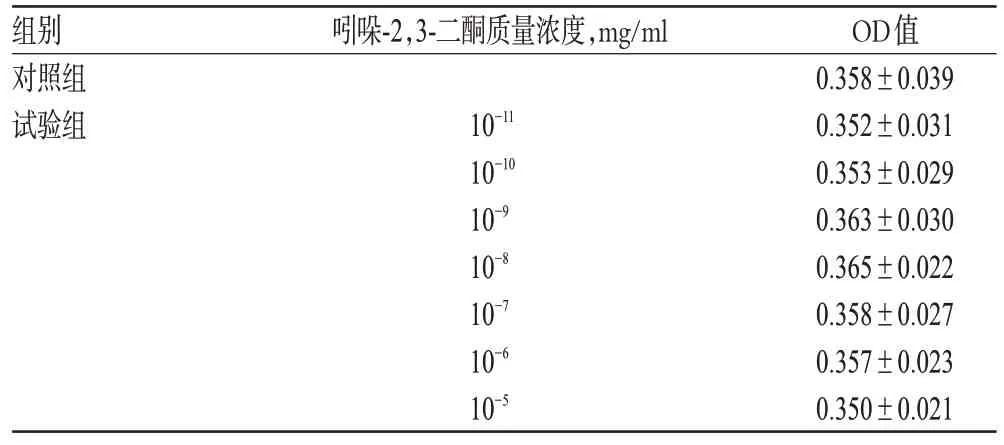
表1 不同質量濃度吲哚-2,3-二酮對A7r5 細胞存活的影響(,n=3)Tab 1 Effects of different concentrations of indol-2,3-dione on A7r5 cell survival(,n=3)
3.2 TNF-α造模質量濃度的確定
與空白組比較,0.078、0.156、0.625、2.5、5、10、20、40、80 ng/ml的TNF-α均能增加A7r5細胞的存活,差異具有統計意義(P<0.01)。其中5 ng/ml TNF-α與其余質量濃度比較,細胞存活增加更明顯,差異具有統計學意義(P<0.01)。因此,確定5 ng/ml為TNF-α的造模質量濃度。不同質量濃度TNF-α對A7r5細胞存活的影響見表2。
表2 不同質量濃度TNF-α對A7r5 細胞存活的影響(,n=3)Tab 2 Effects of different concentrations of TNF-α on A7r5 cell survival(,n=3)
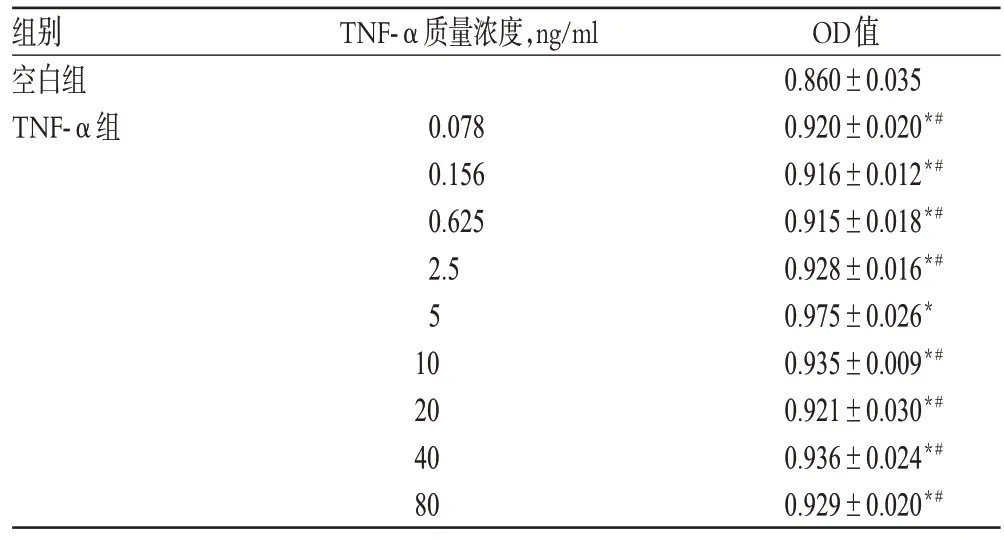
表2 不同質量濃度TNF-α對A7r5 細胞存活的影響(,n=3)Tab 2 Effects of different concentrations of TNF-α on A7r5 cell survival(,n=3)
注:與空白組比較,*P<0.01;與5 ng/ml比較,#P<0.01Note:vs.blank group,*P<0.01;vs.5 ng/ml,#P<0.01
3.3 A7r5細胞的增殖變化
與空白對照組比較,模型組A7r5細胞的OD值明顯增加,差異具有統計學意義(P<0.05)。與模型組比較,10-7、10-6、10-5mg/ml吲哚-2,3-二酮組A7r5細胞的OD值明顯減小,差異具有統計學意義(P<0.01 或P<0.05),其余差異無統計學意義(P>0.05)。各組細胞的增殖變化見表3。
表3 各組細胞的增殖情況(,n=3)Tab 3 The proliferation of cells in each group(,n=3)

表3 各組細胞的增殖情況(,n=3)Tab 3 The proliferation of cells in each group(,n=3)
注:與空白對照組比較,*P<0.05;與模型組比較,#P<0.05,##P<0.01Note:vs.blank control group,*P<0.05;vs.model group,#P<0.05,##P<0.01
3.4 A7r5細胞周期變化
與空白對照組比較,模型組A7r5細胞S期與G2/M期明顯增加,G0/G1期細胞明顯減少,差異具有統計學意義(P<0.05)。與模型組比較,10-8mg/ml吲哚-2,3-二酮組A7r5細胞G2/M 期明顯減少,10-7、10-6mg/ml 吲哚-2,3-二酮組S 期細胞均明顯減少,差異具有統計學意義(P<0.05),其余差異無統計學意義(P>0.05)。各組細胞的細胞周期分布情況見表4。
表4 各組細胞的細胞周期分布情況(,n=3)Tab 4 Distribution of cell cycle in each group(,n=3)
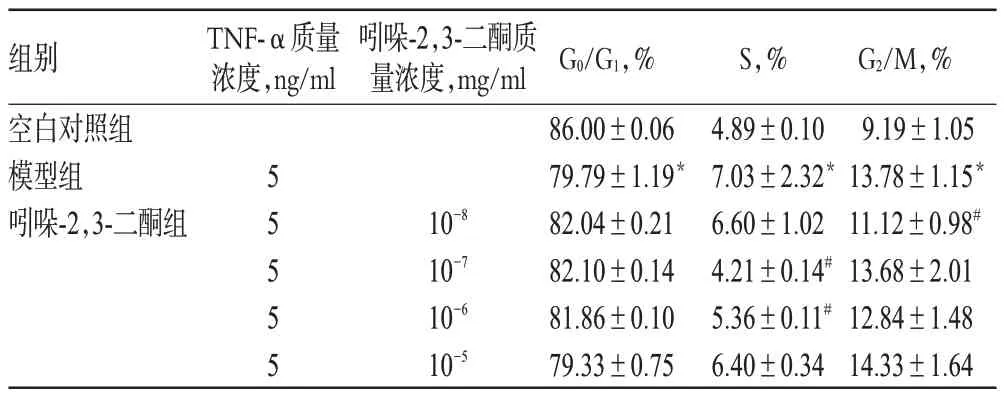
表4 各組細胞的細胞周期分布情況(,n=3)Tab 4 Distribution of cell cycle in each group(,n=3)
注:與空白對照組比較,*P<0.05;與模型組比較,#P<0.05Note:vs.blank control group,*P<0.05;vs.model group,#P<0.05
4 討論
血管平滑肌細胞的移行和過度增殖在動脈粥樣硬化發生和發展過程中起著關鍵的作用[6]。當血管內皮細胞損傷時,釋放大量的TNF-α、IL-6 等炎性因子。在其刺激下,血管平滑肌細胞、內皮細胞和巨噬細胞可以合成并分泌大量的纖維母細胞生長因子、血小板源性生長因子等生長因子,使內膜平滑肌細胞增殖,中膜平滑肌細胞遷移至內皮下間隙,攝取脂質,逐步形成泡沫細胞,產生膠原、彈性纖維及蛋白多糖等,最終形成動脈粥樣硬化。
本文用不同質量濃度的吲哚-2,3-二酮處理平滑肌A7r5細胞,觀察其對A7r5細胞的增殖有無影響,從而為后續研究的試驗質量濃度確定提供依據。本試驗結果表明,吲哚-2,3-二酮在高質量濃度(10-5mg/ml)時,對細胞增殖無影響。結合對吲哚-2,3-二酮的其他藥理作用的研究結果[4],選用10-8、10-7、10-6、10-5mg/ml這4個質量濃度作為本文中吲哚-2,3-二酮的試驗質量濃度。
TNF-α是一種重要的前炎性細胞因子,出現在炎癥早期,呈現出趨化、活化中性粒細胞及單核細胞,促進血管內皮細胞表達黏附分子等多種生物學活性,還能增加平滑肌細胞表達E-selectin,從而促進動脈粥樣硬化斑塊形成[7]。本試驗采用不同質量濃度的TNF-α處理平滑肌A7r5細胞,觀測其對A7r5細胞增殖的影響。結果表明,各質量濃度TNF-α均能明顯促進A7r5 細胞的增殖,以TNF-α 5 ng/ml 促增殖作用最為明顯,因此最終確定5 ng/ml為TNF-α造模質量濃度。結合對吲哚-2,3-二酮最大無毒濃度的探究,探討吲哚-2,3-二酮拮抗TNF-α誘導平滑肌細胞增殖的作用。結果表明,吲哚-2,3-二酮對5 ng/ml TNF-α誘導的A7r5 細胞的增殖有明顯的抑制作用,提示吲哚-2,3-二酮抗動脈粥樣硬化炎性反應的作用機制與抑制平滑肌細胞的增殖有關。
據報道,調控細胞周期也是控制細胞增殖的關鍵環節之一[8-9]。本試驗采用5 ng/ml TNF-α誘導A7r5細胞增殖,同時用不同質量濃度的吲哚-2,3-二酮進行干預,觀測其對A7r5細胞周期的影響。結果表明,TNF-α可增加A7r5 細胞S 期和G2/M期的比例,即促進A7r5 細胞的增殖。經吲哚-2,3-二酮干預后,部分G2/M 期、S 期細胞比例下降,使細胞增殖周期停滯于G0/G1期,從而抑制A7r5細胞的增殖。這提示吲哚-2,3-二酮抑制A7r5細胞增殖的作用可能與阻止細胞周期有關。
本文從細胞水平初步研究表明,吲哚-2,3-二酮對TNF-α所致血管平滑肌細胞增殖和細胞周期具有抑制作用,為進一步尋找天然低毒的抗動脈粥樣硬化藥物提供了參考。
[1]柴惠,余軍偉,馬建龍,等.黃連素對腫瘤壞死因子TNFα介導的炎癥作用機理研究[J].浙江中醫藥大學學報,2011,35(4):489.
[2]楊征,邱敏,郭曉華,等.瓜蔞皮提取物對PDGF-BB所致血管平滑肌細胞增殖周期的影響[J].中國動脈硬化雜志,2012,20(10):899.
[3]方立,李迎,祁珩.內皮祖細胞條件培養液對血管緊張素Ⅱ所致血管平滑肌細胞增殖的抑制作用[J].中國動脈硬化雜志,2013,21(11):997.
[4]黃霞,劉占濤,楊麗卿,等.吲哚-2,3-二酮的抗炎藥理作用[J].齊魯醫學雜志,2008,23(3):258.
[5]劉占濤,岳旺,楊志宏,等.2,3-吲哚醌抗鵪鶉動脈粥樣硬化作用及其機制研究[J].中國藥房,2009,20(4):256.
[6]劉占濤,楊志宏,趙永娟,等.2,3-吲哚醌對實驗性動脈粥樣硬化調血脂作用的研究[J].中國藥理學通報,2006,22(10):1 279.
[7]徐鳳芹,徐浩,劉劍剛,等.芎芍膠囊對動脈粥樣硬化兔血管平滑肌細胞增殖的影響[J].中國中西醫結合雜志,2008,28(10):912.
[8]曹文疆,邢建國,王新春,等.香青蘭總黃酮對TNF-α誘導的大鼠血管平滑肌細胞增殖的影響[J].中國實驗方劑學雜志,2011,17(21):159.
[9]趙海梅,譚翌,楊小端.TNF-α誘導的衰老血管內皮細胞中泛素、細胞周期的變化及意義[J].山東醫藥,2013,53(5):25.

