綠色氫氧燃料電池實驗的設計與優化
張寶軍


【摘 要】根據氫氧燃料電池的構造原理,以實驗室常規儀器搭建、整合的氫氧燃料電池演示臺,操作簡單,現象明顯,能較好提高高中化學課堂教學的效率,幫助學生提升對燃料電池的感性認識。
【關鍵詞】氫氧燃料電池;電解水;演示臺
1.問題的提出
1839年,英國科學家William Grove設計出了第一款燃料電池,之后,燃料電池得到了廣泛的研究。隨著能源危機的出現,因具有能量轉化效率高、產生污染物少等優勢的燃料電池更得到了進一步的關注。
目前氫氧燃料電池按電解質的種類不同,可分為堿性燃料電池(AFC)、質子交換膜燃料電池(PEMFC)、磷酸燃料電池(PAFC)熔融碳酸鹽燃料電池(MCFC)、固體氧化物燃料電池(SOFC)五大類,廣泛應用于航天、汽車等眾多領域。
生活中燃料電池并不常見,學生對其缺乏感性認識。現行人教版教材必修2盡管有對氫氧燃料電池原理的介紹,但缺少相關實驗的設計、呈現。學生通常會錯誤的認為燃料電池就是通過燃料的燃燒而產生電流。筆者想若能讓學生看到一個真實的、可以觸及到的氫氧燃料電池,相信對調動他們學習化學熱情,加深對原電池工作原理的認識應大有裨益。
2.實驗用品與原理
2.1實驗用品 U形管、36伏學生電源、雙孔橡皮塞(2個)、多孔碳棒電極(2支)、30cm的玻璃管(2支)、導線若干(帶有鱷魚夾)、靈敏電流計、小鬧鐘、發光二極管、Na2SO4溶液(或稀硫酸、NaOH溶液)。
2.2實驗原理 利用電解產生的H2、O2(其中含有活性氫,活性氧)吸附的多孔碳棒電極表面構成簡易氫氧燃料電池,產生的電能帶動小型用電器工作。
3.裝置的設計與優化
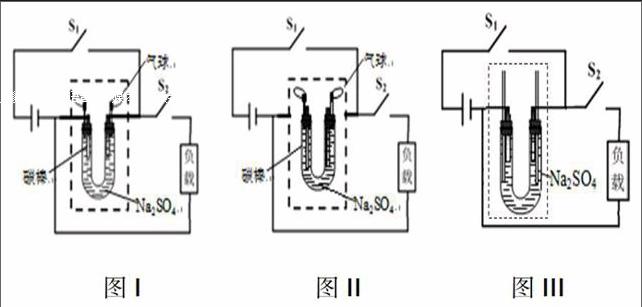
圖I ? ? ? 圖II ? ? ?圖III
在控制電解時的電壓、電解時間及電解液一定的情況下,我們按圖I~III裝置進行實驗,實驗對應編號依次為1號、2號、3號,記錄有關現象并對比分析如下。
4.電解質溶液的選擇
受常見的幾種燃料電池結構的啟發,我們分別向圖III裝置U型管加入了相同濃度Na2SO4、H2SO4、NaOH溶液,在電解相同時間后,將產生氣體構成燃料電池并使用電壓表測量電壓。實驗數據顯示,在Na2SO4溶液作為電解質時電池電壓最大。
實驗中我們還從0.2mol/L~1.4mol/LNa2SO4溶液,每隔0.2mol/L做一個實驗,發現電解質溶液濃度在0.8mol/L~1.1mol/L時電池工作時間最長(小鬧鐘持續運轉的時間)。
5.實驗改進的優勢
⑴實驗中所需多孔碳棒電極來源廣泛。從廢舊的干電池中取出碳棒清洗潔凈即可使用,無需另外進行淬火處理。
⑵實驗裝置的搭建均采用實驗室常規儀器,搭建簡單,可推廣性強。實驗研究的過程中也曾嘗試使用了圖V裝置(山形管)進行實驗,現象同樣非常明顯但考慮制作這樣一種特殊儀器的成本較高,可推廣性不強故選擇了圖IV裝置。
⑶通過排水法收集H2、O2可大幅度提高電極周圍氣體的純度,由于玻璃管中液體的壓力更利于氣體吸附在電極周圍,延長了放電的時間。筆者曾用電解了3分鐘產生的氣體構成燃料電池,并與小鬧鐘相連,結果整整走了一節課。
⑷根據圖III,我們把實驗所需儀器合在一個平臺上(如圖V)。操作簡單,只要將鱷魚夾與電解相連,通過電鍵的斷開和閉合就可以完成所有的檢驗。實驗現象明顯,實驗成功率高、趣味性強,可推廣為學生實驗。同時也為農村中學老師的化學實驗創新提供了一條新的思路。
【參考文獻】
[1]王祖浩.普通高中課程標準實驗教科書·化學2.南京:江蘇教育出版社,2007:42~43
[2]袁青云.制作綠色燃料電池的新實驗.化學教學.2009年第5期
(作者單位:江蘇省如皋中學)

