殼聚糖包埋魔芋組合物對Pb(Ⅱ)和膽固醇的吸附研究
朱唯唯,羅立新,王 玉
(武漢大學化學與分子科學學院,湖北武漢 430072)
殼聚糖包埋魔芋組合物對Pb(Ⅱ)和膽固醇的吸附研究
朱唯唯,羅立新*,王 玉
(武漢大學化學與分子科學學院,湖北武漢 430072)
將魔芋葡甘聚糖顆粒在常溫下溶于殼聚糖稀酸溶液制成的包埋液,制備能夠保持魔芋助消化及降低血中膽固醇濃度等優(yōu)良特性的新品種魔芋,并用紅外光譜儀進行表征。通過靜態(tài)吸附的方法系統(tǒng)探討了吸附質(zhì)初始濃度、吸附劑用量、吸附時間對Pb2+和膽固醇吸附效果的影響,并采用吸附動力學模型和等溫吸附方程進行擬合。結(jié)果表明:產(chǎn)品同時具有魔芋葡甘聚糖和殼聚糖的功能基團;在37 ℃下,Pb2+和膽固醇的最大去除率分別為95.2%和48.7%;吸附過程符合準二級動力學方程和Freundlich吸附等溫模型。說明殼聚糖包埋魔芋組合物可有效地吸附Pb2+和膽固醇,且屬于不均勻表面的吸附。
魔芋葡甘聚糖,吸附,鉛離子,膽固醇,包埋
魔芋是一種廣泛種植于我國西部山區(qū)的經(jīng)濟作物,魔芋葡甘聚糖是其主要成分,也是國際衛(wèi)生組織推薦的理想膳食纖維,具有不產(chǎn)生熱量、強吸水、可凝膠化特性[1],在食品、保健、醫(yī)藥等多方面有重要用途[2],能夠助控體重[3]、排除重金屬離子[4]、控制血脂[5]、緩解便秘[6]及控制血糖[7]等。目前,針對魔芋膳食纖維特性的研究主要集中于直接使用的魔芋或交聯(lián)后的魔芋顆粒[8],但魔芋葡甘聚糖在熱水中會快速溶解,使得魔芋粉劑沖制的飲料會快速凝膠化,飲用方式也不太符合人們的常規(guī)要求,而交聯(lián)又犧牲了魔芋的特性。所以,在保持魔芋原有的優(yōu)良特性的基礎上,開發(fā)出一種便于使用的魔芋產(chǎn)品顯得尤為重要。殼聚糖是甲殼素經(jīng)濃堿脫乙酰基后得到的衍生物,溶于稀酸,因此本文設計了一種殼聚糖包埋魔芋組合物[9],其在水中不溶或慢速溶解,可以保留魔芋葡甘聚糖的大多數(shù)優(yōu)良特性,用于制備魔芋固體飲料原料或用作化妝品的添加劑等。對于這種產(chǎn)品的特性研究,本文選用高血脂代表性物質(zhì)膽固醇和以Pb2+為代表的重金屬離子為對象,考察了吸附效果,分析了吸附質(zhì)濃度、吸附劑質(zhì)量及吸附時間對吸附效果的影響,并用動力學模型和等溫方程對其吸附行為進行了研究,以通過模擬實驗的方式為其應用提供一定的理論基礎。
1 材料與方法
1.1 材料與儀器
魔芋粉(葡甘聚糖含量82.29%,125~180 μm) 武漢纖濃生物科技有限公司;殼聚糖(脫乙酰化度90%) 濰坊海之源生物制品有限公司;殼聚糖包埋魔芋組合物 自制;其他試劑均為國產(chǎn)分析純。
UV752紫外可見分光光度計 上海佑科儀器儀表有限公司;SHA-c數(shù)顯水浴恒溫振蕩器常州博遠實驗分析儀器廠;JZ-2數(shù)顯離心機 金壇市洪科儀器廠;傅里葉紅外光譜儀iS10 美國Thermo公司。
1.2 實驗方法
1.2.1 吸附材料的制備 根據(jù)文獻[9]將1.5 g殼聚糖溶于含有2.25 mL冰醋酸的150 mL 30%乙醇溶液(體積百分數(shù)),配制成包埋液。于室溫下在包埋液中加入20 g魔芋粉,攪拌30 min后再加入4. 5 g碳酸鈉進入體系中,60 ℃固化2 h。經(jīng)離心分離固形物,清洗干燥后即得殼聚糖包埋魔芋組合物原料(KGM@CTS),包埋組合示意圖如圖1,魔芋葡甘聚糖顆粒表面被殼聚糖包裹。包埋前后官能團的變化采用FT-IR進行分析。
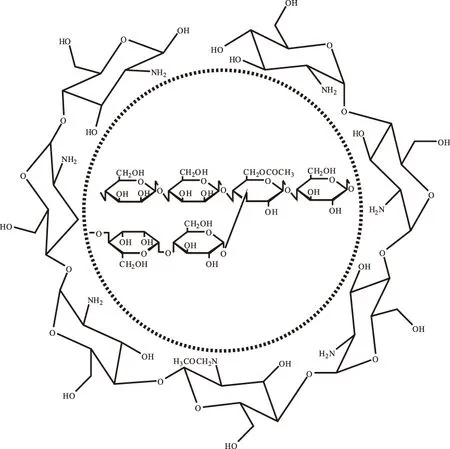
圖1 包埋組合示意圖Fig.1 Scheme of embedding
1.2.2 濃度的測定 Pb2+和膽固醇濃度的測定分別參照GB7470-87水質(zhì)鉛的測定 雙硫腙分光光度法[10]和GB/T5009.128-2003食品中膽固醇的測定[11]。
1.2.3 不同初始濃度對吸附的影響 配制50 mL一系列質(zhì)量濃度的吸附質(zhì)溶液,其中,Pb2+和膽固醇分別處于pH為5.5的緩沖溶液和冰乙酸溶液中,均加入1.0 g/L KGM@CTS,在37 ℃恒溫振蕩120 min,離心分離,取上層清液測定剩余吸附質(zhì)的濃度,每組實驗均重復3次,取平均值,用吸附量[12]表示吸附效果。
1.2.4 不同吸附劑質(zhì)量對吸附的影響 分別配制50 mL 240 mg/L Pb2+溶液和3.0 g/L膽固醇溶液,均加入一系列質(zhì)量濃度的 KGM@CTS,在37 ℃恒溫振蕩120 min,離心分離后測定,用去除率[12]表示吸附效果。
1.2.5 不同吸附時間對吸附的影響 配制50 mL 240 mg/L Pb2+溶液和3.0 g/L膽固醇溶液,分別向其中加入2 g/L和1 g/L KGM@CTS,均在37 ℃恒溫振蕩一系列不同的時間,離心分離后測定,用吸附量表示吸附效果。
1.2.6 不同pH對吸附的影響 研究發(fā)現(xiàn)[13],大多數(shù)膳食纖維在pH為6時對金屬離子的束縛能力最強,pH為0.65時解析釋放,所以,本文考察了pH對于Pb2+吸附的影響,設計了一組實驗:配制50 mL 240 mg/L Pb2+溶液,改變?nèi)芤旱膒H分別為2.5、3.5、4.5、5.5、6.5,加入2.0 g/L KGM@CTS,在37 ℃恒溫振蕩80 min,離心分離后測定,用去除率表示吸附效果。
1.2.7 正交設計實驗 對于Pb2+,在確定的初始濃度、吸附劑質(zhì)量、吸附時間和pH單因素實驗結(jié)果的基礎上,選用L9(34)正交表1進行實驗;在膽固醇正交實驗中,對初始濃度、吸附劑質(zhì)量和吸附時間三個因素選用L9(33)正交表2進行,以去除率為考察指標,找出最佳吸附條件。

表1 Pb2+正交設計表
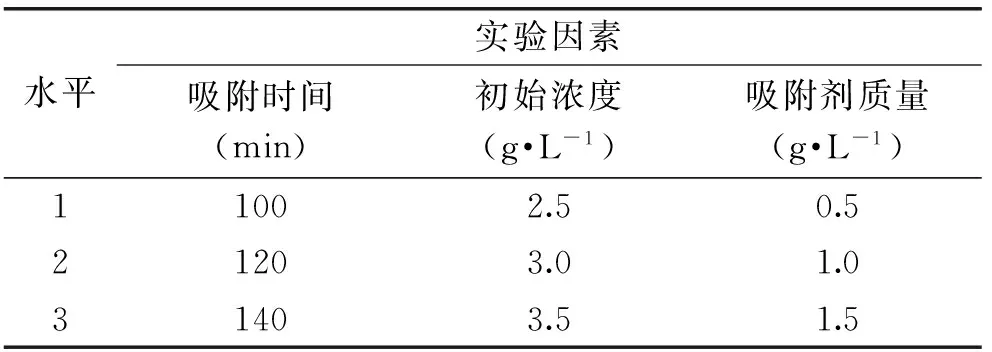
表2 膽固醇正交設計表
2 結(jié)果與討論
2.1 殼聚糖包埋魔芋組合物的表征
在圖2中,a和b的顯著差別在于1600 cm-1處殼聚糖有-NH2面內(nèi)彎曲振動吸收峰,而c中可以看到1574 cm-1的殼聚糖特征峰,說明殼聚糖包埋效果的存在。從d中可以看出,KGM@CTS用稀酸溶洗再用醇析出后的固體成分的譜圖中殼聚糖特征峰幾近消失,可以認為這主要是殼聚糖被溶解后的魔芋成分。
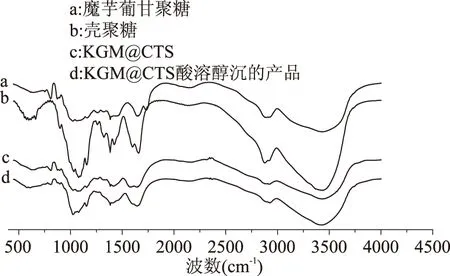
圖2 紅外光譜圖Fig.2 FT-IR spectra
2.2 不同條件對殼聚糖包埋魔芋組合物吸附性能的影響
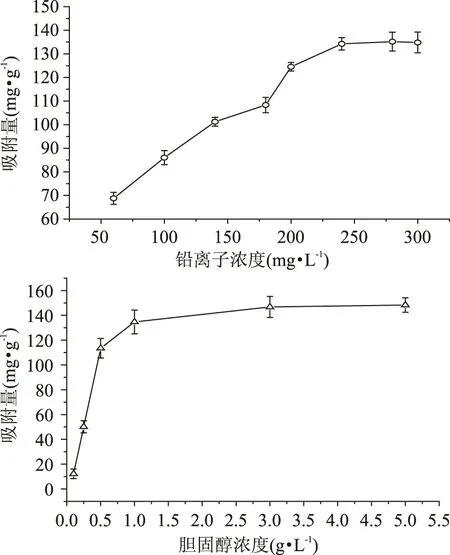
圖3 初始濃度對吸附效果的影響Fig.3 Effect of initial concentration on sorption efficiency
2.2.1 初始濃度對吸附效果的影響 實驗結(jié)果如圖3所示,對于鉛離子,吸附量隨著Pb2+濃度升高而明顯增大,然后趨于平衡達到飽和狀態(tài)。當初始濃度由60 mg/L提高到240 mg/L時,吸附量由68.77 mg/g增至134.26 mg/g,由于魔芋顆粒易溶于水無法形成吸附對比,而羅立新等[8]研究的不溶于水的交聯(lián)魔芋葡甘聚糖微球離子交換容量為約44 mg/g,這說明KGM@CTS對Pb2+的吸附能力要優(yōu)于交聯(lián)魔芋葡甘聚糖,同時也表明,在未達到飽和狀態(tài)之前,Pb2+濃度越大,該材料的利用率也越高。
對于膽固醇,KGM@CTS的吸附作用隨其濃度增加而增大,在膽固醇濃度為0.1~1.0 g/L時,吸附量明顯增加,濃度為1.0~3.0 g/L時,吸附量增幅較小。在3.0 g/L左右時,吸附量達到最大值146.80 mg/g,與陳亞非等[14]研究的水不溶性膳食纖維對膽固醇的作用所得到的最高吸附量40.75 mg/g,本文結(jié)果更好。
2.2.2 吸附劑的質(zhì)量對吸附效果的影響 實驗結(jié)果如圖4所示,可以看出,吸附劑的用量會明顯影響其吸附效率,Pb2+的去除率在吸附劑加入量為2 g/L時達到最大值92.5%,膽固醇的去除率在吸附劑加入量為1 g/L時達到最大值36.0%。研究表明,在同樣的吸附條件下,KGM@CTS對二者的吸附作用有較大不同,這可能跟兩者與KGM@CTS結(jié)合方式的不同及溶液的性質(zhì)有較大關(guān)系。
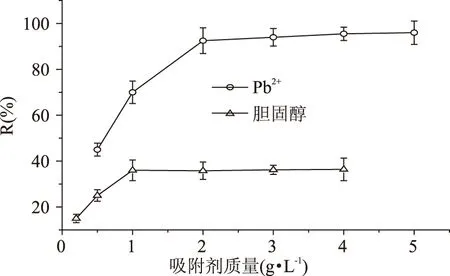
圖4 吸附劑質(zhì)量對吸附效果的影響Fig.4 Effect of adsorbent dosage on sorption efficiency
2.2.3 吸附時間對吸附效果的影響 實驗結(jié)果如圖5所示,可以看出,在吸附初始階段,吸附劑對Pb2+的吸附呈線性遞增趨勢,在進行80 min左右的時候接近最大值并進入平衡狀態(tài),而對于膽固醇,在120 min時,達到了吸附平衡,吸附量為129.76 mg/g,平衡后隨著時間的增大,吸附量基本不變。
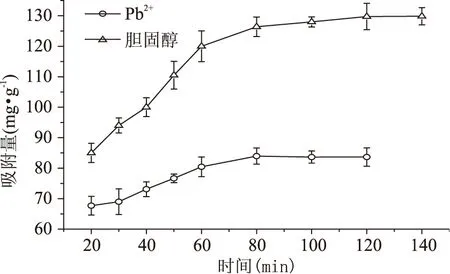
圖5 吸附時間對吸附效果的影響Fig.5 Effect of contact time on sorption efficiency
2.2.4 pH對吸附效果的影響 溶液的pH是影響吸附劑對金屬離子吸附的重要因素之一,pH的大小不僅影響吸附點解離,而且影響重金屬離子的溶液化學。pH>6.5時,溶液中的Pb2+會發(fā)生水解,形成Pb(OH)+、Pb(OH)2、Pb(OH)3-,此時吸附劑表面為負電荷,與Pb(OH)3-互相排斥,不利于吸附。如圖6中實驗結(jié)果所示,在pH從2.5增加到5.5的階段,吸附劑對Pb2+的去除率幾乎呈線性增加,pH為2.5時,去除率為25%,pH為5.5時,去除率增加到93%,當pH比較低時,溶液中主要以Pb2+和Pb(OH)+的形式共存,與存在的大量H+會形成競爭吸附的關(guān)系,pH升高,溶液中H+的數(shù)量減少,競爭關(guān)系減弱,有利于Pb2+的吸附,其去除率隨之增大[15]。

圖6 pH對吸附效果的影響Fig.6 Effect of pH on sorption efficiency
2.2.5 正交實驗 Pb2+吸附的正交實驗結(jié)果如表3所示,由極差R分析可知,各因素對其吸附效果的影響大小順序為:pH>吸附劑質(zhì)量>初始濃度>吸附時間,最優(yōu)組合為A2B2C3D2,即吸附80 min,初始濃度240 mg/L,吸附劑質(zhì)量2.5 g/L,溶液pH為5.5。此條件下,去除率達到95.2%。
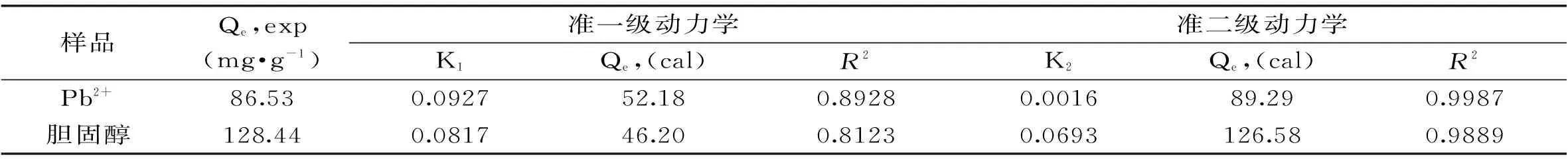
表5 KGM@CTS吸附劑對Pb2+和膽固醇吸附動力學擬合參數(shù)
膽固醇吸附的正交實驗結(jié)果如表4所示,各因素對其吸附效果的影響大小順序為:初始濃度>吸附劑質(zhì)量>吸附時間,最優(yōu)組合為A2B2C3,即吸附120 min,初始濃度為3.0 g/L,吸附劑質(zhì)量為1.5 g/L。此條件下,去除率達到48.7%。
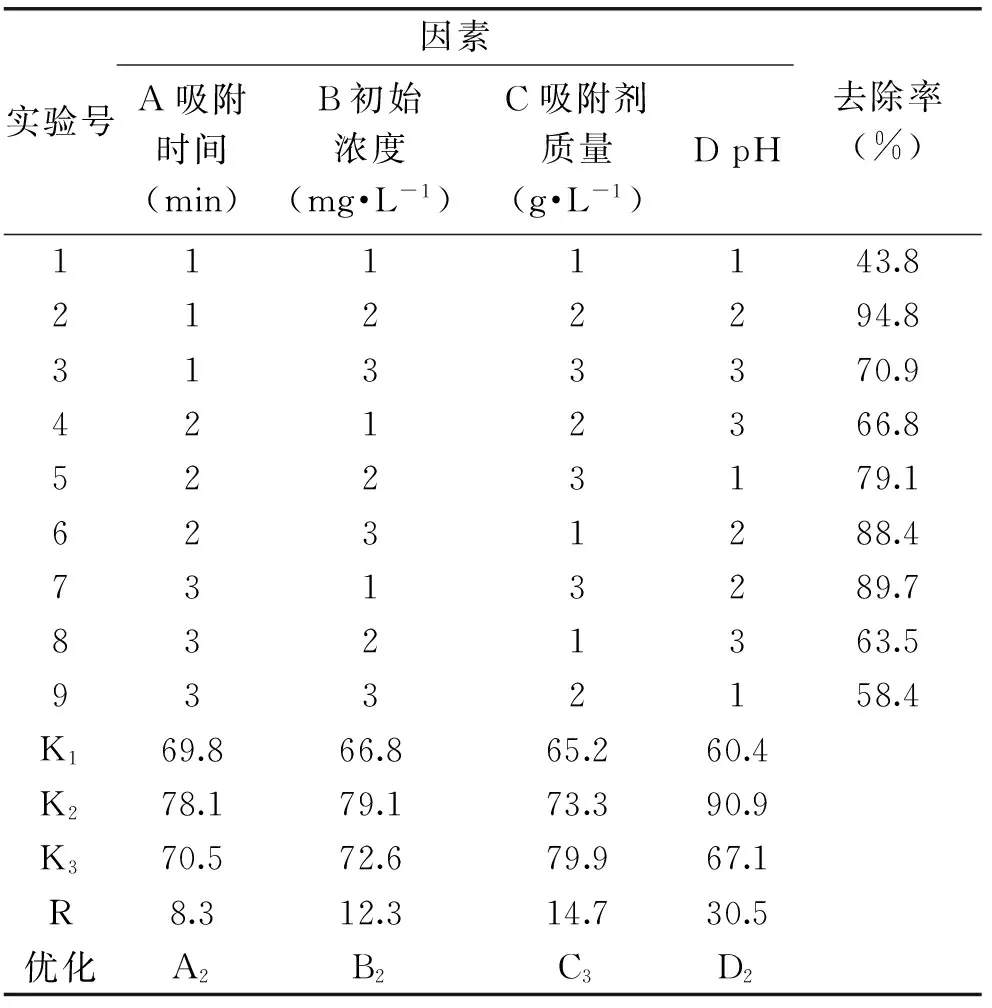
表3 Pb2+正交實驗結(jié)果
2.2.6 吸附動力學研究 對實驗所得數(shù)據(jù)分別采用準一級和準二級動力學模型[16]進行擬合,所得曲線如圖7,參數(shù)列于表5。從圖7可以看出,KGM@CTS對Pb2+和膽固醇吸附的準二級動力學模型擬合的很好(準一級模型圖略)。在準一級動力學模型中,在吸附初始階段擬合較好,但隨著時間的延長,擬合度不高,產(chǎn)生這一現(xiàn)象主要是因為在準一級動力學中反應速率只與濃度因素有關(guān),在吸附的初始,由于吸附劑表面有大量的活性位點,而活性位點隨著時間的延長而減小,當減少到一定程度的時候,其吸附過程不只受到溶液濃度的控制,因此隨著時間的延長會出現(xiàn)非線性的關(guān)系。在準二級動力學模型中吸附反應不僅受濃度一種因素的影響,還受活性位點的影響,從表5中可以看出,準二級動力學擬合曲線計算出的吸附量和實驗值更加相近,也更加證實了此吸附更適合用準二級動力學模型來描述。
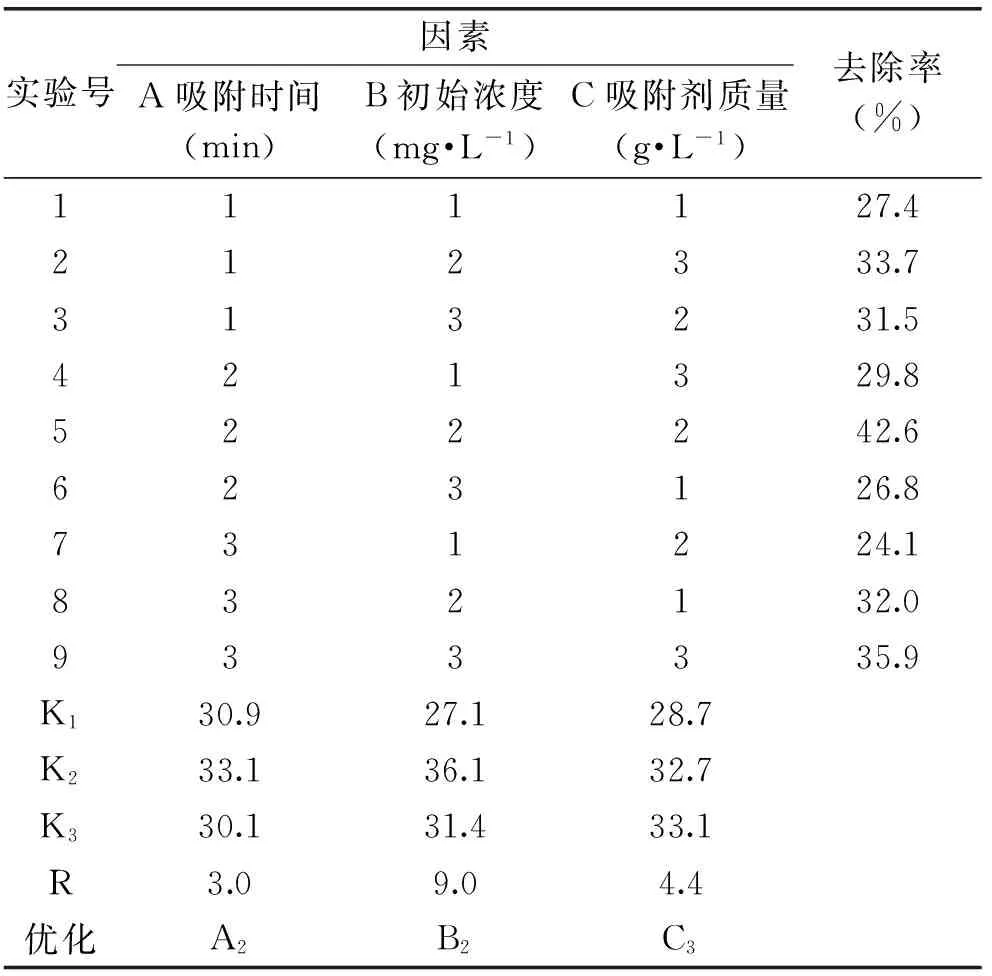
表4 膽固醇正交實驗結(jié)果
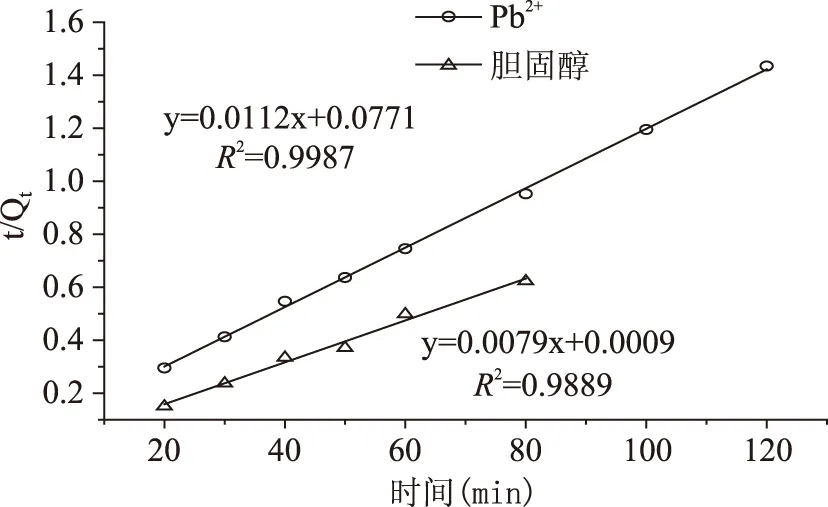
圖7 準二級動力學模型Fig.7 Pseudo-second-order simulation plot
2.2.7 吸附等溫線方程 常用來描述液-固體系吸附過程的是Langmuir和Freundlich吸附方程式。Langmuir[17]模型成立的條件是吸附劑表面均勻,每個吸附位點只吸附一個分子且被吸附的分子之間沒有相互作用力,即單分子層吸附;Freundlich模型則不限定單分子吸附,可以適用于表面不均勻的現(xiàn)象,是一個簡單的經(jīng)驗公式,更適用于低濃度的溶液或氣壓較低的吸附狀態(tài),既能很好地描述不均勻表面的吸附機理,又能夠在更廣的濃度范圍內(nèi)很好地解釋實驗結(jié)果。將實驗所得數(shù)據(jù)用 Langmuir和Freundlich等溫模型[18]進行擬合,擬合曲線如圖8,參數(shù)列于表6。從圖8和表6可以看出,KGM@CTS對Pb2+和膽固醇的吸附過程和Freundlich吸附模型擬合的更好,由表6可以得出,KF和n值均大于1,則表示KGM@CTS吸附劑對Pb2+和膽固醇的吸附能力比較強。

圖8 Freundlich吸附曲線圖Fig.8 The Freundlich adsorption表6 KGM@CTS吸附劑對Pb2+和膽固醇的吸附模型參數(shù)
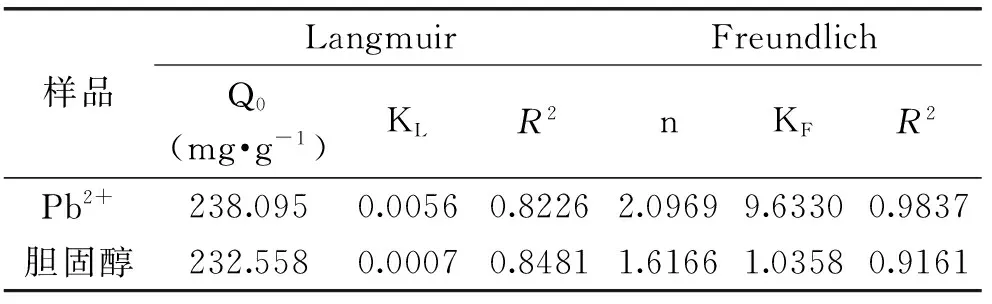
樣品LangmuirFreundlichQ0(mg·g-1)KLR2nKFR2Pb2+238.0950.00560.82262.09699.63300.9837膽固醇232.5580.00070.84811.61661.03580.9161
3 結(jié)論
KGM包埋前后的紅外譜圖顯示KGM@CTS中可檢測出殼聚糖特有的氨基存在,則其可同時具有魔芋和殼聚糖的功能基團,吸附能力優(yōu)于交聯(lián)魔芋葡甘聚糖顆粒。
KGM@CTS對Pb2+和膽固醇的靜態(tài)吸附動力學研究表明:在37 ℃時,對Pb2+的吸附平衡時間為80 min,最佳pH為5.5,初始濃度為240 mg/L,吸附劑質(zhì)量為2.5 g/L,最大去除率為95.2%;對膽固醇的吸附平衡時間為120 min,初始濃度為3.0 g/L,吸附劑質(zhì)量為1.5 g/L,最大去除率為48.7%。吸附過程符合準二級動力學方程和Freundlich吸附等溫模型,說明此吸附屬于不均勻表面的吸附。因此,KGM@CTS在模擬實驗中,表現(xiàn)出了排除重金屬離子及控制血脂等膳食纖維特性,則為產(chǎn)品的價值和進一步的開發(fā)使用提供了一定的理論依據(jù)。
[1]沖增哲,黑田俊朗,岸田典子.魔芋科學[M].古明選,譯.成都:四川大學出版社,1990:157-171.
[2]Abbott PJ. EFSA Panel on Dietetic Products,Nutrition and Allergies. Glucomannan related health claims[J]. EFSA Journal,2010,8(10):1798.
[3]Cairello M,Marchini G. Evaluation of the action of glucomannan on metabolic parameters and on the sensation of satiation in overweight and obese patients[J]. La Clinica Terapeutica,1995,146:269-274.
[4]Hou YH,Zhang LS,Zhou HM. Influences of refined konjac meal on the levels of tissue lipids and the absorption of four minerals in rats[J]. Biomed Environ Sci,1990,3(3):306-314.
[5]Judelson DA,Gomez AL,Kraemer WJ. Effects of a carbohydrate-restricted diet with and without supplemental soluble fiber on plasma low-density lipoprotein cholesterol and other clinical markers of cardiovascular risk[J]. Metabolism,2007,56:58-67.
[6]Staiano A,Simeone D. Effect of the dietary fiber glucomannan on chronic constipation in neurologically impaired children[J]. Journal of Pediatrics,2000,136:41-45.
[7]Vuksan V,Sievenpiper JL. Konjac-mannan and American ginsing:emerging alternative therapies for type 2 diabetes mellitus[J]. Journal of the American College of Nutrition,2001,20:370-380.
[8]羅立新,馮長根.交聯(lián)魔芋葡甘聚糖微球的制備與表征[J].林產(chǎn)化學與工業(yè),2004,24(2):77-79.
[9]羅天瑞,羅立新,肖湘,等.一種殼聚糖包囊魔芋的組合物及其制備工藝和用途:中國,ZL200910272658.7[P]. 2009-11-04.
[10]中國科學院環(huán)境化學研究所.GB/T7470-1987水質(zhì)鉛的測定:雙硫腙分光光度法[S].北京:中國標準出版社,1987.
[11]中國預防醫(yī)學科學院營養(yǎng)與食品衛(wèi)生研究所. GB/T5009.128-2003食品中膽固醇的測定[S].北京:中國標準出版社,2003.
[12]王翼偉,王棟,徐巖,等.黃酒中氨基甲酸乙酯吸附去除的動力學和熱力學研究[J].食品工業(yè)科技,2015,36(1):130-133.
[13]Thompson S,Weber C. Influence of pH on the binding of coper,zinc,and iron in six fiber sources[J]. Journal of Food Science,1979,44(3):752-754.
[14]陳亞非,趙謀明.水溶性與水不溶性膳食纖維對油脂、膽固醇和膽酸鈉吸附作用研究[J].現(xiàn)代食品科技,2005,21(3):58-60.
[15]余亮.Fe3O4/4A沸石復合材料的制備及吸附鉛離子性能的研究[D].長沙:中南大學,2012.
[16]劉莉.魔芋葡甘聚糖交聯(lián)羧甲基改性及其對金屬離子的吸附和解吸性能研究[D].武漢:華中農(nóng)業(yè)大學,2008.
[17]王光信,孟阿蘭,任志華.物理化學[M].第3版.北京:化學工業(yè)出版社,2007:237.
[18]王金玲,沈敏,瞿陽,等.交聯(lián)羧甲基魔芋葡甘聚糖吸附Cu2+的機理[J].湖北農(nóng)業(yè)科學,2009,48(1):161-163.
Adsorption property of Pb(Ⅱ)and cholesterol by chitosan coated konjac glucomannan
ZHU Wei-wei,LUO Li-xin*,WANG Yu
(College of Chemistry and Molecular Sciences,Wuhan University,Wuhan 430072,China)
A new konjac product with a chitosan coating was prepared by konjac glucomannan particles and a solution of chitosan in aqueous acetic acid at room temperature. This product can keep excellent characteristics of konjac such as helping digestion and reducing the concentration of cholesterol in the blood. The properties were characterized by FT-IR. Adsorption performance for Pb2+and cholesterol was evaluated in solutions systematically. Batch experiments were conducted as a function of initial concentration,adsorbent dosage and contact time. The kinetic data were analyzed by the pseudo-first-order,pseudo-second-order kinetics. Also the equilibrium data were examined with the Langmuir and Freundlich isotherm models. The results showed that the new product was characterized with functional groups of konjac glucomannan and chitosan. Adsorption at 37 ℃ resulted in the maximum removal rate of 95.2% and 48.7% for Pb2+and cholesterol,respectively. Kinetics fitted with the pseudo-second-order model. Besides,Freundlich model conformed to the equilibrium data. The results suggested the product can be an effective adsorbent for Pb2+and cholesterol,and the adsorption reaction occurred on an uneven surface.
konjac glucomannan;adsorption;lead ion;cholesterol;coating
2015-03-25
朱唯唯(1991-), 女,碩士,研究方向:天然產(chǎn)物提取和改性,E-mail:13545387147@163.com。
*通訊作者:羅立新(1966-),男,博士,副教授,研究方向:天然高分子改性與功能化,E-mail:lxluo@whu.edu.cn。
2013年湖北省中小企業(yè)技術(shù)創(chuàng)新計劃項目(2013~2015,無編號)。
TS201.1
A
1002-0306(2015)23-0125-05
10.13386/j.issn1002-0306.2015.23.017

