紫外誘變篩選低自溶高產2,3-丁二醇的地衣芽孢桿菌突變子*
郭文逸,潘學瑋,尤甲甲,楊洪江
(天津科技大學生物工程學院工業微生物教育部重點實驗室,天津市工業微生物重點實驗室,天津,300457)
微生物具有生產2,3-丁二醇的能力,其中肺炎克雷伯氏菌為常用的生產菌株,但該菌株為條件致病菌,不利于大規模工業化生產[1]。地衣芽胞桿菌屬于GRAS(generally recognized as safe)菌株,具有生長繁殖迅速、代謝快、產生多種蛋白酶等特點,利于產物的快速生成,并且它能夠產生芽孢,抗逆性強[2],所以近年來有越來越多關于地衣芽孢桿菌產2,3-丁二醇的報道。
在前期實驗中,篩選到1株地衣芽孢桿菌BL41[3]。發酵后期,發酵液的 OD600值逐漸下降,且逐漸變黏稠,與之相對應,2,3-丁二醇的合成能力逐步下降。本文通過分析胞外多糖、聚谷氨酸產量以及細菌數量的變化,最終發現此現象主要由細胞自溶引起。因此推測,如果發酵后期細胞自溶水平下降,即可防止菌株生物量快速減少,2,3-丁二醇產率增加,從而提高2,3-丁二醇的產量。因此對該菌株進行紫外誘變,在篩選平板中獲得自溶水平低的突變株,進而篩選得到高產2,3-丁二醇的菌株。
1 材料與方法
1.1 培養基
LB培養基(g/L):酵母粉5,蛋白胨10,NaCl 10。MR-VP 培養基(g/L):蛋白胨7,葡萄糖5,K2HPO45。種子培養基(g/L):葡萄糖40,酵母粉10,硫酸銨1,K2HPO41。發酵培養基(g/L):葡萄糖100,酵母粉5,蛋白胨 12,MnSO40.025,K2HPO43,MgSO40.2,乙酸鈉5。上述培養基pH值均為7.0,除LB培養基121℃滅菌20 min外,其余培養基均為115℃滅菌20 min。
自溶檢測培養基:將菌株BL41單菌落接種于600 mL的液體LB培養基中,37℃,220 r/min培養3~4 h,菌體濃度達到108,100 ℃煮1 h,殺死細胞,于4 000 r/min離心10 min,棄去上清液,將菌體細胞加到200 mL無菌的LB瓊脂培養基中制備平板,用于篩選自溶水平低的突變株[4]。
1.2 實驗方法
1.2.1 胞外多糖和聚谷氨酸的測定
以葡萄糖為標準,繪制葡萄糖標準曲線。利用醇沉法沉淀發酵液中多糖,沉淀重懸制成多糖溶液,采用苯酚硫酸法測定其胞外多糖產量[5]。
采用生物傳感儀測定發酵液水解前后谷氨酸含量,其差值為 γ-聚谷氨酸的產量[6]。
1.2.2 菌株生物量的測定
將單菌落進行兩級種子培養后,按5%的接種量轉接到30 mL發酵培養基中,37℃,160 r/min培養,選取不同時間點取樣,稀釋10-6后涂布于LB平板上,37℃培養12 h,然后記錄菌落數。
1.2.3 紫外誘變篩選高產2,3-丁二醇菌株
將菌株BL41紫外誘變[3]后避光培養24 h,然后取100 μL轉接于新鮮LB中,37℃,220 r/min培養,每隔12 h轉接1次,轉接30代后將其稀釋涂板,避光培養48 h后觀察菌落周圍透明圈大小。選取自溶水平低的突變株進行肌酸比色實驗,從而獲得高產乙偶姻菌株[4]。將上述菌株分別進行兩級種子培養后接種于初始葡萄糖質量濃度分別為100、120、140、160 g/L的發酵培養基中,利用氣相色譜法分別測定36、42、48 h 時2,3-丁二醇產量,從而篩選高產 2,3-丁二醇菌株。
1.2.4 四聯發酵罐的分批補料實驗
為進一步確定突變株的生產能力,在四聯發酵罐中進行分批補料發酵,菌種經過兩級種子培養后按5%接種量接入600 mL的發酵培養基中,培養溫度為37℃,通氣量2 vvm。前期轉速為400 r/min,14 h后降低為200 r/min。通過補加一定量的葡萄糖,殘糖濃度維持在30 g/L左右。初始pH為7.0,隨著發酵的進行,pH會先下降然后再上升,當pH上升到6.5時,補加氨水使其降到6.0。
1.2.5 分析檢測方法
利用紫外分光光度計測定OD600。發酵上清液過膜后,稀釋100倍利用生物傳感儀測定葡萄糖濃度。發酵上清液過膜后,稀釋10倍利用氣相色譜法測定2,3-丁二醇和乙偶姻含量[3]。
2 結果
2.1 細胞自溶導致生物量下降
地衣芽孢桿菌BL41在發酵過程中發酵液變黏稠,推測為其產生了胞外多糖或γ-聚谷氨酸。然而苯酚硫酸法結果顯示,發酵液中胞外多糖的含量僅為1.0 g/L,含量較低。因此,這不是發酵液黏稠的主要原因。通過生物傳感儀測定發酵液及其水解樣品中谷氨酸含量,結果顯示均為0.2 g/L,說明發酵液中無γ-聚谷氨酸產生,這也不是引起發酵液黏稠的原因。
進一步推測地衣芽孢桿菌BL41在發酵中存在細胞自溶現象,導致OD600值顯著下降和胞內核酸和蛋白質等大分子釋放到培養基中,使發酵液變黏。瓊脂糖凝膠電泳結果顯示,12 h的發酵上清液中沒有DNA條帶產生,此時細胞處于對數期,沒有顯著自溶現象發生,無大分子物質泄露到細胞外;而隨著發酵的進行,在24 h和48 h的樣品中,均出現大于15 kb的DNA條帶,特別是36 h樣品中的DNA數量要顯著多于24 h的樣品,且伴隨明顯的DNA降解現象(圖1)。
同時,采用涂板方法直接測定地衣芽孢桿菌BL41的生物量。發酵前期,細菌數量逐漸增加,12 h時達到最高,菌濃為3.9×109CFU/mL。隨后,細菌數量開始下降,至發酵結束時,細菌細胞數減少了48.7%(圖2)。
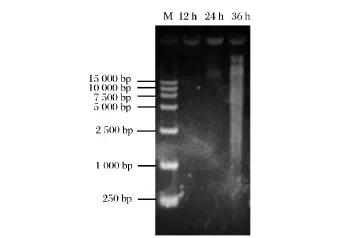
圖1 細胞自溶產生的胞外DNAFig.1 Extracellular DNA produced by autolysis
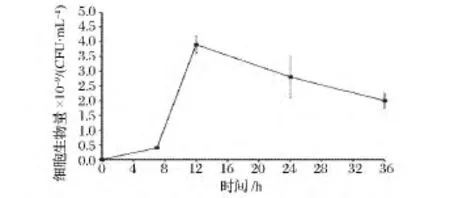
圖2 發酵過程中B.licheniformis BL41生物量Fig.2 Cell biomass of B.licheniformis BL41 during fermentation process
2.2 紫外誘變篩選自溶水平低的突變株
由上述結果得出,發酵后期,細胞大量死亡,導致生產2,3-丁二醇的生物量減少,從而降低2,3-丁二醇的生成。Nagraj以凍干細胞為底物,設計自溶篩選平板,通過觀察自溶圈大小,獲得不產自溶素的菌株[4]。然而冷凍干燥法耗時過長,獲得細胞干粉量較小,因此本文對其進行改造。
菌株BL41的細胞加熱死亡后,以死細胞及細胞碎片作為底物加入到LB瓊脂培養基中,倒平板備用。將菌液稀釋后均勻涂布于上述平板,觀察菌落周圍透明圈大小。如圖3所示,中間白色部分為單菌落,而菌落周圍的黑色部分則為自溶素裂解細胞產生的透明圈,其中圖(A)和(B)分別表示出發菌株和突變菌株的自溶圈,兩菌落直徑大小相似,然而明顯可以看出,出發菌株的透明圈較大。
透明圈直徑與菌落直徑之比可以表征菌株自溶水平高低,比值越高說明自溶水平越高。通過紫外誘變的方法,獲得自溶水平低的突變株。在自溶篩選平板上共得到220株突變子,其中61株突變子的透明圈直徑/菌落直徑比值小于出發菌株1.57,結果如表1所示。
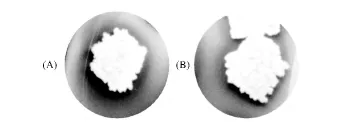
圖3 篩選平板上菌落周圍的透明水解圈Fig.3 Transparent zones around the colonies on the screen plate

表1 突變子的相對自溶水平分析Table 1 Analysis of the relative autolysis level of the mutants
2.3 肌酸比色法篩選高產乙偶姻的菌株
將上述31株透明圈直徑/菌落直徑比值小于1.29的突變子進行肌酸比色實驗,分析乙偶姻含量,從而快速大量篩選出高產乙偶姻菌株,減少復篩工作量。其結果如圖4所示,菌株 BL41-103,BL41-105,BL41-122,BL41-196,BL41-202,BL41-213,BL41-216的乙偶姻產量最高,均高于出發菌株BL41。
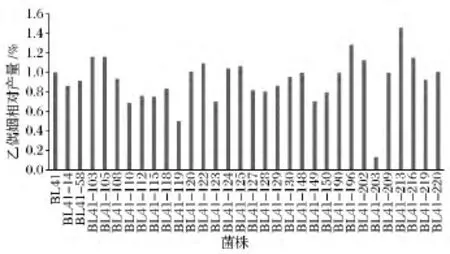
圖4 突變子合成乙偶姻的水平Fig.4 Analysis of acetoin production in mutants
2.4 搖瓶發酵篩選高產2,3-丁二醇的菌株
選取乙偶姻產量高的菌株,進一步通過搖瓶發酵分析其2,3-丁二醇產量。然而,不同菌株的葡萄糖利用能力不同,因此采用不同的初始葡萄糖濃度進行發酵。由表2所示,發酵36 h時,除BL41-103外,大部分菌株在100 g/L的初始葡萄糖濃度下獲得最高2,3-丁二醇產量,然而隨葡萄糖濃度的升高,其產量下降。菌株BL41-213在36 h時2,3-丁二醇產量最高,為54.6 g/L,相比于出發菌株提高了34.2%。
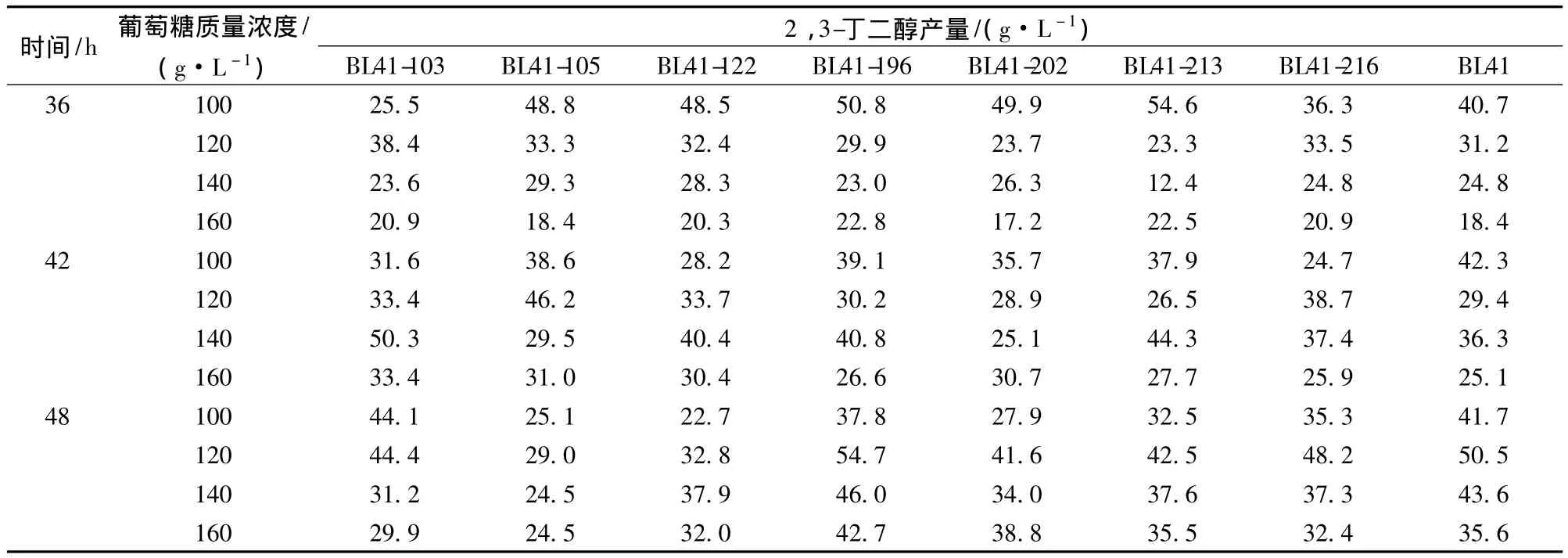
表2 初始葡萄糖質量濃度對2,3-丁二醇產量的影響Table 2 Effect of initial glucose concentration on 2,3-butanediol production
發酵42 h時,在初始葡萄糖質量濃度為100 g/L的情況下,菌株的乙偶姻產量升高,而2,3-丁二醇產量下降。可能是由于培養基中葡萄糖消耗完后,生成的2,3-丁二醇作為儲備碳源可逆的轉化為乙偶姻。而此時,初始葡萄糖濃度大于100 g/L的培養基中,由于葡萄糖未耗盡,仍有2,3-丁二醇生成,因此其產量均較高。
大部分菌株在120 g/L的初始葡萄糖質量濃度下,發酵48 h獲得最大2,3-丁二醇產量。其中菌株BL41-196的2,3-丁二醇的產量達到54.7 g/L,為發酵過程中的最高值。而BL41-103的2,3-丁二醇產量在48 h,初始葡萄糖質量濃度為100 g/L時最高,達到44.1 g/L。
大部分菌株在初始葡萄糖質量濃度為140 g/L和160 g/L時,2,3-丁二醇的產量普遍低于100 g/L和120 g/L時的產量。底物濃度過高,抑制了2,3-丁二醇的生成。
2.5 四聯發酵罐發酵篩選高產2,3-丁二醇菌株
為進一步確定突變株的生產能力,對上述3株高產2,3-丁二醇菌株 BL41-103,BL41-196和 BL41-213進行四聯發酵罐的擴大培養,并以出發菌株BL41為對照。
由圖5(A)所示,發酵前20 h時,4株菌的2,3-丁二醇產量近似相等,此后,2,3-丁二醇產量則出現差別。BL41-103在發酵36 h時即達到最高產量,為60.3 g/L,比出發菌株 BL41提高了25.9%,此后,BL41-103的2,3-丁二醇產量即開始下降。除BL41-103外,其余3株菌的2,3-丁二醇產量均在44 h時達到最高值,其中BL41-196的2,3-丁二醇產量最高,為 65.1 g/L,比出發菌株提高了 36.0%。而BL41-213的產量為56.1 g/L,僅比菌株BL41提高了17.1%。
發酵時間為24 h時,BL41-196的產率達到最高,并且維持1.7 g/(L· h)長達12 h。而BL41-213也在24 h時達到最高產率1.7 g/(L·h),此后,2,3-丁二醇產率則快速下降。BL41-103在28 h時產率為1.7 g/(L·h),并在此產率下維持8 h,發酵36 h后產率則快速下降,因此,BL41-103在較短時間內達到最大2,3-丁二醇產量。BL41在24 h時達到最高產率1.4 g/(L·h),然后,其產率開始下降(圖5(B))。
發酵過程中,副產物乳酸和乙偶姻的產量如圖6(A、B)所示。發酵后期,2,3-丁二醇產量開始下降,轉化為乙偶姻,因此乙偶姻的產量呈逐漸上升趨勢,但是整個發酵過程中其產量都低于3 g/L。乳酸的產量則略高,最高達到12 g/L。
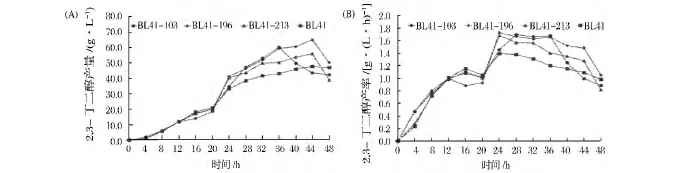
圖5 四聯發酵罐發酵分析2,3-丁二醇的產量和產率Fig.5 Production and productivity of 2,3-BD for mutant strains in multifors
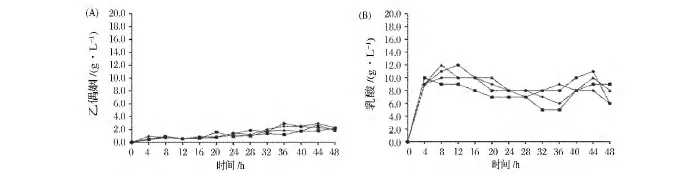
圖6 四聯發酵罐發酵的副產物產量Fig.6 Production of the byproducts of the mutants in fermentation process with a multifors bioreactor
2.6 突變株生物量的測定
上述發酵進行到20 h后,細胞自溶現象明顯,四株菌的OD600均在此時開始下降,其中BL41-103的OD600由14.6下降為12.1。而其余3株菌的OD600則近似相等,均由12.6左右降至11.0左右。同時,由于發酵后期營養成分的不足及副產物的積累,細胞開始死亡,這兩種原因導致細胞生物量快速下降。
如圖7所示,四株菌在發酵后期細菌數量均下降,其中菌株BL41的細胞死亡率最高,發酵36 h時為36.5%,而另外 3株菌(BL41-103,BL41-196,BL41-213)的死亡率分別為 29.0%,23.5% 和31.0%,均小于出發菌株BL41。菌株BL41-196的細胞死亡率最低,且其最終細菌濃度高于BL41,而該菌株的2,3-丁二醇產量最高,生物量與代謝產物的生成保持一致。BL41-103的細胞死亡率也較低,并且在發酵前期BL41-103的生長速率高于另外三株菌,因此其在短時間內獲得較高2,3-丁二醇產量。盡管最終菌株BL41-213細菌數量少于出發菌株,但其細胞死亡率小于出發菌株BL41,因此其2,3-丁二醇產量也略高于出發菌株。
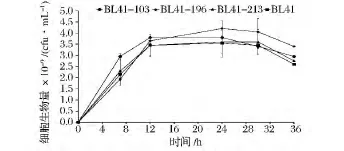
圖7 突變株的生物量變化Fig.7 Biomass production of mutant strains during fermentation
3 討論
地衣芽孢桿菌在植物病害防治、飼料加工、醫藥開發等多方面具有廣泛應用,是非常具有應用價值的菌株[7],其在2,3-丁二醇生產上也有很大潛力。早在1992年,就有研究利用地衣芽孢桿菌生產2,3-丁二醇,發酵72 h后,其2,3-丁二醇的產量為47 g/100 g,為當時的最高產量[8]。而在地衣芽孢桿菌NCIMB 8059中則得到最優培養條件,溫度為37℃,pH 為6.0,接種量10 g/L,初始底物濃度30 g/L[9]。
自溶素普遍存在于細菌之中,它參與細菌的生長發育、細胞分離、孢子形成等重要生理活動[10]。自溶現象在芽孢桿菌中也有多種應用,如蠟狀芽孢桿菌群中,通過不同pH條件下自溶現象的不同,對其進行分類[11]。在蘇云金芽孢桿菌中,利用細胞壁錨定結合性能的自溶素作為運載蛋白,構建芽孢桿菌的表面展示系統[12]。然而,菌體自溶對發酵過程卻具有不良影響。乳酸桿菌的高密度培養過程中,由于菌體自溶,活菌數很難達到較高的增殖水平[13]。而且,自溶素對細胞壁的水解作用導致細胞壁破裂出現孔洞,胞內容物,如DNA、RNA等,流失到細胞外[14]。而胞外DNA在菌體表面間起到了粘結作用,致使發酵液變黏[15]。
本研究通過分析發酵后期培養液粘稠現象產生的原因,證實了該菌株在發酵期間細胞自溶現象比較嚴重。而在金黃色葡萄球菌中,通過轉座子Tn917-lacZ隨機誘變,獲得了2株無法合成自溶素的缺陷型突變株[4]。由于紫外誘變的方法方便簡單,因此本文利用紫外誘變篩選自溶水平降低的突變子,并從這些突變子中挑選出乙偶姻合成水平較高的菌株,最終突變子產2,3-丁二醇水平較出發菌株有了明顯提高。本研究首次將降低細胞自溶水平、提高發酵過程中生物量和提高2,3-丁二醇產量聯系在一起,取得了較好的結果。
4 結論
本研究通過紫外誘變,成功地篩選出自溶水平較低的突變子,并從中進一步篩選出2,3-丁二醇的高產菌株。本研究結果顯示,通過降低菌株的自溶水平,增加發酵過程中的生物量,是提高發酵水平的一條重要途徑。
[1] 林璐.基于知識圖譜的生物制造2,3-丁二醇研究態勢分析[J].情報探索,2014(3):28-31.
[2] 張幟,李理想,馬翠卿.芽胞桿菌發酵產2,3-丁二醇的研究進展及展望[J].生物加工過程,2014,12(3):79-86.
[3] 郭文逸,孫慶惠,宋麗娜,等.地衣芽孢桿菌高產2,3-丁二醇菌株的選育和發酵研究[J].生物技術通報,2014,8:159-163.
[4] Nagraj M,Philip T.Isolation and characterization of autolysis-defective mutants of Staphylococcas aureus created by Tn917-lacZ[J].Journal of Bacteriology,1993,175(5):1 493-1 497.
[5] 張曉玲,牟光慶.響應面法優化枯草芽孢桿菌產胞外多糖培養基[J].食品工業科技,2012,33(15):133-138.
[6] 繆靜,楊在東.碳源對 γ-聚谷氨酸發酵的影響[J].中國釀造,2010(3):70-72.
[7] 唐娟,張毅.地衣芽孢桿菌應用研究進展[J].湖北農業科學,2008,47(3):351 -354.
[8] S.Nilegaonkar.Production of 2,3-butanediol from glucose by Bacillus licheniformis[J].World Journal of Microbiology and Biotechnology,1992,8(4):378 -381.
[9] Perego P.Effects of temperature,inoculum size and starch hydrolyzate concentration on butanediol production by Ba-cillus licheniformis[J].Bioresource Technology,2003,89(2):125–131.
[10] 劉申.細菌自溶素的研究進展[J].中國實用醫藥,2009,4(12):226 -228.
[11] Raddadi N,Cherif A.The autolytic phenotype of the Bacillus cereus group[J].Journal of Applied Microbiology,2005,99(5):1 070 -1 081.
[12] 邵小虎.蘇云金芽胞桿菌自溶素蛋白用于構建表面展示系統的研究[J].武漢:華中農業大學,2009.
[13] 李艾黎,鄧凱波,霍貴成.環境因素對酸奶菌株自溶的影響[J].微生物學通報,2008,35(8):1 262-1 267.
[14] 馮鎮.乳酸菌自溶影響因素及機理研究[D].哈爾濱:東北農業大學,2003.
[15] 黃炎.胞外DNA在細菌生物膜形成中的作用[J].國際檢驗醫學雜志,2013,34(24):3 380-3 382.
[16] Stomer F C.The pH 6 Acetolactate-forming enzyme from Aerobacter aerogenes:I.kinetic studies[J].Journal of Biological Chemistry,1968,243(13):3 735 -3 739.
[17] ZHANG X,BAO T,RAO Z,et al.Two-stage pH control strategy based on the pH preference of acetoin reductase regulates acetoin and 2,3-butanediol distribution in Bacillus subtilis[J].PLoS One,2014,9(3):91187.
[18] Kaloyan Petrov,Penka Petrova.Enhanced production of 2,3-butanediol from glycerol by forced pH fluctuations[J].Applied Microbiology Biotechnology,2010,87(3):943-949.

