Xpert Mtb/RIF檢測技術診斷肺結核和肺外結核的價值
李妍 張天華 鮮小萍 王西娣 陳美玲 楊健 王蕊
?
·論著·
Xpert Mtb/RIF檢測技術診斷肺結核和肺外結核的價值
李妍 張天華 鮮小萍 王西娣 陳美玲 楊健 王蕊
目的 探討利福平耐藥實時熒光定量核酸擴增檢測技術(Xpert Mtb/RIF)在結核病診斷中的臨床應用價值。 方法 對200例初治結核病患者標本,包括痰液、肺泡灌洗液、胸腹腔積液和腦脊液各50例,分別進行抗酸染色法、固體培養法、藥物敏感性試驗(簡稱“藥敏試驗”)及Xpert Mtb/RIF檢測,分別以固體培養結果和藥敏試驗結果為金標準,分析Xpert Mtb/RIF檢測標本中結核分枝桿菌及其利福平耐藥性的敏感度、特異度、陽性預測值、陰性預測值和Kappa值。Xpert Mtb/RIF檢測和金標準檢測進行一致性檢驗(Kappa檢驗),Κ>0.8認為兩者一致性極好。結果 以固體培養法檢測結果為準,Xpert Mtb/RIF檢測技術,以及抗酸染色法總體敏感度、特異度、陽性預測值、陰性預測值、Kappa值分別為94.52%(69/73)、90.55%(115/127)、85.19%(69/81)、96.64%(115/119)和0.83,以及65.75%(48/73)、96.06%(122/127)、90.57%(48/53)、82.99%(122/147)和0.66;以比例法藥敏試驗結果為準,Xpert Mtb/RIF檢測技術檢測利福平耐藥性的總體敏感度、特異度、陽性預測值、陰性預測值和Kappa值分別為93.75%(15/16)、100.00%(53/53)、100.00%(15/15)、98.15%(53/54)和0.96。 結論 Xpert Mtb/RIF法可快速檢測肺內、外結核分枝桿菌及其耐藥性,具有良好的應用前景。
結核, 肺/診斷; 結核/診斷; 抗藥性, 細菌; 利福平; 微生物敏感性試驗; 核酸擴增技術
結核病是危害人類健康的傳染病之一,其早期診斷更具有臨床意義,因此,尋找一種快速、簡便和敏感度高的檢測方法顯得尤其迫切。隨著分子生物學技術的發展,越來越多的分子診斷技術不斷的涌現,利福平耐藥實時熒光定量核酸擴增檢測技術(Xpert Mtb/RIF)便是其中之一。該方法國內以痰標本為研究對象研究較多,而對肺外結核的應用報道尚少[1-2],所以該方法還有許多未知領域值得探討。本課題將抗酸染色法、固體培養法和Xpert Mtb/RIF檢測技術在肺內、外標本中的檢測情況進行比較,初步評價該技術檢測結核分枝桿菌及利福平耐藥的應用效果,報告如下。
資料和方法
一、材料
200例初治結核病患者標本,來自我所及陜西省結核病防治院2014年3月至2015年2月,經臨床或細菌學檢查確診[3]的門診和住院結核病患者。包括痰液、肺泡灌洗液、胸腹腔積液和腦脊液各50份。標本采取前未使用抗結核藥物治療。
二、儀器和試劑
GeneXpert Dx儀器、 GeneXpert Mtb/RIF Cartridge檢測盒(批號:16201)及樣品試劑(sample reagent,SR)(批號:3244C034)均購自美國Cepheid公司;分枝桿菌涂片鏡檢萋-尼氏染色液(批號:4140424)、中性羅氏培養基(批號:20140912)和分枝桿菌藥物敏感性試驗(簡稱“藥敏試驗”)培養基(批號:20140912)均購自珠海貝索生物技術有限公司。
三、方法
所有標本同時采用抗酸染色法、固體培養法、比例法藥敏試驗及Xpert Mtb/RIF檢測。
1. 抗酸染色法:采用離心濃縮法,操作參照《結核病實驗室標準化操作與網絡建設》[4]進行。
2. 固體培養法:采用中和離心法,操作參照《結核病實驗室標準化操作與網絡建設》[4]進行。
3. 藥敏試驗及菌種鑒定:采用比例法,操作參照《結核病實驗室標準化操作與網絡建設》[4]進行。
4. Xpert Mtb/RIF技術:取1 ml標本加入前處理管中,視標本性狀加入2倍標本體積的SR標本處理液,渦旋振蕩15~30 s,靜置15 min。打開檢測盒,吸取2 ml處理后樣品緩慢加入檢測盒,然后將檢測盒放入檢測模塊,儀器開始進行自動化測試。反應結束后,在檢測系統窗口下可直接觀察測試結果。
四、統計學方法
用SPSS 16.0軟件進行統計學處理。率之間的比較采用χ2檢驗,P<0.05表示差異有統計學意義。Xpert Mtb/RIF檢測和金標準檢測進行一致性檢驗(Kappa檢驗),K≤0.40時,表明一致性較差;0.40≤K≤0.60時,表明中度一致;0.60
結 果
一、采用抗酸染色法、固體培養法、Xpert Mtb/RIF技術檢測Mtb結果
200份不同類型樣本(包括痰液、肺泡灌洗液、胸腹腔積液和腦脊液各50份)同時采用抗酸染色法、固體培養法和Xpert Mtb/RIF技術檢測,總體陽性檢出率分別為26.50%(53/200)、36.50%(73/200)和40.50%(81/200)。Xpert Mtb/RIF技術總體陽性率(40.50%)高于抗酸染色法陽性率(26.50%),兩者差異有統計學意義(χ2=8.80,P<0.01);高于固體培養法陽性率(36.50%),兩者差異無統計學意義(χ2=0.68,P>0.05);抗酸染色法陽性率(26.50%)與固體培養法陽性率(36.50%)比較,差異有統計學意義(χ2=4.63,P<0.05)。(表1)。
二、采用抗酸染色法、Xpert Mtb/RIF技術檢測Mtb結果
200份不同類型樣本同時采用3種檢測方法檢測。以固體培養法檢測結果為準,Xpert Mtb/RIF技術檢測總體敏感度、特異度、陽性預測值和陰性預測值分別為94.52%(69/73)、90.55%(115/127)、85.19%(69/81)和96.64%(115/119),對Xpert Mtb/RIF技術和固體培養法進行Kappa檢驗,K=0.83,兩者具有極好的一致性(表2)。
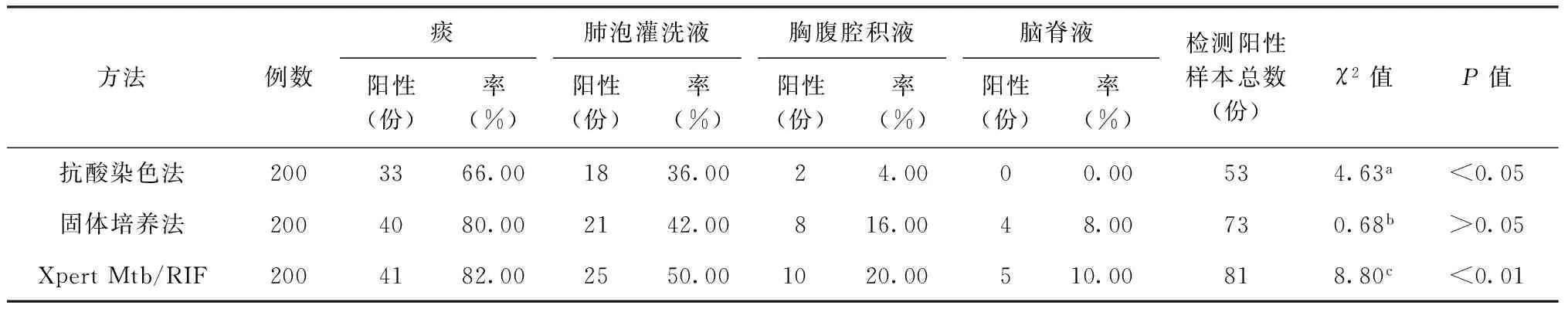
表1 3種檢測方法對不同樣本的陽性檢出率比較
注a:固體培養法相比較;b:與Xpert Mtb/RIF技術相比較;c:與抗酸染色法相比較

表2 不同樣本Xpert Mtb/RIF檢測技術檢測Mtb的結果(以固體培養法檢測結果為準)
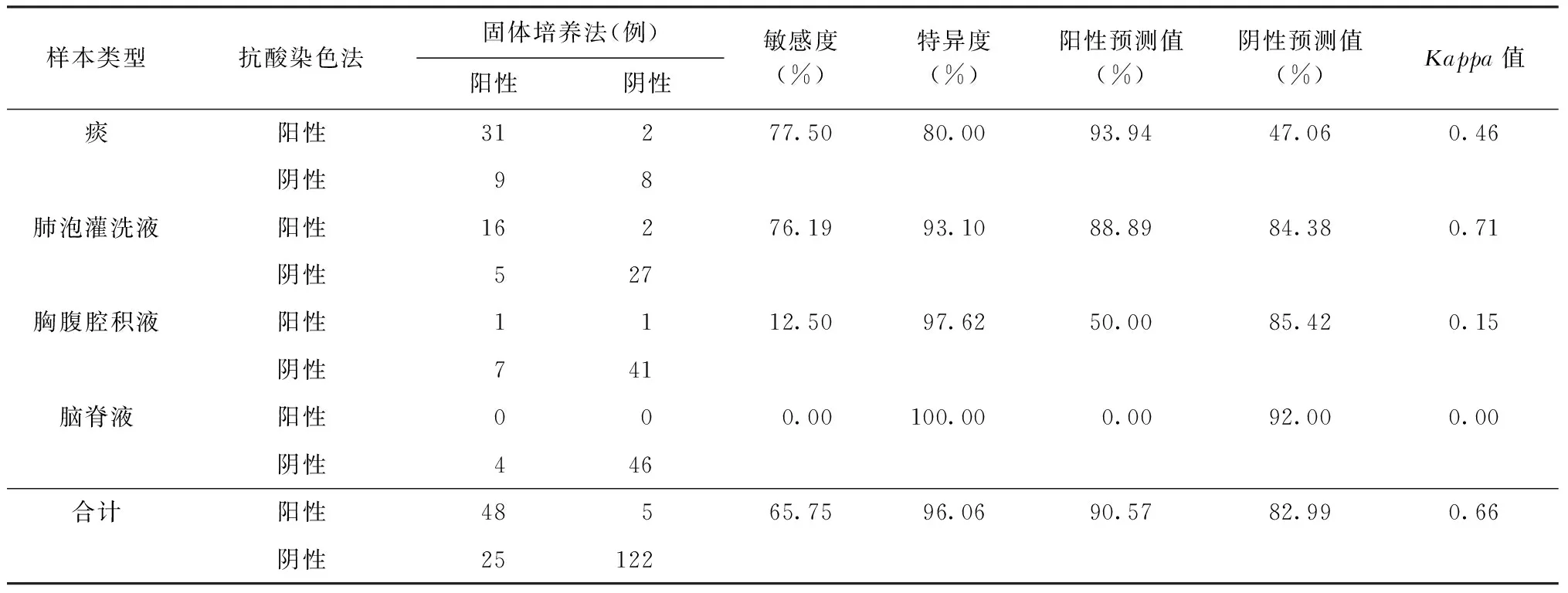
表3 不同樣本抗酸染色法檢測Mtb的結果(以固體培養法檢測結果為準)
以固體培養法檢測結果為準,抗酸染色法檢測總體敏感度、特異度、陽性預測值和陰性預測值分別為65.75%(48/73)、96.06%(122/127)、90.57%(48/53)和82.99%(122/147),對抗酸染色法和固體培養法進行Kappa檢驗,K=0.66,兩者有較好一致性(表3)。
三、Xpert Mtb/RIF技術檢測RFP耐藥的結果
所有樣本通過固體培養共得到73例陽性菌株,經菌種初步鑒定,其中有4例為非結核分枝桿菌(NTM),其余69例均為Mtb。最終可進行Xpert RIF比對分析的結核分枝桿菌為69例。69例結核分枝桿菌,Xpert Mtb/RIF技術與藥敏試驗分別有15例和16例耐RFP結核分枝桿菌,耐藥率分別為21.74%(15/69)和23.19%(16/69),二者間差異無統計學意義(χ2=0.04,P>0.05)。兩種方法檢測對RFP均敏感者53例,均耐藥者15例,二種方法所得結果一致率為98.55 %(68/69)。
以藥敏試驗結果為準,采用Xpert Mtb/RIF技術檢測69例陽性標本中RFP的耐藥性,其敏感度、特異度、陽性預測值和陰性預測值分別為93.75%(15/16)、100.00%(53/53)、100.00%(15/15)和98.15%(53/54),對Xpert Mtb/RIF技術和藥敏試驗進行Kappa檢驗,K=0.96,兩者具有極好的一致性(表4)。
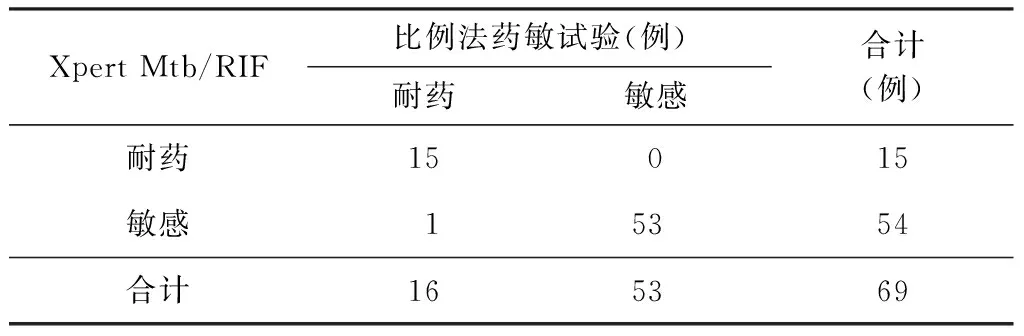
表4 Xpert Mtb/RIF技術檢測RFP耐藥性的結果 (以比例法藥敏試驗結果為準)
討 論
一、Xpert Mtb/RIF技術的檢測原理及特點
在我國,結核病傳統的診斷方法有涂片鏡檢和分枝桿菌培養等。涂片法簡單、快速,但容易漏檢,尤其對于含菌量較低的肺外標本更是難以檢出[5]。培養法是檢測Mtb的“金標準”,但耗時長。至于藥敏試驗,目前常用的方法有絕對濃度法或比例法,但需要2~3個月才能獲到結果,往往影響患者用藥時間。近年來出現的Xpert Mtb/RIF新技術,該技術對結核分枝桿菌利福平耐藥決定區rpoB基因設定引物和探針,進行擴增檢測,根據其是否發生基因突變來檢測標本中是否含有結核分枝桿菌及結核分枝桿菌是否對利福平耐藥。整個過程只需2 h,是將PCR所需的3個步驟即樣品準備、擴增和檢測集于一體的半巢式多重實時熒光半定量檢測技術。該方法快速、簡便,對生物安全要求相對較低,最大程度地減少了操作中污染的可能性。
二、Xpert Mtb/RIF技術檢測肺結核及肺外結核的效能分析
研究表明,Xpert Mtb/RIF技術對肺結核的診斷價值已經逐步得到證實[6],其敏感度為 90.40%、特異度為98.40%,但對肺外診斷研究尚不一致。本實驗選用200例肺內、外結核患者的4種類型標本進行檢測,以固體培養為金標準,肺內痰標本和肺泡灌洗液的敏感度和特異度分別為97.50%(39/40)、80.00%(8/10),95.24%(20/21)和82.76%(24/29),與張治國等[1]和高漫等[7]報道的敏感度稍高、特異度稍低。原因可能與本實驗的選取標本例數較少有關,也可能與入選對象標準不同有關,這就需要在敏感度和特異度之間尋找平衡點。肺外標本中,采用Xpert Mtb/RIF技術,胸腹腔積液敏感度87.50%(7/8)高于Tortoli 等[8]報道的44.40%;腦脊液的敏感度為75.00%(3/4)低于Tortoli等[8]報道的85.70%;總體特異度為90.55%(115/127)略低于Vadwai等[9]報道的97.00%。上述差異可能與本實驗選取的標本數量較少有關,也可能與實驗的金標準不同有關,此研究還有待于在今后的工作中繼續完善和補充。
三、Xpert Mtb/RIF技術與抗酸染色法、固體培養法及藥敏試驗比較的優勢
有報道Xpert Mtb/RIF技術的臨床檢出限為131菌落形成單位(CFU)/ml[10],抗酸染色鏡檢檢出限為5×103CFU/ml以上,培養為10~100 CFU/ml[11]。本實驗同時采用抗酸染色、固體培養及Xpert Mtb/RIF法,4種不同類型標本均以Xpert Mtb/RIF法陽性率最高,其次為培養法,抗酸染色法陽性率最低;并且以固體培養法檢測結果為準,Xpert Mtb/RIF技術的總體敏感度94.52%(69/73)高于抗酸染色法敏感度65.75%(48/73),Xpert Mtb/RIF技術與固體培養法的一致性(Κ=0.83)高于抗酸染色法與固體培養法的一致性(Κ=0.66)。本研究結果還顯示,以藥敏試驗檢測結果為準,Xpert Mtb/RIF和藥敏試驗具有極好的一致性,該結果與Boehme 等[1]的報道基本一致。因此,Xpert Mtb/RIF技術相對于傳統抗酸染色、培養技術而言,不但提高了敏感度,而且最大程度上縮短了檢測時間,尤其對結核分枝桿菌的耐藥性檢測更具優勢。
Xpert Mtb/RIF檢測技術是世界衛生組織(WHO)及國家結核病參比實驗室推薦的一種全新的結核病快速檢測新方法,具有快速、簡單和敏感度高,而生物安全要求不高,且能同時檢測利福平耐藥菌株等優點,尤其對于陽性檢出率極低的肺外標本更具臨床意義。然而,該技術所用儀器、試劑價格昂貴,其后續模塊維護校準也需較大費用。因此,在資源允許及結核病高發地區,Xpert Mtb/RIF技術的臨床應用價值較高,對結核病的早期診斷及規范化治療能夠起到很好的作用。
[1] 張治國,歐喜超,孫倩,等.利福平耐藥實時熒光定量核酸擴增技術檢測痰標本中結核分枝桿菌及其耐藥性的研究.中國防癆雜志,2013,35(1):13-16.
[2] 趙冰,歐喜超,夏輝,等.Xpert Mtb/RIF檢測技術在結核病診斷中的應用評估.中國防癆雜志,2014,36(6):462-466.
[3] 中華醫學會.臨床診療指南-結核病分冊.北京:人民衛生出版社,2005:1-46,122.
[4] 趙雁林,劉志敏.結核病實驗室標準化操作與網絡建設.北京:人民衛生出版社,2013:227-280.
[5] 賈留群,龍虹羽,胡倩婧,等.Xpert MTB/RIF 試驗對肺外結核診斷價值的 Meta分析.中華臨床醫師雜志,2013, 7(6): 2587-2591.
[6] Chang K,Lu W,Wang J,et al.Rapid and effective diagnosis of tuberculosis and rifampicin resistance with Xpert MTB/RIF assay: a meta-analysis.J Infect,2012,64(6): 580-588.
[7] 高漫,鄒遠嫵,白廣紅,等.Xpert Mtb/RIF Assay在結核病診斷中的應用.國際檢驗醫學雜志,2015,36(3):413-414.
[8] Tortoli E,Russo C,Piersimoni C,et al. Clinical validation of Xpert MTB/RIF for the diagnosis of extrapulmonary tuberculosis.Eur Respir J,2012,40(2):442-447.
[9] Vadwai V,Boehme C,Nabeta P,et al.Xpert MTB/RIF:a new pillar in diagnosis of extra pulmonary tuberculosis? J Clin Microbiol,2011,49(7):2540-2545.
[10] Helb D,Jones M,Story E,et al.Rapid detection ofMycobacteriumtuberculosisand rifampin resistance by use of on-demand, near-patient technology.J Clin Microbiol,2010,48(1):229-237.
[11] 李輝,譚耀駒,李洪敏,等.利福平耐藥實時熒光定量核酸檢測技術的診斷效果對比研究.中國防癆雜志,2014,36(6):472-476.
(本文編輯:范永德)
The value of Xpert Mtb/RIF detection assay in the diagnosis of pulmonary tuberculosis and extrapulmonary tuberculosis
LIYan,ZHANGTian-hua,XIANXiao-ping,WANGXi-di,CHENMei-ling,YANGJian,WANGRui.
Referencelaboratory,ShaanxiProvincialInstituteforTuberculosisControlandPrevention,Xi’an710048,China
ZHANGTian-hua,Email:zhthfzhk@126.com
Objective To investigate clinical value of XpertMycobacteriumtuberculosis/Rifampicin(Xpert Mtb/RIF)assay on detection of tuberculosis. Methods We tested 200 samples from initial treatment of tuberculosis patients including sputum, bronchoalveolar lavage fluid, Hydrothorax and ascites, cerebrospinal fluid, each of which had 50 cases, respectively. These samples were detected by acid-fast stain,solid culture,proportional method drug sensitivity tests and Xpert Mtb/RIF assay. Using solid culture result and drug sensitivity tests result as gold standard respectively. The sensitivity, specificity, positive predictive value, negative predictive values andKappavalue of Xpert Mtb/RIF assay in detecting Mycobacterium and refampin resistance were analyzed. In the consistency test for Xpert Mtb/RIF assay and the gold standard test (Kappatest), both of the two test had an excellent agreement whenkappavalue was more than 0.8. Results According to the solid culture result as gold standard, the sensitivity, specificity, positive predictive value, negative predictive values andKappaof Xpert Mtb/RIF assay and acid-fast stain in detecting tuberculosis were 94.52%(69/73),90.55%(115/127),85.19%(69/81),96.64%(115/119) and 0.83 and 65.75%(48/73),96.06%(122/127),90.57%(48/53),82.99%(122/147) and 0.66 respectively. According to the drug sensitivity tests result as gold standard, the sensitivity, specificity, positive predictive value, negative predictive values andKappain detecting refampin resistance are 93.75%(15/16),100.00%(53/53),100.00%(15/15),98.15%(53/54) and 0.96. Conclusion Xpert Mtb/RIF assay has a good application prospect in rapidly detecting pulmonary and extrapulmonary tuberculosis and refampin resistance.
Tuberculosis, pulmonary/diagnosis; Tuberculosis/diagnosis; Drug resistance, bacterial; Rifampin; Microbial sensitivity tests; Nucleic cid amplification techniques
10.3969/j.issn.1000-6621.2015.06.003
陜西省衛生廳資助項目(2014D25)
710048 西安,陜西省結核病防治研究所參比實驗室(李妍、王西娣、陳美玲、楊健、王蕊),所長辦公室(張天華、鮮小萍)
張天華,Email:zhthfzhk@126.com
2015-04-10)

