點擊實驗核心考點 把握實驗復習方向
劉樹載
一、儀器的識別與選取
例l 僅用各選項提供的儀器和藥品,就能達到相應實驗目的的是()。
A.儀器有托盤天平(帶砝碼)、膠頭滴管、量筒、燒杯、藥匙、玻璃棒,藥品有NaCI固體、蒸餾水,實驗H的為配制一定質量分數的NaCl溶液
B.儀器有分液漏斗、燒瓶、錐形瓶、導管及橡皮塞,藥品有鹽酸、大理石、碳酸鈉溶液,實驗目的為證明C、Si、C1三種元素的非金屬性強弱(CI>C>Si)
C.儀器有酸式滴定管、膠頭滴管、鐵架臺(帶鐵夾).藥品有已知濃度的鹽酸、待測NaOH溶液,實驗目的為測定NaOH溶液的物質的量濃度
D.儀器有燒杯、分液漏斗、膠頭滴管、鐵架臺,藥品有待提純的AICI3溶液、NaOH溶液,實驗目的為提純混有MgCl2雜質的AICl3溶液
解析
B項,應將鹽酸改成HC104;C項,缺少滴定管夾、錐形瓶等儀器;D項,正確的實驗過程為:加入過量NaOH溶液,過濾,通入CO2氣體,過濾得A1(OH)3沉淀,加適量鹽酸,得AlCl3溶液。本題選A。
解題策略:解答此類試題,首先應根據實驗目的,聯想達到此目的需要哪些儀器和哪些基本操作,然后對照題目所給的儀器、藥品等比較分析,即可得到正確答案。
二、實驗基本操作
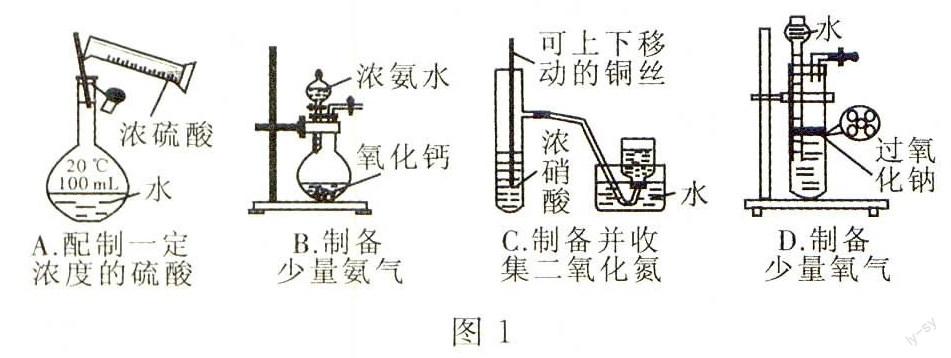
例2 某課外實驗小組設計了圖1所示的幾組實驗,合理的是()。
解析
A項,濃硫酸溶于水,溶液溫度升高,影響配制的精確度,應在燒杯中稀釋濃硫酸,冷卻后l耳轉入容量瓶中;B項,將濃氨水滴在氧化鈣上.氧化鈣和其中的水反應放熱,使氨水分解生成氨氣,可以制備少量氨氣;C項,二氧化氮和水反應生成硝酸和一氧化氮,陔實驗不能收集少量的二氧化氮;D項,過氧化鈉和水劇烈反應生成氫氧化鈉和氧氣.能快速制取氧氣,但該裝置不能達到“隨時反應、隨時停止”的要求。本題選B。
解題策略:應該從原理上來理解實驗基本操作,如為什么要這樣操作,為什么不能那樣操作,操作不當可能引起什么后果等,這樣才能深入理解其本質,避免死記硬背。
三、物質的分離和提純
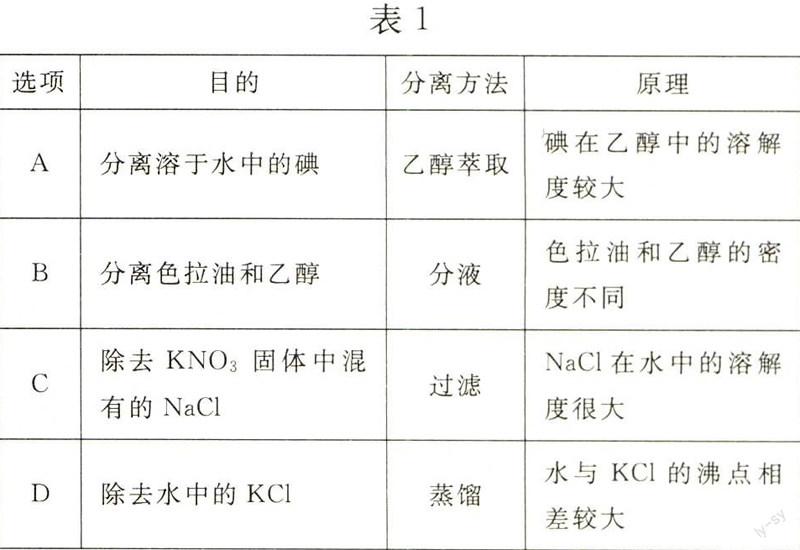
例3 表1所示的實驗中,所采取的分離方法與對應的原理都正確的是()。
A項,乙醇易溶于水,不能用于分離
水中的碘;B項,色拉油和乙醇互溶,采用分液的方法無法將它們分離;C項.KNO3的溶解度隨溫度的變化比NaCI大,應該采用重結晶的方法分離;D項,在室溫下,先將水加熱到100℃時使水沸騰,再冷凝可得純水。本題選D。
解題策略:分離、提純混合物時要遵循“原理正確,操作簡便,少用試劑,(主要成分)量不減少,保護環境”的原則。可根據被提純物質和雜質的性質差異,先選擇合適的藥品,采用轉化的方式除去雜質,然后再采用過濾、萃取、分液、蒸發、重結晶、蒸餾等方法提純。
四、物質的檢驗和鑒別
例4 茶葉中鐵元素的檢驗可經過以下四個步驟完成,各步驟中選用的實驗用品(如圖2所示)正確且完整的是()。
A.將茶葉灼燒灰化,選用①②
B.用濃硝酸溶解茶葉灰并加蒸餾水稀釋,選用④⑥⑦
C.過濾得到的濾液,選用④⑤
D.檢驗濾液中的Fe3+,選用③⑧⑩
A項,用到的實驗用品有①②⑨,必
要時還可用到三腳架或鐵架臺(帶鐵圈);B項,應在燒杯中進行,可用玻璃棒攪拌;C項,用到的實驗用品有④⑤⑦;D項,可用膠頭滴管取少量濾液置于小試管中,用KSCN溶液檢驗,用到的實驗用品有③⑧⑩。本題選D。
解題策略:解答物質檢驗題的方法可歸納為“取試樣,加試劑,說操作,寫現象,定結論”。要注意檢驗、分離、提純物質的區別,注意把握實驗的原理、步驟和儀器,掌握常見陰、陽離子及一些物質的檢驗方法。
五、研究物質的性質
例5 某化學興趣小組為研究生鐵(含碳)與濃硫酸的反應情況及產物性質,設計了如圖3所示的實驗。請回答下列問題:
(1)按圖3所示裝置進行實驗(夾持裝置及尾氣處理裝置未畫出)。儀器b的名稱為_____。實驗過程中,裝置B中觀察到的現象是_____;裝置C中有白色沉淀生成,該沉淀是______(填化學式)。
(2)裝置A中還會產生CO2氣體,請寫出產生CO2的化學方程式:_______。
(3)為了驗證裝置A中產生的氣體含有CO2,應先從圖4所示的①~④中選出必要的裝置連接裝置A中c處管口,從左到右的順序為______(填序號);然后再進行的操作是從a處多次鼓入N2,其目的是_____ 。
(4)某同學通過驗證證明實驗后期裝置A中產生的氣體還含有H2,理由是______(用離子方程式表示)。
解析
(l)由裝置圖可知,儀器b為分液漏斗。生鐵(含碳)與濃硫酸反應生成的SO2,可使濕潤的品紅試紙褪色,濕潤的藍色石蕊試紙變紅;把SO2通入Ba(N03)3。溶液中,“H++NO-3”具有氧化性,能將BaSO3氧化成BaSO4。(3)C()。和S()。都能使澄清石灰水變渾濁,因此應先用酸性高錳酸鉀溶液吸收SO2,然后通過品紅溶液檢驗SO2是否除盡,最后通人澄清石灰水檢驗CO2。(4)隨著反應的進行,濃硫酸變為稀硫酸,鐵和稀硫酸反應生成H2。
答案:(l)分液漏斗 濕潤的品紅試紙褪色,濕潤的藍色石蕊試紙變紅BaSO4(2)C+2H2SO4(濃)=C02↑十+2S02↑十+2H2O(3)③②④趕盡裝置中的空氣,防止空氣中的CO2影響實驗(4)Fe+2H+=Fe2++H2↑
解題策略:研究物質性質的方法一般有觀察法、實驗法、比較法等,根據不同的研究方法可以設計出不同的研究程序來研究物質的性質。如本題通過研究生鐵(含碳)與濃硫酸的反應情況及產物的性質,使同學們體驗到研究物質的程序和方法,認識到化學實驗與物質性質、用途之間的關系。
六、實驗數據處理
例6 小蘇打(NaHC03)試樣中含有碳酸鈉晶體(Na2C03·10H20),為測定其中小蘇打的質量分數w(NaHC03),某實驗小組同學設計了如圖5所示的裝置進行實驗。實驗過程如下:
①按圖組裝儀器,檢查裝置的氣密性。②將m1g試樣放人硬質玻璃管中,裝置B、C、D中的藥品如圖所示。已知加藥品后裝置B的質量為m2g,裝置C的質量為m3g。③關閉活塞a,點燃酒精燈加熱試樣,直到裝置B中無氣泡冒出后,打開活塞a,向裝置中通人N2,一段時間后,拆掉酒精燈,關閉活塞a。④稱得裝置B的質量為m4g,裝置C的質量為m5g。
請回答以下問題(裝置中原有空氣對實驗的影響忽略不計):
(l)裝置A中發生反應的化學方程式為____。
(2)裝置B的作用為_____,裝置C的作用為____。
(3)實驗過程中通人N z的目的是
。
(4)用表2中各項所提供的數據能計算出w(NaHC03)的是____(填序號)。
(5)實驗結束后發現裝置A中硬質玻璃管右端有水珠,你認為利用實驗中所提供的數據還能否得到準確的叫(NaHC03)?若能,則w(NaHCO3)的計算式為_____;若不能,此問不作答。
解析
(l)裝置A中,樣品中的NaHCO3受熱分解產生NaCO3、CO2、H2O(g),NalC03·lOH2O受熱失去結晶水。(2)裝置B中的濃硫酸能吸收樣品分解產生的H2O(g),裝置C中的堿石灰能吸收樣品分解產生的CO2。(3)試樣受熱分解后,裝置中含有。通人N2能將裝置中的排出而被裝置B、C吸收,從而降低實驗誤差。(4)根據實驗原理可知,樣品分解產牛的只能被裝置C吸收,根據得出分解的NaHCO3的質量,也可得出分解產生的的質量。再根據并結合NaHC03分解產生的的質量,則可得出的質量。為此可得出樣品的總質量和的質量,所以b組數據能計算出。由和,可得出的質量,故c組數據能計算出。由和可得出的質量,故e組數據能計算出叫(NaHC03)。(5)選擇e組數據計算則與裝置A中的水珠無關,根據反應可知生成CO2的質量為,則樣品中NaHCO3的質量為,從而得出
答案:(1)
(2)吸收反應生成的H20(g) 吸收反應生成的CO2(3)將裝置中的H2O(g)、CO2排出,被裝置
解題策略:解答數據處理實驗問題,首先要分析所給數據在實驗中的具體作用,找出哪些是有效數據,哪些是無效數據,經過正確的分析處理,從而得出正確結果。如果是識圖并結合數據的試題,大家應先弄清實驗原理,再進行全面分析,對所測數據進行合理分配和組合,并剔除無效數據。
七、聯系化工生產
例7 明礬石的組成和明礬相似,此外還含有氧化鋁和少量的氧化鐵雜質。明礬石是制取鉀肥和氫氧化鋁的重要原料,具體實驗流程如圖6所示,請回答下列問題:
(1)操作1所用到的玻璃儀器的名稱是
。
(2)由溶液3制取氫氧化鋁的離子方程式為
。
(3)明礬石焙燒時產生S02,請你寫出能驗證S02具有還原性且實驗現象明顯的化學方程式:
(4)請你寫出驗證溶液1中含有的實驗過程:
。
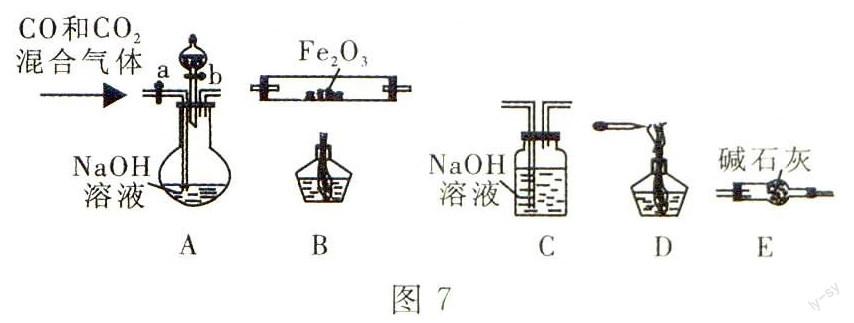
(5)實驗室用Fe2O3。與CO反應來制取單質Fe
①請按氣流由左到有的方向連接圖7中的各裝置,順序為:A→_____。
②檢查裝置A氣密性的方法是______。
③在點燃圖7中B處的酒精燈前、應進行的操作是_______。
④裝置C的作用是______
(l)操作1是過濾,需要的玻璃儀器
為玻璃棒、燒杯和漏斗。(2)經氨水浸泡,過濾得到固體氫氧化鋁和少量氧化鐵固體,再加入試劑1并過濾,得到溶液3(偏鋁酸鈉溶液).最后通人CO2得到氫氧化鋁。(3)檢驗SO2具有還原性的方法較多,常用的試劑有氯水、溴水或酸性高錳酸鉀溶液。(4)檢驗時,應先加入濃NaOH溶液,然后加熱,再用濕潤的紅色石蕊試紙或蘸釘濃鹽酸的玻璃棒進行檢驗。(5)先用NaOH溶液除去CO中的CO2雜質,再通過堿石灰吸收水蒸氣和未除盡的CO2,然后通過B中紅熱的Fc2O3再通過NaOH溶液洗氣,除去反應中產生的CO2最后點燃未反應的CO。
答案:(l)玻璃棒、燒杯和漏斗 (2)(其他合理答案也可)
(4)取少量溶液1,加入濃NaOH溶液,加熱,產生能使濕潤的紅色石蕊試紙變藍的氣體,證明有(其他合理答案也可) (j)①E→B→C→D②將導氣管插入水槽中,關閉彈簧夾a和活塞b,微熱圓底燒瓶,導管口有氣泡產生,撤去熱源,導管中形成一段水柱 ③檢查CO的純度 ④除去CO中的CO2有利于點燃CO
解題策略:解答此類題時,首先要明確原料和產品(包括副產品),即箭頭進出方向。其次依據流程圖分析反應原理,緊扣信息,搞清流程中每一步發生了什么反應,弄清有關反應原理,明確目的(如沉淀的反應、除雜、分離)。最后聯系儲存的知識,有效地進行信息的利用,準確表述和工整書寫。

