不同生長速率下水華束絲藻儲磷能力研究
閆 彬
(重慶大學城市建設與環境工程學院,重慶 400044)
不同生長速率下水華束絲藻儲磷能力研究
閆 彬
(重慶大學城市建設與環境工程學院,重慶 400044)
對不同生長速率的水華束絲藻體內顆粒態聚合磷酸鹽含量進行了分析,討論了藻種不同生長階段對磷的儲存特點,促進對藻類儲磷能力的進一步認識。
水華束絲藻,生長速率,聚合磷酸鹽
磷是浮游藻類細胞膜、核酸的主要組成元素,藻類的生長與胞外磷濃度、胞內磷濃度均有關,主要受胞內濃度的影響。柵藻的批次培養研究中發現在胞外磷被耗盡的情況下,柵藻仍能維持指數生長[1]。藻類對磷存在“奢侈吸收”(luxury absorption)現象[2],并以聚合磷酸鹽(polyphosphate,以下簡寫為“PolyP”)的形式儲存在體內,用于維持外界磷匱乏時細胞對磷的需求。藻類對外部環境中不同形態磷酸鹽的吸收利用特點已有大量研究,然而藻細胞內部磷儲存的研究相對較少。
本文以一種常見水華藻種——水華束絲藻為研究對象,通過恒化培養的方式來獲得處于不同生長速率階段的藻種,避免了批次培養后期營養物限制及半連續培養過程中穩定期難以維持的問題[3,4]。討論處于不同生長速率狀態的藻種對于磷的儲存特點,以期闡釋該水華藻種的磷策略。
1 材料與方法
1.1 藻種及培養
實驗藻種為水華束絲藻(Aphanizomenon flos-aquae,FACHB-1029),購于中國科學院武漢水生生物研究所淡水藻種庫。藻種培養及實驗開展均在光照培養箱中進行,培養溫度25 ℃,光照強度27 μmol/(m2·s),光暗比為12 h∶12 h,培養基為BG-11[5]。
1.2 實驗設計
藻種在實驗前先使用無磷的BG11培養基饑餓培養1周。藻種的培養分為間歇培養和連續培養兩個階段:間歇培養即特定濃度的藻種(1.5×107cell/mL)在BG11培養基中生長并達到穩定生長期;連續培養則在間歇培養階段達到穩定后對培養裝置進行一定稀釋速率的稀釋,稀釋液為無菌BG11培養基。當葉綠素濃度連續6 d的數值變化在±5%以內時,認為系統達到穩定狀態,此時系統的稀釋速率即為藻類的生長速率[6]。藻種培養于1 L錐形瓶中,連續培養階段的培養體積為600 mL,稀釋速率分別為0.1 d-1,0.2 d-1,0.4 d-1,0.6 d-1,0.8 d-1。為保證藻細胞在培養裝置中的均勻分布,培養過程中均連續通入針頭過濾器(pore size:0.22 μm)過濾后的無菌空氣,同時提供藻類生長需求的無機碳。
葉綠素濃度每天檢測,采樣時間為每天8:00。當系統處于穩定狀態時,測定細胞總磷、顆粒態聚合磷酸鹽含量,同時使用熒光顯微技術對藻類聚合磷酸鹽進行定性分析。
1.3 測試方法
藻液的葉綠素濃度由葉綠素a代替,根據酒精冷凍提取法測定[7]。將藻液置于離心機(Eppendorf,5804R)中離心收集(6 500 rpm,10 min)藻細胞,蒸餾水離心清洗三次。向離心管中加入4 mL乙醇(95%)并使藻種重新混勻。將上述處理后的樣品放于4 ℃冰箱中提取12 h,離心收集上清液,然后使用紫外分光光度計在649 nm,665 nm波長下分別測定溶液吸光度。
細胞總磷(Total Cellular Phosphorus,簡寫為“TCP”)的測定參考總磷的測定方法[8]:藻細胞收集及清洗后,先用5%過硫酸鉀氧化(120 ℃,30 min),冷卻至室溫后使用GF/F濾膜濾去雜質,使用鉬銻抗分光光度法測定濾液中磷含量。文中各類磷酸鹽的含量均以P計。
顆粒態聚合磷酸鹽(Polyphosphate granules,簡寫為“PolyP”)的測定使用熱水提取方法。將藻液置于離心機(Eppendorf,5804R)中離心收集(6500 rpm,10 min)藻細胞,蒸餾水離心清洗三次后轉移至50 mL比色管,蒸餾水定容至25 mL,使用配套的磨口塞封閉比色管,并在管口使用紗布包裹,將比色管放入高壓滅菌鍋中進行提取(105 ℃,30 min)。待提取液冷卻至室溫后使用GF/F濾膜(Whatman)過濾并使用蒸餾水定容至50 mL。將濾液均分為兩份(a,b),使用鉬銻抗分光光度法[8]在700 nm波長下測定a份中的正磷酸鹽含量,即可提取正磷酸鹽(extracted Soluble reactive Phosphorus,簡寫為“e-SRP”)。向b份中加入4 mL過硫酸鉀(5%),密封后放入高壓滅菌鍋消解(120 ℃,30 min),冷卻后按鉬銻抗分光光度法[8]測定消解后磷酸鹽含量,即為可提取的總磷酸鹽(total extractable cellular phosphorus,簡寫為“e-TCP”)。e-TCP與 e-SRP的差值即為顆粒態PolyP的含量。
PolyP的熒光染色:細胞中PolyP能夠與DAPI結合后在紫外光激發下發出黃色熒光[9]。具體操作如下:取1 mL藻液,離心并蒸餾水清洗三次后(6 500 rpm,10 min)加入1 mL 2%戊二醛,固定10 min;離心后棄上清液,取10 μL固定后的藻液,然后加入10 μL DAPI試劑(DAPI濃度為50 mg/L),染色10 min后以330 nm~385 nm紫外光作為激發光,在熒光顯微鏡(BX53FL+MP5.0,Olympus)下觀察PolyP染色情況。
2 結果與討論
2.1 藻種培養過程

連續培養開始后,系統中生物量受到培養基稀釋和藻種生長的共同作用,藻種隨著培養基的稀釋而被大量沖走的同時,新補充的營養物質促進藻種的生長。本實驗所涉及的稀釋速率梯度中,系統中葉綠素濃度最終均能達到動態平衡,即實現該生長速率的長時間維持。在不同生長速率穩定階段,裝置內的葉綠素濃度隨稀釋速率的增加而降低(見圖1),葉綠素濃度最大值和最小值為(8 233±217)μg/L(0.1 d-1)和(652±30)μg/L(0.8 d-1)。
2.2 不同生長速率藻種PolyP的熒光顯微分析
除磷饑餓處理的藻種以外,其他藻種的DAPI熒光染色圖像均表現出黃色熒光(見圖2)。說明在培養過程中,藻類出現對磷的“奢侈吸收”并以PolyP的形式儲存在體內。
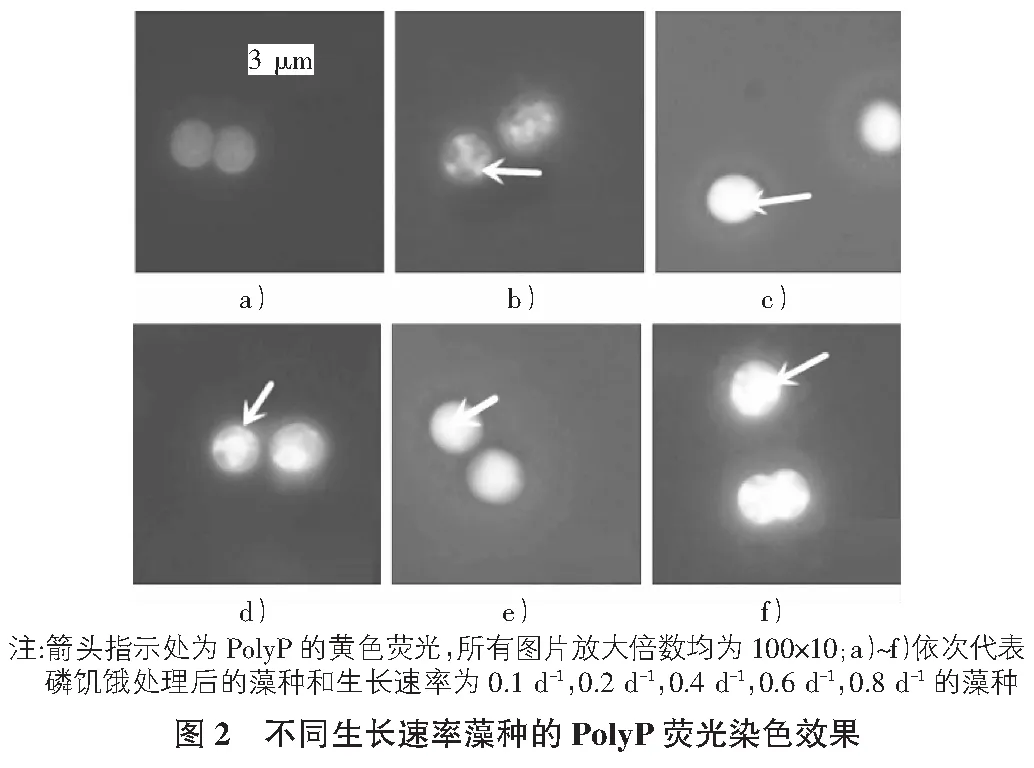
2.3 不同生長速率藻種PolyP的含量
水華束絲藻細胞內顆粒態PolyP含量隨生長速率的升高呈緩慢增高現象(見圖3)。在生長速率為0.1 d-1,0.2 d-1,0.4 d-1,0.6 d-1時,水華束絲藻細胞內顆粒態PolyP含量無明顯差異(P>0.05),為(0.25±0.03)μgP/μgChl-a,(0.26±0.04)μgP/μgChl-a,(0.29±0.09)μgP/μgChl-a,(0.39±0.04)μgP/μgChl-a。在生長速率為0.8 d-1時,顆粒態PolyP含量大幅增加并達到最大值,為(0.49±0.07)μgP/μgChl-a。低生長速率階段穩定期所存在的高生物量一方面加劇了藻種對營養鹽的競爭。另一方面高濃度藻種自身造成的遮蔽效應不利于PolyP的合成,Kanai等的研究表明在有光條件下,小球藻會快速吸收正磷酸鹽并將以PolyP的形式儲存;無光條件下,PolyP的合成則會減弱[10]。
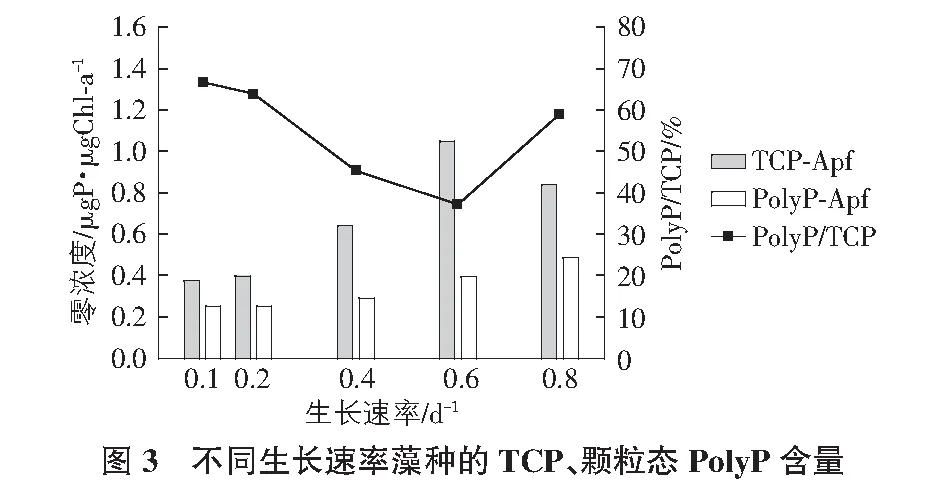
藻細胞TCP含量隨生長速率的提高而增加(見圖3),顆粒態PolyP在TCP中的比例(顆粒態PolyP/TCP)隨著生長速率的提高呈現出先降低再升高的現象(見圖3),在生長速率為0.6 d-1時達到最低值,為(37.33±3.63)%。
3 結語
恒化培養利于研究藻類在不同生長階段的營養物吸收特點。水華束絲藻對磷的吸收與細胞自身所處的生長階段有關,胞內顆粒態PolyP含量在高生長速率時略高于低生長速率,生長速率為0.8 d-1時顆粒態PolyP含量是所有實驗梯度中最高的,為(0.49±0.07)μgP/μgChl-a。隨著生長速率的增加,細胞含磷量不斷增加,使得顆粒態PolyP在TCP中的比例(顆粒態PolyP/TCP)呈現不同的變化趨勢。在低生長速率時,細胞內磷含量以顆粒態PolyP為主(65%左右)。當生長速率為0.6 d-1時,藻細胞中顆粒態聚合磷酸鹽在細胞總磷中的比例最小,為(37.33±3.63)%。高生長速率階段的快速新陳代謝不利于藻種對磷的儲存,在使用藻類處理高濃度含磷污水時需控制藻種的生長速率在較低水平。
[1] Rhee G.Competition between an alga and an aquatic bacterium for phosphate[J].Limnology and Oceanography,1972,17(4):505-514.
[2] Powell N,Shilton AN,Pratt S,et al.Factors influencing luxury uptake of phosphorus by microalgae in waste stabilization ponds[J].Environ Sci Technol,2008,42(16):5958-5962.
[3] 蔣禮玲,張亞杰,李瀟萍,等.微藻培養模式研究進展[J].可再生能源,2010,28(1):56-62.
[4] 王宗靈,李瑞香,朱明遠,等.半連續培養下東海原甲藻和中肋骨條藻種群生長過程與種間競爭研究[J].海洋科學進展,2006,24(4):495-503.
[5] 中國科學院武漢水生生物研究所.淡水藻種庫——淡水藻種培養基(BG11)[EB/OL]. http://algae.ihb.ac.cn/Products/ProductDetail.aspxproduct=4.html,2015-1-24/2015-01-24.
[6] Droop MR.Vitamin B12 and marine ecology Ⅲ.an experiment with a chemostat[J].J mar bio Ass UK,1966,46(3):659-671.
[7] Farga ová A.Inhibitive effect of organotin compounds on the chlorophyll content of the green freshwater alga Scenedesmus quadricauda[J].Bulletin of environmental contamination and toxicology,1996,57(1):99-106.
[8] 魏復盛.水和廢水監測分析方法[M].第4版.北京:中國環境科學出版社,2002:243-250.
[9] Eixler S,Selig U,Karsten U.Extraction and detection methods for polyphosphate storage in autotrophic planktonic organisms[J].Hydrobiologia,2005(533):135-143.
[10] Franklin MH.Inorganic polyphosphates in biology:structure,metabolism,and function[J].Bacterilolgical Reviews,1966,30(4):772-794.
Phosphorus storage capacity of Aphanizomenon flos-aquae living at different growth rates
Yan Bin
(UrbanConstructionandEnvironmentalEngineeringCollege,ChongqingUniversity,Chongqing400044,China)
The polyphosphate granules content in Aphanizomenon flos-aquae living at several growth rates were detected. Characters of phosphorus storage in algae were discussed. It made a further understanding on algae’s phosphorus storage capacity.
Aphanizomenon flos-aquae, growth rate, polyphosphate
2015-04-02
閆 彬(1989- ),男,在讀碩士
1009-6825(2015)17-0194-02
X131
A

