不同形態納米銀的制備及其殺菌性能的研究
孫彩華 何佳奇 余朝輝
浙江中醫藥大學附屬第一醫院藥劑科,浙江 杭州 310004
納米銀是一種新型材料,其殺菌能力強、殺菌廣譜、應用安全,在殺菌領域有很大的應用價值。納米銀的形態有多種,已經發現的有球形、立方體、銀納米線、八面體、三角片等,其形態不同,則制備方法各異。傳統的物理法不易控制條件,且費用較高,化學法操作簡單且條件易控制[1-2]。其中微波法以操作簡單、制備速率快等優點受到大量重視,本文以微波法制備不同形態納米銀,并對其殺菌性能進行研究。
1 納米銀的制備
1.1 材料
微波爐(Galanz G80F23CN1L-SD)、掃描電子顯微鏡(NOVANANOSEM 430)、透射電子顯微鏡(JEOL JEM-2100HR)、紫外-可見光分光光度儀(HACH DR 5000)、X 射線衍射儀(Bruker D8 ADVANCE)、電子天平(奧豪斯 AR2140)、高速離心機(中佳 HC-3017)。
1.2 儀器
硝酸銀(AgNO3)(國藥集團化學試劑有限公司)、聚乙烯吡咯烷酮 (PVPK30)(上海生物科技有限公司)、乙二醇(EG)(國藥集團化學試劑有限公司)、氯化鈉(NaCl)(廣州化學試劑廠)、乙醇(廣州化學試劑廠)、丙酮(國藥集團化學試劑有限公司)、去離子水與超純水為實驗室(浙江中醫藥大學附屬第一醫院實驗室)自制。
1.3 制備方法
利用微波合成法制備納米銀的步驟如下:在50 mL聚四氟乙烯反應容器中加入經準確稱取的AgNO3、聚乙烯吡咯烷酮(PVP)、EG以及NaCl,可見在加入NaCl后溶液由澄清透明狀逐漸變渾濁,溶液泛白、透光性變低,表示反應中產生了不溶于水的AgCl;充分攪拌溶液后獲得納米銀溶膠;溶液經分離、洗滌后得到目標產物納米銀[3]。制備過程中設定的變量分別為NaCl的投入量(NaCl加入量設置為 0、0.05、0.1、1、5 mg)、反應條件(微波爐320 W加熱,加熱時間為30 min)、反應的時間(1.5~4 min)、PVP/AgNO3比例(0、2∶1、8∶1),對不同條件下制備的納米銀產物進行分析。利用X線衍射確定物相,區分納米銀的形態;利用紫外-可見光分光光度計區分銀納米線,判定銀納米線的產率及線粒比;利用電子顯微鏡觀察產物的形貌,以確定晶體結構(單晶、孿晶或多晶);通過紅外光譜分析測定產物中是否存在有機物來判定納米銀清洗是否干凈。
1.4 結果
1.4.1 不同NaCl加入量下的納米銀形態 對不同NaCl加入量所得的納米銀產物進行形態分析顯示,反應體系中沒有NaCl或NaCl加入量少時,得到的納米銀顆粒未見結構整齊、形態單一的準球形,其粒徑為(60±10)nm;NaCl的量增加到0.1 mg時所得到的產物中不僅有準球形,還出現了立方體、右椎體、納米棒等球形以外的結構;NaCl的加入量再增加后,所得到的產物中納米顆粒所占的比例減少,銀納米線所占比例增加;將5 mg NaCl加入反應中所得到的產物中納米銀顆粒含量很少,而是以銀納米線為主,其線徑為(60±10)nm,線長為 2~4 μm。
1.4.2 不同反應時間的納米銀形態 在反應溶液中不加NaCl時,隨著反應時間的延長,所得產物的形態沒有改變,均為準球形的納米銀顆粒,結構整齊、形態單一,粒徑為(60±10)nm;而且紫外-可見光分光光度計掃描的結果顯示,隨著反應時間延長,所得產物的波長吸收峰沒有改變,為430~440 nm,據文獻[4]報道此吸收峰對應的是準球形納米銀顆粒,實驗結果與報道相符;隨著反應時間的延長,波長掃描特征吸收峰的吸收強度增高,說明所獲得的準球形納米銀顆粒的量增加。
在反應溶液中加入5 mg NaCl溶液后,隨著反應時間的延長,得到的產物不一樣,在1.5 min時得到的為納米銀顆粒,其大小不一、形態不規則,表明納米銀生長階段在初期;反應2 min時得到納米銀顆粒,顆粒粒徑為(60±10)nm,形態以立方體為主,也有右椎體、準球體顆粒,還夾雜少許銀納米棒,表明出現了納米銀的完整結構;在時間逐漸延長到3 min時,銀納米線的產量增加,其產生的量與納米顆粒的量一樣多,測量線長為1~2 μm;反應時間到4 min時,產物中主要是銀納米線,僅有很少的納米銀顆粒,銀納米線的線長也延長到2~4 μm。通過紫外-可見光分光光度計波長掃描,隨著時間的延長,吸收峰有變化,在1.5 min處的吸收峰為460 nm,吸收峰的強度稍低,因此處的吸收峰對應納米顆粒的立方體,故此時納米銀顆粒還少;在反應到2 min時吸收峰為460 nm,此時的吸收峰強度很高,說明此時產物中主要是納米銀顆粒的立方體;反應時間延長到3 min時,有兩個吸收峰,分別在390 nm處與460 nm處,而390 nm處代表銀納米線,表示此時納米銀顆粒與銀納米線的產量一樣多;反應到4 min時,吸收峰為390 nm,即此時產物中主要含有銀納米線,結果如表1所示。
1.4.3 不同比例PVP/AgNO3時產物中納米銀的形態反應溶液中不加NaCl時,在不同比例的PVP/AgNO3反應體系中,得到的產物均為納米銀顆粒,在不加入PVP時產物中納米銀顆粒大小不規則,而在加入PVP后,產物中納米銀顆粒形狀為準球形,大小均勻,形態規則,粒徑為60~70 nm。

表1 不同反應時間下納米銀產物的分析
反應溶液中加入5 mg NaCl后,不同比例PVP/AgNO3反應體系中,得到的產物形態明顯不同,反應液中未加PVP時,所得結果為納米銀顆粒,其形態不規則;加入PVP使得PVP/AgNO3比例為2∶1時,所得產物主要為納米線;而加入更多PVP使得PVP/Ag-NO3比例為8∶1時,產物中主要是納米顆粒,而納米線的量很少,結果如表2所示。

表2 不同比例PVP/AgNO3時產物中納米銀的形態
2 不同形態納米銀的殺菌性能
2.1 儀器
2.1.1 儀器 96孔板(廣州普博儀器有限公司)、電子天平(美國奧豪斯,AR2140)、高速離心機(安徽中科中佳科學儀器有限公司,HC-3017)、恒溫振蕩器(上海智誠分析儀器制造有限公司,ZHWY-2102C)、透射電子顯微鏡(上海日立高新技術國際貿易有限公司,H-7650)。
2.1.2 試劑 LB培養基、瓊脂均購自廣東環凱微生物科技有限公司;NaCl、碳酸氫鈉(NaHCO3)、磷酸鈉(Na3PO4)、硫化鈉(Na2S)、硝酸(HNO3)均購自國藥集團化學試劑有限公司;去離子水為研究組自制。
2.1.3 菌種及培養 大腸埃希菌 (E.coil)(廣東省微生物所菌種保藏中心)在LB液體培養基上進行培養。
2.2 方法
2.2.1 測量納米銀的最低抑菌濃度 (MIC)采用對倍稀釋法,把96孔板LB培養基中加入不同形態的納米銀(銀立方體、銀納米線、準球形顆粒)與大腸埃希菌液,以2倍稀釋法設定濃度,納米銀濃度設定為3~100 μg/mL,大腸埃希菌濃度為 1×103、1×104、1×105、1×106cfu/mL,將孔板放于37℃、200 r/min振蕩器中培養24 h,判定 MIC。
2.2.2 測定納米銀的殺菌效果 把大腸埃希菌懸浮液中加入2 mmol/L NaHCO3緩沖液以1∶10的比例稀釋,使得大腸埃希菌濃度為1×106cfu/mL,在離心管中以移液槍加入稀釋后的細菌液,在加入3種形態的納米銀,將其濃度設定為 3、6.25、12.5、25、50、100 μg/mL,并設置空白對照,對照組中未加入納米銀,其他成分則相同。樣品反應時間為1 min,各取100 μL樣品接種在LB培養基中培養24 h(放于37℃恒溫搖床),查看大腸埃希菌生長情況。
2.2.3 透射電鏡觀察 通過透射電鏡觀察納米銀與大腸埃希菌的接觸情況,步驟為:大腸埃希菌稀釋液中加入納米銀,納米銀濃度為100 μg/mL,取一滴混合液經銅網固定2 min、濾紙吸去液體、經磷鎢酸染色2 min后去掉多余染色液,在透射電鏡下觀察處理后的樣品。
2.3 結果
2.3.1 不同形態納米銀的MIC 納米銀能抑制大腸埃希菌的生長,且隨著大腸埃希菌濃度的增加,抑制其生長所需的納米銀的量增加,不同形態納米銀的MIC不同,銀立方體形態納米銀的MIC最小,即抑制細菌生長的能力最強,準球形顆粒抑制細菌生長的能力次之,銀納米線MIC最大,即抑制細菌生長的能力最弱,結果如表3所示。
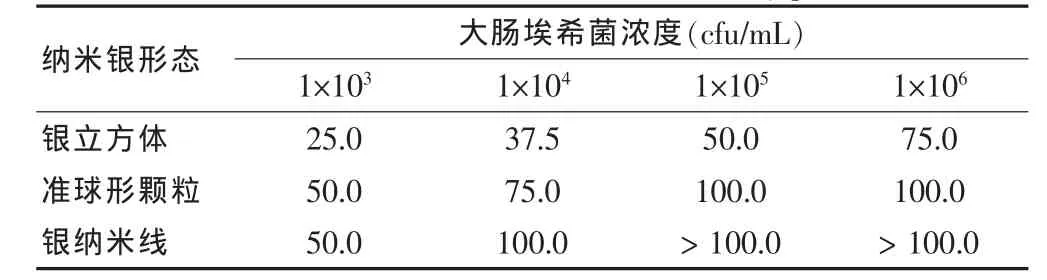
表3 不同形態納米銀的最低抑菌濃度(μg/mL)
2.3.2 納米銀的殺菌效果 將大腸埃希菌中加入不同形態納米銀進行培養的結果中,隨著納米銀濃度的增加,對大腸埃希菌的抑制作用增強,3種形態納米銀對大腸埃希菌抑制能力不同,銀立方體的濃度為25 μg/mL時即能滅活大腸埃希菌,而準球形顆粒濃度為100 μg/mL時使大腸埃希菌滅活,銀納米線濃度超過100 μg/mL時仍不能完全滅火大腸埃希菌,可見銀立方體的滅菌效果最優,銀納米線滅菌效果最差,準球形顆粒介于兩者之間,結果如圖1顯示。
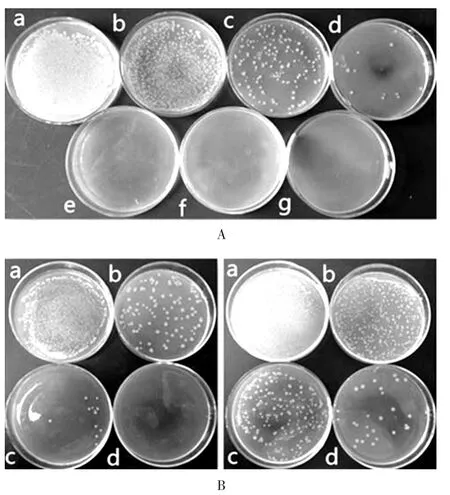
圖1 不同形態納米銀培養皿中大腸埃希菌培養情況
2.3.3 不同形態納米銀與細菌混合后投射電鏡觀察結果 大腸埃希菌中沒有加入納米銀時,透射電鏡下觀察到大腸埃希菌表面并無多余的雜質,其表面光滑、平整。在大腸埃希菌液中加入3種形態的納米銀后,大腸埃希菌表面不平整,吸附著不同形態的納米銀。透射電鏡顯示3種形態的納米銀與細菌的接觸情況不同,銀立方體與大腸埃希菌能有效接觸,兩者接觸面積大;球形納米銀能與大腸埃希菌有效接觸,兩者的接觸面積亦很大;銀納米線不能與大腸埃希菌有效接觸,兩者的接觸面積小。
3 討論
納米銀的制備方法大體分為物理方法、化學方法、生物方法[5]。物理法是把較大的單質銀以物理學方法制備成納米大小的納米銀,有機械球磨法、蒸發冷凝法、霧化法等。其中機械球磨法的產物主要是納米銀顆粒,顆粒分布不均,純度低。據有關報道,低溫高能機械球磨法制備出了平均粒徑為20 μg的納米銀顆粒;蒸發冷凝法能夠制備清潔界面納米銀粉,有報道利用氣象冷凝法得到了懸浮的納米銀粉;霧化法的產物為粉劑,有報道利用霧化法制備出超細顆粒,粒徑在5~20 nm[6-7]。化學法是利用化學反應原理把銀離子還原成單質銀,有化學還原法、微乳液法、溶膠-凝膠法等。其中化學還原法以水或有機溶劑將金屬鹽溶解,再通過還原劑或表面活性劑使粒子結晶后脫水,制備得到粉體,制備的成本低、產量大,條件易控制,可制備出5~30 nm大小的納米銀粒子;微乳液法是使兩種不相溶的溶劑混合成乳液,再從中析出固體成分,制備到納米粉體,制備到的納米顆粒多為球形,可制備6 nm的納米顆粒,粒徑均一;溶膠-凝膠法是利用特殊方法水解金屬化合物為溶膠、凝膠,然后處理得到納米粉體,產物粒度小、純度高[8-9]。生物方法是將生物材料天然合成納米微粒,采用的生物材料有龍眼葉、山茱萸、芳樟葉、梔子干粉、茶葉等,以其諸多優點而成為近年來研究的熱點。鑒于納米銀的制備方法有多種,粒子形態也各異,且不同形態的納米銀性質和殺菌性能不同,近年來的研究中提出了納米銀形貌的可控制備方法[10-11]。
20多年來,不同形態納米銀的制備有了很大發展,新的制備方法也克服了傳統方法中價格昂貴、純度不高等缺點,其中微波法以其操作簡單、制備速度快、產量多等優點而備受關注,本研究借用前人的研究成果,并結合本研究組多年的研究經驗,通過控制微波法制備納米銀的條件來得到不同形貌的產物,對研究結果的分析如下:
首先,制備不同形態的納米銀是在熱力學與動力學中改變制備的條件來完成的,且沉淀性離子是考慮的條件之一,Cl-能通過控制使Ag+形成沉淀的速率來調控反應的速率,而且Cl-通過與氧氣結合來控制對晶種的選擇,據此筆者研究不同NaCl的量對納米銀形態的影響,沒有NaCl或少量NaCl時產物中以準球形納米銀顆粒為多,隨著NaCl量增多,非球形產物比例增加,球形顆粒比例減少,NaCl增加到5 mg時產物以銀納米線為多,可見控制Cl-的量能夠實現對納米銀形態的控制[12-13]。
其次,由于納米銀晶體的生長是按照成核-聚集-生長過程進行的,反應時間的長短不同則納米銀形態亦不同。本研究通過控制微波中的反應時間發現,在反應時間為1.5 min時,產生不規則的納米銀顆粒,隨著時間的推延,產物中混有更多形態的納米銀顆粒,并逐漸出現納米銀棒,時間更長時產生長度更長的銀納米線,而納米銀顆粒的量逐漸減少,因此通過控制反應的時間能調控納米銀顆粒和銀納米線的制備[14]。
鑒于PVP具有的空間位阻特性,能夠影響納米銀的分散性,控制納米銀的異性生長,據此考慮PVP加入量不同時對產物形態的影響,本研究在不加入PVP時得到不規則的納米銀顆粒,加入適量的PVP制備的產物以銀納米線為主,加入大量PVP時主要產生納米顆粒,可見PVP的加入量能夠影響納米銀的形態[15]。
納米銀是新型的殺菌材料,其殺菌效果強、廣譜且應用安全,在殺菌領域具有不可估量的應用價值,查閱相關報道,分析其殺菌機制為:銀能夠緊密地結合含硫或含磷的化合物,而在細胞膜上存在含硫的蛋白質,納米銀結合硫蛋白后能夠吸附在細胞膜表面并累積于此,也可以穿透細胞膜抵達細胞內部。相關研究也證實納米銀對細菌的殺滅作用是物理接觸與化學反應共同作用完成的[16]。納米銀與細菌的物理接觸是限制性步驟,一旦接觸就會吸附在細胞膜表面,納米銀與細胞膜表面的含硫蛋白結合并反應,導致細胞膜功能受損,通透性改變,細胞隨即死亡,因此,納米銀對細菌有抑制作用的重要機制是納米銀能夠直接接觸細菌表面[17]。
鑒于不同納米銀的性質不同,其殺菌能力也有強弱差異,本次研究中為比較不同形態納米銀的殺菌能力,制備了銀立方體、準球形顆粒、銀納米線3種形態納米銀,結果顯示不同形態納米線的殺菌性能有差異,比較3種形態納米銀的MIC,銀立方體的MIC最小,即殺菌效果最好,準球形顆粒的MIC稍高,其殺菌效果稍弱,而銀納米線的MIC最高,亦即殺菌效果最弱[18-20]。通過透射電鏡觀察,分析不同形態納米銀的殺菌性能強弱不同的原因,是由于納米銀形態能夠影響其與細菌的接觸面積,銀立方體與球形顆粒能充分暴露接觸面,接觸更多的細菌,故殺菌性能強,而銀納米線的一維結構減少了暴露面積,其殺菌性能相對弱。對于銀立方體與準球形顆粒為何表現出不同的殺菌效果,就需要用納米銀的晶體結構來解釋,現已經明確銀立方體表面主要覆蓋{100}晶面,準球形顆粒表面主要覆蓋{111}晶面,而γ{100}的表面能比γ{111}的表面能大,所以銀立方體的反應活性更強,而具有較為穩定的{111}晶面結構的準球形顆粒反應活性稍弱,根據資料結果本研究推測,銀立方體的殺菌性能比準球形顆粒的殺菌性能強是因為銀立方體暴露有{100}晶面,反應活性比暴露{111}晶面的準球形顆粒強。
綜上所述,不同形態的納米銀其制備流程不同,在微波法制備納米銀過程中,改變反應中所加NaCl的量、反應的時間、反應中PVP的量均能影響產物中納米銀的形態,據此,本研究可通過控制制備納米銀的材料或條件探究各種形態納米銀的最佳制備條件,來實現不同形態納米銀的可控制備。納米銀的形態不同則性質不同,導致其與細菌接觸的有效面積大小也不同,則對細菌的滅活效果不同,本次研究的結果提示銀立方體的殺菌性能比準球形顆粒強,準球形顆粒的殺菌效果又優于銀納米線,而對于改變殺菌試驗中某一條件時對殺菌效果的影響,還需要進一步的研究加以證實。
[1]蔡璇,魏源源,劉燕,等.飲用水化學消毒方法及其影響因素研究進展[J].衛生研究,2011,40(5):660-663.
[2]LiWR,XieXB,ShiQS,etal.Antibacterialactivityandmechanism of silver nanoparticles on Escherichia coli[J].Applied Microbiology and Biotechnology,2010,85(4):1115-1122.
[3]Schoen DT,Schoen AP,Hu L,et al.High speed water sterilization using one-dimensional nanostructures[J].Nano Letters,2010,10(9):3628-3632.
[4]Xiu ZM,Zhang QB,Puppala HL,et al.Negligible particlespecific antibacterial activity of silver nanoparticles[J].Nano Letters,2012,12(8):4271-4275.
[5]Suresh AK,Pelletier DA,Doktycz MJ.Relating nanomaterial properties and microbial toxicity[J].Nanoscale,2013,5(2):463-474.
[6]Haase A,Arlinghaus HF,Tentschert J,et al.Application of laser postionization secondary neutral mass spectrometry/time-of-flight secondary ion mass spectrometry in nanotoxicology:visualization of nanosilver in human macrophages and cellular responses[J].ACS Nano,2011,5(4):3059-3068.
[7]KimS,Ryu DY.Silver nanoparticle-induced oxidative stress,genotoxicity and apoptosis in cultured cells and animal tissues[J].Journal of Applied Toxicology,2013,33(2):78-89.
[8]El Badawy AM,Silva RG,Morris B,et al.Surface chargedependent toxicity of silver nanoparticles[J].Environmental Science Technology,2010,45(1):283-287.
[9]Yu SJ,Yin YG,Liu JF.Silver nanoparticles in the environment[J].Environmental Science:Processes&Impacts,2013,15(1):78-92.
[10]孫檬茜,陳耀斌,李良超,等.無機抗菌劑的研究進展[J].科技創新導報,2011,18(1):20-21.
[11]韓秀秀,何文,田修營,等.銀系無機抗菌材料抗菌機理及應用[J].山東輕工業學院學報,2010,24(1):25-26.
[12]EI Badawy AM,Silva RG,Morris B,et al.Surface chargedependent toxicity of silver nanoparticles[J].Environmental Science Technology,2011,45(1):283-287.
[13]Chernousova S,Epple M.Silver as antibacterial agent:ion,nanoparticle,and metal[J].Angewandte Chemie International Edition,2013,52(6):1636-1653.
[14]Steinigeweg D,Schlücker S.Monodispersity and size control in the synthesis of 20-100 nm quasi-spherical silver nanoparticles by citrate and ascorbic acid reduction in glycerol-water mixtures [J].Chemical Communications,2012,48(69):8682-8684.
[15]Li X,Lenhart JJ,Walker HW.Dissolution-accompanied aggregation kinetics of silver nanoparticles[J].Langmuir,2010,26(22):16690-16698.
[16]劉芳.納米銀抗菌材料的制備及其抗菌性能研究[J].中國消毒學雜志,2012,29(12):1089-1090.
[17]劉敏,胡嘉想,秦光和,等.納米銀抗菌凝膠劑的毒理學評價[J].中國消毒學雜志,2010,27(3):260-261.
[18]Sosenkova LS,Egorova EM.The effect of particle size on the toxic action of silver nanoparticles [J].Journal of Physics:Conferences Series,2011,291(1):210-211.
[19]湯京龍,王碩,劉麗,等.納米銀顆粒的細胞毒性作用及機制初探[J].北京生物醫學工程,2013,32(5):485-489.
[20]黃念,林清,蘇永華,等.納米銀敷料治療燒傷創面的療效與安全研究進展[J].北京生物醫學工程,2015,34(4):427-431.

