奧拉西坦的逐步凍凝結晶
杜世超,李康麗,張育,高志峰,王晨光,郭柏松,李代禧,湯偉偉,龔俊波
(1 國家工業結晶工程技術研究中心,天津 300072;2 天津化學化工協同創新中心,天津 300072; 3 石藥集團歐意藥業有限公司,河北 石家莊 050051;4 上海東富龍科技股份有限公司,上海 201109; 5 上海理工大學,上海 200093)
引 言
奧拉西坦,英文名Oxiracetam,化學名為4-羥基-2-氧代-1-吡咯烷乙酰胺,其結構式如圖1 所示,分子式為C6H10N2O3。奧拉西坦是一種被廣泛應用的治療腦損傷及記憶障礙等疾病的處方藥,它的多種臨床功效已被廣泛證實[1-3]。奧拉西坦有左旋、右旋兩種異構體,目前藥品中多用其外消旋體,左旋奧拉西坦及外消旋奧拉西坦分別有多晶型、水合物及共晶被報道[4-6],不同的晶型可能會導致不同的藥效。現在被廣泛使用的奧拉西坦處方藥劑多為膠囊和針劑,其中奧拉西坦針劑是由“凍干”技術制成,經過凍干技術得到的奧拉西坦處方粉針劑復水性好,藥效明顯。
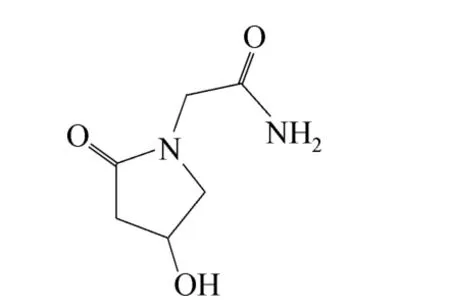
圖1 奧拉西坦結構式Fig.1 Chemical structure of oxiracetam
“凍干”技術是真空冷凍干燥技術的簡稱,是將濕物料凍結到共晶點溫度以下,使溶劑和溶質均變成固態,然后在一定的溫度和真空度下利用溶劑的升華脫除溶劑而獲得干燥制品的技術[7-9]。凍干過程中一般要加入凍干保護劑,凍干保護劑可以提高凍干濕物料的的共熔點和共晶點,從而提高預凍溫度和升華干燥及解析干燥的溫度,加快凍干過程,節省能量[10-11]。凍干的一個核心步驟為預凍步驟,預凍過程的好壞對后期的干燥尤其是升華干燥影響很大,而預凍結果的好壞取決于預凍過程中各組分的晶體形態。預凍過程事實上就是一個降溫逐步凍凝的結晶過程[12-15],目前對預凍工藝的研究基本上集中在確定預凍溫度和預凍速率上[16-17],而對預凍過程中的微觀粒子變化(結晶)研究較少,無文獻報道奧拉西坦的凍干相關內容。
奧拉西坦凍干粉針劑的處方為奧拉西坦、山梨醇和水[18],不同于傳統的低濃度的凍干過程,奧拉西坦和山梨醇處方利用高濃度(固體質量分數超過40%)的水溶液進行凍干生產。由于體系的黏度較大,不利于藥物活性組分奧拉西坦和凍干保護劑山梨醇的晶體的形成,利用傳統的簡單預凍工藝,極易使溶液凍凝成玻璃態,造成升華干燥困難,甚至引起“噴瓶”的現象,導致凍干時間長、成品率低。本文從分子角度分析預凍過程,從逐步凍凝結晶的角度考慮改善預凍工藝。首先,通過分子模擬計算了山梨醇和奧拉西坦之間的相互作用能,從理論上評估山梨醇對奧拉西坦結晶的影響。并通過離線測試手段確定奧拉西坦處方凍干產品的晶體形態。通過在線手段探究不同的預凍工藝對凍干過程中各組分結晶過程的影響,分析玻璃態形成的原因。然后改變預凍工藝,避免處方溶液凍凝成玻璃態,利用各組分在逐步凍凝過程中的出晶順序,使得奧拉西坦、水和山梨醇組分分別凍凝形成微晶,從而制造通暢的孔道,極大縮短了凍干所需時間,提高了藥品的成品率。
1 實驗材料和方法
1.1 材料
奧拉西坦(純度>99%,石藥集團歐意藥業);山梨醇(純度>99%,石藥集團歐意藥業);去離子水(市售)。
1.2 實驗裝置
凍干機(上海東富龍科技股份有限公司)。
1.3 分析測試儀器
粉末X 射線衍射儀(PXRD,D/Max-250,日本理學電機株式會社):X 射線發生器CuKαλ= 0.15418 nm;電壓/電流40 kV/100 mA;掃描范圍2°~50°;掃描步長0.02°;掃描速度8(°)·min-1。單晶X 射線單晶衍射儀(SXRD,Riguku R-rapid II日本理學電機株式會社):X 射線發生器MoKαλ=0.071073 nm;電壓/電流50 kV/90 mA。
差示掃描量熱儀(DSC,DSC1/500,瑞士梅特勒托雷多公司):高純氮氣流速50 ml·min-1;測量溫度范圍-40~25℃,降溫速率0.35~10℃·min-1。
熱臺顯微鏡(LTS350,德國徠卡公司):控溫部分型號TMs94,降溫速率0.35~10℃·min-1。
拉曼光譜(RXN2,美國Kaiser 公司):激發波長785 nm;掃描范圍100~1890 cm-1;掃描步長4 cm-1;曝光時間30 s。
1.4 單晶培養
取奧拉西坦2 g,室溫下溶于5 ml 的去離子水中,用0.22 μm 的濾膜過濾至試管中,室溫下緩慢蒸發7 d,即可得到奧拉西坦晶體,挑選較好的晶體做X 射線單晶衍射。
1.5 逐步凍凝結晶實驗
奧拉西坦處方的制備:奧拉西坦(40 g)+山梨醇(12 g)+水,配備100 ml 溶液,過0.22 μm 濾膜備用。
玻璃態預凍:分別以0.35、1、5 和10℃·min-1的降溫速率將奧拉西坦處方溶液從25℃連續降溫至-40℃,-40℃恒溫2 h。分別用DSC 和熱臺顯微鏡觀測預凍凍凝結晶過程。
晶體態預凍:分別以0.5、1、5 和10℃·min-1的降溫速率將奧拉西坦處方溶液從25℃連續降溫至-17℃,在-17℃恒溫2 h 以上,再降溫至-40℃,-40℃恒溫2 h 以上。分別用DSC 和熱臺顯微鏡觀測預凍過程中各組分的結晶行為。
1.6 凍干實驗
將配好的奧拉西坦處方放置在凍干機中,分別用1.5 節所述預凍方法預凍處方溶液,再用相同的條件進行升華干燥和解析干燥,得到凍干產品,用PXRD 和拉曼測試凍干產品。
2 實驗結果與討論
2.1 山梨醇對奧拉西坦結晶的影響
由于粉針劑產品的復水性和溶解速率與產品的晶習和粒度大小相關,因此需要探究山梨醇對奧拉西坦晶習的影響。山梨醇本身具有多個羥基,理論上很容易跟水及奧拉西坦分子發生分子間相互作用,為了探究山梨醇對奧拉西坦晶習的影響,用Material Studio 軟件計算山梨醇和奧拉西坦分子間的相互作用。
經過單晶衍射,解析出奧拉西坦的晶體結構。由單晶數據可以看出本實驗所用的外消旋奧拉西坦的原料在水中得到的晶體為無水晶型,晶體為正交晶系,空間群為Pca21,晶胞參數見表1。
根據單晶數據計算出的粉末圖譜和原料本身的粉末衍射圖譜衍射峰位置一致,如圖2 所示,說明解析出的單晶和原料是同一晶型,可以用單晶數據進行進一步的分子模擬計算。
對晶體結構進行幾何優化和動力學優化后,選用BFDH 模型對奧拉西坦進行晶習模擬,得到奧拉西坦為塊狀晶習,和奧拉西坦的原料比較接近。選取主要的3 個晶面:100、010 和001,如圖3 所示。
切出晶面,構建真空層,弛豫晶體表面的單層晶體分子,進行分子動力學計算,步長1 fs,動力學時長為200 ps。構建山梨醇聚合物分子,進行動力學優化,待分子處于平衡后,將其置于晶面上方的真空層中。弛豫晶體表面的單層分子和聚合物分子,進行分子動力學計算,步長為0.01 fs,動力學時長為200 ps。計算山梨醇和奧拉西坦各個晶面的相互作用,通過體系總能量、晶面能和凍干保護劑山梨醇的能量得到[19-21]。晶面的相互作用由式(1)計算,得到的結果見表2。
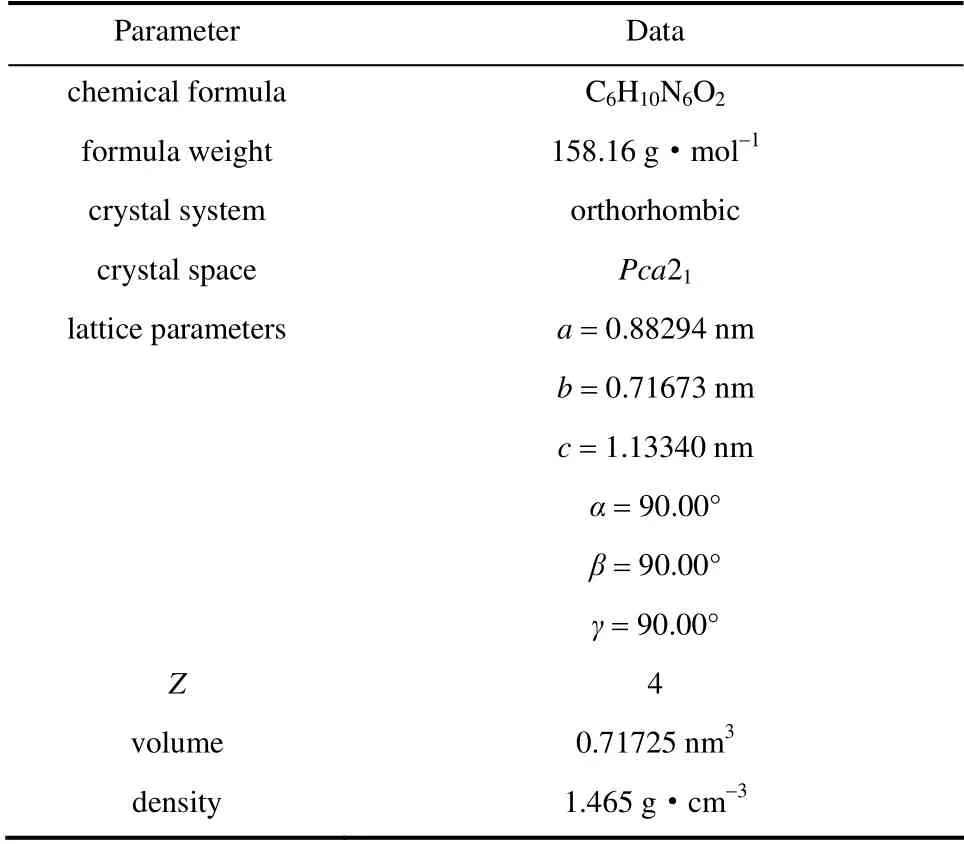
表1 奧拉西坦的單晶結構數據Table 1 Crystal structure data of oxiracetam
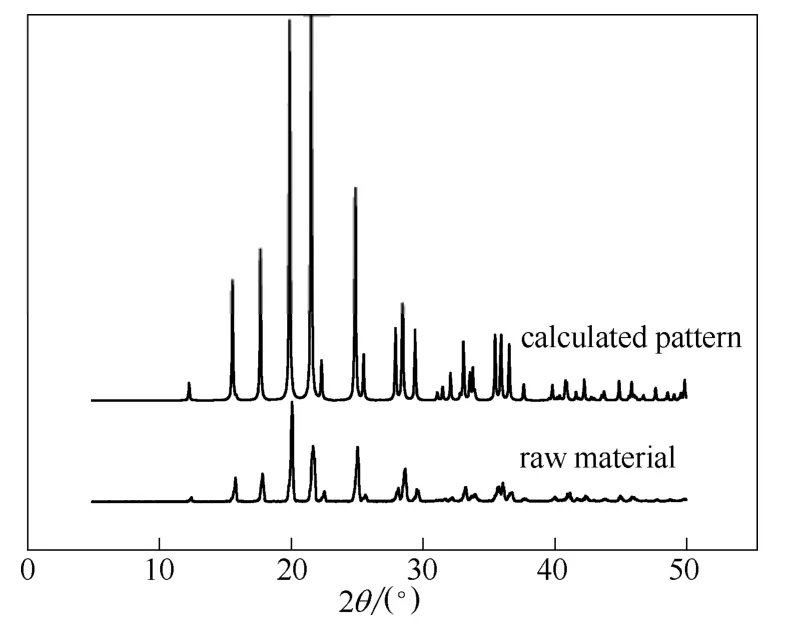
圖2 奧拉西坦粉末衍射Fig.2 PXRD patterns of oxiracetam
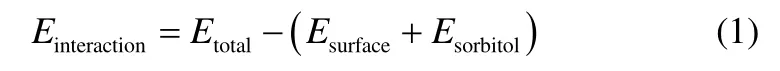
式中,Einteration為山梨醇和奧拉西坦之間的相互作用能;Etotal為奧拉西坦和山梨醇的總能量;Esurface為奧拉西坦的晶面能;Esorbital為山梨醇的總能量。
表中,Einteraction為總的晶面相互作用能, EvanderWaals為范德華力導致的山梨醇分子對晶面的相互作用能,由計算數值可以看出,山梨醇分子對各個晶面的相互作用能都很小。這是因為奧拉西坦3 個主要晶面中暴露的基團都很少,尤其是羥基,幾乎都在晶體內部,這樣很難與山梨醇形成氫鍵等相互作用。即便是在模擬環境的真空條件下,山梨醇對奧拉西坦各個晶面的作用都很小,對奧拉西坦的晶習影響很微弱。而在處方溶液中,山梨醇更容易和水形成氫鍵,對奧拉西坦的晶習影響更小。實驗也驗證了這個結論。因此,在凍干過程中山梨醇并不會影響奧拉西坦的晶習。

圖3 奧拉西坦主要晶面剖析圖Fig.3 Main crystal surface of oxiracetam

表2 山梨醇對奧拉西坦各晶面的作用能Table 2 Interaction energy of sorbital on oxiracetam crystal surface
綜合上面的研究發現,山梨醇的濃度可以適當增大而不會影響奧拉西坦的晶型和晶習,同時又能提高共熔點和共晶點。
2.2 凍干過程中各組分晶型的變化

圖4 奧拉西坦凍干產品粉末衍射圖譜Fig.4 PXRD patterns of freeze-dried product of oxiracetam
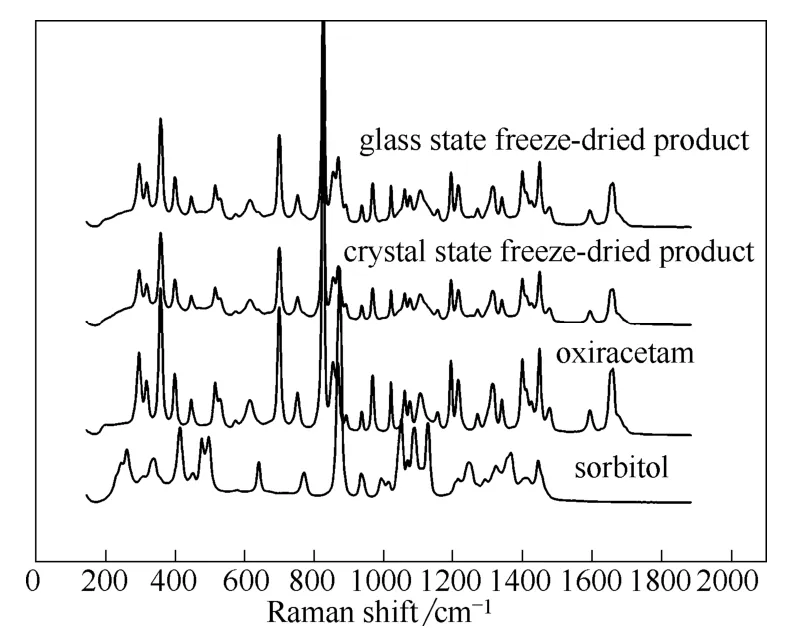
圖5 奧拉西坦凍干產品的拉曼圖譜Fig.5 Raman patterns of freeze-dried product of oxiracetam
藥物晶型會對藥效產生影響,因此必須確認凍干前后處方中各組分的晶型變化。分別按照玻璃態預凍和晶態預凍工藝對奧拉西坦處方進行預凍,并冷凍干燥至無水狀態,對所得凍干產品進行PXRD 和拉曼光譜測試,結果如圖4 和圖5 所示。PXRD圖譜顯示,不同的凍干工藝得到的產品的粉末衍射的特征吸收峰,基本上和奧拉西坦原料吻合,并未發現山梨醇的晶體特征峰,山梨醇只有類似于無定形的峰出現。因此,凍干產品中奧拉西坦是以晶體態存在,而山梨醇最終是以無定形態存在。
拉曼圖譜顯示,兩種凍干工藝得到的產品也只顯示晶體奧拉西坦的特征峰,山梨醇的特征峰幾乎全都消失。因此,山梨醇在最終的產品中是以無定形的形式存在,這說明凍干保護劑山梨醇不影響奧拉西坦的晶型。同時拉曼圖譜中奧拉西坦的吸收峰位置均和原料一樣,并沒有產生峰的偏移或者不同于山梨醇和奧拉西坦的新峰出現,說明奧拉西坦和山梨醇并不形成共晶或者鹽,而是以單獨的組分混合存在。
2.3 奧拉西坦處方簡單凍凝過程研究
實驗中所用的幾種降溫速率的預凍條件下,凍干所需時間均很長,而且降溫速率越快,最后越不易升華干燥和解析干燥,運用此種預凍工藝,一批產品凍干時間要7 d 左右,成品率卻只有20%左右。運用凍干技術中經常采用的“退火”技術,效果也不明顯。為了探究其原因,用在線的熱臺顯微鏡,觀察預凍過程中體系逐步凍凝的結晶狀態。
以0.35℃·min-1的降溫速率為例,分析奧拉西坦處方玻璃態凍凝過程中的結晶過程。熱臺顯微鏡分析結果顯示(圖6):從初始溫度的澄清溶液(a,25℃)開始逐漸降溫,溶液中逐漸出現六邊形塊狀晶體,并慢慢生長(b,3.6℃到c,-5.7℃),直至近飽和狀態,經判斷改晶體為奧拉西坦晶體。此過程在快速降溫過程中未發現,說明逐步凍凝前期奧拉西坦的過飽和度并不大,而且在快速降溫時介穩區更寬,不易出晶。繼續降溫,有雪花狀晶體出現和生長(d,-11.8℃到e,-14.1℃),判斷該晶體為冰晶體。到-16.5℃左右,冰晶體周圍出現一些性狀同奧拉西坦相似的晶體(f 中的黑色固體),這是由于水快速結晶后奧拉西坦的濃度快速上升,導致其過飽和度急劇升高而爆發出晶。繼續降溫,溶液變 得致密,不再有晶體折光性(f,-21.3℃),分析為山梨醇及溶液體系內各組分同時凍凝為玻璃態。繼續降溫和養晶,凍凝產品仍然為玻璃態(h,-40℃)。

圖6 奧拉西坦處方玻璃態預凍過程熱臺圖片Fig.6 Hot-stage microcopy pictures of glass state prefreezing process
DSC 測試結果如圖7 所示,熱量曲線中顯示一個大的吸熱峰,結合熱臺顯微鏡的結果綜合分析:在-10℃之前幾乎沒有看到奧拉西坦的結晶放熱峰,這說明前期奧拉西坦出晶量比較少,降溫速率越快前期奧拉西坦的出晶越少。該放熱峰的主體部分(-17~-11℃)對應著冰晶體的產生,同時伴隨著奧拉西坦的部分爆發出晶產生的熱量(圖6 的d到f 過程),但是緊接著產生了一個玻璃化轉變的峰-21.3℃,進一步證明山梨醇和剩余組分凍凝成玻 璃態。
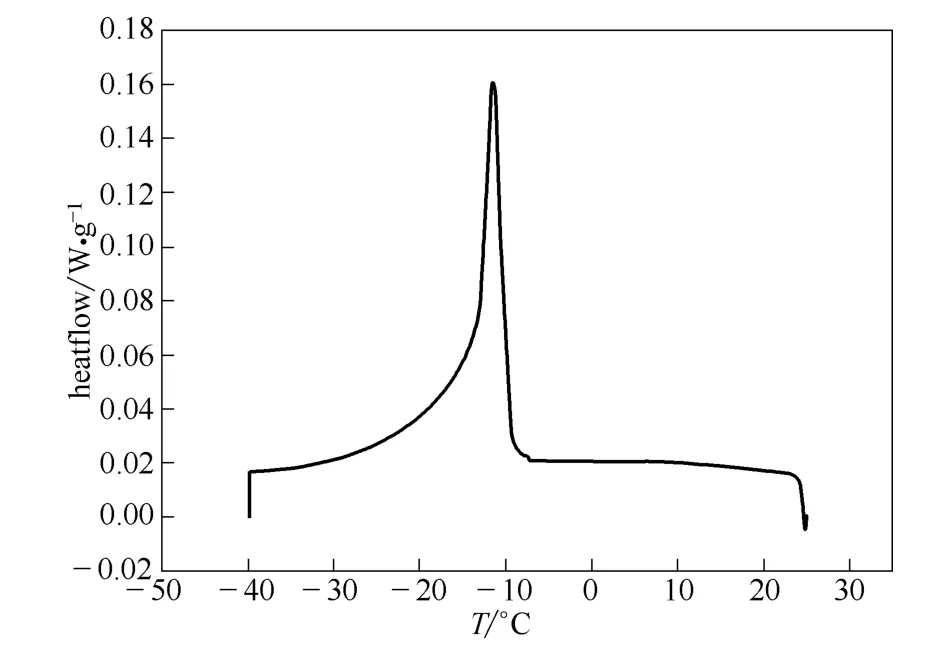
圖7 奧拉西坦處方玻璃態預凍過程Fig.7 DSC curve of glass state prefreezing process
綜合分析得出結論:連續降溫至預凍溫度,會使處方凍凝形成致密的類玻璃態,使得山梨醇、奧拉西坦和水不能通過凍凝結晶分離出來,而是緊密地連在一起。這導致水分很難升華出來,升華速度極慢,還容易造成產品上移、噴瓶等殘次品,這就是導致目前凍干工藝有缺陷的關鍵問題。而形成玻璃態的原因是該凍凝過程使山梨醇凍凝成玻璃態,進而使整個體系凍凝成玻璃態。
2.4 奧拉西坦變速降溫逐步凍凝結晶過程研究
為了防止預凍過程中各組分凍凝成玻璃態,需要改變預凍工藝,使各組分分別凍凝成微晶。上面實驗已經發現單純改變降溫速率的恒速連續降溫凍凝不能避免玻璃態的產生,可以考慮變速降溫的逐步凍凝。奧拉西坦處方是三組分體系,而且體系黏度很大,同時奧拉西坦和山梨醇在水中的溶解度都很大,由于傳質困難,很容易在逐步凍凝過程中形成玻璃態。如果能確定一個溫度點,同時確定一個平衡時間,使三組分能分別凍凝結晶出各組分晶體,就可以避免玻璃態的形成。
首先,需要確定凍凝分離的溫度點。根據上面玻璃態凍凝過程的研究發現,在-21.3℃之前,處方溶液中并未形成玻璃態,而是逐漸凍凝出了奧拉西坦晶體和冰晶體。而從圖7 可以看出,從-17℃開始,放熱峰開始變緩,直至出現玻璃態,而山梨醇在上述凍凝過程中始終沒有從體系中結晶出來。分析發現,-17℃可能為晶態到玻璃態轉變的一個關鍵節點,如果在-17℃增加一個恒溫段,可能會使各組分充分地平衡,進而凍凝分離出各組分的晶體,因此先確定-17℃為分離溫度點。
其次需要確定分離平衡時間,初步設定恒溫時間為10 h,可以根據DSC 的結果確定實際需要的平衡時間。因此,確定新的預凍凍凝條件為25℃處方溶液先恒速降溫至-17℃,恒溫10 h,再恒速降溫至-40℃恒溫一段時間。
熱臺顯微鏡顯示了整個預凍凍凝過程,如圖8所示:澄清溶液(a,25℃),奧拉西坦先出晶和生長(b,-5.3℃到c,-8.1℃),直至近飽和狀態;然后冰晶體出現和生長(d,-10.9℃到e,-12.3℃),藥液被濃縮;到-17℃恒溫過程時,先是奧拉西坦產生微晶,一段時間后顯微鏡下出現不同于奧拉西 坦和冰晶的晶體(f 中的黑色晶體),分析確定是山梨醇的結晶,繼續降溫直至-40℃,凍凝產品為晶體態。
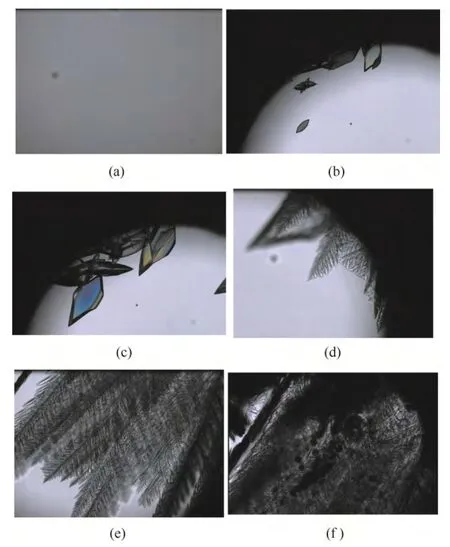
圖8 奧拉西坦處方晶體預凍過程Fig.8 Hot-stage microcopy pictures of crystal state prefreezing process
圖9 為DSC 監測結果:除了和前面相同的奧拉西坦晶體和冰晶產生的放熱峰,在-17℃恒溫過程中,DSC 圖譜上產生了一個新的結晶放熱峰[圖9 (b)],對應著山梨醇的結晶峰,該結晶峰在恒溫2 h之后趨于平緩,證明體系在該溫度下達到平衡,繼續降溫又有放熱效應,對應著各組分緩慢析出微晶。山梨醇結晶與否是控制整個預凍凍凝結晶過程的關鍵因素。
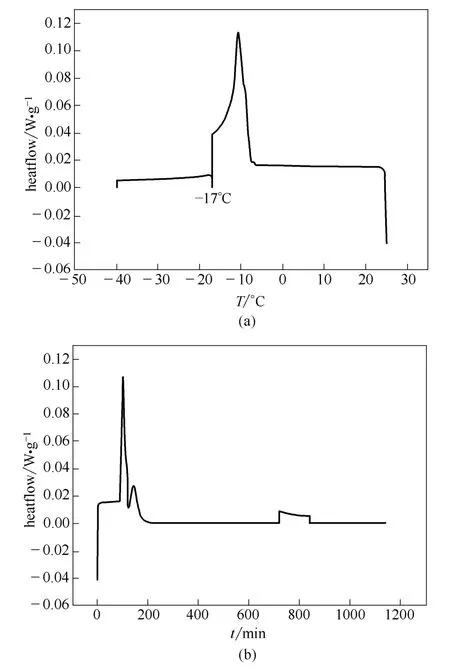
圖9 奧拉西坦處方晶體預凍過程Fig.9 DSC curve of crystal state prefreezing process
改變預凍工藝條件后,形成的是晶態凍凝產品,里面的藥物活性組分(奧拉西坦)以微晶的形式存在,形成了通暢的升華孔道,十分有利于升華干燥過程,而且能有效避免吹瓶現象的發生,使生產周期由7 d 左右縮短到2 d,成品率達到95%以上,所得產品為松散的塊狀固體,復水性很好。但是最終經過升華干燥和解析干燥后,奧拉西坦仍然為晶態,而山梨醇卻轉變成無定形的形式存在,山梨醇晶型的轉化機理還在研究之中。
根據實驗結果,開發出一種新型的預凍工藝,即將室溫下的奧拉西坦處方溶液以 0.5 ~10℃·min-1的降溫速率恒速降溫至-17℃,接著在 -17℃恒溫2 h 以上,然后以一定的降溫速率降溫至 -40℃,再恒溫凍晶2 h 以上。通過以上預凍工藝,各組分可分別逐步凍凝結晶為微晶態,很容易進行后續的升華干燥和解析干燥。目前該工藝已在石藥集團歐意藥業實現放大和產業化,該工藝使凍干時間和能耗大幅度減少,產品質量得到很大提高,經濟效益十分顯著。
3 結 論
(1)經過分子模擬計算得出山梨醇和奧拉西坦晶體各晶面的相互作用能很小,在奧拉西坦處方的凍干過程中幾乎不影響奧拉西坦的晶習。實驗驗證山梨醇在凍干過程中也不影響奧拉西坦的晶型,凍干產品中奧拉西坦以晶體態存在,而山梨醇以無定形形式存在。
(2)簡單逐步凍凝工藝(玻璃態預凍),會使山梨醇凍凝成玻璃態,導致3 個組分一起凍凝成玻璃態,進而使后續凍干步驟非常困難。
(3)通過改變預凍的降溫曲線,在產生玻璃態之前增加了一個低溫養晶的過程,使山梨醇、奧拉西坦和水都逐步凍凝出微晶,制造了通暢的升華孔道,大大加速了后期的升華干燥。
(4)從分子角度和逐步凍凝結晶的角度分析預凍過程,首創了低溫養晶、結晶、凍晶升華工藝,凍干所需時間大幅度縮短,產品質量得到很大提高。突破了低共熔點高濃度物質凍干的技術瓶頸,解決了類玻璃態物質凍干產業化的技術難題,為類似產品開發新的凍干工藝提供了新思路。
符 號 說 明
a,b,c ——分別為晶軸長度
Einteration——相互作用能
Esorbital——山梨醇分子間的能量
Esurface——晶面能
Etotal——奧拉西坦和山梨醇的總能量
EvanderWaals——基于范德華力的相互作用能
Z ——晶胞分子數
α, β, γ ——晶軸角
[1]Belfiore P, Ponzio F, Biagetti R, Berettera C, Magnani M, Pozzi O.Oxiracetam prevents the hippocampal cholinergic hypofunction induced by the NMDA receptor blocker AP7 [J].Neuroscience Letters, 1992, 143 (1): 127-130.
[2]Spignoli G, Pepeu G.Oxiracetam prevents electroshock- induced decrease in brain acetylcholine and amnesia [J].European Journal of Pharmacology, 1986, 126 (3): 253- 257.
[3]Saletu B, Linzmayer L, Grünberger J, Pietschmann H.Double-blind, placebo-controlled, clinical, psychometric and neurophysiological investigations with oxiracetam in the organic brain syndrome of late life [J].Neuropsychobiology, 1985, 13 (1/2): 44-52.
[4]Ye Lei.(S)-4-hydroxy-2-oxo-1-pyrrolidineacetamide racemate crystal form ii and preparation method therefor [P]: US, 14/237894.2012-4-24.
[5]Iriuchijima S, Kobayashi H, Aoki K, et al.Process for producing oxiracetam [P]: U.S, 4686296.1987-8-11.
[6]Wang Z Z, Chen J M, Lu T B.Enhancing the hygroscopic stability of S-oxiracetam via pharmaceutical cocrystals [J].Crystal Growth & Design, 2012, 12(9): 4562-4566.
[7]Mellor J D.Fundamentals of Freeze-Drying [M].London: Academic Press Inc.Ltd., 1978.
[8]Pikal M J.Freeze-drying of proteins.Process, formulation, and stability [J].ChemInform, 1995, 26(4).DOI: 10.1002/chin.199504315.
[9]Liapis A I, Pim M L, Bruttini R.Research and development needs and opportunities in freeze drying [J].Drying Technology, 1996, 14 (6): 1265-1300.
[10]Yu Jianping, Liu J H, Pu L Q, Cui Xiangdong, Wang Changzheng, Ouyang S L, Gao Dayong.Freeze-drying of human red blood cells: influence of carbohydrates and their concentrations [J].Cell Preservation Technology, 2004, 2 (4): 270-275.
[11]Zhou Xinli (周新麗), Liu Jianfeng (劉建峰), Zhang Shaozhi (張紹志), Chen Guangming (陳光明).Thermal analysis on lyoprotectants for biomaterials [J]Journal of Refrigeration (制冷學報), 2008, 29 (5): 54-57.
[12]Wang Jingkang (王靜康).Crystallization (結晶)//Shi Jun (時鈞), Wang Jiading (汪家鼎), Yu Kuo Tsung (余國琮), Chen Minheng (陳敏恒).Handbook of Chemical Engineering (化學工程手冊) [M].Beijing: Chemical Industry Press.1996.
[13]Dubochet J, Chang J J, Freeman R, Lepault J, McDowall A W.Frozen aqueous suspensions [J].Ultramicroscopy, 1982, 10 (1): 55-61.
[14]Liu H, Lelièvre J.Transitions in frozen gelatinized-starch systems studied by differential scanning calorimetry [J].Carbohydrate Polymers, 1992, 19 (3): 179-183.
[15]Varshney D B, Kumar S, Shalaev E Y, Kang S W, Gatlin L A, Suryanarayanan R.Solute crystallization in frozen systems—use of synchrotron radiation to improve sensitivity [J].Pharmaceutical Research, 2006, 23 (10): 2368-2374.
[16]Zhu Liang(朱亮).Effects of pre-freeze in the freeze drying process [J].Drying Technology & Equipment (干燥技術與設備), 2014, 12 (1): 32-34.
[17]López-Urue?a E, Alvarez M, Gomes-Alves S, et al.Tolerance of brown bear spermatozoa to conditions of pre-freezing cooling rate and equilibration time [J].Theriogenology, 2014, 81 (9): 1229-1238.
[18]Gao Zhifeng(高志峰).A freeze-dried powder and preparation method of oxiracetam [P]: CN, 102274195 A.2011-07-18.
[19]Yani Y, Chow P S, Tan R B H.Molecular simulation study of the effect of various additives on salbutamol sulfate crystal habi [J].Molecular pharmaceutics, 2011, 8 (5): 1910-1918.
[20]Schmidt C, Ulrich J.Morphology prediction of crystals grown in the presence of impurities and solvents—an evaluation of the state of the art [J].Journal of Crystal Growth, 2012, 353 (1): 168-173.
[21]Gupta P, Thilagavathi R, Chakraborti A K, Bansal A K.Role of molecular interaction in stability of celecoxib-PVP amorphous systems [J].Molecular Pharmaceutics, 2005, 2 (5): 384-391.

