胞漿-5'-核苷酸酶-Ⅱ在非小細胞肺癌組織中的表達及其臨床意義*
曲莉莉 劉曉晴 王偉霞 湯傳昊 李儉杰 李曉燕 高紅軍李曉兵 劉廣賢
·臨床研究與應用·
胞漿-5'-核苷酸酶-Ⅱ在非小細胞肺癌組織中的表達及其臨床意義*
曲莉莉①劉曉晴①王偉霞①湯傳昊①李儉杰①李曉燕①高紅軍①李曉兵②劉廣賢③
目的:胞漿-5'-核苷酸酶-Ⅱ(CN-Ⅱ)是一種核苷酸酶,具有水解酶及磷酸轉移酶的活性,其異常表達可能與多種核苷類藥物耐藥有一定相關性。本研究旨在探討CN-Ⅱ在非小細胞肺癌(non-small cell lung cancer,NSCLC)組織中的表達及其與臨床病理因素的關系。方法:應用免疫組織化學方法檢測116例NSCLC原發及轉移病灶中CN-Ⅱ的表達并分析其中67例曾接受過吉西他濱方案化療的患者其CN-Ⅱ表達與吉西他濱近期療效及生存的相關性,采用χ2檢驗及Fisher精確檢驗分析其表達水平與臨床病理因素的相關性,采用Kaplan-Meier方法分析TTP及OS(overall survival,OS),采用對數秩和檢驗比較不同CN-Ⅱ表達情況之間的差異。結果:116例NSCLC標本中CN-Ⅱ陽性表達率為53.4%,其表達水平與患者的年齡、性別、KPS評分、臨床分期、腫瘤病理類型及分化程度等均無顯著相關性。NSCLC原發病灶與淋巴結等轉移病灶中CN-Ⅱ的表達水平亦無顯著性差異。對67例接受含吉西他濱方案化療NSCLC患者腫瘤組織標本的檢測發現,吉西他濱化療有效組(CR+PR)、疾病控制組(CR+PR+SD)及無效組(PD)的CN-Ⅱ陽性表達率分別為30.4%、36.7%及57.6%,前兩者與后者相比均有顯著性差異(CR+PR vs.PD組,P=0.008;CR+PR+SD vs.PD組,P=0.013);28例CN-Ⅱ陽性及39例陰性患者中位腫瘤進展時間(progeression free survival,PFS)分別為4.0個月及5.5個月,有顯著性差異(95%CI:4.452-6.148,P=0.041),兩組患者中位OS分別為9.5個月及11.0個月,無顯著性差異(95% CI:8.667-13.333,P=0.282)。結論:CN-Ⅱ異常表達與吉西他濱治療療效有一定相關性,有可能成為潛在的療效預測因子。
5'-核苷酸酶吉西他濱耐藥性非小細胞肺癌
Correspondence to:Xiaoqing LIU;E-mail:liuxq@medmail.com.cn
1Department of Lung Cancer,2Department of Pathology,3Department of Hematology,the Affiliated Hospital of the Academy of Military Medical Science,Beijing 100071,China
This work was supported by grants from the Capital Medical Development Foundation(No.2007-3042)
吉西他濱(gemcitabine,Gem)是晚期非小細胞肺癌(non-small cell lung cancer,NSCLC)的一線化療藥物,與其他化療藥物一樣,原發與繼發性耐藥使得其臨床療效受阻。近年來以Gem耐藥相關基因指導NSCLC個體化治療的研究多見報道,其中核糖核苷酸還原酶亞基1(ribonucleotide reductase subunit 1,RRM1)是目前研究較為廣泛的分子指標,但RRM1并不能完全解釋Gem的耐藥,僅采用此一項指標來預測Gem療效有一定局限性,因此研究與探索新的分子預測指標具有重要臨床意義。研究發現胞漿-5'-核苷酸酶-Ⅱ(cyto-solic 5'-nucleotidaseⅡ,CN-Ⅱ)可能與Gem耐藥有一定相關性[1],其異常表達可能影響藥物在腫瘤細胞內的代謝過程,從而影響Gem化療療效[2]。
本研究篩選出67例曾接受過含Gem方案化療患者的腫瘤組織標本,初步觀察其CN-Ⅱ蛋白表達情況與Gem近期療效及患者生存之間的關系,為臨床個體化治療提供理論依據。
1 材料與方法
1.1一般資料
收集2000年3月至2007年9月于軍事醫學科學院附屬醫院就診的116例NSCLC患者腫瘤組織標本,檢測其CN-Ⅱ蛋白表達情況。患者年齡21~76歲,中位年齡54歲。臨床分期采用1997年國際抗癌聯盟(UICC)TNM分期標準,Ⅰ期0例,Ⅱ期1例,ⅢA期8例,IIIB期39例,Ⅳ期68例。116例標本中手術切除的組織標本8例,纖維支氣管鏡活檢或經皮肺穿刺活檢標本49例,轉移淋巴結穿刺活檢標本56例,其他轉移部位穿刺活檢標本3例。由醫院兩位高年資病理醫師根據WHO(2004年)新分類標準結合免疫組織化學結果進行病理診斷。本研究經醫院倫理委員會批準,患者及家屬知情同意并簽署協議書。
篩選67例曾接受含Gem方案化療的NSCLC患者腫瘤組織標本,回顧性分析其CN-Ⅱ表達情況與Gem近期療效及患者生存的關系。化療療效的評定采用RECIST1.0實體瘤近期療效評價標準(2003年前采用WHO標準)。從治療第1天計算至影像學或臨床進展日期。總生存(overall survival,OS)從NSCLC確診計算至死亡日期。67例患者的隨訪截止日期為2010年2月1日,中位隨訪時間3年。
1.2方法
1.2.1實驗方法標本均10%甲醛固定,常規脫水,石蠟包埋,4 μm厚切片。采用免疫組織化學SP二步法檢測116例標本中CN-Ⅱ蛋白表達情況。兔抗人CN-Ⅱ多克隆抗體購自北京博奧森公司。操作嚴格按產品說明書進行。以人正常胰腺組織陽性片作為
陽性對照,用PBS代替一抗作為空白對照。
1.2.2結果判定CN-Ⅱ蛋白表達以胞漿內出現彌漫的棕黃或棕褐色顆粒為陽性。結合染色強度和陽性細胞數進行分級。兩人雙盲法分別觀察切片,隨機選取10個高倍視野(×400),評分后取平均值。按染色強度評分標準:不著色0分,淡黃色1分,深黃色或褐色2分,深褐色3分。按陽性細胞比例評分標準:<10%為0分,10%~25%為1分,26%~50%為2分,>50%為3分。二分法以乘積等于3為界,乘積≤3記為低表達(陰性),乘積>3記為高表達(陽性)。1.3統計學分析
應用SPSS 17.0統計學分析軟件,采用配對χ2檢驗和Fisher精確檢驗分析不同臨床病理特征的患者其CN-Ⅱ表達有無差異性。采用Kaplan-Meier方法估計TTP及OS,采用對數秩和檢驗(Long rank test)比較不同CN-Ⅱ表達情況之間的差異。以P<0.05為差異具有統計學意義。
2 結果
2.1CN-Ⅱ在NSCLC組織中的表達
免疫組織化學方法顯示CN-Ⅱ在NSCLC組織中主要定位于腫瘤細胞胞漿,呈棕黃或棕褐色,部分細胞可見胞核與胞漿同時著色(圖1)。在NSCLC組織中CN-Ⅱ的陽性表達率為53.4%(62/116)。
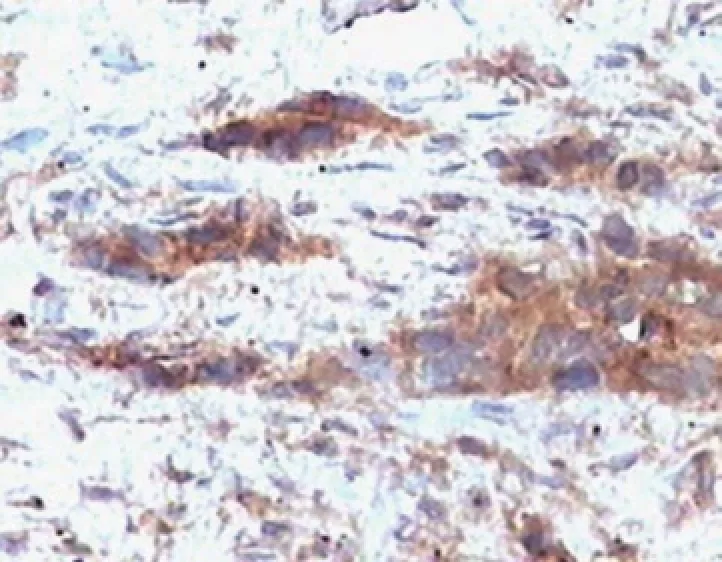
圖1 CN-Ⅱ在NSCLC細胞中的表達(IHC×400)Figure 1 Expression of CN-II in non-small cell lung cancer(NSCLC)tissues(IHC×400)
2.2CN-Ⅱ表達與臨床病理特征的關系
表達CN-Ⅱ蛋白的NSCLC患者的年齡、性別、ECOG評分、臨床分期、腫瘤組織學分型均無顯著相關性(表1)。NSCLC原發病灶組織57例,其CN-Ⅱ陽性表達率49.1%,轉移病灶組織共59例,原發灶與轉移灶中CN-Ⅱ的表達無顯著性差異(表2)。
2.3CN-Ⅱ表達水平對吉西他濱近期療效及患者生存期的影響
67例患者曾接受含Gem方案化療,其CN-Ⅱ陽性表達率為41.7%(28/67),CN-Ⅱ表達水平與患者的年齡、性別、腫瘤分期及病理類型無顯著相關性(表3)。67例患者中26例接受了吉西他濱聯合順鉑方案(吉西他濱1.0 g/m2d1,d8、順鉑75 mg/m2),40例為吉西他濱聯合卡鉑方案(吉西他濱1.0 g/m2d1,d8、卡鉑AUC=5 d1),1例為吉西他濱聯合多西紫杉醇方案(吉西他濱1.0 g/m2d1,d8、多西紫杉醇75 mg/m2d1)。

表1 CN-Ⅱ表達與116例NSCLC患者臨床病理特征之間的關系Table 1 Relationship between CN-Ⅱ expression and clinicopathological characteristics in 116 NSCLC patients

表2 NSCLC原發病灶與轉移灶中CN-Ⅱ表達水平比較Table 2 Correlation analysis of CN-Ⅱexpression and gemcitabine efficacy in primary and metastatic lesions
54例為一線治療,治療周期1~6周期,客觀有效率(CR+PR)為38.9%(21/54),疾病控制率(CR+PR+ SD)為77.8%(42/54),疾病控制患者的中位無進展生存期(progression free survival,PFS)為6.0個月。13例為二線治療,治療周期1~4周期,其客觀有效率15.4%(2/13),疾病控制率53.9%(7/13),疾病控制患者的中位PFS為3.5個月。所有患者總的客觀有效率34.3%(23/67),疾病控制率73.1%(49/67)。Gem治療有效(CR+PR)及疾病控制(CR+PR+SD)與疾病進展(PD)的患者相比其CN-Ⅱ表達有顯著性差異(P= 0.027,P=0.031,表4)。

表3 CN-Ⅱ表達與67例接受Gem治療的NSCLC患者臨床病理特征的關系Table 3 Relationship between CN-Ⅱexpression and clinicopathological characteristics in 67 NSCLC patients treated with gemcitabine

表4 CN-Ⅱ表達與吉西他濱近期療效的相關性分析Table 4 Relationship between CN-Ⅱexpression and gemcitabine efficacy
67例患者中有28例CN-Ⅱ陽性(41.8%),39例CN-Ⅱ陰性(58.2%),兩組患者中位PFS分別為4.0個月及5.5個月,二者相比有顯著性差異(95%CI:4.452-6.148,P=0.041,圖2A)。49例隨訪到生存期,中位隨訪時間3年,18例患者失訪(記為刪失數據)。所有患者OS 4.5~25.0個月,中位OS 11.0個月。CN-Ⅱ陽性及陰性組患者中位OS分別為9.5個月及11.0個月,CN-II陰性組優于陽性組,但二者相比未發現有顯著性差異(95%CI:8.667-13.333,P=0.282,圖2B)。
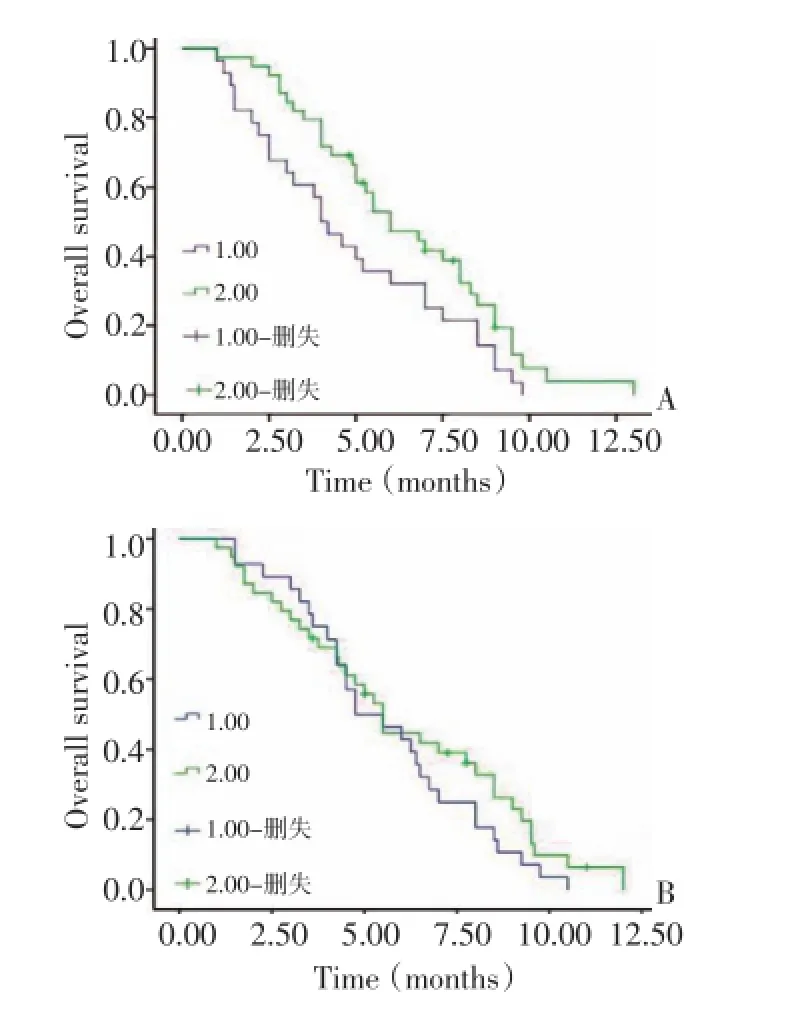
圖2 67例不同CN-Ⅱ表達狀態的NSCLC患者接受吉西他濱治療Figure 2 Kaplan-Meier survival curve of CN-Ⅱ expression in 67 NSCLC patients who received gemcitabine chemotherapy.
3 討論
目前,驅動基因指導下的分子靶向治療在NSCLC中取得較好的療效,且根據EGFR及ALK基因突變狀態制定一線治療方案,已為NCCN指南所推薦,這使得肺癌的治療已走上基因為導向的個體化治療之路[3-4]。然而作為NSCLC標準治療之一的化療,始終未能突破瓶頸,可否實現分子標志物指導下的個體化化療,目前還無肯定的答案,2013年ASCO年會報道兩項有關化療生物標志物前瞻性研究均宣告失敗[5-6],這使得探索之路更加艱難。
Gem是目前NSCLC常用的一線化療藥物,其在治療初診或既往化療失敗患者的總有效率僅20%~40%[7-8]。Gem具水溶性,需特殊的核苷轉運蛋白將其轉運至腫瘤細胞內,之后其經過兩步磷酸化反應被轉化為具有活性的Gem磷酸鹽,干擾DNA合成及修復,誘導腫瘤細胞凋亡[9-10]。Gem的耐藥機制較為復雜,目前研究認為主要與攝取轉運過程障礙和胞漿內活化及分解酶異常有關[10]。
CN-Ⅱ系鹵酸脫鹵酶(haloacid dehalogenase,HAD)超家族成員之一,分子量65 kDa,其分布廣泛,具有水解酶及磷酸轉移酶的活性[11],呈底物專一性,是細胞內重要的代謝調解酶[12-13]。CN-Ⅱ由APT激活變構調節以及可被無機磷酸鹽抑制[13]。在5'-核苷酸酶家族中,CN-Ⅱ與核苷類藥物耐藥的關系最為密切[14]。研究表明純化的CN-Ⅱ酶可將多種核苷類似物作為其催化底物,水解其磷酸活化產物,使得藥物不能繼續磷酸化活化,從而降低其抗腫瘤活性[15],而且其可將IMP或GMP的磷酸基團轉移到外源性的核苷類似物,使得其活化受阻[13]。體外細胞實驗發現,Gem耐藥腫瘤細胞中CN-ⅡmRNA表達水平明顯高于其親代細胞[16],且已有多個研究顯示,抑制CN-II活性可直接導致腫瘤細胞凋亡,且可增加細胞毒藥物的抗腫瘤活性[17-18],目前已有專門以CN-Ⅱ作為靶點的抗腫瘤藥物β羥基磷酸酯核苷類似物(β-hydroxyphosphonate nucleoside analogues)在研發中,體外實驗已初步顯示出較好的抗腫瘤活性[19]。
臨床研究中無論檢測CN-ⅡmRNA,還是蛋白表達水平,因受臨床標本量以及檢測方法簡便、可操作性強等因素影響,采用免疫組織化學方法檢測CN-Ⅱ蛋白水平的表達更具可行性,但此方法缺點是檢測結果僅為半定量,可信度較差。目前檢索到的CN-Ⅱ在NSCLC組織中的表達研究即采用了免疫組織化學的方法,Pascal等[20]檢測了43例接受含吉西他濱方案化療的NSCLC患者腫瘤組織中CN-Ⅱ的表達水平,其以40%為界將組織標本分為陽性組與陰性組,結果顯示CN-Ⅱ高表達率72.1%,表達水平低的患者生存期較短(180天vs.330天,P=0.047),預后較差,而研究并未顯示兩組患者之間含吉西他濱方案化療客觀有效率以及PFS有顯著性差異。文獻中未明確其判定CN-Ⅱ表達水平高低的依據,由于其判定CN-Ⅱ陽性時未考慮細胞定位及染色深淺問題,腫瘤細胞的胞漿和(或)胞核著色均將其判定為陽性表達。本研究顯示CN-Ⅱ在NSCLC組織中的陽性表達率為53.4%,低于文獻報道的72.1%,這可能與本研究選用的陽性判定標準較為嚴格有關,腫瘤細胞胞漿著色或胞漿與胞核同時著色計為陽性,僅胞核著色計為陰性,同時亦綜合考慮了細胞染色的深淺來判定結果。本研究認為免疫組織化學檢測方法的標準化以及判定標準的統一化將可能是研究的關鍵點,這將增加不同研究結果之間的可比性,以進一步推動CN-Ⅱ的臨床研究。
有關CN-Ⅱ在NSCLC腫瘤組織中表達情況的研究可檢索到的文獻較少,本研究結果顯示CN-Ⅱ表達與NSCLC患者的年齡、性別、ECOG評分、腫瘤臨床分期均無相關性,腺癌與鱗癌患者其表達亦無顯著性差異,此結果與文獻報道相一致[20]。通過比較含Gem方案化療不同療效患者其腫瘤組織中CN-Ⅱ表達情況發現,治療無效的患者其CN-Ⅱ陽性率顯著高于治療有效及疾病控制的患者,且CN-Ⅱ陰性組患者PFS較陽性組患者長,由此推測CN-Ⅱ陽性表達的患者接受含Gem方案化療可能療效欠佳。另通過生存分析顯示,CN-Ⅱ陰性表達的患者OS相對較長,但與陽性組患者相比未發現有顯著性差異。這與Pascal等[20]文獻報道的結果有一定差異,文獻中并未發現CN-Ⅱ與吉西他濱治療療效有相關性,相反,CN-Ⅱ可作為預測接受吉西他濱治療患者預后的獨立預測因子,CN-Ⅱ高表達的患者OS要優于低表達者。本研究中兩組均受回顧性資料限制,雖文獻中接受含吉西他濱方案化療的患者均為一線治療,但治療方案較雜,這在一定程度上可能影響了實驗結果;且兩組研究所納入的病例數均有限,如能在此基礎上更進一步擴大樣本量也許能提高結果的可信度;此外,患者OS影響因素較多,尤其是患者在接受吉西他濱治療后的多線治療,方案及療程、療效均有較大的差異,如能在前瞻性研究的基礎上進行多因素分析將更有利于明確CN-Ⅱ的臨床意義。
目前研究顯示CN-Ⅱ可能與含吉西他濱方案化療療效有一定相關性,但研究多局限于小樣本的回顧性研究,亟待臨床前瞻性的大規模研究來驗證,且CN-Ⅱ聯合多個分子指標建立起療效預測模型可能更具意義。目前分子標志物指導下的個體化化療尚未真正應用于臨床,是否其可以如分子靶向治療一樣獲得較好的療效,仍需高級別的循證醫學證據。
1 Hunsucker SA,Mitchell BS,Spychala J.The 5'-nucleotidases as regulators of nucleotide and drug metabolism[J].Pharmacol Ther,2005,107(1):1-30.
2 Jordheim LP,Cros E,Galmarini CM,et al.F-ara-AMP is a substrate of cytoplasmic 5'-nucleotidase II(CN-II):HPLC and NMR studies of enzymatic dephosphorylation[J].Nucleosides Nucleotides Nucleic Acids,2006,25(3):289-297.
3 Minuti G,Dincecco A,Cappuzzo F.Target therapy for NSCLC with driver mutations[J].Expert Opiin Biol Ther,2013,13(10):1401-1412. 4National Comprehensive Cancer Network.NCCN clinical practice guidelines in oncology[J].Non-small cell lung caner version2,2013. 5Bepler G,Williams CC,Schell ML,et al.Molecular analysis directed,international,phaseⅢtrial in patients with advanced non-small cell lung cancer[J].J Clin Oncol,2013,31(15s):abstr 8001.
6 Moran T,Cobo M,Domine M,et al.Interim analysis of the Spanish Lung Cancer Group(SLCG)BRCA1-RAP80 Expression Customization(BREC)randomized phase III trial of customized therapy in advanced non-small-cell lung cancer(NSCLC)patients(p)(NCT00617656/GECP-BREC)[J].J Clin Oncol,2013,31(18s):abstr LBA8002.
7 Manegold C,Von Pawel J,Zatiouka P,et al.B017704(AVAIL):A phaseⅢ randomised study of first-line bevacizumab combined with cisplatin/gemcitabine(CG)in patients(TS)with advanced or recurrent non-squamous,non-small cell lung cancer(NSCLC)[J]. Ann Oncol,2008,19:viii 1.
8 Li Y,Wang LR,Chen J,et al.First-line gemcitabine plus cisplatin in nonsmall cell lung cancer patients[J].Dis Markers,2014,2014:960458. 9Mini E,Nobili S,Caciagli B,et al.Cellular pharmacology of gemcitabine[J].Ann Oncol,2006,17(5):7-12.
10 Wonganan P1,Lansakara-P DS,Zhu S,et al.Just getting into cells is not enough:mechanisms underlying 4-(N)-stearoyl gemcitabine solid lipid nanoparticle's ability to overcome gemcitabine resistance caused by RRM1 overexpression[J].J Control Release,2013,169(1-2):17-27.
11 Kroep JR,Loves WJ,van der Wilt CL,et al.Pretreatment deoxycytidinekinaselevelspredictinvivo gemcitabine sensitivity[J]. Mol Cancer Ther,2002,1(6):371-376.
12 Oqawa M,Hori H,Ohta T,et al.Sensitivity to gemcitabine and its metabolizing enzymes in neuroblastoma[J].Clin Cancer Res,2005,11(9):3485-3493.
13 Itoh R.Enzymatic properties and physiological roles fo cytosolic 5'-nucleotidase II[J].Curr Med Chem,2013,20(34):4260-4284.
14 Allegrini S,Scaloni A,Careddu MG,et al.Mechanistic studies on bovine cytosolic 5'-nucleotidase II,an enzyme belonging to the HAD superfamily[J].Eur J Biochem,2004,271:4881-4891.
15 Wu Jz,Larson J,Walker H,et al.Phosphorylation of ribavirin and viramidine by adenosine kinase and cytosolic 5'-nucleotidase II:Implications for ribavirin metabolism in erythrocytes[J].Antimicrob Agents Chemother,2005,49(6):2164-2171.
16 Dumontet C,Bauchu EC,Fabianowska K,et al.Common resistance mechanisms to nucleoside analogues in variants of the human erythroleukemic line K562[J].Adv Exp Me Biol,1999,457:571-577.
17 Jordheim LP,Chaloin L.Therapeutic perspectives for CN-II in cancer[J].Curr Med Chem,2013,20(34):4292-4303.
18 Gallier F,Lallemand P,Meurillon M,et al.Structural insights into the inhibition of cytosolic 5'-nucleotidase II(CN-II)by ribonucleoside 5'-monophosphate analogues[J].PloS Comput Biol,2011,7(12):e1002295.
19 Meurillon M,Marton Z,Hospital A,et al.Structure-activity relationships of β-hydroxyphosphonate nucleoside analogues as cytosolic 5'-nucleotidase II potential inhibitors:synthesis,in vitro evaluation and molecular modeling studies[J].Eur J Med Chem,2014,77:18-37. 20 Pascal S,John RM,Sylvie I,et al.CN-Ⅱexpression predicts survival in patients receiving gemcitabine for advanced non-small cell lung cancer[J].Lung Cancer,2005,49(3):363-370.
(2014-10-07收稿)
(2014-11-10修回)
(編輯:楊紅欣)

曲莉莉專業方向為肺癌的基礎及臨床研究。E-mail:qulili1130@126.com
Expression and clinical significance of CN-Ⅱ in non-small cell lung cancer tissues
Lili QU1,Xiaoqing LIU1,Weixia WANG1,Chuanhao TANG1,Jianjie LI1,Xiaoyan LI1,Hongjun GAO1,Xiaobing LI2,Guangxian LIU3
Objective:Cytosolic 5'-nucleotidase(CN-Ⅱ),a nucleotide kinase,exhibits both 5'-nucleotidase and nucleoside phosphotransferase activities.Abnormal CN-Ⅱexpression may be correlated with the resistance of nucleoside analogs in anticancer drugs. This study was designed to investigate CN-Ⅱexpression in human non-small cell lung cancer(NSCLC)tissues and its correlation with the clinicopathological parameters as well as the prognosis of patients treated with gemcitabine.Methods:Immunohistochemistry was used to detect CN-Ⅱexpression in 116 cases of paraffin-embedded NSCLC samples.The correlations with the clinicopathological parameters and the response to gemcitabine chemotherapy of CN-Ⅱwere analyzed through the Chi-square test.Log-rank test was used to determine whether or not CN-Ⅱexpression is correlated with the overall survival of patients.Results:The positive rate of CN-Ⅱwas 53.4%in 116 NSCLC tissues.No significant correlation existed between CN-Ⅱexpression and the clinicopathological parameters. Among the 67 of the 116 patients who received gemcitabine chemotherapy,those with tumor progression(positive rate of 57.6%)exhibited higher CN-Ⅱexpression than those with therapeutic efficacy(positive rate of 30.4%,P=0.008)and disease-control chemotherapy (positive rate of 36.7%,P=0.013).The progression-free survival was 4.5 and 5.5 months in the CN-Ⅱ-positive and CN-II-negative groups,respectively,with significant differences(95%CI:4.452 to 6.148,P=0.041).Correspondingly,the overall survival was 9.5 and 11.0 months in the two groups(95%CI:8.667 to 13.333,P=0.282).Conclusion:CN-Ⅱmay be a prognostic factor for gemcitabine chemotherapy in NSCLC patients.
cytosolic 5'-nucleotidase,gemcitabine,resistance,non-small cell lung cancer
10.3969/j.issn.1000-8179.20141672
①軍事醫學科學院附屬醫院肺部腫瘤內科(北京市100071);②病理科;③血液內科*本文課題受首都醫學發展科研基金(編號:2007-3042)資助
劉曉晴liuxq@medmail.com.cn

