肝動脈變異在肝門淋巴結廓清中的臨床意義
霍 明 生魯 正 崔培元 吳斌全 吳 華 吳 維 許文青
·臨床研究與應用·
肝動脈變異在肝門淋巴結廓清中的臨床意義
霍明生魯正崔培元吳斌全吳華吳維許文青
目的:探討肝動脈變異在肝門淋巴結廓清中的識別與預防損傷策略。方法:回顧性分析2013年1月至2014年7月蚌埠醫學院第一附屬醫院肝膽外科62例肝門淋巴結廓清中12例肝動脈變異患者術中處理情況。結果:12例肝動脈變異類型分為:MichelsⅢ型3例(25.0%),MichelsⅥ型2例(16.7%),MichelsⅨ型1例(8.3%),Hiatt 6型1例(8.3%),肝右動脈與肝總管空間位置變異2例(16.7%),肝左右動脈共同起源于肝總動脈2例(16.7%),以及肝右動脈起自胃十二指腸動脈1例(8.3%)。12例患者無肝動脈損傷;2例發生術后并發癥,其中1例胰漏,另1例切口感染;無術后出血、膽漏及肝膿腫等并發癥發生。整體恢復良好。結論:在熟知各種肝動脈解剖變異類型的前提下,術前完善的影像學檢查與評估,加以術中謹慎且精細的操作,將使肝動脈損傷明顯減少。
肝動脈變異肝門淋巴結廓清腸系膜上動脈肝動脈損傷
肝膽外科的惡性腫瘤如膽囊癌、肝門膽管癌、壺腹周圍癌及胰頭癌的根治性切除都需要廓清肝門部的淋巴脂肪組織。淋巴結狀態是以上腫瘤患者一個重要的預后因素,影響患者生存率。肝動脈和門靜脈走行于肝門部脂肪淋巴組織中,相對于門靜脈,肝外肝動脈變異出現概率高且類型多。正常型肝動脈在手術中容易確認,便于保護和處理。肝動脈變異的存在增加了其損傷的危險性[1],若腫瘤尤其是膽管癌常浸潤動脈周圍神經叢,廓清更為困難。任何供應肝實質的動脈血管意外損傷可能會導致肝臟缺血和膽道并發癥[2]。對肝動脈的變異認識不足,而導致術中處理不當,是造成術后并發癥的重要原因[3],研究肝動脈變異在肝門淋巴結廓清中具有重要臨床意義。
1 材料與方法
1.1臨床資料
回顧性分析2013年1月至2014年7月蚌埠醫學院第一附屬醫院肝膽外科62例肝門淋巴結廓清中12例存在肝動脈變異患者的臨床資料(表1)。
所有患者術前常規行胸片、心電圖、腹部超聲、腫瘤標記物、肝功能、上腹部CT平掃+增強、CT血管成像(CTA)及核磁共振胰膽管造影(MRCP)等檢查;肝門膽管癌患者在高質量亞毫米CT數據基礎上應用腹部醫學圖像三維可視化系統(MI-3DVS)行三維重建,部分梗阻性黃疸的患者需行經皮經肝膽管引流(PTBD)。
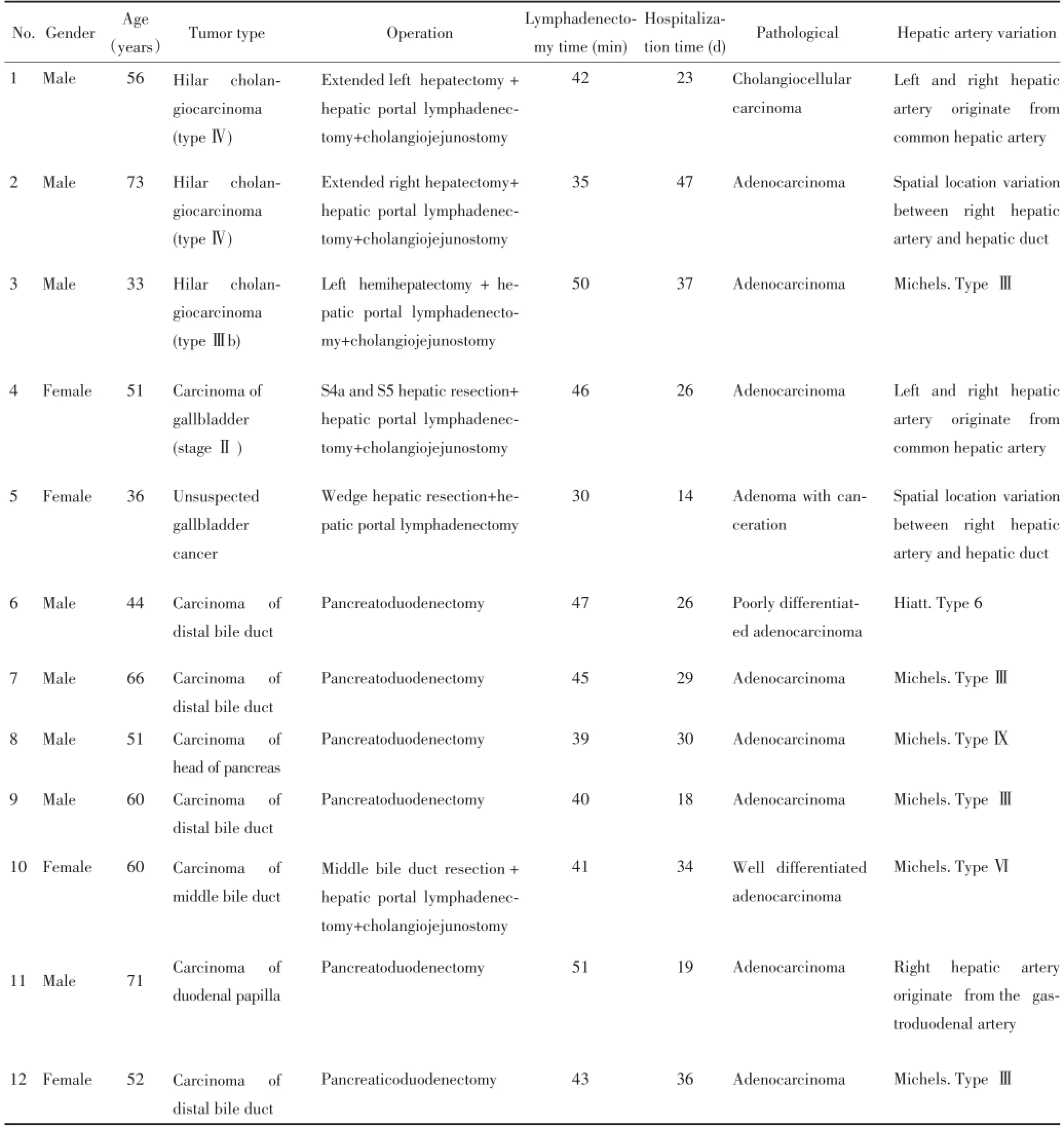
表1 肝門淋巴結廓清患者的臨床資料Table1 Clinical data of patients with hepatic portal lymphadenectomy
1.2手術方法
患者術前一天均接受腸道準備,術前置胃管并常規使用預防性抗生素;淋巴結廓清和病灶一并切除、堅持整塊切除的原則。胰十二指腸切除中肝門淋巴結廓清步驟:1)切開肝門板表面漿膜并延續到膽囊漿膜,解剖膽囊三角,分離出膽囊動脈、膽囊管,切斷、結扎膽囊動脈,于根部預扎膽囊管,將膽囊從肝床游離,暫不切除;2)打開膽總管前面的漿膜顯露肝總管然后橫斷,從肝臟側向十二指腸上緣解剖肝左、右動脈及匯合的肝固有動脈,可分別將其懸吊后輕輕牽開使分離面有適當的張力,緊貼血管外膜廓清周圍組織;3)分離顯露胃十二指腸動脈和肝總動脈,檢查各分支無誤后,切斷胃十二指腸動脈;4)最后全程顯露肝十二指腸韌帶內的門靜脈,懸吊后廓清門靜脈周圍組織。肝門膽管癌及膽囊癌中肝門淋巴結廓清步驟:1)打開膽總管前面的漿膜顯露膽總管,懸吊后于胰腺上緣切斷、遠端斷面予以縫合(膽囊癌無此步驟);2)解剖、顯露胃十二指腸動脈,向上解剖肝固有動脈及肝左右動脈,從十二指腸上緣向肝臟側廓清肝門淋巴脂肪組織,可分別將其懸吊后輕輕牽開使分離面有適當的張力,緊貼血管外膜廓清周圍組織;3)繼續分離顯露門靜脈及左、右主干,一一懸吊。
1.3統計學分析
采用SPSS 19.0軟件將患者年齡、術中廓清時間、平均住院時間及各肝動脈變異類型比率進行分析;計量資料以均數±標準差表示,計數資料以率表示。
2 結果
2.1手術情況及各肝動脈變異類型比率
12例肝動脈變異患者中男性8例,女性4例,男女比例2:1;年齡33~73(54.4±12.1)歲;平均廓清時間(42.4±6.0)min;平均住院天數(28.3±9.3)d。各型肝動脈變異比率:MichelsⅢ型3例(25.0%),MichelsⅥ型2例(16.7%),MichelsⅨ型1例(8.3%),Hiatt 6型(肝總動脈起于腹主動脈)1例(8.3%),肝右動脈與肝總管空間位置的變異2例(16.7%),肝左右動脈共同起源于肝總動脈2例(16.7%),以及肝右動脈起自胃十二指腸動脈1例(8.3%)。
2.2變異肝動脈走行和起源
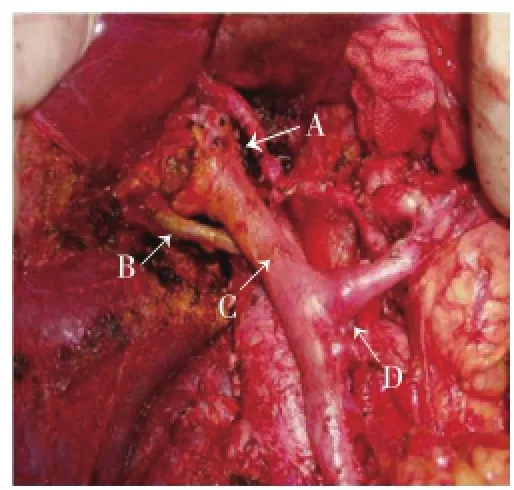
圖1 MichelsⅢ型Figure 1 Michels'TypeⅢ
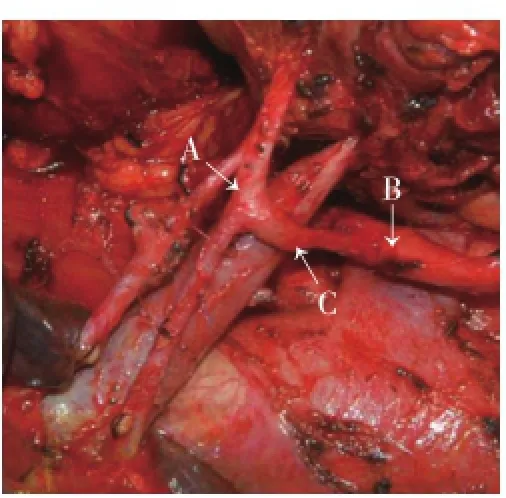
圖2 MichelsⅨ型Figure 2 Michels'Type IX
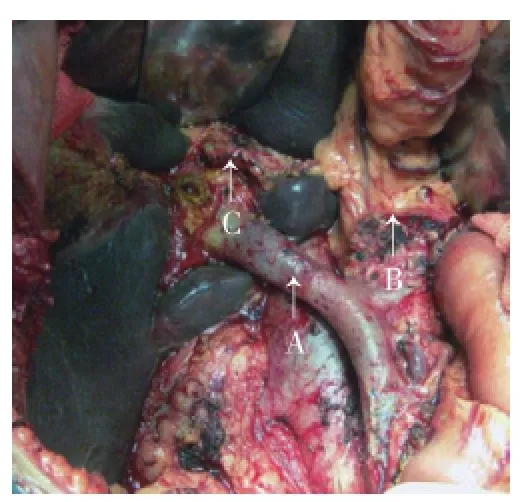
圖3 Hiatt 6型Figure 3 Hiatt's Type 6
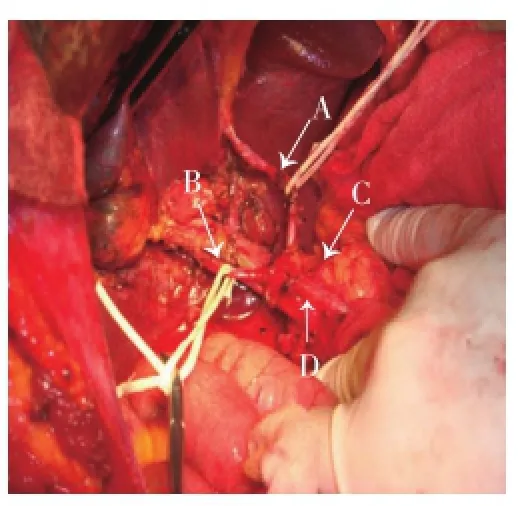
圖4 肝左動脈、肝右動脈共同起源于肝總動脈Figure 4 Left and right hepatic artery that originate from a common hepatic artery
分別描述如下:MichelsⅢ型(替代肝右動脈起自腸系膜上動脈,圖1)術中見替代肝右動脈起自腸系膜上動脈,經過胰頭、門靜脈后方近肝門處于門靜脈的右側入肝。MichelsⅥ型(副肝右動脈起自腸系膜上動脈),術中見肝固有動脈分出肝左動脈、(肝中動脈)及肝右動脈,但肝右動脈直徑明顯小于肝左動脈;門靜脈的右側還有一支起自腸系膜上動脈的副肝右動脈入肝。MichelsⅨ型即Hiatt 5型(肝總動脈起自腸系膜上動脈,圖2),門動脈左側無肝動脈結構,肝總動脈由門靜脈下方的腸系膜上動脈發出。Hiatt 6型(肝總動脈起于腹主動脈,圖3),肝十二指腸韌帶內僅有門靜脈而無動脈結構,肝總動脈于門靜脈左上方直接由腹主動脈發出。肝右動脈與肝總管空間位置的變異,在正常型中,肝固有動脈在肝總管左緣分出肝左、右動脈后,右肝動脈穿過肝總管后方于右肝管右側入肝;而此型變異右肝動脈卻在肝總管前方跨過后入肝。觀察到的Michels分型和Hiatt分型未能概括的兩種肝動脈變異:肝左右動脈共同起源于肝總動脈(圖4),在胃十二指腸動脈匯入肝總動脈處,無肝固有動脈結構,肝總動脈向上直接發出兩個分支,即肝左動脈和肝右動脈。此外,發現肝右動脈起自胃十二指腸動脈,此型系筆者在日本交流訪問期間所見;日本的同行在胃十二指腸動脈根部將胃十二指腸動脈及肝右動脈誤切斷,后及時發現將右肝動脈與肝固有動脈吻合,避免了并發癥的發生。
2.3術后恢復
術后無死亡病例。術后發生并發癥2例(16.7%),1例出現胰漏,另1例出現切口感染,經保守治療后延期出院;期間無術后出血、膽漏、肝膿腫、胸水、腹水及肺部感染等并發癥發生。
2.4隨訪情況
經術后病理檢查12例均為腫瘤患者,采用門診隨訪,術后隨訪時間6~14個月,有1例患者因腫瘤復發和轉移并發多器官功能衰竭死亡,1例患者出現肺轉移,轉腫瘤內科繼續治療;余均生存良好、無復發,無不明原因的高熱、寒顫,復查肝功能、腫瘤標記物及腹部超聲等均正常,未發現肝臟、膽道缺血所致肝膿腫等并發癥。
3 討論
變異肝動脈分為替代肝動脈和副肝動脈兩類,前者指替代正常同名肝動脈供血的變異肝動脈,后者是指正常肝動脈以外的一支參與正常動脈供血區域中部分供血的動脈。Michels[4]于1966年通過200例尸體解剖發現,肝動脈變異率45%(90/200);將如上的兩類分成10種類型:Ⅰ型:正常型即肝固有動脈分出肝動脈、(肝中動脈)及肝右動脈;Ⅱ型:替代肝左動脈起自胃左動脈;Ⅲ型:替代肝右動脈起自腸系膜上動脈;Ⅳ型:替代肝左動脈起自胃左動脈+替代肝右動脈起自腸系膜上動脈;Ⅴ型:副肝左動脈起自胃左動脈;Ⅵ型:副肝右動脈起自腸系膜上動脈;Ⅶ型:副肝左動脈起自胃左動脈+副肝右動脈起自腸系膜上動脈;Ⅷ型:替代肝右動脈+副左肝動脈或者替代肝左動脈+副右肝動脈;Ⅸ型:肝總動脈起自腸系膜上動脈;Ⅹ型:肝總動脈起自胃左動脈。1994年Hiatt等[5]分析了1 000例肝移植手術患者的肝動脈,發現肝動脈變異率24.3%(243/1 000);并將Michels分型簡化為6型,與Michels分型相比去掉了MichelsⅩ型,增加了肝總動脈起自腹主動脈型即Hiatt 6型。本研究通過肝門淋巴結廓清中對肝外動脈變異的統計,肝動脈變異發生率19.35%(12/62),發現肝動脈變異發生率高,以來源于腸系膜上動脈和胃左動脈的變異最為常見,肝門淋巴結廓清中尤以來自腸系膜上動脈的變異(MichelsⅢ型、Ⅵ型及Ⅸ型)最常見。此外,所遇變異中有58.3%(7/12)在以上2種經典分型未能概括。羅東等[6]在分析1 810例患者的多層螺旋CT血管造影后,發現17例替代肝右動脈和(或)副右肝動脈起自胃十二指腸動脈。在實踐中也發現有肝右動脈與肝總管空間位置變異、肝左右動脈共同起源于肝總動脈和肝右動脈起自胃十二指腸動脈等變異。可以得出,肝動脈解剖變異同時具有多樣性和復雜性。
肝門淋巴結廓清中,術者不僅需熟知肝動脈常見變異類型,經典分型之外的變異類型也要充分了解。術前仔細復習已完善的影像學資料,其中CTA和三維重建模型更具指導價值。64層螺旋CT掃描極大地提高了時間分辨率和空間分辨率,其肝臟血管圖像可以媲美DSA,且有無創、可多角度觀察的優勢[7]。使用MI-3DVS重建的3D模型能夠真實反映個體化的肝外膽管及供血動脈立體解剖結構[8]。近年,在肝門膽管癌手術之前利用腹部醫學圖像三維可視化系統重建的三維模型可以更加立體地觀察腫瘤與周邊組織的毗鄰,方便了解血管受累程度和范圍、幫助預定半肝切除(擴大半肝切除)預切線、估算殘余肝體積,以此更加準確評估手術切除的可行性;同時三維模型也便于多角度、全方位觀察肝動脈的走行、起源及有無變異,為研究活體肝動脈解剖開辟了新的途徑,如觀察到解剖變異和(或)需合并血管切除,需詳細告知并做好充足的術前準備。
本研究方法是解剖時使用無損傷鉗夾持血管周邊組織,形成與血管之間的張力,打開血管鞘、緊貼血管壁分離,可使用血管吊帶將血管懸吊后輕輕牽開再行骨骼化。若使用電刀游離,可將單極電凝功率調至較小的功率(≤20W)并將電刀頭套上硅膠“保護套”僅留出遠端2~3 mm,這樣可減少對血管的熱源性損傷。在處理束帶樣結構時,注意多觀察并可通過對其的觸摸加以辨認。在未能確認走行或起源之前,切記切斷任何管道樣結構以免損傷變異肝動脈,最好分離至管道根部辨清后再處理之。局部出現滲血、小血管出血,禁忌在血泊中盲目地鉗夾,以免造成更大的血管損傷。原因主要是動脈內膜脆弱、易斷,老年人或動脈硬化者尤甚[9]。應立即指壓出血點,使用沖洗球注水沖洗,洗凈術野后看清出血點再行處理;若是可結扎的小動脈,可采用6-0 Prolene線直接縫扎;若是需保留動脈,可將出血血管兩頭游離一段后使用無損傷組織鉗夾住再行修補。肝門淋巴結廓清后肝門部血管失去了周圍結締組織的保護,局部積液或繼發感染會侵蝕血管壁,而造成術后出血[10]。術后肝門區域常規置管引流,以減少積液對血管的侵蝕,也便于觀察術后出血。亦可置雙套管,一旦發現膽漏、胰漏或感染,可接負壓吸引持續沖洗引流。
對各型變異具體經驗如下:MichelsⅢ型特點是其起始位置較低且深,廓清時可能將其誤認為門靜脈右側腫大的淋巴結或神經束;應先于近肝門板處游離出肝右動脈,再使用血管吊帶將其懸吊由上及下尋其起源。因替代肝右動脈是供應右肝唯一的動脈,誤傷后將會造成右肝及肝內膽道的缺血,甚至肝膿腫的形成。MichelsⅥ型常被誤認為Michels正常型,如發現肝固有動脈的右肝分支直徑小于左肝分支時,應高度警惕、妥善處理門靜脈右側的“淋巴結或神經束帶”。副肝右動脈是正常肝右動脈以外的一支參與右肝動脈供血的動脈。誤傷后,由于右肝動脈的代償作用,可能不會發生右肝及右肝膽道的缺血。MichelsⅨ型變異,仍存在肝固有動脈向上分出肝左動脈、肝右動脈的結構形態,借此先辨認出肝固有動脈,再耐心向下尋找肝總動脈,需將門靜脈向上向左牽起后才能發現其起源系腸系膜上動脈。一旦損傷,由于動脈壓力高以致瞬間出血量大且難以控制;若誤扎,術后將出現肝臟及肝內膽道的缺血和肝膿腫。以上3種變異共同特點是變異肝動脈均發自腸系膜上動脈。來自腸系膜上動脈的迷走肝右動脈多起源于腸系膜上動脈起始部2 cm以內[11]。在胰十二指腸切除術中處理胰腺鉤突部可徹底解剖顯露其起源,切斷鉤突時應特別注意保護腸系膜上動脈和變異肝動脈。Hiatt 6型即肝總動脈起自腹主動脈型,肝總動脈是于門靜脈左上方由腹主動脈直接發出后入肝,其肝外走行長度短且不影響肝門淋巴結廓清,損傷可能小,注意識別即可。肝十二指腸韌帶前方的漿膜應少量提起后再切開,解剖時不宜過快過深,以免傷及跨過肝總管前方走行的右肝動脈。可使用血管吊帶將各管道懸吊辨清肝右動脈與肝總管前后關系來預防損傷。對于肝左動脈、肝右動脈和胃十二指腸動脈共同起源于肝總動脈的變異和肝右動脈起自胃十二指腸動脈的解剖變異。在胰十二指腸切除術中,需將肝總動脈各個分支走向辨清,最好在確定肝右動脈起源后再切斷胃十二指腸動脈,以免將肝右動脈誤認為胃十二指腸動脈切斷。切斷后也將造成右肝及右肝膽道的缺血。
綜上所述,如對肝動脈的變異認識不足,可能導致術中動脈損傷,將造成術后并發癥。術者應熟知各型肝動脈解剖變異,意識到預防的重要性。術前影像學檢查對手術有指導作用,術中肝門淋巴結廓清時使用合理的技術和方法,精細的解剖操作,這樣不僅能有效預防變異肝動脈損傷及各并發癥的出現,還能提高腫瘤根治性。
1 Zhang GW,Zhou J.The experience about preventing hepatic artery injury during hepatic graft repair[J].Chinese Journal of Clinical Anatomy,2012,30(2):237-238.[張國偉,周杰.供肝修整過程中防止肝動脈損傷的解剖方法[J].中國臨床解剖學雜志,2012,30(2):237-238.]
2 López-Andújar R,Moya A,Montalva E,et al.Lessons learned from anatomic variants of the hepatic artery in 1 081 transplanted livers[J].Liver Transplantation,2007,13(10):1401-1404.
3 Yin YF,Nie SX,Tu ZT,et al.The anatomy variations of hepatic artery and its clinical correlation[J].Chinese Journal of Clinical Anatomy,2011,29(2):174-178.[殷永芳,聶詩鑫,涂植濤,等.肝動脈解剖變異及其臨床意義[J].中國臨床解剖學雜志,2011,29(2):174-178.]
4 Michels NA.Newer anatomy of the liver and its variant blood supply and collateral circulation[J].The American Journal of Surgery,1966,112(3):337-347.
5 Hiatt JR,Gabbay J,Busuttil RW.Surgical anatomy of the hepatic arteries in 1000 cases[J].Annals of Surgery,1994,220(1):50-52.
6 Luo D,Zhang YH,Fan ZZ,et al.Study on MSCTA manifestations of anatomical variation of gastroduodenal artery[J].Chinese Journal of CT and MRI,2013,11(4):78-81.[羅東,張應和,范真真,等.胃十二指腸動脈解剖變異的多層螺旋CT血管造影研究[J].中國CT 和MRI雜志,2013,11(4):78-81.]
7 Yuan J,Chen R,Luo XG,et al.Comparative study on anatomic variations of hepatic artery by DSA and CTA[J].Chongqing Medicine,2009,38(23):2973-2974.[袁晶,陳蓉,羅香國,等.肝動脈解剖變異的DSA與CTA對比分析[J].重慶醫學,2009,38(23):2973-2974.]
8 Yang J,Fang CH,Fan YF,et al.Construction of a three-dimensional visualization model of artries supplying the extrahepatic bile duct based onsubmillimeter CT data[J].Journal of Southern Medical University,2014,34(7):945-949.[楊劍,方馳華,范應方,等.基于亞毫米CT掃描數據的肝外膽管供血動脈三維可視化模型構建[J].南方醫科大學學報,2014,34(7):945-949.]
9 Lu Z,Peng CH,Chen QN,et al.The management of vasculature extended radical resection for pancreatic cancer[J].Chinese Journal of General Surgery,2008,23(10):742-746.[魯正,彭承宏,陳泉寧,等.胰腺癌擴大根治術中的血管處理[J].中華普通外科雜志,2008,23 (10):742-746.]
10 Zhu AD,Liu Q,Chen DX.Laparoscopic radical resection of hilar cholangiocarcinoma and lymph node dissection[J].Chinese Journal of Minimally Invasive Surgery,2010,10:922-924.[朱安東,劉奇,陳德興.腹腔鏡下肝門部膽管癌根治術中淋巴結廓清方法的探討[J].中國微創外科雜志,2010,10:922-924.]
11 Li GM,Zhu JY,Huang L,et al.The analysis for the variation of the donor livers[J].Chinese Journal of Surgery,2005,43(7):447-449.[栗光明,朱繼業,黃磊,等.供肝切取中肝動脈的變異分析[J].中華外科雜志,2005,43(7):447-449.]
(2014-07-10收稿)
(2014-09-20修回)
(編輯:周曉穎)

霍明生專業方向為肝膽胰腫瘤的外科治療。E-mail:camus0131@126.com
Clinical significance of hepatic artery variation in hepatic portal lymphadenectomy
Mingsheng HUO,Zheng LU,Peiyuan CUI,Binquan WU,Hua WU,Wei WU,Wenqing XU
Correspondence to:Zheng LU;E-mail:luzhengdr@163.com
Department of Hepatobiliary Surgery,the FirstAffiliated Hospital of Bengbu Medical College,Bengbu 233004,China
Objective:To investigate the recognition and injury prevention strategies of hepatic artery variations during hepatic portal lymphadenectomy.Methods:A retrospective analysis was performed,and 12 patients of hepatic arterial variation among 62 patients with hepatic portal lymphadenectomy were the subjects.The study was conducted in the FirstAffiliated Hospital of Bengbu Medical College between January 2013 and July 2014.The intraoperative treatment and postoperative complications were recorded.Results: Among 12 cases of hepatic artery variation,we found the following cases:3 cases(25.0%)of Michels'Type III,2 cases(16.7%)of Michels'Type VI,1 case(8.3%)of Michels'Type IX,1 case(8.3%)of Hiatt's Type 6,2 cases(16.7%)of spatial location variation between right hepatic artery and hepatic duct,2 cases(16.7%)of left and right hepatic artery originating from a common hepatic artery,and 1 case(8.3%)of right hepatic artery originating from the gastroduodenal artery.No injury of hepatic artery occurred.Two cases had postoperative complications,including 1 case of pancreatic leakage and 1 case of incision infection;postoperative hemorrhage,bile leakage, hepatic abscess did not occur in these two cases.Patients recovered well in general.Conclusion:Hepatic arterial injury can be significantly reduced by the following:increased familiarity with the various types of hepatic artery variations;complete imaging examinations for inspection and evaluation before surgery;and careful and meticulous operations in surgery.
hepatic artery variation,hepatic portal lymphadenectomy,superior mesenteric artery,hepatic arterial injury
10.3969/j.issn.1000-8179.20141159
蚌埠醫學院第一附屬醫院肝膽外科(安徽省蚌埠市233004)
魯正luzhengdr@163.com

