熔鹽電解-區域熔煉法制備太陽能級硅的工藝研究
孫東亞,何麗雯,廉冀瓊,謝 安,曾小蘭,楊若綿
(1廈門理工學院 材料科學與工程學院,福建 廈門 361024;2華僑大學 材料科學與工程學院,福建 廈門 361021)
太陽能級硅(SG-Si)是組建太陽能發電站的主要材料,隨著近年來光伏產業的快速發展,對SG-Si的需求量急劇增加。目前,工業上制取多晶硅的傳統工藝是西門子法,但是,由于其工藝流程長、能耗較高、生產成本較高且環境污染嚴重,其廣泛應用受到限制。而熔鹽電解法制取硅流程短、成本低、環境友好,因而越來越受到關注[1-6]。近年來,研究者們在熔鹽電解法制取和精煉金屬硅方面進行了卓有成效的研究[7-11],但利用熔鹽電解SiO2生成硅合金制取純硅的報道較少[4,6,12]。
本工作選用提純后的SiO2粉和高純電極材料,從原料和器具上減少了硼和磷等雜質元素的引入;實驗選取較適宜的電解電壓(2.6V)和電解溫度(850℃),在CaCl2-LiCl電解質體系中先熔鹽電解制備出Ca-Si合金,再通過區域熔煉提純,制得了純度符合太陽能電池使用的多晶硅。
1 實驗
1.1 試劑及工具
SiO2(150~200目),CaCl2(國藥 AR),LiCl(國藥AR),起弧機。
1.2 實驗裝置及預電解
實驗電解槽為自制裝置,如圖1所示。按照CaCl2∶LiCl=9∶1(摩爾比)進行混料配成混合電解質,原料SiO2及混合電解質在150℃的烘箱中烘干48h,然后放在干燥箱中備用。先將電解質粉末若干投入到電解槽中預電解:用電弧產生的高溫將電解質熔融,電解質部分熔解后,撤離起弧裝置,由熔融電解質在外加電流作用下自行導電加熱,溫度達到600℃后保溫2~3h。預電解可以有效驅除電解質中的水分和易揮發性雜質,提高熔鹽體系的初始溫度。
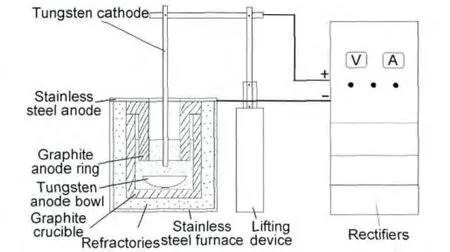
圖1 實驗裝置圖Fig.1 Equipment sketch of experiment
1.3 原理與制備流程
因為由熔鹽直接電解SiO2還原制備硅單質與其他物質的水溶液電解不同(Si-O系沒有導電性的氧化相),所以,只能采取以金屬或化合物導體代替Si-O系氧化物,直接由金屬來傳遞電子完成電解還原反應。當外加電極電動勢足夠低,直至低于SiO2的理論分解電動電勢時,脫氧反應就會在SiO2、金屬導體及熔融鹽的三相界面處發生[10]。脫氧反應發生后,生成的金屬和Si單質將會充當新的導體提供電子轉移,整個脫氧反應就會繼續在新的三相界面處發生,直至全部還原生成單質。在實際的電解過程中,由于電解質中金屬化合物的存在,SiO2電解還原時通過的電流并非全部用于生成目的產物單質Si,導致實際單質Si的量M1低于理論產物的量M0,SiO2直接熔鹽電解制備單質硅的電流效率η可表示為

式中:M1為通過單位電量電解實際得到的單質硅的質量;M0為通過單位電量按照法拉第定律計算得到的單質硅的質量。
SG-Si的制備過程如圖2所示。將SiO2粉末緩慢加入到電解爐槽中,用溫控系統調節控制爐內實際溫度,整流器控制輸入電壓電流參數。每隔4h左右收集沉積在電解槽底部的產物。陰離子在陽極失去電子形成氣體釋放,產生的氣體經過通風管道進行吸收凈化達標后排放。產物在真空條件下進行兩次區域熔煉后,得到的硅錠削去頂部、底部和四側的表皮,得到目標產物。
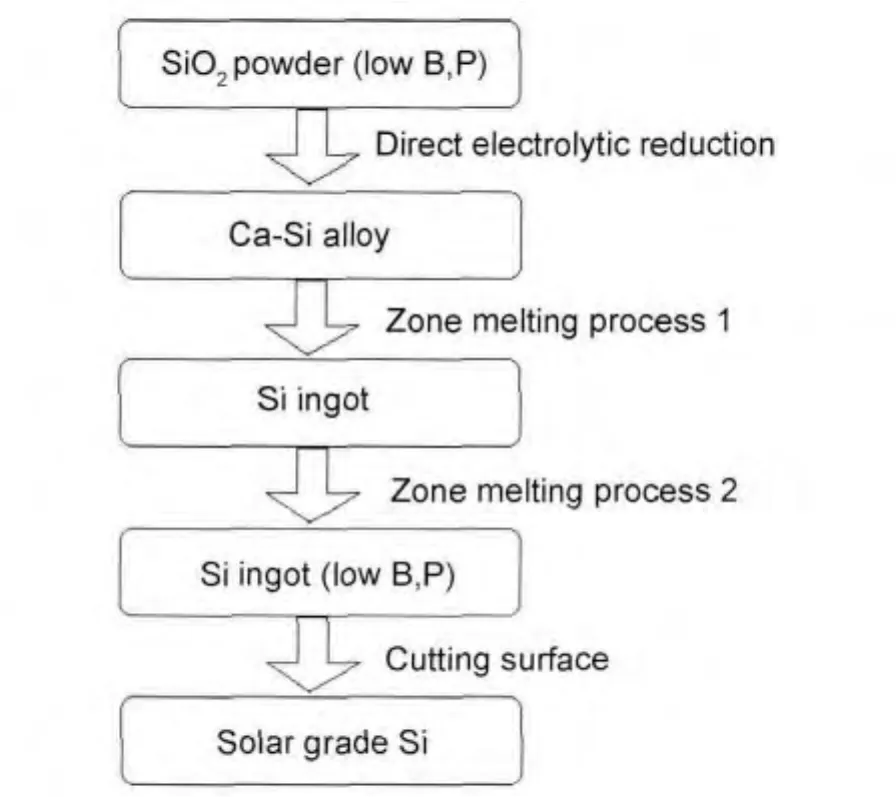
圖2 SG-Si的制備過程Fig.2 Schematic diagram of preparation processing for SG-Si
1.4 產物的表征
采用D8Advance型X射線衍射儀(XRD)進行產物的物相表征,X射線源為經Ni濾波的CuKα射線,波長為1.5418nm;使用EVO MA10/LS10型掃描電鏡(SEM)觀測其微觀形貌;原料及產物的雜質元素含量采用7700型電感耦合等離子發射質譜儀(ICP-MS)進行檢測。
2 結果與討論
2.1 原料提純及電解質選取
原料SiO2的提純工藝:將SiO2先磨細至一定目級(小于150目),然后用含有氫氟酸的混合酸溶液進行充分酸洗,再進行清洗、過濾和烘干。氫氟酸能滲透到顆粒中雜質富集的縫隙和晶界處與雜質反應,除去絕大部分金屬雜質,并對硼和磷有一定去除作用。提純后的SiO2雜質含量測試數據如表1所示,其中硼元素和磷元素含量均小于0.2×10-6。
氯化鈣及其電解質體系較多地用于固體石英和精煉金屬硅制備高純硅的熔鹽電解研究[11-14]。從CaCl2-LiCl二元熔度圖 可知,CaCl2-LiCl混合可以按任何比例互溶,逐步增加氯化鈣中氯化鋰的加入量到10%時,可降低混合熔鹽的熔點(約30℃),同時可提高熔鹽的流動性和電導率。故本工作選擇CaCl2為主,LiCl為熔解助劑的混合熔鹽。另外,在850℃下,相對 SiO2(-2.02V),CaCl2(-3.45V)和 LiCl(-3.74V)具有更低的電解電動勢[15],說明它們的穩定性強于前者,在熔鹽中施加槽電壓的瞬間不會先于SiO2分解而富集過多的鈣鋰金屬。
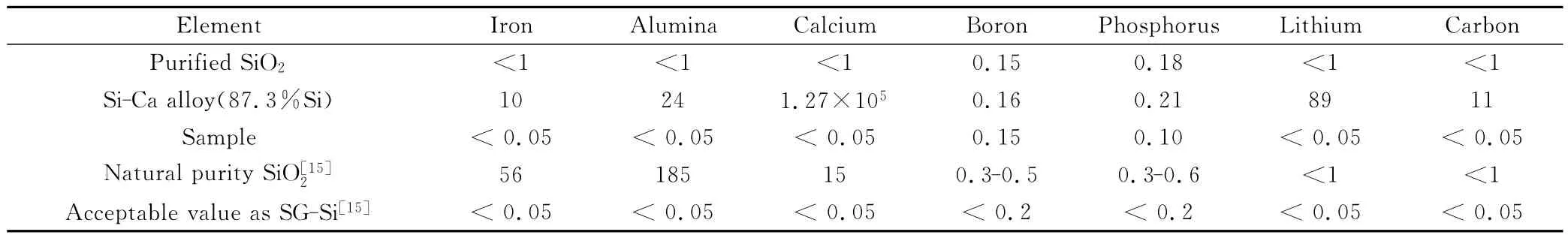
表1 原料及產物中的雜質含量/10-6Table 1 Impurity contents in production and raw material/10-6
鎢陰極的使用等同于文獻[16]報道的鉬絲,作為SiO2“接觸電極”,可有效地傳導電解過程中遷移電子。石墨套陽極附近SiO2顆粒中的O2-首先遷移出來與石墨發生反應,生成CO2和CO氣體,而在鎢陰極上會析出金屬和硅單質。考慮到減少電解過程中的雜質對產物的滲透污染,自制實驗電解槽中直接接觸電解質的材料均選擇雜質含量較少、且本身具有良好的高溫惰性及化學惰性的物質。電解的陰陽極主要電極反應為
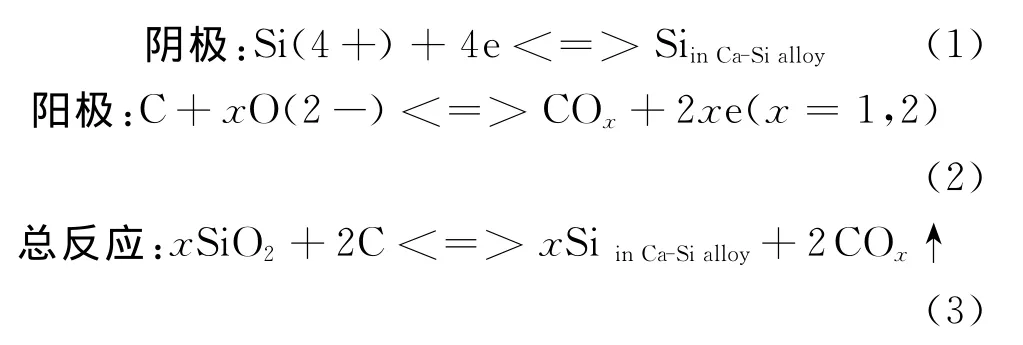
2.2 電解溫度的選擇
電解過程中溫度對電解質的密度、黏度、表面張力及還原反應速率等物理化學性質都有重要影響。所以,電解溫度選擇必須考慮電解體系中的熔鹽與原料的熔點特性,以CaCl2-LiCl體系為例,CaCl2與LiCl以摩爾比9∶1互熔時,混合熔鹽的熔點約為727℃,而SiO2的熔點為1670℃,其混合物的熔點隨著各組分含量的不同變化范圍較大。為探索合理的電解溫度,在其他條件相同的情況下選擇不同的電解溫度進行實驗,根據收集到的陰極產物計算出不同溫度下的電流效率η,如圖3所示。
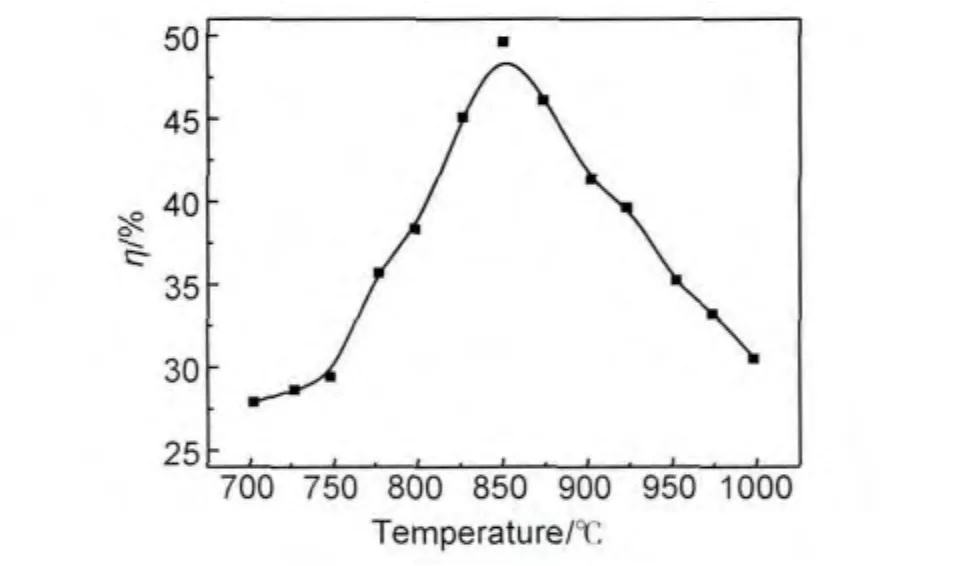
圖3 電解溫度對電流效率的影響Fig.3 Effect of electrolytic temperature on current efficiency
從圖3可以看出,電解溫度為700℃時的電流效率為28%左右,隨著溫度的升高,電流效率增大,在850℃時達最大值49.6%,之后溫度進一步升高,電流效率反而減小。這是因為,溫度較低時,電解質呈膠著狀態,體系的黏度和表面張力較大,影響了離子的遷移和擴散,電流效率較低。隨著溫度的升高,黏度逐漸減小,離子遷移的動能增加,阻力減小,電流效率得到提高。同時,陽極氣體量增大,使得O2-在電解質溶液中的遷移擴散距離減小,電化學還原速度加快,到850℃左右達到峰值。當溫度再升高時,電流效率降低的可能原因是:一方面,O2-在電解質中的溶解度增大,實際參與反應的O2-濃度減小,根據化學反應動力學可知不利于其在陽極反應析出;另一方面,高溫也加速了電解質的揮發,造成CaCl2與LiCl電解質的損失。故反應溫度設定為 850℃,這與Yasuda 等[13,14,16,17]在CaCl2熔鹽中SiO2陰極脫氧制取硅時的電解溫度相當。
2.3 電解槽電壓的選擇
圖4為電解產物組成與槽電壓的關系。可以看出,電解槽電壓低于2.0V時,生成產物量較少,之后隨著電壓值的增大,產物中硅及產物總量逐漸增加,到2.6V左右時產物中硅的含量達到最大值(87.3%)。當電壓高于2.6V后,產物中硅的含量也會降低。這說明,較低電壓時,由于熔鹽與電極極化現象不可避免引起歐姆電壓和超電壓的消耗。另外,由于陽極為析氣反應,氣體的生成吸附在陽極上形成氣膜,使電解液在電極上的潤濕性變差,也會消耗一定的電動勢。這樣,加在SiO2顆粒上的實際分解電動勢可能遠小于槽電壓值,O2-脫離出Si═ O鍵的動力不足,Si4+實際濃度較小,Si4+由熔體向雙電層移動并繼續經雙電層向陰極電極表面的擴散過程變緩,故產物中硅含量較低。同時,低電壓也會造成Si4+向Si2+副反應的發生,從而形成鈣硅合金。隨著電壓的升高,加在電極上的電動勢達到理論電動勢(2.02V),硅析出為主要陰極反應,產物中硅含量增多。槽電壓到2.6V時,單位時間內有效電流密度達到最大值,產物的總量也接近最大值(89.4g)。之后,由于槽電壓升高,電流密度達到最大值后,擴散不能及時向電極表面供應足夠數量的陽離子而開始使電極反應速率變慢。同時,槽電壓值逐漸接近Ca2+析出的電動勢,Ca在產物中的含量增多,硅的相對含量降低。
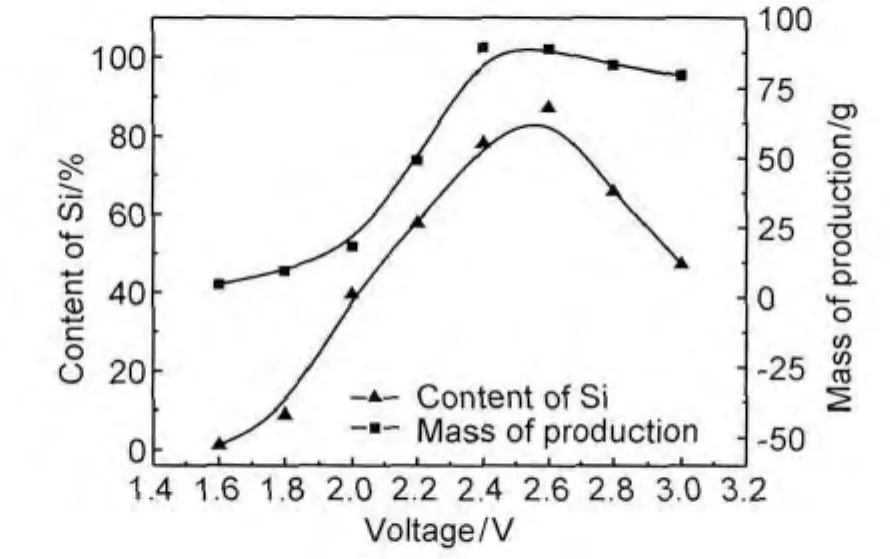
圖4 產物組成與槽電壓的關系Fig.4 Relationship with the product composition and electrolytic voltage
陰極金屬離子沉積模型如圖5所示。硅及雜質金屬原子在鎢陰極上的沉積是由里向外沉積的,每層由硅和少量金屬原子組成,由于硅導電性較差,電子不容易通過硅進行遷移,每多沉積一定數量的硅,有效電流密度就發生一定的下降,Si4+在陰極的吸附越來越困難,且下一層電解沉積只能發生在里層金屬部位。由于靠近金屬的部位優先沉積分解電動勢較小的硅,外層的金屬粒子越來越少,沉積一定的層厚(約幾百納米)后,有效傳導電流很小,電流空耗嚴重,硅沉積的速度變得越來越緩慢。電壓再升高時,并不能增加電流密度和硅沉積的速度,只會縮短沉積開始到沉積平衡的時間,相同時間內電解沉積產物的總量反而會減小,硅含量也會隨之減小,故較為適宜的電解電壓為2.6V。從電解產物SEM圖像(圖6)也可以看出,合金粉呈不規則片狀,這進一步說明上述階段性的沉積過程的可能性。到達沉積反應階段后,再用增大極化的方法已不可能再增大電極反應速率,只能靠采取強化擴散的措施。為確保電解反應的有效持續,本工作采取定時將鎢陰極上的沉積層清理的方法,取得了較好的效果。
2.4 物相分析
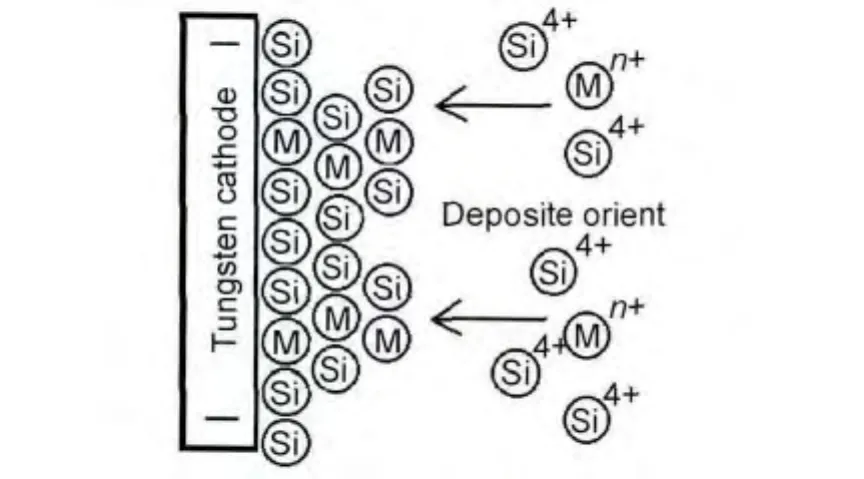
圖5 陰極離子沉積示意圖Fig.5 Schematic diagram of ion deposition on cathode

圖6 電解產物的SEM圖Fig.6 SEM image of electrolytic product
圖7為電解產物的XRD圖譜。對照單質硅(PDF:27-1402)、CaSi合金相(PDF:26-0324)及 CaSi2合金相(PDF:01-1276)標準譜線,電解產物圖譜除了Si的特征峰出現外,CaSi及CaSi2的衍射峰也存在,說明在此條件下,有鈣硅合金生成。由于硅鋰合金特征衍射峰的角度分布范圍較寬,且許多特征衍射峰的位置與鈣硅合金非特征衍射峰可能重疊,單從XRD圖譜上很難確定是否有硅鋰合金的生成。電解產物的ICP-MS元素分析結果顯示,鋰元素的含量小于100×10-6,說明幾乎沒有鈣鋰合金的生成,這可能與氯化鋰較大的分解電動勢有關。另外,從衍射峰強度來看,鈣硅合金相的特征峰強度較硅小,說明產物中合金相生成的量較少,這與合金含量分析中鈣的結果(12.7%)相符。
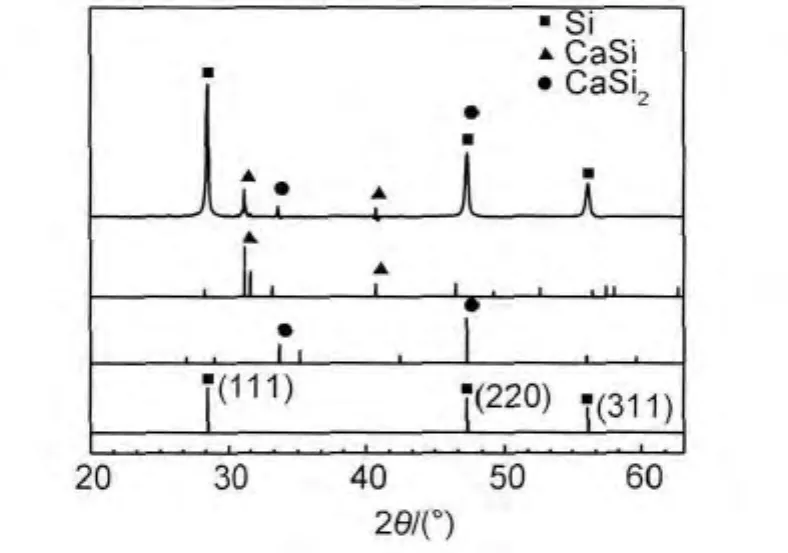
圖7 電解產物的XRD圖譜Fig.7 XRD patterns of electrolytic product
2.5 電解產物的后處理
表1列出了電解及區熔提純后產物中的雜質含量數據。說明用提純后的SiO2粉末為原料,電解后合金粉中硼、磷、金屬和碳含量均有升高,這說明熔鹽、電極材料及電解槽中存在的雜質在電解過程中會滲透到產物中,需要電解后提純處理。表2為各元素在硅熔點下的分凝系數[19]。可知,除B外,合金產物中的鈣及其他雜質元素比硅的分凝系數小,通常可以通過真空凝固的方法來進行分離去除[13]。區域熔煉的過程在真空下石英坩堝中進行,鈣等金屬雜質會分離于固液界面處,最終凝固在硅錠的頂部、底部及四個側面。經過兩次區熔提純,并將硅錠的頂部、底部及側面部分表皮切割后,剩余的硅錠(約85%區域)中金屬雜質去除率在99.9%以上,磷和碳元素降低,硼含量變化很小,這與各元素在真空下分凝系數的差異有關。從最終產物的元素含量看來,硼的含量為0.15×10-6,磷的含量為0.10×10-6,其他各雜質元素及總含量水平均符合太陽能級硅的標準。

表2 各元素在硅熔點下的分凝系數[19]Table 2 Distribution coefficient in silicon at the melting point of silicon[19]
3 結論
(1)以高純SiO2粉末為原料,在CaCl2與LiCl的混合熔鹽(摩爾比9∶1)中,高純鎢和石墨坩堝為電極材料,電解溫度850℃、槽電壓2.6V,經4h以上電解可在陰極上沉積鈣硅合金。
(2)電解產物經過兩次區域熔煉后,最終產物中硼的含量為0.15×10-6,磷的含量為0.10×10-6,其他各雜質元素及總含量水平均符合太陽能級硅的標準。
[1]RAO G M,ELWELL D,FEIGELSON R S.Electrowinning of silicon from K2SiF6-molten fluoride systems[J].Journal of the Electrochemical Society,1980,127(9):1940-1944.
[2]BIEBER A L,MASSOT L,GIBILARO M,et al.Silicon electrodeposition in molten fluorides[J].Electrochimica Acta,2012,62(2):282-289.
[3]HU Y,WANG X,XIAO J,et al.Electrochemical behavior of silicon(IV)ion in BaF2-CaF2-SiO2melts at 1573K[J].Journal of the Electrochemical Society,2013,160(3):81-84.
[4]ERGüL E,KARAKAYAī,ERDOGˇAN M.Electrochemical decomposition of SiO2pellets to form silicon in molten salts[J].Journal of Alloys and Compounds,2011,509(3):899-903.
[5]HAARBERG G M,FAMIYEH L,MARTINEZ A M,et al.Electrodeposition of silicon from fluoride melts[J].Electrochimica Acta,2013,100:226-228.
[6]XIAO W,JIN X B,DENG Y,et al.Rationalisation and optimisation of solid state electro-reduction of SiO2to Si in molten CaCl2in accordance with dynamic three phase interlines based voltammetry[J].Journal of Electroanalytical Chemistry,2010,639(1):130-140.
[7]MASSOT L,BIEBER A,GIBILARO M,et al.Silicon recovery from silicon-iron alloys by electrorefining in molten fluorides[J].Electrochimica Acta,2013,96:97-102.
[8]YASUDA K,NOHIRA T,KOBAYASHI K,et al.Improving purity and process volume during direct electrolytic reduction of solid SiO2in molten CaCl2for the production of solar-grade silicon[J].Energy Technology,2013,1(4):245-252.
[9]CAI J,LUO X,LU C,et al.Purification of metallurgical grade silicon by electrorefining in molten salts[J].Transactions of Nonferrous Metals Society of China,2012,22(12):3103-3107.
[10]王淑蘭,陳曉云.CaCl2-NaCl-CaO熔鹽中電解精煉Si的研究[J].金屬學報,2012,48(2):183-186.WANG Shu-lan,CHEN Xiao-yun.Study on the electro-refining silicon in molten salt CaCl2-NaCl-CaO[J].Acta Metallurgica Sinica,2012,48(2):183-186.
[11]CAI J,LUO X,HAARBERG G M,et al.Electrorefining of metallurgical grade silicon in molten CaCl2based salts[J].Journal of the Electrochemical Society,2012,159(3):155-158.
[12]OISHI T,WATANABE M,KOYAMA K,et al.Process for solar grade silicon production by molten salt electrolysis using aluminum-silicon liquid alloy[J].Journal of the Electrochemical Society,2011,158(9):93-99.
[13]YASUDA K,NOHIRA T,HAGIWARA R,et al.Direct electrolytic reduction of solid SiO2in molten CaCl2for the production of solar grade silicon[J].Electrochimica Acta,2007,53(1):106-110.
[14]NOHIRA T,YASUDA K,ITO Y.Pinpoint and bulk electrochemical reduction of insulating silicon dioxide to silicon[J].Nature Materials,2003,2(6):397-401.
[15]梁英教,車陰昌.無機物熱力學數據手冊[M].沈陽:東北大學出版社,1993.LIANG Ying-jiao,CHE Yin-chang.Handbook of Thermodynamic Data of Inorganic Substances[M].Shengyang:Northeastern University Press,1993.
[16]YASUDA K,NOHIRA T,ITO Y.Effect of electrolysis potential on reduction of solid silicon dioxide in molten CaCl2[J].Journal of Physics and Chemistry of Solids,2005,66(2):443-447.
[17]YANG X,YASUDA K,TOSHIYUKI N,et al.Reaction be-havior of stratified SiO2granules during electrochemical reduction in molten CaCl2[J].Metallurgical and Materials Transactions B,2014,45(4):1337-1344.
[18]TOBA T,YASUDA K,NOHIRA T,et al.Fundamental study on reduction rate for electrolytic reduction of SiO2powder in molten CaCl2[J].ECS Transactions,2013,50(11):119-126.
[19]TRUMBORE F A.Solid solubilities of impurity elements in germanium and silicon[J].Bell System Technical Journal,1960,39(1):205-233.

