HPLC同時(shí)測(cè)定加味逍遙丸中梔子苷和芍藥苷的含量
楊慶勝,馮朝嶺,司根令
(1.河南省醫(yī)藥藥材有限公司,河南 鄭州 450003;2.河南漢方藥業(yè)有限責(zé)任公司,河南 鄭州 450003)
HPLC同時(shí)測(cè)定加味逍遙丸中梔子苷和芍藥苷的含量
楊慶勝1,2*,馮朝嶺1,司根令2
(1.河南省醫(yī)藥藥材有限公司,河南 鄭州 450003;2.河南漢方藥業(yè)有限責(zé)任公司,河南 鄭州 450003)
目的:建立加味逍遙丸中梔子苷、芍藥苷的含量測(cè)定方法。方法:高效液相色譜法,色譜柱為KromasilC18;流動(dòng)相為乙腈-0.1%磷酸溶液(15∶85);檢測(cè)波長(zhǎng)為230 nm;進(jìn)樣量為10 μL;室溫;流速為1.0 mL·min-1。結(jié)果:梔子苷在0.24~2.16 μg進(jìn)樣量與峰面積間呈良好的線性關(guān)系,r=0.999 6,平均回收率為99.29%;芍藥苷在0.12~1.08 μg進(jìn)樣量與峰面積間呈良好的線性關(guān)系,r=0.999 7,平均回收率為99.62%。符合測(cè)定方法學(xué)研究的要求。結(jié)論:本方法操作方便,專屬性強(qiáng),重復(fù)性好,可作為該制劑的含量測(cè)定方法。
加味逍遙丸;梔子苷;芍藥苷;高效液相色譜法;含量測(cè)定
加味逍遙丸是收載于《中國(guó)人民共和國(guó)藥典》2010版一部的品種,處方由柴胡、當(dāng)歸、白芍、白術(shù)(麩炒)、茯苓、甘草、牡丹皮、梔子(姜炙)、薄荷九味中藥組成,具有舒肝清熱、健脾養(yǎng)血的功能,用于肝郁血虛、肝脾不和、兩脅脹痛、頭暈?zāi)垦!⒕氲∈成佟⒃陆?jīng)不調(diào)、臍腹脹痛[1]。梔子苷、芍藥苷分別為梔子、白芍的特征性有效成分,梔子苷、芍藥苷是加味逍遙丸的活性成分之一。原質(zhì)量標(biāo)準(zhǔn)只有芍藥苷的含量測(cè)定,為了控制加味逍遙丸的質(zhì)量,保證其療效,在對(duì)該品種進(jìn)行研究提高的過程中,采用高效液相色譜法,同一條件下測(cè)定梔子苷、芍藥苷在該制劑中的含量,并對(duì)測(cè)定方法學(xué)進(jìn)行研究。
1 儀器與試劑
1.1 儀器
FA-2004型電子分析天平(上海上平儀器公司);KG3200超聲波振蕩器(昆山市超聲波儀器有限公司);Agilent 1100型高效液相色譜儀、Agilent化學(xué)工作站(美國(guó))。
1.2 試劑
梔子苷對(duì)照品(中國(guó)食品藥品檢定研究院,批號(hào):110749-201115,);芍藥苷對(duì)照品(中國(guó)食品藥品檢定研究院,批號(hào):110736-201035);加味逍遙丸三批樣品為項(xiàng)目研發(fā)時(shí)自制(批號(hào)分別為130619,130622,130625);缺梔子、白芍、牡丹皮的陰性樣品也為自制;乙腈為色譜純(天津四友公司),其它試劑均為分析純,水為重蒸水。
2 方法與結(jié)果
2.1 色譜條件與系統(tǒng)適用性試驗(yàn)
色譜柱為KromasilC18柱(250 mm×4.6 mm,5 μm);流動(dòng)相為乙腈-0.1%磷酸溶液(15∶85);流速為1.0 mL·min-1;檢測(cè)波長(zhǎng)為230 nm;柱溫為室溫;進(jìn)樣量為10 μL。理論板數(shù)按芍藥苷峰計(jì)算應(yīng)不低于3000。
2.2 對(duì)照品溶液的制備
精密稱取梔子苷對(duì)照品30 mg、芍藥苷對(duì)照品15 mg,同置于250 mL量瓶中,加甲醇至刻度,搖勻,即得梔子苷質(zhì)量濃度為120 μg·mL-1、芍藥苷質(zhì)量濃度為60 μg·mL-1的混合對(duì)照品溶液。
2.3 供試品溶液的制備
取加味逍遙丸5 g,研細(xì),混勻,取細(xì)粉約1 g,精密稱定,置具塞錐形瓶中,精密加入甲醇50 mL,密塞,稱定重量,浸漬過夜,超聲處理(功率為260 W,頻率為40 kHz)30 min,放冷,再稱定重量,用甲醇補(bǔ)足減失的重量,搖勻,用微孔濾膜(0.45 μm)濾過,取續(xù)濾液,即得。
2.4 陰性樣品溶液的制備
取缺白芍、牡丹皮、梔子的處方藥材,按加味逍遙丸制備工藝制成缺白芍、牡丹皮、梔子的陰性樣品,按2.3方法制備陰性樣品溶液。
2.5 線性關(guān)系考察
分別精密吸取混合對(duì)照品溶液2、6、10、14、18 μL,注入液相色譜儀,按2.1色譜條件進(jìn)樣分析,記錄峰面積。以進(jìn)樣量(X)與對(duì)應(yīng)的峰面積(Y)作回歸處理,得到芍藥苷回歸方程為Y=1709.717X+27.910,r=0.999 7;梔子苷回歸方程為Y=1646.308X+66.086,r=0.999 6。結(jié)果表明,芍藥苷在0.12~1.08 μg、梔子苷在0.24~2.16 μg進(jìn)樣量與峰面積間均具有良好的線性關(guān)系。
2.6 專屬性試驗(yàn)
分別精密吸取對(duì)照品溶液、供試品溶液及陰性樣品溶液各10 μL,注入液相色譜儀,按2.1色譜條件進(jìn)行測(cè)定,記錄色譜圖,從色譜圖中可以看出,本測(cè)定條件的專屬性強(qiáng),陰性樣品對(duì)芍藥苷、梔子苷的含量測(cè)定無干擾。見圖1~3。

圖1 梔子苷、芍藥苷對(duì)照品色譜圖
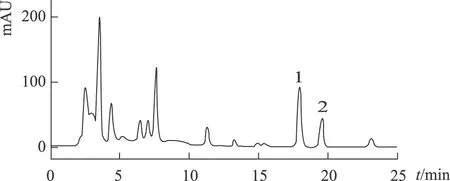
圖2 供試品色譜圖

圖3 陰性樣品色譜圖
2.7 精密度試驗(yàn)
精密吸取上述混合對(duì)照品溶液10 μL,注入液相色譜儀,重復(fù)進(jìn)樣6次,分別測(cè)定芍藥苷、梔子苷的峰面積積分值,芍藥苷RSD=1.16%(n=6);梔子苷RSD=1.39%(n=6)。表明本法精密度較好,符合定量分析要求。
2.8 穩(wěn)定性試驗(yàn)
精密吸取同一供試品溶液(批號(hào):130622),分別于0、2、4、6、8、10 h各進(jìn)樣10 μL,測(cè)定芍藥苷、梔子苷的峰面積積分值,芍藥苷RSD=1.28%(n=6);梔子苷RSD=1.32%(n=6)。表明供試品溶液在10 h內(nèi)基本穩(wěn)定。
2.9 重復(fù)性試驗(yàn)
取同一批號(hào)供試品(批號(hào):130622),按2.3方法平行制備5份供試品溶液,各吸取10 μL,分別注入液相色譜儀,進(jìn)行含量測(cè)定,梔子苷的平均質(zhì)量分?jǐn)?shù)為3.561 8 mg·g-1,RSD=1.42%;芍藥苷的平均質(zhì)量分?jǐn)?shù)為2.281 2 mg·g-1,RSD=1.36%。表明本方法重復(fù)性良好。
2.10 加樣回收率試驗(yàn)
取已知含量的同一供試品(批號(hào):130622)細(xì)粉6份,每份約5 g,研細(xì),混勻,分別取細(xì)粉0.5 g,精密稱定,置具塞錐形瓶中,每份分別精密加入混合對(duì)照品溶液稀釋液50 mL(精密吸取上述對(duì)照品混合溶液20 mL,用甲醇稀釋至50 mL,即得。稀釋液中梔子苷質(zhì)量濃度為48 μg·mL-1、芍藥苷質(zhì)量濃度為24 μg·mL-1),余下按2.3方法操作,分別吸取供試品液各10 μL,按2.1色譜條件,分別測(cè)定梔子苷、芍藥苷的含量,計(jì)算加樣回收率,結(jié)果見表1、表2。

表1 梔子苷加樣回收率試驗(yàn)
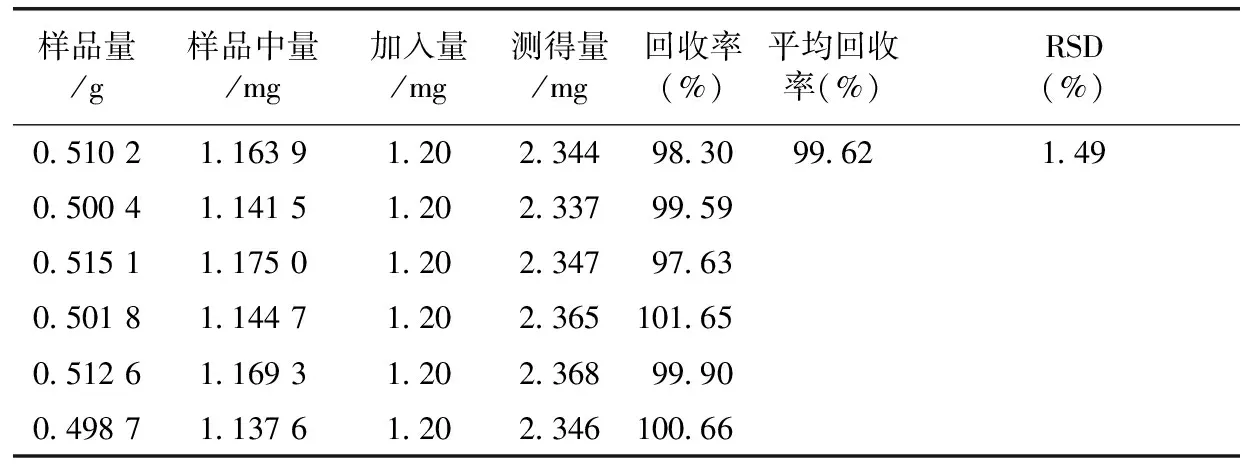
表2 芍藥苷加樣回收率試驗(yàn)
2.11 供試樣品的含量測(cè)定
分別取不同批號(hào)的樣品,按2.3方法制備。精密吸取對(duì)照品溶液和供試品溶液各10 μL,注入液相色譜儀,按2.1色譜條件分別測(cè)定各樣品中梔子苷和芍藥苷的含量,測(cè)定結(jié)果見表3。
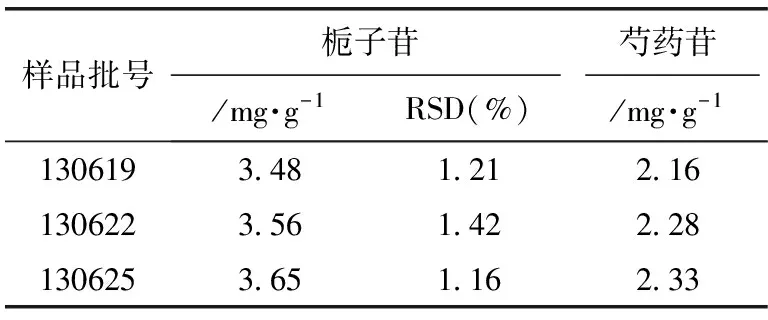
表3 三批供試品中梔子苷和芍藥苷的含量測(cè)定結(jié)果
注:加味逍遙丸規(guī)格為6 g/袋。
3 討論
3.1 檢測(cè)波長(zhǎng)的選擇
文獻(xiàn)資料[1]顯示,梔子苷、芍藥苷二者的檢測(cè)波長(zhǎng)非常接近,為了確保檢測(cè)的靈敏度,本研究對(duì)梔子苷、芍藥苷對(duì)照品溶液進(jìn)行了紫外掃描分析,結(jié)果波長(zhǎng)為230 nm,兩者的檢測(cè)靈敏度均較好,峰形好,峰面積變化較小,故本研究選擇230 nm作為檢測(cè)波長(zhǎng)。
3.2 流動(dòng)相的選擇
本研究曾選用不同比例的乙腈-水[1]、乙腈-0.05 mol·L-1磷酸二氫鉀溶液[2]、乙腈-0.1%磷酸溶液[3]、乙腈-0.1%醋酸溶液[4]、甲醇-0.2%磷酸溶液[5]等系統(tǒng)為流動(dòng)相作了系統(tǒng)地比較,結(jié)果表明,以乙腈-0.1%磷酸溶液(15∶85)作為流動(dòng)相時(shí),梔子苷、芍藥苷峰形較好,分離度也好。因此,選擇乙腈-0.1%磷酸溶液(15∶85)作為流動(dòng)相。
3.3 溶劑和超聲時(shí)間的選擇
本研究在供試品溶液的制備過程中,曾選用甲醇、50%甲醇、乙醇、50%乙醇四種溶劑分別超聲處理20 min,結(jié)果四種溶劑所得供試液色譜基本一致,以甲醇為溶劑測(cè)定的含量最高。再以甲醇為溶劑分別超聲處理20、30、40 min,結(jié)果超聲處理30 min與超聲處理40 min的供試液測(cè)定值高于超聲處理20 min的測(cè)定值,但二者基本相同,故確定以甲醇超聲處理30 min作為制備供試品溶液的條件。
3.4本研究按照測(cè)定方法學(xué)研究的要求,對(duì)加味逍遙丸中梔子苷、芍藥苷的含量測(cè)定過程中的色譜條件、線性關(guān)系、專屬性、精密度、穩(wěn)定性、重復(fù)性、加樣回收率等因素條件分別進(jìn)行了考察,結(jié)果表明,本方法操作方便,線性關(guān)系良好,專屬性強(qiáng),穩(wěn)定性、重現(xiàn)性好,加樣回收率符合要求,可作為該制劑的含量測(cè)定方法。
[1] 國(guó)家藥典委員會(huì).中華人民共和國(guó)藥典:一部 [S].北京:中國(guó)醫(yī)藥科技出版社,2010:96-97,231-232,667-668.
[2] 王玉鵬,趙麗華,王杰松.高效液相色譜法測(cè)定調(diào)經(jīng)活血片中芍藥苷的含量[J].武警醫(yī)學(xué),2008,19(07):617-618.
[3] 周卿,兌丹華,代廣會(huì),等.RP-HPLC法同時(shí)測(cè)定清胰湯顆粒中梔子苷、芍藥苷的含量[J].重慶醫(yī)科大學(xué)學(xué)報(bào),2007,32(3):268-270.
[4] 周瑾,莊惠清.HPLC法測(cè)定丹梔逍遙丸中梔子苷和芍藥苷的含量[J].中國(guó)藥事,2007,21(7):495-497.
[5] 趙江紅,董文玲,劉伏先,等.HPLC法測(cè)定降脂排毒片中梔子苷的含量[J].中醫(yī)研究,2011,24(11):26-28.
DeterminationofGeniposideandPaenoiflorininJiaweiXiaoyaoWanbyHPLC
YANG Qingsheng1,2*,F(xiàn)ENGChaoling1,SIGenling2
(1.HenanPharmaceuticalMedicinesCo.,Ltd,Zhengzhou450003,China;2.HenanHanfangPharmaceuticalCo.,Ltd,Zhengzhou450003,China)
Objective:To establish a method for determination of geniposide and paenoiflorin in Jiawei Xiaoyao Wan.Methods:The separation was performed on Kromasil C18column at 25 ℃,using acetonitrile -0.1% phosphoric(15∶85)as a mobile phase,injecting amount 10μL,the flow rate was 1.0 mL·min-1,the UV detection wavelength was 230 nm.Results:Geniposide showed a good linear relationship in range of 0.24-2.16 μg,r=0.999 6,the average recovery was 99.29%.Paenoiflorin showed a good linear relationship in range of 0.12-1.08 μg,r=0.999 7,the average recovery was 99.62%.Conclusion:The method is sample,accurate and practical,and suitable for the determination of Jiawei Xiaoyao Wan.
Jiawei Xiaoyao Wan;geniposide;paenoiflorin;HPLC;determination
2014-04-10)
*
楊慶勝,男,副主任藥師,研究方向:中藥的成分分析與新產(chǎn)品開發(fā); Tel:(0371)60986969,E-mail:yangqsheng@126.com
10.13313/j.issn.1673-4890.2015.1.016

