季銨鹽鏈長及用量對CnTA+/蒙脫石納米復合物吸附PAEs的影響
李莉,孫紅娟,彭同江
?
季銨鹽鏈長及用量對CTA+/蒙脫石納米復合物吸附PAEs的影響
李莉1,2,孫紅娟1,2,彭同江1,2
(1西南科技大學固體廢物處理與資源化省部共建教育部重點實驗室,四川綿陽 621010;2西南科技大學礦物材料及應用研究所,四川綿陽 621010)
用具有相同結構但不同烷基碳鏈長度的系列季銨鹽制得CTA+/蒙脫石納米復合物,并對水溶液中鄰苯二甲酸酯進行吸附實驗。探討了季銨鹽烷基碳鏈鏈長和用量對制得的CTA+/蒙脫石納米復合物吸附水溶液中PAEs效果的影響。結果表明:CTA+/蒙脫石納米復合物能有效地吸附溶液中的PAEs,季銨鹽烷基碳鏈鏈長及用量均對CTA+/蒙脫石納米復合物的吸附效果產生影響。當季銨鹽用量較低時,隨著季銨鹽烷基鏈長的增加,PAEs的吸附去除率增加;增大季銨鹽用量,隨著季銨鹽烷基鏈長的增加,PAEs的吸附去除率先增大后減小。
季銨鹽;CTA+/蒙脫石納米復合物;納米結構;鄰苯二甲酸酯;水溶液;吸附
引 言
蒙脫石是由硅氧四面體和鋁氧八面體形成的2:1型層狀硅酸鹽礦物,其層間的水化陽離子具有良好的可交換性,經陽離子交換改性后的蒙脫石廣泛應用于環境污染治理和環境修復中[1-3]。季銨鹽陽離子(CTA+)可通過離子交換作用進入蒙脫石層間形成CTA+/蒙脫石納米復合物,CTA+在蒙脫石層間形成有機疏水環境,對有機污染物的吸附去除具有優良的效果[4-5]。然而,不同的季銨鹽烷基碳鏈鏈長和用量會影響季銨鹽陽離子在蒙脫石層間的排布模式[6-7],形成具有不同結構和性質的CTA+/蒙脫石納米復合物,并直接影響對有機污染物的去除能力[8]。
鄰苯二甲酸酯(PAEs)是鄰苯二甲酸的非鹵代酯,在各種工業消費品如塑料包裝、建材、玩具、醫療器具中作為增塑劑聚合物廣泛使用[9]。這種形式的鄰苯二甲酸酯不會與聚合物形成化學鍵合,在使用過程中會逐漸釋放進入環境之中,具有較強的疏水性和難降解性,對動物和人體的內分泌系統造成干擾,已被多個國家列為環境污染物中的優先控制污染物[10-12]。由于鄰苯二甲酸酯的疏水性和難降解性,吸附法作為一種能有效處理含有鄰苯二甲酸酯類污廢水的方法廣泛使用[13-14]。
本文以不同用量和不同烷基碳鏈鏈長的系列季銨鹽經陽離子交換制備CTA+/蒙脫石納米復合物,以兩種鄰苯二甲酸酯類物質DMP、DEP作為目標污染物進行靜態吸附實驗;探討季銨鹽烷基碳鏈鏈長和用量對兩種鄰苯二甲酸酯類物質吸附性能的影響,分析DMP、DEP在CTA+/蒙脫石納米復合物上的吸附機制。
1 實驗材料和方法
1.1 實驗原料及試劑
實驗原料:蒙脫石樣品采自四川三臺膨潤土礦,研磨至0.074 mm。經沉降法提純,85℃烘干,采用X射線熒光光譜對樣品進行礦物成分和化學成分分析。其主要化學成分為SiO2,54.93%;Al2O3,16.84%;Fe2O3,2.04 %;MgO,6.33%;CaO,2.21%;Na2O,0.46%;K2O,0.40%。樣品陽離子交換容量(CEC)為CEC=112.96 mmol·(100 g)-1。
試劑:十烷基三甲基溴化銨(C10TAB)、十二烷基三甲基溴化銨(C12TAB)、十四烷基三甲基溴化銨(C14TAB)、十六烷基三甲基溴化銨(C16TAB)、十八烷基三甲基溴化銨(C18TAB)、甲醇、無水乙醇、碳酸鈉,分析純,成都市科龍化工試劑廠;鄰苯二甲酸二甲酯(DMP)、鄰苯二甲酸二乙酯(DEP),分析純,上海晶純生化科技股份有限公司。
1.2 實驗
1.2.1 CTA+/蒙脫石納米復合物的制備 參考文獻[15]中的方法,先將原樣鈣蒙脫石鈉化改型得到鈉蒙脫石,按物質的量(CTAB)相當于倍蒙脫石陽離子交換量的CTAB加入充分分散的5%的蒙脫石懸濁液中。在微波功率320 W下進行插層處理3 min,經過濾洗滌至無Br-后,在85℃下干燥得CTA+/蒙脫石納米復合物,樣品編號為C-M (為季銨鹽用量,為季銨鹽烷基碳鏈鏈長)。
1.2.2 原料液的配制及靜態吸附實驗 取DMP、DEP標準品適量,置于100 ml容量瓶中用甲醇溶解并定容,得到濃度為1000 mg·L-1的儲備液,再由儲備液加入超純水配制所需濃度的溶液作為實驗水樣。取配制好的一定濃度的實驗水樣50 ml于200 ml錐形瓶中,分別加入0.5 gC-M并固定到恒溫振蕩器中,在120 r·min-1、25℃的搖床內恒溫振蕩達到吸附平衡后,取出將溶液通過0.45mm的濾膜過濾,用HPLC測定濾液中DMP、DEP的剩余含量,以保留時間定性,外標法定量;并計算DMP、DEP的吸附量和去除率。
1.3 分析及表征
溶液中DMP、DEP的分析檢測采用高效液相色譜HPLC( Agilent 1260,美國)和UV檢測器,色譜柱為Zorbax SB-C18(150 mm×4.6 mm)。色譜條件:柱溫30℃,檢測器波長254 nm,流動相采用甲醇和水兩相淋洗,流速1.0 ml·min-1,流量梯度為0~10 min,甲醇:水=60%:40%,進樣量為10ml。
XRD采用荷蘭帕納科X’pert MPD Pro型X射線衍射儀。測試條件:Cu靶(=0.15406 nm),管壓40 kV,管流40 mA,狹縫系統(DS)0.5°,放散射狹縫(SS) 0.04 rad,接受狹縫(AAS) 5.5 nm,連續掃描。
比表面積測定采用美國康塔NOVA3000型全自動表面分析儀,在77 K條件下測定氮吸附等溫曲線,采用BET法計算比表面積。
2 結果與討論
2.1 CTA+/蒙脫石納米復合物的結構分析
圖1分別為0.5 CTAB、1.0 CTAB、2.0 CTAB制得系列CTA+/蒙脫石納米復合物的XRD圖譜。
由圖1可知,相同用量的季銨鹽制備的CTA+/蒙脫石納米復合物的層間距001值隨季銨鹽的鏈長增長而呈增加趨勢;相同鏈長的季銨鹽制備的CTA+/蒙脫石納米復合物的層間距001值隨用量的增加而增加。
由圖1(a)可知,季銨鹽用量為蒙脫石0.5CEC時,CTA+/蒙脫石納米復合物的層間距001值隨鏈長的增加不明顯,原因是當季銨鹽用量低時,季銨鹽陽離子呈單層平臥在蒙脫石層間,季銨鹽烷基碳鏈所在的平面垂直于蒙脫石結構平面層[16-18]。
由圖1(b)可知,季銨鹽用量為蒙脫石1.0 CEC時,CTA+/蒙脫石納米復合物的層間距001值隨鏈長的增加明顯增大,原因是當增加季銨鹽的用量時,季銨鹽陽離子在蒙脫石層間的排布發生改變,同時因季銨鹽烷基鏈長的不同排布模式不同,C10TA+在蒙脫石層間呈鏈鎖嵌合雙層平臥排列[18-19],C12~18TA+在蒙脫石層間為單層傾斜排列[19-20]。
由圖1(c)可知,季銨鹽用量為蒙脫石2.0CEC時,CTA+/蒙脫石納米復合物的層間距001值隨鏈長的增加進一步增大,原因是繼續增大季銨鹽的用量,季銨鹽陽離子在蒙脫石層間的排列由鏈鎖嵌合雙層平臥和傾斜單層轉變為雙層平臥和雙層傾斜以及假三層結構[16-20]。
為考察經CTAB對有機插層后CTA+/蒙脫石納米復合物結構的影響,采用BET比表面積測試樣品的比表面積,結果見表1。
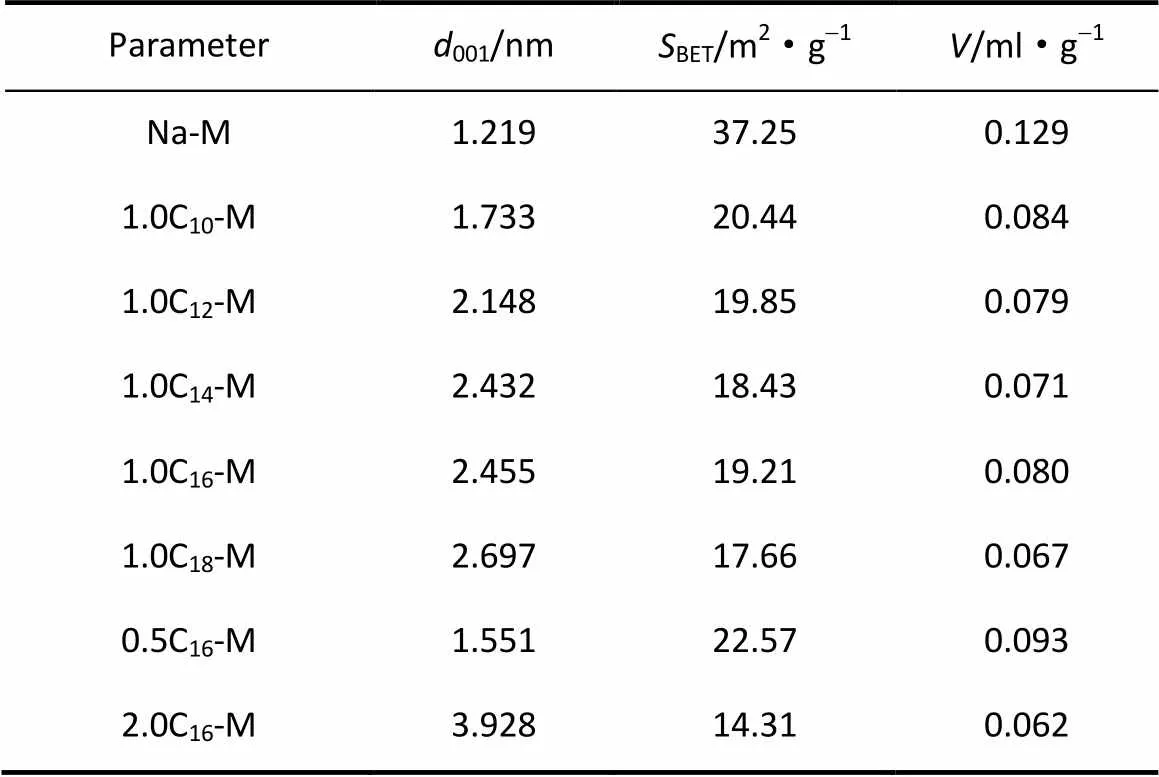
表1 Na-M和CnTA+/蒙脫石納米復合物的孔結構參數
由表1可知,經有機插層后的CTA+/蒙脫石納米復合物的比表面積和微孔體積均減小,這是因為有機改性進入層間,填充了一定的蒙脫石層間微孔孔道,同時隨著烷基鏈長的增加,所填充的微孔孔道增加而使微孔體積隨著鏈長及用量的增加而減小。
2.2 季銨鹽用量及烷基碳鏈鏈長對PAEs去除率的影響
圖2~圖4中,圖(a)分別為0.5 CTAB、1.0 CTAB、2.0 CTAB制得CTA+/蒙脫石納米復合物吸附初始濃度為50 mg·L-1的PAEs溶液后的HPLC圖;圖(b)分別為根據色譜峰的響應面積計算吸附前后溶液中兩種鄰苯二甲酸酯的含量,得到季銨鹽烷基碳鏈鏈長對CTA+/蒙脫石納米復合物吸附兩種鄰苯二甲酸酯的去除率。
從圖2(a)可以看出,0.5C-M吸附后溶液中剩余的DMP、DEP色譜峰響應值相對于原溶液減小(原樣中DMP峰高:167.2×10-3,DEP峰高:80.1×10-3,圖中未列出)。隨著0.5C-M中季銨鹽烷基碳鏈鏈長的增加,吸附后溶液中剩余兩種PAEs色譜峰響應值逐漸減小,表明溶液中剩余兩種PAEs含量逐漸減少。由圖2(b)可知,隨著0.5C-M中季銨鹽烷基碳鏈鏈長的增加,兩種PAEs的去除率和吸附量都逐漸增加,其中DMP的去除率從52.52%增加到75.55%,DEP的去除率從73.09%增加到91.14%。
從圖3(a)可以看出,1.0C-M吸附后溶液中剩余的DMP、DEP的色譜峰響應值隨著季銨鹽烷基碳鏈的增加先減小再增大。由圖3(b)可知,1.0C-M對DMP、DEP的去除率先增加后減小,當季銨鹽為C16TAB時,對兩種物質的去除率均達到最大值,分別為79.11%和93.15%。
從圖4(a)可以看出,2.0C-M吸附后溶液中剩余的DMP、DEP高效液相色譜峰響應值隨著季銨鹽烷基鏈長的增加,呈現先減小后增大的趨勢。由圖4(b)可知,當季銨鹽陽離子為C10TA+、C12TA+、C14TA+時,對DMP、DEP的去除率變化不大;當季銨鹽陽離子為C16TA+時,對兩種PAEs物質的去除率開始下降,而當季銨鹽陽離子為C18TA+時,去除率達到最低,分別為43.37%和49.52%。
結合上述結果分析認為,CTA+/蒙脫石納米復合物對水中有機物的去除率與季銨鹽陽離子的烷基碳鏈長度及用量有關。CTA+/蒙脫石納米復合物對PAEs的去除率隨烷基碳鏈鏈長的增長而增大;隨季銨鹽用量的增加先增大后減小。
當季銨鹽用量為0.5CEC時,季銨鹽陽離子均呈單層平臥在蒙脫石層間,隨著烷基碳鏈長度的增加,0.5C-M的最大底面間距001逐漸增大,CTA+/蒙脫石納米復合物的吸附能力也隨著CTA+烷基鏈長的增加而增大。
增加季銨鹽的用量到1.0CEC時,CTA+在蒙脫石層間的排布轉變為雙層平臥和單層傾斜結構,隨著烷基碳鏈長度的增加,1.0C-M的最大底面間距比原蒙脫石樣品(001=1.219 nm)以及0.5C-M系列樣品的最大底面間距明顯增大,對DMP、DEP的吸附性能也增強。
季銨鹽用量為2.0CEC時,CTA+在蒙脫石層間的排布模式轉變為雙層傾斜及假三層結構,隨著烷基碳鏈長度的增加,季銨鹽陽離子在礦物層間的排列方式趨向于復雜,表現為對溶液中PAEs的吸附去除率降低。
對比0.5C-M、1.0C-M和2.0C-M對DMP、DEP的吸附去除率可知[圖2(b)、圖3(b)、圖4(b)],當季銨鹽烷基碳鏈鏈長相同時,用量為2.0CEC時的去除率大于0.5CEC時的去除率而小于1.0CEC時的去除率,表明CTA+/蒙脫石納米復合物對PAEs的吸附受季銨鹽烷基碳鏈鏈長的影響,而相同用量不同烷基碳鏈的季銨鹽在蒙脫石層間的排布模式也不同,這也證明了季銨鹽在蒙脫石層間的不同排布模式對CTA+/蒙脫石納米復合物吸附性能的影響。
2.3 吸附等溫線
為了更好地描述CTA+/蒙脫石納米復合物對兩種PAEs的吸附行為,分別采用Langmuir和Freundlich等溫吸附模型對1.0CEC CTA+/蒙脫石納米復合物對DMP、DEP的吸附數據進行擬合。其中Langmuir和Freundlich吸附等溫模型方程表達式[21-23]如下。
Langmuir模型
Freundlich模型
式中,e為平衡時的吸附容量,mg·g-1;e為平衡時的濃度,mg·L-1;m為最大吸附容量,mg·g-1;L為Langmuir方程結合常數,L·mg-1;F和為Freundlich吸附常數。其中m和L的值由e/e-e線性方程的截距和斜率計算得到;F和1/的值由lne-lne線性方程的截距和斜率計算得到。
方程吸附結合系數(L和F)以及其他參數(Langmuir方程中m和Freundlich方程中1/值)都可以在一定程度上表示吸附反應機制。通常情況下,按分子間引力和化學鍵(如離子鍵和共價鍵作用)等吸附作用力的不同,可將吸附反應分為物理吸附和化學吸附。物理吸附過程中吸附劑的最大吸附容量隨著溫度的升高而減小;而化學吸附則是當溫度達到一定條件時吸附容量隨溫度升高而增大[24]。圖5、圖6分別為DMP、DEP在CTA+/蒙脫石納米復合物上的吸附數據與Langmuir模型方程和Freundlich模型方程的擬合曲線,表2為方程的擬合參數。
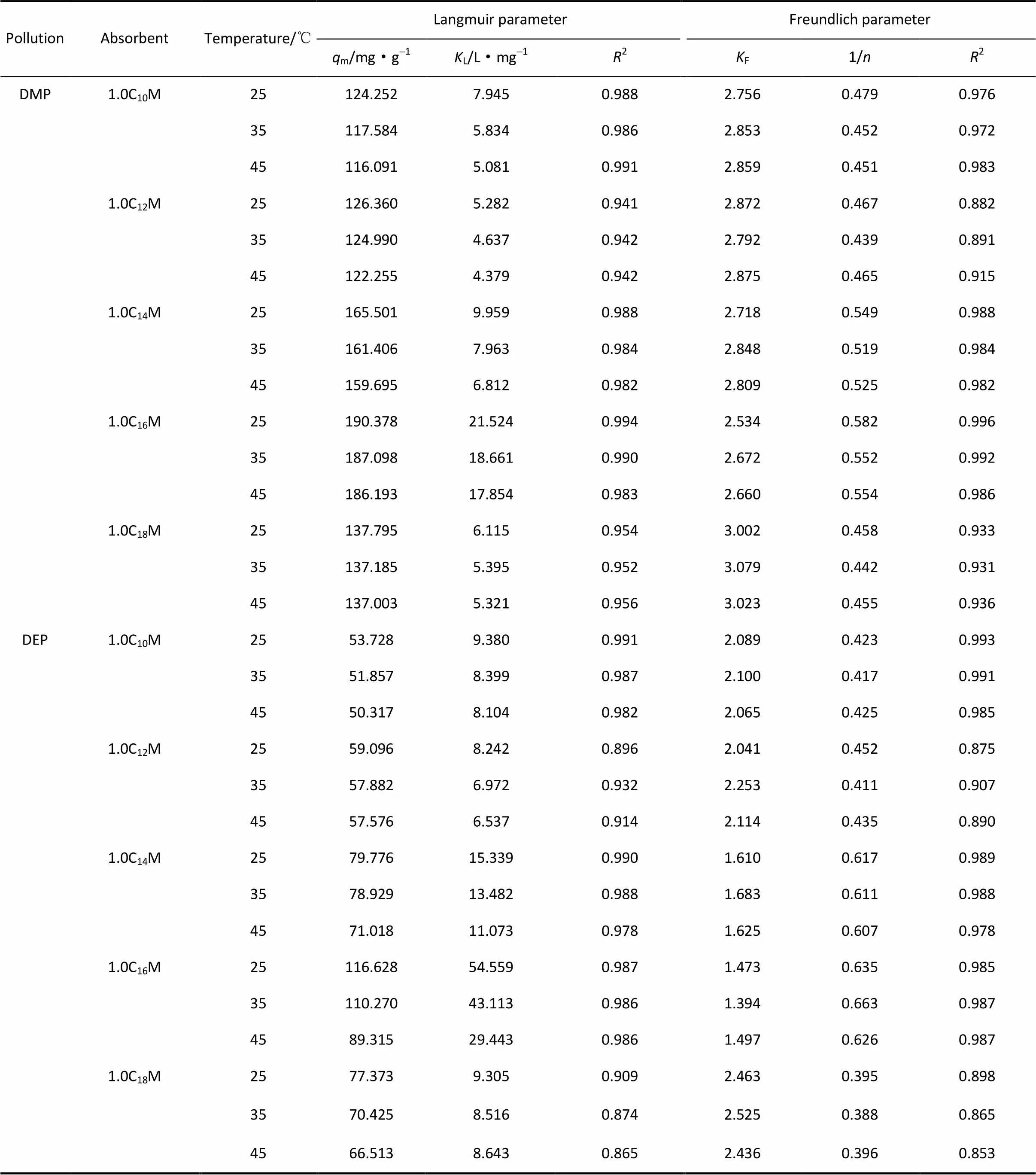
表2 CnTA+/蒙脫石納米復合物吸附等溫模型的擬合參數Table 2 Adsorption isotherm fitting parameters of adsorption isotherm model
從表2中可以看出,CTA+/蒙脫石納米復合物吸附劑對兩種PAEs的吸附線性相關系數2均較高,表明Langmuir方程和Freundlich方程均能在實驗濃度范圍內較好地描述CTA+/蒙脫石納米復合物對水中DMP、DEP的等溫吸附過程。
Langmuir擬合參數中,隨著溫度的升高,最大吸附容量(m)和吸附親和系數(L)減小,分析認為是由于溫度升高使PAEs在水中的溶解度增加而使得吸附容量減小,同時也表明PAEs在CTA+/蒙脫石納米復合物上的吸附過程是物理吸附作用起主導作用[21]。
同種CTA+/蒙脫石納米復合物樣品對DEP的去除率大于對DMP的吸附去除率,即DEP在溶液中更易與有機插層蒙脫石發生吸附,分析認為這是兩種鄰苯二甲酸酯類物質在溶液中的疏水性不同而導致的(lgO/W:DMP,1.66;DEP,2.65)[25],物質的疏水性越強,越易與有機吸附劑發生分配作用[26]。
從Langmuir和Freundlich擬合參數回歸系數2值可知,Langmuir吸附等溫曲線能更好地描述吸附反應過程。Langmuir吸附等溫模型參數中L值的大小與吸附劑、吸附質的性質以及溫度有關,表2中L的值隨著季銨鹽烷基碳鏈長度的增加先增大后減小,說明CTA+/蒙脫石納米復合物的吸附能力受季銨鹽烷基碳鏈鏈長的影響,L值越大,吸附能力越強,最大吸附容量m值也越大[27-28]。
Freundlich吸附等溫模型方程中1/值的大小表示濃度對吸附量影響的強弱。1/越小,吸附性能越好。1/在0.1~0.5,則易于吸附;1/>2時難以吸附。由表2可知,DMP、DEP在CTA+/蒙脫石納米復合物上易于吸附,吸附過程不僅是表面物理吸附作用,還有層間有機物的分配作用或氫鍵作用存在[29-30]。
3 結 論
(1)CTA+/蒙脫石納米復合物能較好地吸附溶液中的兩種PAEs,且對DEP的吸附作用大于對DMP的吸附作用。
(2)Langmuir和Freundlich吸附等溫模型方程均能與實驗數據較好地擬合,吸附屬于自發吸附,吸附作用包括表面吸附作用和有機物質的分配作用。
(3)在吸附過程中,隨著季銨鹽的用量和季銨鹽烷基碳鏈鏈長的增加,對兩種PAEs的去除率先增加后減少。影響的機制是季銨鹽的用量及烷基碳鏈影響CTA+在蒙脫石層間的分布模式,進而影響對兩種PAEs的吸附。
References
[1] Zhou Q, Frost R L, He H, Xi Y. Changes in the surfaces of adsorbed-nitrophenol on methyltrioctadecylammonium bromide organoclay—an XRD, TG, and infrared spectroscopic study [J]., 2007, 314(2): 405-414
[2] Beall G W. The use of organo-clays in water treatment [J]., 2003, 24(1/2): 11-20
[3] Fuller M, Smith J A, Burns S E. Sorption of nonionic organic solutes from water to tetraalkylammonium bentonites: mechanistic considerations and application of the Polanyi-Manes potential theory [J]., 2007, 313(2): 405-413
[4] Xi Y, Frost R L, He H. Modification of the surfaces of Wyoming montmorillonite by the cationic surfactants alkyl trimethyl, dialkyl dimethyl, and trialkyl methyl ammonium bromides [J]., 2007, 305(1): 150-158
[5] Ahmaruzzaman M. Adsorption of phenolic compounds on low-cost adsorbents: a review [J]., 2008, 143(1/2): 48-67
[6] Yui T, Fujii S, Matsubara K, Sasai R, Tachibana H, Yoshida H, Takagi K, Inoue H. Intercalation of a surfactant with a long polyfluoroalkyl chain into a clay mineral: unique orientation of polyfluoroalkyl groups in clay layers [J]., 2013, 29(34): 10705-10712
[7] Zhu J, Shen W, Ma Y, Ma L, Zhou Q, Yuan P. The influence of alkyl chain length on surfactant distribution within organo- montmorillonites and their thermal stability [J]., 2012, 109(1): 301
[8] Chun Y, Sheng G, Boyd S A. Sorptive characteristics of tetraakylammonium-exchanged smectite clays [J]., 2003, 51(4): 415-420
[9] Stales C A, Peterson D R, Parkerton T F, Adams W J. The environmental fate of phthalate esters: a literature review [J]., 1997, 35(4): 667-749
[10] Giam C S, Atlas E, Powers Jr M A, Leonard J E. Phthalic Acid Esters//Anthropogenic Compounds [M]. Berlin: Springer Verlag Berlin Heidelberg, 1984: 67-142
[11] Magdouli S, Daghrir R, Brar S K, Drogui P, Tyagi R D. Di 2-ethylhexylphtalate in the aquatic and terrestrial environment: a critical review [J]., 2013, 127: 36-49
[12] Matsumoto M, Hirata-Koizumi M, Ema M. Potential adverse effects of phthalic acid esters on human health: a review of recent studies on reproduction [J]., 2008, 50(1): 37-49
[13] Martino Andrade A J, Chahoud I. Reproductive toxicity of phthalate esters [J]., 2010, 54(1): 148-157
[14] Julinová M, Slavík R. Removal of phthalates from aqueous solution by different adsorbents: a short review [J]., 2012, 94(1): 13-24
[15] Chen Yancui(陳彥翠), Sun Hongjuan(孫紅娟),Peng Tongjiang(彭同江). Study on montmorillonite intercalated by a series of quaternary ammonium [J].(非金屬礦), 2008, 31(3): 18-21
[16] Favre G L H. Organo-bentonites with quaternary alkylammonium ions [J]., 1991, 26: 19-32
[17] Moraru V N. Structure formation of alkylammonium montmorillonites in organic media [J]., 2001, 19(1-6): 11-26
[18] Heinz H, Vaia R A, Krishnamoorti R, Farmer B L. Self-assembly of alkylammonium chains on montmorillonite: effect of chain length, head group structure, and cation exchange capacity [J]., 2007, 19(1): 59-68
[19] Kwolek T, Hodorowicz M, Stadnicka K, Czapkiewicz J. Adsorption isotherms of homologous alkyldimethyl-benzylammonium bromides on sodium montmorillonite [J]., 2003, 264(1): 14-19
[20] Zhu Jianxi(朱建喜), He Hongping(何宏平), Guo Jiugao(郭九皋), Yang Dan(楊丹), Xie Xiande(謝先德). Study on the relationship between the arrangement models of organic cation in HDTMA+- montomorillonite and its theoretic sizes [J].(礦物巖石), 2003, 23(4): 1-4
[21] Ong L K, Soetaredjo F E, Kurniawan A, Ayucitra A, Liu J, Ismadji S. Investigation on the montmorillonite adsorption of biocidal compounds incorporating thermodynamical-based multicomponent adsorption isotherm [J]., 2014, 241: 9-18
[22] Venkata Mohan S, Shailaja S, Rama Krishna M, Sarma P N. Adsorptive removal of phthalate ester (di-ethyl phthalate) from aqueous phase by activated carbon: a kinetic study [J]., 2007, 146(1/2): 278-282
[23] Peng Changjun(彭昌軍), Jiang Xiuli(姜秀麗), Ji Hongfang(計紅芳), Wang Yuanpeng(王遠鵬), Ouyang Tong(歐陽通), Li Qingbiao(李清彪).Adsorption behavior of Fe-Mn binary oxide towards As(Ⅲ) and As(Ⅴ) and its application in biogas slurry [J].(化工學報), 2014, 65(5): 1848-1855
[24] Xu Xiaoyu(徐曉宇), Sun Yue(孫悅), Shen Jian(沈健), Zhai Yulong(翟玉龍). Adsorption behavior of basic nitrides in model oil on HY and USY [J].(化工進展), 2014, 33(4): 1035-1040
[25] Serodio P, Nogueira J. Considerations on ultra-trace analysis of phthalates in drinking water [J]., 2006, 40(13): 2572-2582
[26] Nguyen T H, Goss K U, Ball W P. Polyparameter linear free energy relationships for estimating the equilibrium partition of organic compounds between water and the natural organic matter in soils and sediments [J].2005, 39(4): 913-924
[27] Wang J, Zhou Y, Li A, Xu L. Adsorption of humic acid by bi-functional resin JN-10 and the effect of alkali-earth metal ions on the adsorption [J]., 2010, 176(1/2/3): 1018-1026
[28] Xu Zhengwen(許正文), Zhao Yunlong(趙云龍), Shi Jing(史靜), Lu Jiangang(陸建剛), Cheng Ling(承玲), Li Saichao(李賽超), Liu Cong(劉聰). Removal of mono--butyl phthalate in aqueous phase by bifunctional polymeric adsorbent NXD-2 [J].(化工學報), 2014, 65(4): 1462-1468
[29] Tang Yini(唐旖旎), Wu Pingxiao(吳平霄), Hou Yakun(侯雅琨). Adsorption properties of salmon sperm DNA on organic and inorganic modified montmorillonite [J].(功能材料), 2012, 43(13): 1712-1717
[30] Liu Zhiping(劉芝平), Zhang Qiangqiang(張嬙嬙), Ma Jinghong(馬靜紅), Li Ruifeng(李瑞豐). Adsorption of-paraffins on mesoporous 5A zeolites [J].(化工學報), 2014, 65(3): 934-941
Effect of chain length and amount of quaternary ammonium salts on CTA+/montmorillonite nanocomposites adsorption of PAEs
LI Li1,2, SUN Hongjuan1,2, PENG Tongjiang1,2
(Key Laboratory of Ministry of Education for Solid Waste Treatment and Resource RecycleSouthwest University of Science and TechnologyMianyangSichuanChina;Institute of Mineral Materials & Application, Southwest University of Science and TechnologyMianyangSichuanChina
Quaternary ammonium salts cation and montmorillonite nanocomposites (CTA+/montmorillonite nanocomposites) were prepared from a series of quaternary ammonium salts with the same structure but different alkyl carbon chain lengths to adsorb phthalate ester (PAEs) in aqueous solution. The effects of CTA+/montmorillonite nanocomposites prepared with different alkyl carbon chain lengths and amounts of quaternary ammonium salts on PAEs adsorption efficiency were investigated. CTA+/montmorillonite nanocomposites as-prepared could adsorb PAEs effectively. Alkyl carbon chain length and amount of quaternary ammonium salts both affected adsorption results. At a smaller amount of quaternary ammonium salts, the adsorption removal of PAEs increased with increasing alkyl chain length of quaternary ammonium salts. However, at a larger amount of quaternary ammonium salts, the adsorption removal of PAEs increased firstly and then decreased with increasing alkyl chain length of quaternary ammonium salts.
quaternary ammonium salts; CTA+/montmorillonite nanocomposites; nanostructure; phthalic esters; aqueous solution; adsorption
2014-09-15.
Prof. SUN Hongjuan, sunhongjuan@swust. edu. cn
10.11949/j.issn.0438-1157.20141376
X 705;X 506
A
0438—1157(2015)03—1042—09
國家自然科學基金項目(41372052);四川省教育廳項目(11ZB103)。
2014-09-15收到初稿,2014-11-15收到修改稿。
聯系人:孫紅娟。第一作者:李莉(1988—),女,碩士研究生。
supported by the National Natural Science Foundation of China (41372052) and the Project in Sichuan Province Department of Education (11ZB103)

