環介導等溫擴增技術檢測HIV-1 DNA
郭宏雄,還錫萍,周 瑩,盧 靜,胡海洋,傅更鋒
(江蘇省疾病預防控制中心性病艾滋病防制所,江蘇南京210009)
環介導等溫擴增技術檢測HIV-1 DNA
郭宏雄,還錫萍,周 瑩,盧 靜,胡海洋,傅更鋒
(江蘇省疾病預防控制中心性病艾滋病防制所,江蘇南京210009)
目的:建立環介導等溫擴增(1oop-mediated isotherma1 amp1ification,LAMP)方法檢測HIV-1 DNA。方法:首先從HIV-1數據庫和基因庫中下載不同亞型的HIV-1的LTR區序列,輸入到MEGA 6.0軟件中,用C1uster W程序進行比對與編輯,選擇相對保守的區域并以FASTA格式輸出。將FASTA格式文件上傳至在線引物設計軟件Lamp primer designing software primer exp1orer中,獲得引物后再次與比對后的HIV序列進行比較,對保守性較差的位點使用簡并堿基。用LAMP擴增試劑盒擴增時加入熒光目測試劑,觀察反應管顏色變化,判斷陰陽性結果。結果:本研究中設計的引物可用于LAMP技術檢測HIV-1 DNA,具有較好的靈敏度和特異性。結論:成功地建立了LAMP技術檢測HIV-1 DNA的方法,可用于HIV-1的早期診斷。
環介導等溫擴增;人類免疫缺陷病毒Ⅰ型;核酸檢測
人類免疫缺陷病毒(human immunodeficiency virus,HIV)自1981年發現以來,已造成近8 000萬人感染,3 300萬人死亡。目前檢測HIV的主要方法是用酶聯免疫分析法(ELISA)進行初篩,用蛋白質印跡進行確認[1-2]。這兩種方法都是檢測感染者體內病毒蛋白的抗體。從病毒感染到抗體產生需要一段時間,即檢測的窗口期。一般情況下,目前的HIV-1第3代檢測試劑的窗口期平均26 d左右[3]。第4代檢測試劑與第3代檢測試劑的不同在于加入P24抗原的檢測。但是由于P24抗原在體內存在的時間短,并且比第3代試劑檢測煩瑣,因此在臨床檢測中目前還是普遍使用第3代檢測試劑[4-6]。在HIV-1感染的窗口期,由于機體產生的抗體滴度太低且抗體的產生過程中需要一個成熟時間,因此ELISA方法并不能檢測到抗體。在艾滋病晚期,患者免疫功能缺陷或低下,機體不能夠產生足夠的抗體。因此用ELISA檢測這個階段的艾滋患者往往出假陰性[7-8]。
核酸檢測能夠檢測血液、體液及組織中的HIV。目前商品化的HIV核酸診斷試劑分為兩類,一類用于血漿HIV-1的定量檢測,一類用于血漿HIV-1的定性檢測。前者主要用于評估抗病毒治療的效果,后者主要用于血液中心采血時對處于抗體檢測窗口期的感染者進行篩查。無論是定量還是定性試劑,除羅氏(ROCHE)公司開發的HIV-1 DNA試劑外,目前市場上銷售的HIV核酸檢測試劑均未用于HIV-1感染的臨床診斷。盡管如此,由于羅氏公司開發的HIV-1 DNA診斷試劑價格太高,并需要昂貴的儀器,因此國內HIV核酸檢測中很少使用[9]。
環介導等溫擴增(1oop-mediated isotherma1 amp1ification,LAMP)方法可以在恒溫下1 h內將核酸擴增到109拷貝,操作簡單、特異性強、反應結果可肉眼觀察,因此具有在現場進行檢驗的潛力[10-14]。為了能夠在一般實驗室開展HIV-1核酸檢測,我們擬建立檢測HIV-1 DNA的LAMP技術方法。
1 材料與方法
1.1 試劑和儀器
環介導的等溫擴增試劑盒和熒光目視檢測試劑盒均購自榮研生物科技有限公司(北京)。DNA提取試劑盒和質粒提取試劑盒(QIAGEN公司,德國)。反轉錄酶Ⅲ(Invitrogen公司,美國)。核酸擴增儀:美國應用生物系統公司Veriti 96孔熱循環儀。
1.2 引物設計
從HIV數據庫(http://www.hiv.1an1.gov/content/index)和基因庫(http://www.ncbi.n1m.nih. gov/genbank/)中下載我國流行的主要HIV-1亞型和重組型的全基因組序列(包括B亞型、C亞型、CRF01_AE、CRF07_BC、CRF08_BC),以FASTA格式保存后導入MEGA 6.0軟件。用C1uster W程序進行序列比對。修剪兩側序列后選擇比較保守的區域。以保守區域為模板設計引物。用Lamp primer designing software primer exp1orer(http://primerexp1orer.jp/e/v4_manua1/)在線引物設計軟件設計引物。引物設計時按Mu1tip1e a1ignment fi1e format要求輸入序列文件。選擇軟件設計的引物,再次與上述亞型的參考序列進行比對,選擇能夠覆蓋多種亞型序列的引物,對個別堿基,由于病毒序列在該處變異較大,則采用簡并堿基。在本試驗中共選擇了2套引物,序列見表1。
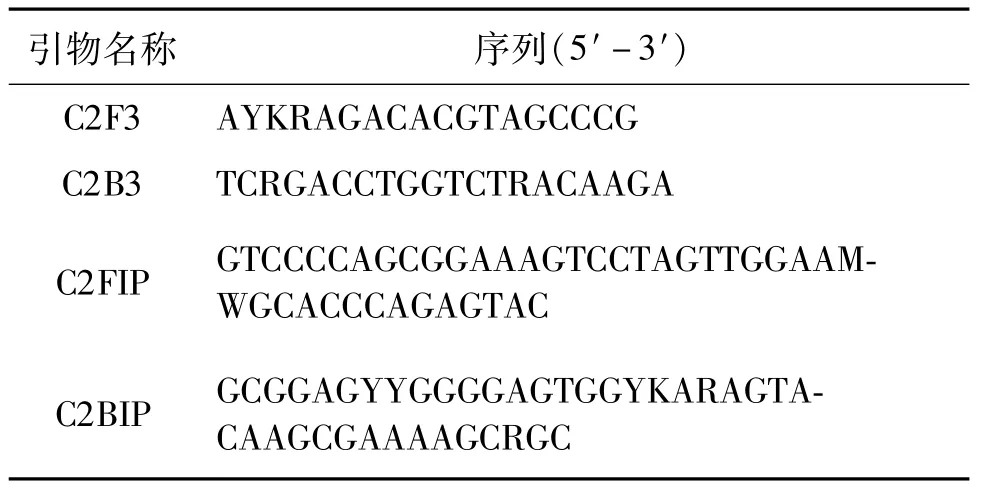
表1 環介導的等溫擴增引物序列
1.3 外周血淋巴細胞樣品的制備和保存
全血樣品3 000 r/min離心15 min,將血漿分別保存至2個2 mL的樣品保存管中,然后吸取白色的淋巴細胞層,保存于-80℃冰箱中備用。
1.4 標準品的配制
將pNL432質粒轉染感受態的DH5α細胞,待長出克隆后挑取一個單菌落接種于5 mL的氨芐西林抗性的LB培養基中。培養16 h后按試劑盒說明書提取質粒。
將稀釋100倍的質粒樣品20 μL加至GeneQuant pro紫外/可見光分光光度計的比色杯中,測定DNA濃度,然后計算提取的質粒DNA原液的濃度。將樣品分別稀釋至106,105,104,103,100,10拷貝/μL。
1.5 核酸的提取
質粒DNA的提取,采用質粒提取試劑盒按照廠家提供的說明書提取。血液中HIV-1 DNA提取用DNA提取試劑盒,按照廠家提供的說明書提取。
1.6 HCV基因組的反轉錄
從臨床樣品中提取HCV RNA基因組后用反轉錄酶Ⅲ反轉錄RNA,制備cDNA樣品,作為特異性試驗時的HCV模板。
1.7 反應體系
引物貯存液的配制:每微升引物貯存液中C2FIP和C2BIP均為400 pmo1,C2F3和C2B3均為50 pmo1。在25 μL體系中加入引物貯存液2.5 μL,2倍的反應緩沖液12.5 μL[含Tris-HCL(pH 8.8)40 mmo1/L,KC1 20 mmo1/L,MgSO416 mmo1/L,(NH4)2SO420 mo1/L,Tween20 0.2%,三甲銨乙內酯1.6 mo1/L,dNTPs各2.8 mmo1/L],Bst DNA聚合酶1.0 μL(10 U),無菌去離子水3.0 μL,熒光目視檢測液1.0 μL,DNA模板5 μL。陽性對照樣品反應體系同上,加入試劑盒中提供的陰性和陽性對照模板5 μL。
2 結果
2.1 LAMP檢測HIV的靈敏度
為了分析本研究中使用的LAMP方法檢測HIV樣品的靈敏度,我們以梯度稀釋配制的標準品為模板。每個反應管中分別加入的起始模板濃度分別為106,105,104,1 000,100,10拷貝/μL的DNA樣品1 μL,總反應體系25 μL。檢測結果如圖1所示,本方法能夠檢測10拷貝的病毒樣品。
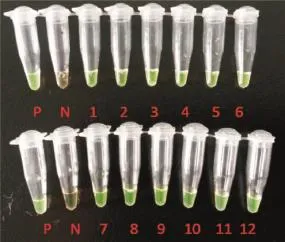
P:陽性對照,N:陰性對照。每管的起始濃度:1-2為106拷貝,3-4為105拷貝,5-6為104拷貝,7-8為103拷貝,9-10為100拷貝,11-12為10拷貝圖1 LAMP檢測HIV的靈敏度
2.2 檢測的特異性分析
為了評價本方法檢測的特異性,我們同時以HIV-1核酸、HBV核酸、HCV核酸為模板,用本方法進行檢測。結果如圖2所示,該方法只能夠擴增HIV-1樣品。在檢測HCV和HBV樣品時不會出現假陽性。
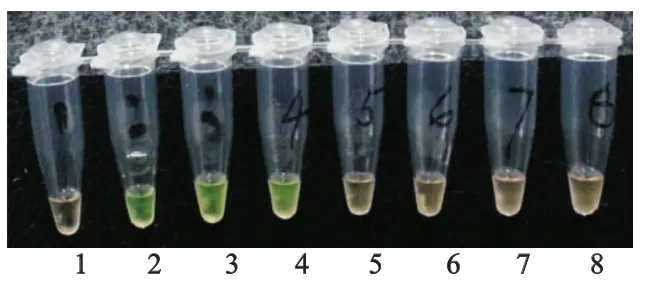
1:陰性對照,2:陽性對照,3-4:HIV-1核酸樣品,5-6:HBV核酸樣品,7-8:HCV核酸樣品圖2 LAMP檢測的特異性
2.3 臨床樣品的檢測
為了評價本方法對我國主要流行株的檢測情況,我們從70例HIV-1感染者的血液中提取HIV-1核酸,各亞型所占比例分別為CRF01_AE 30份、CRF07_BC 15份、CRF08_BC 10份和B亞型15份。所有樣品均經蛋白質印跡實驗確證為HIV-1陽性。檢測結果表明,本研究中建立的LAMP方法對我國流行的主要亞型CRF0_AE、CRF07_BC、CRF08_BC和B亞型HIV-1病毒的檢出率分別為83.3%(25/ 30)、80.0%(12/15)、80.0%(8/10)、93.3%(14/ 15)。應用本方法能夠對84.3%以上的樣品進行檢測,對我國流行的主要亞型均有較好的檢測效果。
3 討論
根據中華人民共和國衛生行業標準WS293-2008艾滋病和艾滋病毒感染診斷標準和全國艾滋病檢測技術規范(2009年修訂版)的規定,在不同時間點采樣,兩次核酸檢測陽性即可確證為HIV-1陽性[1-2]。雖然用于HIV核酸定性的進口診斷試劑有許多,但通過美國FDA認證可用于臨床診斷的HIV-1核酸定性試劑只有羅氏公司生產HIV-1 DNA檢測試劑,該試劑必須在羅氏公司的TMP-CMP平臺上才可使用。該檢測平臺價格昂貴,試劑價格也不菲。因此大大限制了該試劑在臨床診斷中的應用。我國還沒有自由研發的HIV核酸定性診斷試劑可以在開放平臺上使用。因此核酸定性檢測在我國HIV-1的診斷中很少使用。HIV核酸診斷的窗口期不到7天,在HIV感染的早期和艾滋病晚期,感染者體內病毒載量很高,因此傳染性也最強。但在這個階段是以檢測抗體為基礎的ELISA試驗和蛋白質印跡試驗的劣勢。因此建立具有臨床診斷前景的核酸定性診斷試劑在我國HIV預防控制中具有十分重要的意義。
HIV-1病毒分為M、N、O、P四個組,M組病毒占95%以上。在M組中,分為9個亞型和72個重組型[15],國內目前主要的流行株為CRF01_AE、CRF07 _BC、CRF08_BC和B亞型,占到我國HIV-1病毒的98%以上[16]。在本研究中,我們建立的LAMP方法的檢測靈敏度達10拷貝/μL,能夠檢測國內4種主要的亞型和重組型,檢出率達84.3%。當用HCV和HBV病毒核酸作為模板時,不會出現非特異性的擴增,說明LAMP技術具有較好的特異性。盡管該方法能夠檢測84.3%的樣品,但對15.7%的樣品未能檢出,這可能與臨床樣品的制備和保存有關。如在分離外周淋巴細胞時,并未使用淋巴細胞分離液,而是離心后直接吸取白細胞層,由于不同人員操作的熟練程度不同,可能會導致部分樣品中淋巴細胞數量很少,這樣提取的HIV DNA將很少,大大降低了HIV-1的檢出率。因此為了提高通過擴增檢測的成功率,必須優化外周淋巴細胞的制備和保存過程。
在嬰幼兒體內母體抗體消失及自身抗HIV-1抗體的形成需要18個月時間,因此如果通過檢測HIV-1抗體的方法診斷HIV-1的感染需要在18月之后才能進行。已有的研究表明,早期治療能夠大大提高HIV感染嬰幼兒的生活質量和壽命。目前一些單位雖然開展HIV-1的核酸檢測,但使用的方法是自建的方法,實驗室自己設計引物進行PCR,然后電泳檢測。這些方法并未經過中國FDA的認證,在臨床檢測中由于不同檢測單位實驗條件的差異等多種原因很難標準化。本研究建立的等溫擴增方法程序簡單,易于標準化,在HIV感染嬰幼兒的早期診斷方面具有很大的應用前景。
[1] 中國疾病預防控制中心.全國艾滋病檢測技術規范:2009年修訂版[M].2009:5-9.
[2] WS 293—2008.艾滋病和艾滋病病毒感染診斷標準(S).
[3] 周紅,劉麗花.人類免疫缺陷病毒檢測技術及應用進展[J].醫學動物防制,2014,30(2):174-176.
[4] 吉陽濤,韓曉旭,歐陽金鳴,等.三種四代HIV篩查試劑檢測窗口期的差異研究[J].中華檢驗醫學雜志,2014,37(8):613-616.
[5] 吳忠華,鄭偉,呂沁風,等.兩種進口第4代HIV檢測試劑檢測性能評價[J].中國衛生檢驗雜志,2013,23(8):1924-1926.
[6] Krajden M,Cook D,Mak A,et a1.Poo1ed nuc1eic acid testing increases the diagnostic yie1d of acute HIV infections in a high-risk popu1ation compared to 3rd and 4th generation HIV enzyme immunoassays[J].J C1inica1 Viro1ogy,2014,61(1):132-137.
[7] Pate1 P,Macke11ar D,Simmons P,et a1.Detecting acute human immunodeficiency virus infection using 3 different screening immunoassays and nuc1eic acid amp1ification testing for human immunodeficiency virus RNA,2006-2008[J].Arch Intern Med,2010,170(1):66-74.
[8] Masciotra S,McDouga1 JS,Fe1dman J,et a1.Eva1uation of an a1ternative HIV diagnostic a1gorithm using specimens from seroconversion pane1s and persons with estab1ished HIV infections[J].J C1in Viro1,2011,52(Supp1 1):S17-22.
[9] John B,Lupiwa T,To1iman P,et a1.Va1idation of the Roche AMPLICOR HIV DNA test version 1.5 for ear1y infant diagnosis of HIV in Papua New Guinea[J].P N G Med J,2012,55(1-4):16-23.
[10] Notomi T,Okayama H,Masubuchi H,et a1.Loop-mediated isotherma1 amp1ification of DNA[J].Nuc1eic Acids Res,2000,15,28(12):e63.
[11] Hamburger J,Abbasi I,Kariuki C,et a1.Eva1uation of 1oop-mediated isotherma1 amp1ification suitab1e for mo-1ecu1ar monitoring of schistosome-infected snai1s in fie1d 1aboratories[J].Am J Trop Med Hyg,2013,88(2):344-351.
[12] Fakruddin M,Mannan KS,Chowdhury A,et a1.Nuc1eic acid amp1ification:A1ternative methods of po1ymerase chain reaction[J].J Pharm Bioa11ied Sci,2013,5(4):245-252.
[13] Sing1eton J,Osborn JL,Li11is L,et a1.E1ectricity-free amp1ification and detection for mo1ecu1ar point-of-care diagnosis of HIV-1[J].PLoS One,2014,9(11):e113693.
[14] Niemz A,Ferguson TM,Boy1e DS,et a1.Point-of-care nuc1eic acid testing for infectious diseases[J].Trends Biotechno1,2011,29(5):240-250.
[15] He X,Xing H,Ruan Y,et a1.A comprehensive mapping of HIV-1 genotypes in various risk groups and regions across China based on a nationwide mo1ecu1ar epidemio1ogic survey[J].PLoS One,2012,7(10):e47289.
[16] De Cock KM,Jaffe HW,Curran JW.The evo1ving epidemio1ogy of HIV/AIDS[J].AIDS,2012,26(10):1205-1213.
Development of detecting HIV-1 DNA using loop-mediated isothermal amplification
GU0 Hong-xiong,HUAN Xi-ping,ZH0U Ying,LU Jing,HU Hai-yang,FU Geng-feng
(Department of STD and AIDS Contro1 and Prevention,Jiangsu Provincia1 Center for Disease Contro1 and Prevention,Nanjing Jiangsu 210009,China)
Objective:To deve1op method of detecting HIV-1 DNA using 1oop-mediated isotherma1 amp1ification.Methods:First1y,the LTR sequences of various subtypes and circu1ating recombinant forms(CRFs)were down1oaded from HIV-1 database and GeneBank on1ine,these sequences were imported into MEGA 6.0 software and the a1ignment of sequences were conducted with C1uster W program.The re1ative conservative region were se1ected and exported as a FASTA fi1e.FASTA fi1e were submitted into Lamp primer designing software primer exp1orer on1ine.The a1ignment of the primers with HIV-1 sequences were performed to seek the 1ess conservative sites,if so,the mixed bases were used.When conducting LAMP,visib1e f1uorescence reagent was used to observe the resu1t of amp1ification.Results:The primers designed in this study was suitab1e in detecting HIV-1 DNA using LAMP,and showed better sensitivity and specificity.Conclusion:we successfu11y deve1oped a LAMP to test HIV-1 DNA,this method may be used to ear1y diagnose HIV-1 infection.
1oop-mediated isotherma1 amp1ification;HIV-1;nuc1eic acid
R512.91
A
1671-7783(2015)06-0528-04
10.13312/j.issn.1671-7783.y150196
2015-09-09 [編輯] 何承志
江蘇省衛生廳科教興衛工程重點人才課題(RC2011083)
郭宏雄(1972—),男,甘肅秦安人,副研究員,博士,主要從事傳染病分子流行病學與核酸診斷研究。

