大鼠皮質受損區域Cdk5與細胞凋亡的相關性研究
蔡學堅王東軍陳苑新魏長新黃劍
大鼠皮質受損區域Cdk5與細胞凋亡的相關性研究
蔡學堅①王東軍②陳苑新①魏長新①黃劍①
目的:研究皮質受損區域細胞周期素依賴蛋白激酶5(Cyclin-dependent kinase 5,Cdk5)與細胞凋亡的關系。方法:采用Feeney’s自由落體模型制作大鼠顱腦損傷模型,隨機分為2 h、1 d、3 d及7 d組,用免疫組化的方法檢測創傷性腦損傷后受損腦皮質區域中Cdk5的表達情況;TUNEL方法檢測該區域神經細胞的凋亡情況;WesternBlotting方法檢測蛋白Cdk5時序表達水平變化的情況。結果:大鼠受損皮質區域Cdk5表達隨時間增加而增加,7 d達到高峰;受損皮質區域凋亡陽性細胞變化趨勢與Cdk5基本一致;細胞凋亡系數與Cdk5呈正相關性(r=0.88,P<0.05)。對照組無明顯變化。結論:大鼠皮質區域損傷可誘導Cdk5數量及激酶活性增加,從而參與神經細胞凋亡。
顱腦損傷; 細胞周期素依賴蛋白激酶5; 細胞凋亡
Cdk5為絲/蘇氨酸胞周期素依賴蛋白激酶(Cyclin-dependent kinase,Cdk)家族一類成員,存在于神經系統中,含292個氨基酸殘基,相對分子質量為33×103,激活后可磷酸化不同的相關底物。到目前為止鑒定出的Cdk5底物約有20余種,包括蛋白激酶K、Tau蛋白、神經絲蛋白及β-連環蛋白等[1-5]。近年來,在腦缺血再灌注損傷研究中發現Cdk5是神經細胞凋亡過程中重要的上游因子[6-7]。然而,到目前為止關于Cdk5與細胞凋亡的相關性在大鼠損傷模型中國內外鮮有報道,因此闡明顱腦損傷后Cdk5與細胞凋亡的相關性,對臨床尋找新的治療靶點有重要意義。
1 材料與方法
1.1 試劑 免疫組化染色試劑盒:北京中杉金橋生物公司。Anti -Cdk5:貨號bs-1090R,北京博奧森。DAB顯色試劑盒:北京中杉金橋生物公司。PVDF膜(0.22um)品牌pall:廣州譽維生物科技儀器有限公司。TUNEL凋亡檢測試劑盒:武漢博士德生物工程有限公司。
1.2 實驗動物及分組 將大鼠48只(雄性,體重180~220 g,來源于南方醫科大學實驗動物中心)隨機分為兩組,即造模組(顱腦損傷組)和對照組(空白組)各24只,各組再隨機均分為4個小組(n=6);各小組時間點確定在損傷后2 h、1 d、3 d及7 d(以縫合頭皮結束開始計時為0時)。實驗過程中不符合實驗要求的大鼠予以相應替換。
1.3 大鼠顱腦損傷模型的制作方法 造模組采用Feeney’s自由落體模型制作大鼠顱腦損傷模型(Trauma Brain injure,TBI)。大鼠麻醉成功后固定,在無菌條件下操作,選取左頂部前囟點和人字點中間偏離正中線約3.5 mm處縱形切開頭皮,持牙科鉆去除骨瓣,大小約0.6 cm×0.6 cm,注意勿損傷硬腦膜。安裝自由落體撞擊裝置,撞擊點設為左側頂葉皮層,祛碼重量為20 g,撞擊高度為30 cm,撞擊力為600 g·cm,制造中度顱腦損傷模型。撞擊后行傷口及板障止血后縫合頭皮。對照組僅切開頭皮打開骨窗并行傷口板障止血后即縫合頭皮。大鼠處死前行大鼠神經運動功能評分。
1.4 標本的處理及切片的制備 用3%戊巴比妥鈉(45 mg/kg)腹腔注射麻醉大鼠后打開胸腔,用PBS緩沖液經左心室灌注,打開右心耳至留出清亮液體,再用4%多聚甲醛PBS緩沖液10~15 d/min灌注,處死動物并固定60 min后斷頭。在冰盒上快速開顱取腦,切取左側損傷側大腦,再以損傷灶為中心冠狀面水平切取左側大腦為前后兩半,一半行切片免疫組化檢查,另一半行Western Blotting蛋白檢測。行切片免疫組化檢查的受損區域腦組織用石蠟包埋,然后以冠狀位由損傷皮質區中心向后連續切片,切片厚約5 μm。另外一半行Western Blotting蛋白檢測的腦組織行受損區
域腦皮質分離,在冰盒上操作,剝離硬腦膜,用小鑷子從切面處將腦皮質向外側分離,完整分離出腦皮質,放入凍存管,做好標記,保存于-80 ℃液氮瓶里。
1.5 免疫組織化學染色 石蠟切片行免疫組化染色,方法為兔超敏二步法,切片用3%的H2O2封閉10 min后,用pH=6.0的枸橘酸溶液加熱孵育15 min行抗原修復。冷卻至室溫后用5%山羊清室溫封閉20 min。滴加Cdk5一抗4 ℃過夜。PBS清洗后依次滴加試劑1和試劑2室溫孵育20 min。DAB顯色劑顯色,沖洗,蘇木素復染,常規乙醇脫水,二甲苯透明,中性樹脂封片。Cdk5的表達均以細胞漿和胞膜內側出現黃色或棕黃色著色為陽性。
1.6 Western Blotting蛋白檢測 蛋白提取試劑盒提取冰凍腦皮質組織(約80mg)總蛋白,BCA法測定蛋白濃度,蛋白定量試劑盒進行蛋白定量,蛋白濃度定量到每孔60 μg。依次加入5 x上樣緩沖液煮沸(94 ℃,10 min)、上樣(每孔30 μL)、電泳、轉膜、封閉;Cdk5一抗(比例1:300)4 ℃冰箱孵育過夜16 h,TBST洗膜5 min×5次,滴加山羊抗兔二抗(比例1∶6000),常溫搖床1 h,TBST洗膜5 min×5次,ECL發光顯色,膠片曝光,掃入凝膠成像系統進行灰度比值分析。
1.7 TUNEL法檢測細胞凋亡 組織切片入新鮮配制的4%多聚甲醛室溫固定30 min;PBS洗3次,5 min/次;入3%過氧化氫溶液甲醇中30 min以封閉內源過氧化物酶;入0.1%Triton X-100枸櫞酸鈉緩沖液中冰浴2 min;PBS洗滌3次;加TUNEL反應混合液37 ℃反應1~1.5 h;PBS沖洗3次;加POD反應液37 ℃ 30 min;PBS沖洗3次;DAB顯色5~10 min;蘇木精復染核,脫水,透明,封片,鏡檢。染色結果判定:結果判定以胞核、胞質中有棕黃色或者棕褐色顆粒者為陽性細胞。計算神經細胞凋亡指數(apoptosis index,AI)。
1.8 統計學處理 采用SPSS 16.0統計軟件進行分析。計量資料用(±s)表示,兩樣本均數間比較采用t檢驗(t-test);雙變量關聯性分析采用直線相關方法分析。P<0.05表示差異有統計學意義。
2 結果
2.1 大鼠顱腦損傷模型結果的觀察 48只大鼠實驗過程中發現,除對照組24只外,造模組24只大鼠均出現不同程度神經功能缺損癥狀體征,表現為不同程度的肢體功能癱瘓,出現意識障礙的有4只。開顱取出大腦后見撞擊點出現腦挫裂傷灶(見圖1)。參照Longa等[8]大鼠神經功能缺損評分方法,選取評分為1~3分的動物損傷模型組及參照組。

圖1 大鼠TBI模型的整體觀
2.2 免疫組化染色 損傷側Cdk5陽性細胞隨著時間的增加而增多,損傷后2 h、1 d、3 d及7 d時間點各組間比較差異均有統計學意義(P<0.05);而對照組各組間比較差異無統計學意義(P>0.05)。見表1、圖2、圖3。

表1 造模組和對照組大鼠腦皮質區Cdk5的免疫組化實驗iOD值(累計光密度)(x-±s)
2.3 TUNEL法檢測 損傷側TUNEL陽性細胞隨著時間的增加而增多,損傷后2 h或1 d與3 d及7 d時間點各組間比較差異均有統計學意義(P<0.05),而2 h與1 d兩組間比較差異無統計學意義(P>0.05);而對照組各組間比較差異無統計學意義(P>0.05)。見表2、圖4、圖5。
2.4 相關性統計分析 造模組免疫組化染色及TUNEL檢測結果的直線相關性分析顯示:Cdk5的表達水平與細胞凋亡系數AI%存在正相關性,Pearson積距相關系數r=0.88,P<0.05。見圖6。
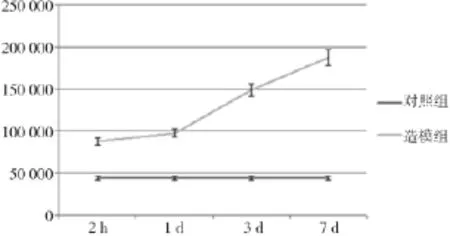
圖2 造模組和對照組大鼠腦皮質區Cdk5的免疫組化實驗iOD值比較
2.5 Western blot 定量分析損傷不同時間點Cdk5的表達。隨著時間的增加,造模組的Cdk5表達量增加。見圖7。

表2 大鼠腦皮質區TUNEL細胞凋亡AI%
3 討論

圖3 大鼠皮質受損區域Cdk5免疫組化圖
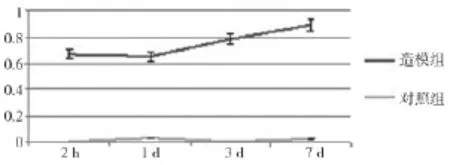
圖4 大鼠腦皮質區TUNEL細胞凋亡AI%時序圖
細胞凋亡是指細胞在一定的生理或病理情況下,在自身基因調控下按照自身的程序出現的主動死亡過程,與細胞壞死不同,由Kerr等[9]在1972年提出。1995年Rink等[10]發現在顱腦損傷模型大鼠的腦皮質等大腦區域均出現凋亡的神經細胞,從而證實創傷性腦損傷后存在細胞凋亡。在TBI后幾小時至數周內,大腦皮質、海馬和紋狀體等中樞神經系統一般都有神經元的丟失和損傷,其中常見的病理改變為核濃縮及皺縮[11]。

圖5 大鼠皮質受損區域TUNEL圖
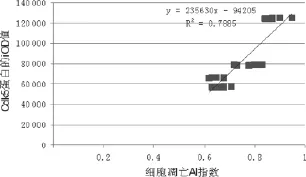
圖6 造模組Cdk5蛋白的iOD值與細胞凋亡AI指數的相關性線圖

圖7 造模組4個時間點Cdk5的WB結果
越來越多的實驗證明,Cdk5與神經細胞凋亡的關系更加密切,它是神經細胞凋亡的重要上游因子[7]。研究發現,小鼠短暫性腦缺血后,Cdk5活性和P25表達增加與海馬CAl區的神經細胞凋亡有關[12]。Sakaue等[13]應用二甲基汞誘導大鼠小腦顆粒培養細胞死亡,
證實低濃度二甲基汞可導致胞內Ca2+內流增多,使胞內calpain激活,將p35裂解成p25,形成P25-Cdk5復合體,從而使神經細胞凋亡。可見,調控Cdk5活性對神經細胞凋亡的影響已成為研究的熱點。
Cdk5特定調節因子為分子量為34.8 kD的非周期素蛋白P35,其特異地存在于中樞神經系統中。P35主要存在于大腦皮質,并存在于細胞膜組分中。P35為不穩定蛋白質,半衰期只有20~30 min,泛素化后被激活的蛋白酶裂解而失活。在興奮性氨基酸及自由基等刺激下,被鈣激活蛋白酶(Calpain)裂解成P25和另一10 kD片段[14],P25半衰期比P35長5~10倍,具備完全激活Cdk5的功能,且激活能力更強,可造成Cdk5不可調控性激活[14-15]。顱腦損傷后,被激活的Cdk5可結合多種細胞凋亡相關底物,啟動不同的凋亡途徑,引起神經細胞凋亡。
本研究表明大鼠皮質區域損傷后,Cdk5的活性表達與神經細胞凋亡呈正相關性。通過免疫組化及免疫印跡法筆者觀察到大鼠皮質區域損傷后2 h即有Cdk5表達增加,與此同時通過TUNEL法亦觀察到在2 h組即有凋亡細胞出現;隨后從2 h~1 d時間段Cdk5活性及凋亡細胞的數量均呈現平緩上升;2 d開始Cdk5表達活性急劇上升,腦細胞損傷也呈現迅速擴大趨勢,表現為凋亡細胞數量急劇增加,1 d組可稱為腦損傷后的一個“拐點”;其后兩者逐漸上升,于7 d達到觀察范圍內的高峰。這與通過時間-量變分析表明Cdk5與凋亡細胞之間有高度相關性的研究相符合[16]。結果提示,顱腦損傷后2 h之前可能是顱腦損傷誘發各種損傷因子形成初級階段,是引發進一步腦損傷的重要拐點;因此進一步研究由Cdk5引導的顱腦損傷后神經細胞凋亡新途徑有可能找到新的治療靶點及有效時間窗。
總之,顱腦損傷后Cdk5與神經細胞凋亡密切相關,為顱腦損傷的臨床治療提供新的實驗依據。如果能夠尋找到Cdk5特異性抑制劑,抑制其活性,對于進一步探討Cdk5與細胞凋亡的關系和尋找顱腦損傷新的治療方法具有重要的意義。
[1] Ishiguro K, Kobayashi S, Omori A, et al. Identification of the 23 kDa subunit of Tau protein kinase II as a putative activator of CDK5 in bovine brain[J]. FEBS Lett, 1994, 342(15):203-208.
[2] Pigino G, Paglini G, Bulloa L, et al. Analysis of the expression/ distribution and function of cyclin dependent kinase (cdk5) in developing cerebellar macroneurons[J]. J Cell Sci, 1997, 110(45):250-270.
[3] Paglini G, Pigino G, kunda P, et al. Evidence for the participation of theneuronspecific cdk5 activator p35 during lamininenhanced a xonal growth[J]. J Neurosci, 1998, 18(156):9858-9869.
[4] Paudel H K, Lew J, Ali Z, et al. Brain prolinedirected protein kinase phlsphorylates Tau on sites that are abnormally phosphorylated in tau Associated with Alzheimer’s paired helical filaments[J]. J Biol Chem,1993, 268(256):23 512-23 518.
[5] Baumann K, Mandelkow E M, Biemat J, et al. Abnormal alzheimerlike phosphorylation of tauprotein by cylin-dependent kinases cdk2 and cdk5[J]. FEBS Lett,1993, 336(568):417-424.
[6] Nguyen M D, Mushynski W E, Julien J P, et al. Cycling at the interface between neurodevelopment and neurodegeneration[J].Cell death differ, 2002,9(15):1294-1306.
[7] Weishaupt J H, Neusch C, Bhr M, et al. Cyclin-dependent kinase 5(cdk5) and neuronal cell death[J]. Cell Tissue Res , 2003, 312(98):1-8.
[8] Longa E Z, Weinstein P R, Carlson S, et al. Reversible middle cerebral artery occlusion without craniectomy in rats[J]. Stroke, 1989,20(1):84-91.
[9] Kerr J F R, Wyllie A H, Currie A R, et al. Apoptosis:a basic biological phenomenon with wide-ranging implications in tissue kinetics[J]. Br J Cancer, 1972, 26(54):239-257.
[10] Rink A,Fung K M,Rojanowski J Q,et al.Evidence of apoptosiscell death after experience traumatic brain injure in rat[J].Am Jpathol,1995,147(6):1575.
[11] Takizama H, Gabra-Sanders T, Milledr J D, et al. Analysis of changes in intracranial pressure and pressure volume index at different locations in the cranio spinal axis during supratentorial epidural balloon inflation[J]. Neurosurg, 1986, 19(1):1-8.
[12] Jian Wang, Shuhong Liu, Yangping Fu, et al. Cdk5 activation induces hippocampal CA1 cell death by directly phosphorylating NMDA receptors[J]. Nature neurosci, 2003,6(45):1039-1047.
[13] Sakaue M, Okazaki M, Hara S, et al. Very low levels of methylmercury induce cell death of cultured rat cerebellar neurons via calpain activation[J]. Toxicology, 2005, 213(1-2): 97-106.
[14] Patzke H, Tsai L H. Cdk5 sinks into ALS[J]. Trends Neurosci, 2002,25(45):8-10.
[15] Patrick G N, Zukerberg L, Nikolic M, et a1.Conversion of p35 to p25 Deregulates cdk5 activity and promotes neurodegeneration[J].Nature,1999,402(6762):615-622.
10.3969/j.issn.1674-4985.2015.08.006
2014-11-11) (本文編輯:陳丹云)
①廣東省東莞市大嶺山醫院 廣東 東莞 523819
②廣東醫學院
王東軍

