體育運動中結締組織生長因子對肌腱干細胞分化的影響
竇海波,文秀麗
體育運動中結締組織生長因子對肌腱干細胞分化的影響
竇海波,文秀麗
肌腱是連接骨骼和肌肉的結締組織,在神經的支配下可完成有效的動作。肌腱主要由成纖維細胞和胞外基質組成,本身為致密結締組織,其胞外基質主要由I型和II型膠原組成,是致密而平行排列的膠原纖維束,纖維之間由少量的蛋白多糖與糖胺聚糖相連接。以往的研究認為肌腱是一種惰性組織,代謝并不活躍。然而,近來的多項研究表明,肌腱內同樣存在著活躍的代謝過程,運動可對肌腱的組織形態、力學性能和代謝過程產生重要的影響[1]。其中,肌腱成纖維細胞起著重要作用,其可將肌腱組織所承受的力學負荷轉化為電信號,并將力學刺激在細胞間傳遞,從而調控對肌腱的動態更新和平衡1。
隨著干細胞研究的深入,肌腱干細胞可以從人、大鼠、小鼠等一系列哺乳動物的肌腱中分離獲得。肌腱干細胞相比成纖維細胞體型較小,呈靜電的鵝卵石狀,表達包括OCT4、SSEA-4、CD29、CD44等多種干細胞表面標記物2。且有研究發現CD44是多種組織損傷后修復期的標志[2]。同時,肌腱干細胞通過不對稱分裂,有效的補充肌腱內成纖維細胞,保持整個肌腱的動態活性平衡,因而對整個肌腱起著至關重要的作用。研究表明,肌腱干細胞具有多向分化潛能,可以向骨、軟骨、脂肪和肌腱成纖維細胞分化3。對于調控肌腱干細胞定向分化的信號機制及誘導因素并不十分明確,但是細胞生長的微環境及各種外界刺激對干細胞的分化方向有重要的影響。目前有研究表明肌腱干細胞可以受力學刺激、生物活性因子等影響,從而進行分化、胞外基質分泌和促進肌腱組織形成[3]。
在體育運動中,急性和慢性的肌腱損傷比較常見,由于肌腱自身再生能力較差,肌腱損傷后恢復后比較緩慢,而傳統治療再生的肌腱主要是瘢痕組織構成,很難恢復結構的完整性及滿足生理活動所需的強度2。因而尋求有效的治療方法,促進肌腱干細胞向肌腱成纖維細胞分化是一種迫切的辦法。因此,尋求有效的治療方法尤為重要。促進肌腱干細胞向肌腱成纖維細胞分化是一種迫切的辦法。結締組織生長因子(Connective tissue growth factor,CTGF)是1991年首先在人臍靜脈內皮細胞中發現的,由349個氨基酸組成。最初發現CTGF對成纖維細胞具有趨化及促進有絲分裂的作用,后來的研究發現,CTGF可對不同的細胞具有促進細胞增殖、遷移和分化等作用[4]。由于它們在創傷修復中的特殊意義,尤其是人CTGF可以啟動一系列介導組織創傷修復和再生的生物學過程4,故具有潛在的應用前景5。近年來,也有研究者發現CTGF對骨髓間充質干細胞向成纖維細胞分化的作用,發現其有促進干細胞向成纖維細胞分化的作用[5]。因此將從大鼠肌腱中分離肌腱干細胞,并研究CTGF對其向肌腱成纖維細胞分化的影響。
1 研究對象與方法
1.1 研究對象
研究對象是結締組織生長因子在體育運動中對肌腱干細胞分化的影響。
1.2 研究方法
1.2.1 實驗法
1)實驗材料。DMEM培養基和胎牛血清購自GIBCO公司;Trizol試劑盒以及所有的反轉錄試劑均購自北京Invitrogen生物技術服務有限公司;PCR引物由北京賽百盛生物有限公司合成;鼠抗人CD44、CD29抗體購自Bethyl Laboratories公司;兔抗人GAPDH和羊抗大鼠多克隆tenascin C抗體(1:100),小鼠抗大鼠多克隆Ⅰ型膠原抗體(1∶100)抗體、辣根過氧化物酶偶聯的IgG抗體購自SantaCruz公司。
2)細胞分離及培養。實驗取1只150g雄性大鼠,腹腔麻醉后,取大鼠雙側跟腱組織,提取周圍結締組織并將其剪碎至大小為1mm×1mm×1mm,然后將組織平鋪至培養皿,加入含100u/mL青霉素、100U/mL鏈霉素的10%胎牛血清的DMEM培養基,在37℃、5%CO2的條件下培養。3天后,細胞從組織塊周圍遷移出來,繼續培養5-7天,待細胞密度達80%時,胰酶消化、傳代。取P2-P3代進行相關實驗。
3)CD44、CD29細胞免疫熒光染色。取P2代細胞爬片,以2×104個/mL密度接種于24孔板,加300μL10%胎牛血清的DMEM培養基,37℃、5%CO2條件下培養,待細胞密度達60% -70%時,取兩孔細胞,行免疫細胞化學檢測細胞表型抗原標記CD44、CD29,方法如下:PBS洗3次,4%多聚甲醛固定30min,PBS洗3次,加入含0.5%Triton100和1%羊血清的PBS,冰上滲透10m in;再用含1%羊血清的PBS封閉,然后兩孔分別加鼠抗人CD44、CD29,一抗4℃過夜。去除一抗,PBS沖洗,加FITC標記山羊抗小鼠二抗反應液,室溫1 h,避光。去除二抗,PBS沖洗。甘油封片,熒光顯微鏡下觀察細胞膜。
4)肌腱干細胞多向分化能力鑒定。取P3代細胞接種于6孔板,每孔分別加入2m l的成脂和成骨誘導培養液,分別培養至14天和21天,然后分別進行油紅和茜素紅染色,觀察其成脂和成骨情況。同時收集一部分分離提取的肌腱干細胞,3 000rpm,離心10min,去上清,并用成軟骨誘導培養液重懸,制成細胞團。誘導28天,進行阿利斯藍染色觀察軟骨形成情況。備注:成骨誘導培養液含DMEM、10%FBS、1%PSN、0.1μmol/L地塞米松、0.2mmol/L維生素C及10mmol/Lβ甘油磷酸。成軟骨分化:含無血清DMEM、0.1μmol/L地塞米松、0.2mmol/L維生素C、1mmol/L丙酮酸鈉、1∶100胰島素-鐵傳遞蛋白-硒稀釋液、10ng/mLTGF-β1。成脂分化:含DMEM、10%FBS、1%PSN、1×10-6 mol/L地塞米松、0.5mmol/L甲基異丁基黃嘌呤及50μmol/L吲哚美辛。
5)總RNA的提取。收集未處理的肌腱干細胞和分化后的肌腱細胞,用PBS洗1遍后吸去,加1mLTrizol后,用槍吹打后吸入EP管中。室溫放置5min,使其充分裂解。按200μL氯仿/ mLTrizol加入氯仿,振蕩混勻后室溫放置15min。4℃12 000g離心15min。吸取上層水相至另一離心管中。按0.5mL異丙醇/ mLTrizol加入異丙醇混勻,室溫放置5-10min。4℃12 000g離心10min,棄上清,RNA沉于管底。按1mL 75%乙醇/mLTrizol加入75%乙醇,溫和振蕩離心管,懸浮沉淀。4℃8 000g離心5min,盡量棄上清。室溫晾干干燥5-10min。用50μLDEPC水溶解RNA樣品,55-60℃,5-10min。測O.D值定量RNA濃度。
6)實時定量PCR。取500ngRNA根據First Strand cDNA kit的方法進行反轉錄,將獲得的cDNA稀釋10倍。然后,用qPCR試劑盒SYBR premix Ex Taq進行PCR擴增反應。βactin上游引物:5′-ATCGTGGGCCGCCCTAGGCA-3′;下游引物:5′-TGGCCTTAGGGTTCAGAGGGG-3′。
Tenascin C 上 游 引 物 :5′-CAGAAGCTGAACCGGAAGTTG-3′;下游引物:5′-GGCTGTTGTTGCTATGGCQCT-3′。Ⅰ型膠原 (Collagen type I)上游引物:5′-CTGGATCATATTGCACA-3';下游引物:5′-CATCGGTGGTACTAAC-3′。上述引物均由北京賽百盛基因技術有限公司合成。取之前合成的cDNA作為模板,上游引物下游引物各取0.4μl,SYBRμ-Green Master Mix 10.2μl。將上述樣品加入到專用的PCR管中,PCR反應條件為:95℃15min,94℃15s,55℃30s,70℃30s,40 ycles。利用熒光實時定量PCR儀(CFX96,BiO Rad公司)進行反應,后對其熔解曲線進行分析,并計算出基因表達的相對量。
7)Western印跡。收集未處理的肌腱干細胞和分化后的肌腱細胞,加入SDS加樣緩沖液,煮沸10m in,離心后取上清液進行SDS-PAGE,電轉移至硝酸纖維素膜,用5%脫脂奶粉于4℃封閉1h,加入用5%脫脂奶粉1∶1 000稀釋的I型膠原抗體和 1∶1 000稀釋的 Tenascin-C抗體或 1∶10 000稀釋的GAPDH抗體,室溫輕搖1h,TBST洗膜3次,每次7min,加入用5%脫脂奶粉稀釋的辣根過氧化物酶偶聯的羊抗兔IgG,室溫輕搖1h,TBST洗膜3次,每次7min,用化學發光法顯色5min,壓片顯影。
1.2.2 數理統計法
采用SPSS統計軟件包16.0進行統計學分析。所有實驗數據均以平均值±標準差表示,兩組之間比較采用t檢驗,以P<0.05認為有統計學意義。
2 結果與分析
2.1 肌腱干細胞的分離和鑒定
分離得到的組織細胞呈梭狀,如圖1A所示。同時免疫熒光染色檢測顯示,細胞表面抗原CD29和CD44呈陽性反應,如圖1B所示。表明提取的組織細胞為肌腱干細胞。
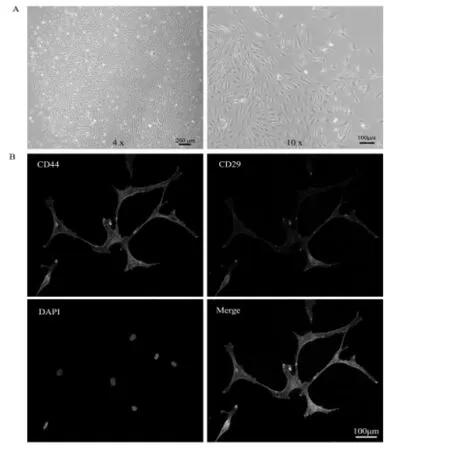
圖1 分離出的肌腱干細胞圖
2.2 肌腱干細胞可向脂肪細胞、骨細胞、軟骨細胞分化
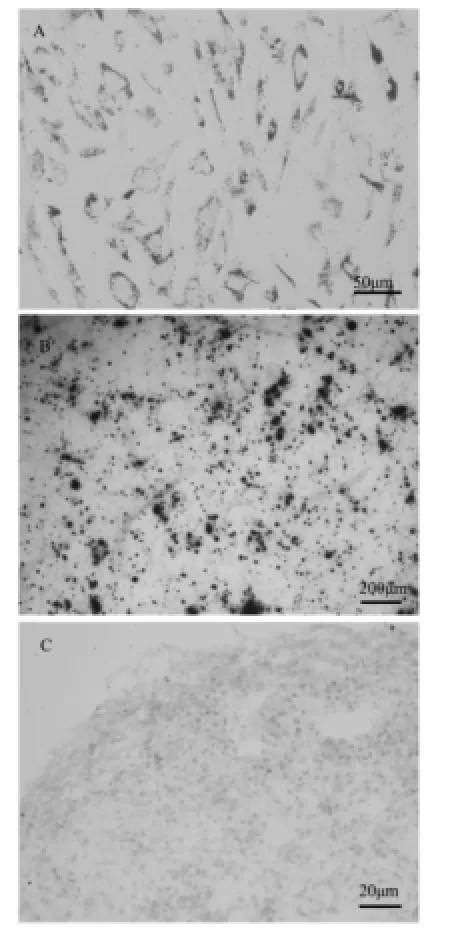
圖2肌腱干細胞分化圖
肌腱干細胞在分化14天后,大量的細胞開始分泌油滴,油紅染色可見明顯脂質空泡形成,如圖2A所示,表明分離的肌腱干細胞具有向脂肪細胞分化的能力;同時肌腱干細胞在分化21天后,茜素紅染色顯示可見明顯鈣結節形成,如圖2B所示,表明大量的細胞可以分化為成熟的成骨細胞;同時細胞球內的細胞開始分泌大量的軟骨胞外基質,阿爾新藍染色可見細胞外有明顯的軟骨樣基質生成并呈藍染,如圖2C所示,表明大量的細胞可以分化為成熟的軟骨細胞。
2.3 結締組織生長因子可促進肌腱干細胞向成纖維細胞分化
I型膠原和Tenascin-C是成纖維細胞的蛋白標志物。我們將結締組織生長因子刺激肌腱干細胞14天,用熒光定量PCR儀檢測上述兩種標志物的mRNA的含量。實驗發現,與對照組相比,I型膠原的 mRNA水平含量升高了 5.3倍,Tenascin-C升高了2.1倍(P<0.01),如圖3A;同時,用Western Blot檢測,結果發現,與對照組相比,I型膠原的表達升高了3.3倍,Tenascin-C的表達升高了1.8倍(P<0.05),如圖3。以上結果表明,結締組織生長因子可以有效的促進肌腱干細胞向肌腱成纖維細胞分化。
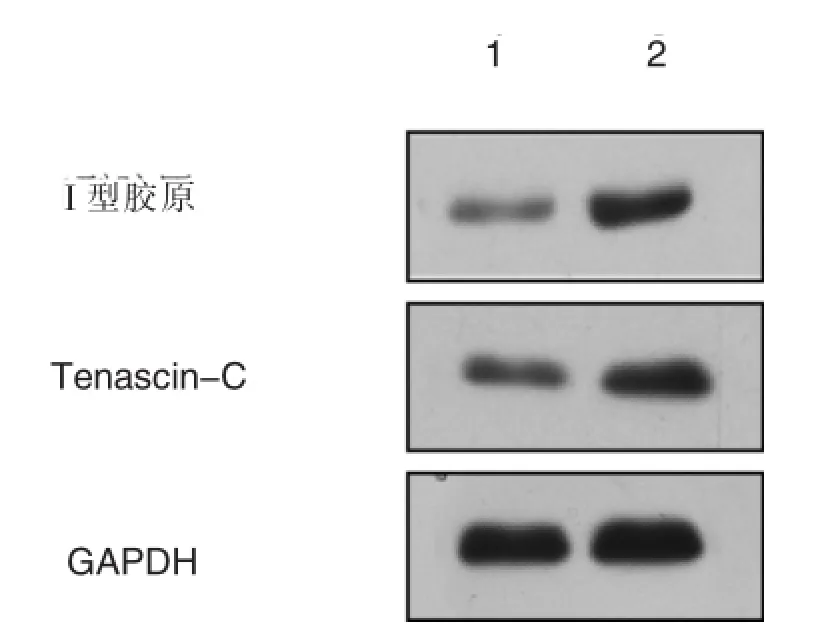
圖3 分化后的肌腱干細胞
3 討論
隨著越來越多的人參與到體育鍛煉和競技活動中,運動損傷也越來越多,其中韌帶肌腱損傷占50%以上。雖然目前臨床上有自體移植、同種異體移植和假體材料修復等技術,但這些手術仍存在著并發癥、疾病傳播、免疫排斥等缺陷。因此,采用人體自身干細胞進行修復無疑是更好的辦法。目前多種細胞因子已被證明可用于肌腱修復,如TGF-b1,IGF等,被證明可以有效提高損傷肌腱的修復。在機體中,CTGF可以刺激結締組織細胞,使其胞外基質的再生作用加強創傷處纖維填充、毛細血管生長加快等[6]。肌腱中分離出來的干細胞不僅能像骨髓間充質干細胞一樣具有干細胞特性,并在特定誘導條件下分化為脂肪、骨、軟骨、心肌等多種組織細胞。
本研究分離獲取的肌腱干細胞鏡下觀察細胞形態呈梭狀,經過成骨、成軟骨及成脂誘導后可分化為成骨細胞、軟骨細胞和脂肪細胞,且在結締組織生長因子的刺激下可以向肌腱細胞分化。肌腱細胞分化的特異標記物為tenomodulin、scleraxis、tenascin C,而Ⅰ型膠原是肌腱組織的主要成分。本研究發現分化后的肌腱細胞中tenascin C和Ⅰ型膠原mRNA水平和蛋白表達水平是均有升高,且差異均有統計學意義,因此確定了提取的肌腱干細胞可以向肌腱細胞分化。
綜上所述,本實驗針對肌腱干細胞,成功證明了結締組織生長因子對肌腱干細胞的刺激分化作用,此種生長因子可以直接應用之損傷局部,包括注射及局部包裹生長因子的封閉劑或指甲等從而可以為細胞因子療法提供一個新的選擇。然而,直接注射存在生長因子半衰期較短等缺陷,因而未來可以采用生物材料緩釋載體來解決這一問題。同時還有研究表明,這種干細胞參與了多種肌腱修復的活動如血小板富集療法。因此,針對肌腱干細胞進行修復療法的研究將成為未來的一個方向。
[1]安小團.運動訓練對肌腱細胞外間質及IGFIMRNA和蛋白表達的影響[D].蘇州:蘇州大學,2009.
[2]宋海新,陳 曉,李建華.激活肌腱干細胞:啟動肌腱再生的條件[J].中國康復醫學雜志,2012,27(5):485-488.
[3]Bi Y,Ehirchiou D,Kilts TM,et al.Identification of tendon stem/ progenitor cellsand the role of the extracellularmatrix in theirniche [J].NatMed,2007,13(10):1 219-1 227.
[4]Igarashi A,OkochiH,Bradham H,et al.Regulation of connective tissue growth factor gene expression in human skin fibroblasts and duringwound repair[J].Mol BiolCell,1993,4:637-645.
[5]李琦涵,趙紅玲,王 炯.結締組織生長因子的基因克隆[J].中國醫學科學院學報,2000,22(1):48-51.
Effectsof Connective Tissue Growth Factor on Cells Differentiation of Tendon in Sports
DOU Haibo,WEN Xiuli
運用實驗法和數理統計法探究體育運動中結締組織生長因子對肌腱干細胞分化產生的影響。將周圍結締組織從活體中進行細胞分離及培養;取P2代細胞爬片進行免疫細胞化學檢測細胞表型抗原標記CD44、CD29。取P3代細胞進行肌腱干細胞多向分化能力鑒定,收集未處理的肌腱干細胞和分化后的肌腱細胞,分別用實時熒光定量PCR和Western印跡檢測I型膠原和Tenascin-CmRNA和蛋白水平的表達。實驗結果表明:細胞免疫熒光染色CD44、CD29陽性,表明我們分離提取的組織細胞為肌腱干細胞;肌腱干細胞可以向脂肪細胞、骨細胞、軟骨細胞分化;分化后的肌腱細胞,I型膠原的mRNA水平含量升高了5.3倍,Tenascin-C升高了2.1倍(P<0.01),I型膠原的蛋白表達升高了3.3倍,Tenascin-C的表達升高了1.8倍(P<0.05)。結論:結締組織生長因子可以促進肌腱干細胞分化。
體育運動;肌腱;干細胞;分化;結締組織;生長因子
To investigate the effect of Connective tissue growth factor(CTGF)on the differentiation of tendon stem/progenitor cells(TSPCs)in sports,this paper uses the experimentalmethod and mathematical statistics method.Cells were isolated from the surrounding connective tissue of the living;the protein expressions of CD44、CD29 were detected by immunocy to chemistry staining from the cells at passage 2.Cells at passage 3 were used to demonstrate themulti-differentiation potential of the TSPCs,themRNA expression of tenascin C and collagen type Iwere determined by real-time PCR,and the protein expressions of tenascin C and collagen type Iwere determined byWestern blot.Results indicates that immunocy to chemistry staining showed that the protein expressions of CD44、CD29 were detected in cells we isolated;chondrogenic,osteogenic,and adi pogenic differentiation assays were used to demonstrate themulti-differentiation potential of the TSPCs;the mRNA expressions of collagen type Iand Tenascin-Cwere 5.3 and 2.1 times higher than that in cellswith no differentiation(P<0.01),the protein expressions of tenascin C and collagen type Iwere 3.3 and 1.8 times higher than that in cellswith no differentiation(P<0.05).Conclusion:Connective tissue growth factor(CTGF)can be used to promote tenogenic differentiation of the TSPCs?in vitro.
sports;muscle tendon;stem cells;differentiation;connective tissue;growth factor
G804.5
A
1003-983X(2015)03-0217-04
2015-01-05
北京市青年英才計劃(YETP0407);教育部中央高校基本科研業務費(FRFBR13038)
竇海波(1981-),男,河南鄧州人,博士,講師,研究方向:高校競技體育.
北京科技大學體育部,北京100083 Physical Education Department,University of Science and Technology Beijing,Beijing,100083

