培養基質對蛹蟲草中蟲草酸及核苷類物質的影響*
劉桂君,周思靜,林金星
1(北京林業大學生物科學與技術學院,北京,100083)2(北京市輻射中心,北京,100015)
蛹蟲草(Cordyceps militaris(L.)Link)[1]是我國傳統的食藥用菌,含有豐富的蟲草酸及蟲草素等核苷類活性物質[2]。蟲草酸即甘露醇,是蛹蟲草的重要活性成分,具有鎮咳、平喘及祛痰等作用[3],對人體內羥基自由基具有良好的清除作用,還可降低顱內壓和眼內壓,也是良好的利尿劑和食品甜味劑[4]。蟲草素(cordycepin)即3'-脫氧腺苷,是 Cunningham 等在1950年從蛹蟲草寄生的昆蟲不腐爛組織中分離得到的抗菌物質,也是第一個從真菌中分離出來的核苷類抗菌素[5-6]。蟲草素具有免疫調節、抗腫瘤、抗菌、抗病毒和治療白血病等功效[7-11]。此外,蛹蟲草還含有腺苷、尿苷、鳥苷、胸苷及腺嘌呤等核苷類成分。
目前,蟲草素等核苷類物質的主要來源還是蛹蟲草培養物,因此蛹蟲草固體培養方法優化一直是蛹蟲草研究中的熱點。顧冬艷等按照大豆粉與麥麩4∶1的質量比,再添加特定配方的營養液,得到蛹蟲草的蟲草素產量為 5 499.12 μg/g[12],此研究僅是單一的對培養基配方進行優化,且以蟲草素一種物質的含量作為衡量指標;張紅霞等研究蛹蟲草不同栽培菌株之間蟲草素及腺苷的差異,蟲草素含量為600~3 900 μg/g,腺苷含量為1 000 ~1 700 μg/g[13],該研究僅以蟲草素和腺苷2種物質為衡量指標,考察不同菌株之間的差異,并未考慮培養基質的影響;李辰等研究蛹蟲草及其培養殘基中腺苷和蟲草素含量的快速測定方法,采用高效液相色譜法僅同時測定腺苷及蟲草素2種物質的含量[14];樂昕等研究不同栽培基質對蛹蟲草子實體中腺苷、蟲草素、SOD及粗多糖含量的影響[15],未對核苷類物質全面測定;郭濤等研究糯米、粳米及添加家蠶蛹浸提液對蛹蟲草中蟲草素和腺苷的影響[16];溫魯等以大米為主要原料,添加豆粉、奶粉、魚粉、蛹粉等,進行試管斜面培養,僅測定固體培養物中蟲草素和腺苷含量[17];史敏等建立了多糖以及蟲草素、腺苷、尿苷3種核苷類物質的測定方法[18];雷寧等建立了蟲草素、腺苷、尿苷及腺嘌呤的測定方法[19]。現有研究主要是集中在蛹蟲草活性成分的分離提取、測定方法優化、核苷類物質中1種或2種成分含量的測定等方面。
本實驗研究了不同種類培養基質對蛹蟲草子座中蟲草酸及5種主要核苷類物質含量的影響。實驗表明,不同種類培養基質對蛹蟲草子座中蟲草酸及蟲草素等核苷類物質含量影響各有不同,因此,可根據不同的實驗目的,選擇適合的培養基質。
1 材料與方法
1.1 材料與儀器設備
菌種:蛹蟲草(Cordyceps militaris)CM-7,北京市輻射中心微生物實驗室保存。
培養基質:大麥、燕麥、大米、小米,均為食品級材料,由超市購得。
蛹蟲草液體培養基配方:葡萄糖20 g,蛋白胨20 g,KH2PO41 g,MgSO40.5 g,蒸餾水 1 000 mL,pH 值自然,121℃滅菌30 min。
固體培養基:將培養基質(大麥、燕麥、大米、小米)70 g放入培養瓶中,加入90 mL蛹蟲草液體培養基,121℃滅菌30 min。
試劑:甘露醇、高碘酸鈉、L-鼠李糖、醋酸銨、冰醋酸、鹽酸、乙酰丙酮(均為分析純),購自國藥集團北京化學試劑公司;甲醇(色譜純),購自CNW公司;尿苷(尿嘧啶核苷,uridine)、鳥苷(鳥嘌呤核苷,guanosine)、胸苷(胸腺嘧啶核苷,thymidine)、腺苷(腺嘌呤核苷,adenosine)、蟲草素(cordycepin)為液相色譜純,購自Sigma試劑公司。
儀器:M3型多功能酶標儀,美國分子儀器公司;1260型高效液相色譜儀,美國安捷倫儀器公司;A10型純水價,美國密理博儀器公司;REX-500A型人工氣候箱,寧波江南儀器廠;ZHWY-2112B型搖床,上海智誠分析儀器制造有限公司。
1.2 蛹蟲草固體培養方法
首先培養蛹蟲草種子液,將PDA平板上蛹蟲草菌種用打孔器打成直徑為1 cm的接種塊,裝有400 mL蛹蟲草液體培養基的1 000 mL的三角瓶中每瓶接入5塊,搖床180 r/min,25℃培養7 d。將蛹蟲草種子液用無菌移液器吸取5 mL均勻的接種到滅菌的固體培養基質表面,25℃恒溫避光培養7~10 d,待菌絲布滿取出,在超凈臺中用無菌鑷子將上層的菌絲皮翻開打散,使長滿菌絲的米粒均勻的分散,然后移入人工氣候箱中進行光照培養,溫度為20~23℃,設定白天黑夜交替,培養35~40 d,將蛹蟲草子座收集,50℃烘干后粉碎備用。
1.3 甘露醇測定方法
1.3.1 標準曲線的制作
標準溶液制備:甘露醇標樣100 mg,加蒸餾水100 mL配制成濃度為1 000 μg/mL的甘露醇溶液,然后用蒸餾水分別稀釋成所需濃度。取濃度分別為0、31.25、62.5、125、250、500 μg/mL 的甘露醇標準溶液各 1 mL,置于不同試管中,加入1 mL 15 mmol/L高碘酸鈉溶液混勻,室溫放置10 min,加2 mL 0.1%L-鼠李糖溶液以除去過多的高碘酸鹽,混合后加4 mL新配制的Nash試劑(150 g醋酸銨+2 mL冰醋酸+2 mL乙酰丙酮,用蒸餾水稀釋定容1 000 mL),53℃水浴加熱15 min顯色,冷卻,在412 nm處測定吸光度值(OD值)[20],根據樣品濃度與OD值關系制作標準曲線。
1.3.2 樣品處理及甘露醇測定方法
分別準確稱量蛹蟲草子座粉末1.0 g,各加入20 mL超純水沸水浴提取1 h,將提取液離心取上清液補水至20 mL,保存樣品,待測。取樣品提取液1 mL,分置不同試管中,按照1.3.1中的方法,依次加入試劑,水浴加熱,測定412 nm時吸光度值,每個樣品測定3個平行。
1.4 核苷類物質測定方法
1.4.1 標準曲線的制作
分別準確稱取蟲草素、腺苷、尿苷、鳥苷及胸苷標樣,梯度稀釋得到不同濃度標準溶液,腺苷、尿苷、鳥苷及胸苷均為:0、5、10、20、40、80、100 μg/mL,蟲草素為:0、31.25、62.5、125、250、500 μg/mL,采用高效液相色譜法(HPLC)測定核苷類物質的含量,具體測定條件如下:DAD檢測器;檢測波長為260 nm;色譜柱:XDB-C18,4.6 ×250 mm,5 μm;流動相∶V(甲醇)∶V(水)=15∶85;流速 1 mL/min;進樣量 10 μL;柱溫箱溫度為25℃。根據標樣濃度與峰面積響應值制作標準曲線。
1.4.2 樣品處理及核苷類物質測定方法
分別準確稱量蛹蟲草子座粉末1.0 g,加入20 mL甲醇,放入磨口三角瓶中,連接回流冷凝裝置,70℃回流提取1 h,將提取液8 000 r/min離心5 min,取上清液補甲醇至20 mL,0.22 μm無菌濾膜過濾待測。
2 結果與分析
2.1 甘露醇標準曲線及樣品含量測定結果
根據甘露醇濃度 0、31.25、62.5、125、250、500 μg/mL與吸光度值(OD值)之間的關系,得到標準曲線方程為:y=0.005 4x+0.031,R2=0.999 0,表明甘露醇濃度在0~500 μg/mL線性關系良好,適宜測定甘露醇濃度在該區間范圍內的樣品。將樣品測定得到的OD值代入標準曲線方程,計算溶液中甘露醇濃度,再根據溶液濃度計算子座粉末中蟲草酸(甘露醇)含量,結果如圖1所示。由圖1得到,4種培養基質培養獲得的子座中,小米子座蟲草酸(甘露醇)含量最高,為9.00 mg/g,大米子座含量最低,為7.43 mg/g,燕麥子座和大麥子座蟲草酸(甘露醇)含量分別為7.46 mg/g和8.28 mg/g;小米培養基質最利于子座中蟲草酸的合成。
2.2 核苷類物質標準曲線
根據尿苷、鳥苷、胸苷、腺苷、蟲草素濃度與峰面積響應值之間的關系,得到標準曲線方程分別為:y=30.941x-16.477,R2=0.999 9;y=28.704x+2.589 7,R2=0.999 9;y=31.122x-24.159,R2=0.999 7;y=43.035x-42.977,R2=0.999 7;y=46.317x-20.774,R2=0.999 7。這5種核苷類物質在測定的濃度范圍內峰面積響應值與濃度線性關系良好。
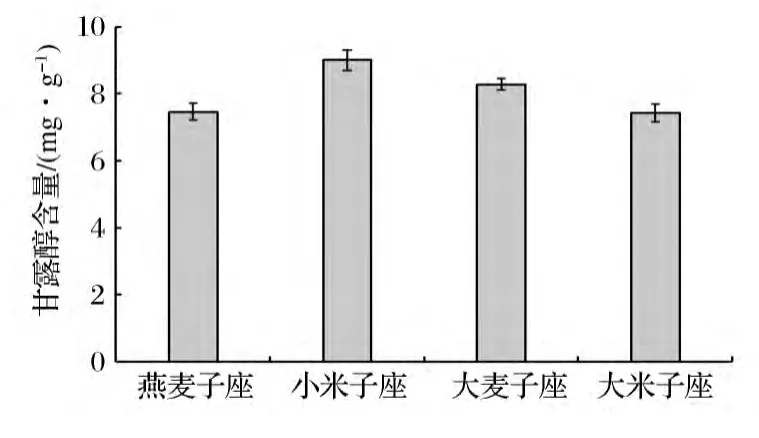
圖1 蛹蟲草子座中甘露醇含量Fig.1 Content of mannitol in stromata of Cordyceps militaris
2.3 核苷類物質混合標樣圖譜
將100 μg/mL的蟲草素、腺苷、尿苷、鳥苷及胸苷5種標準液等體積混合,得到終濃度為20 μg/mL的混合標樣標準溶液,HPLC測定得到混合標樣的色譜峰及保留時間圖譜,5個色譜峰所代表的化合物依次為:尿苷、鳥苷、胸苷、腺苷、蟲草素,保留時間分別為,3.315、4.402、6.199、8.622、11.232 min,在此條件下5種核苷類化合物分離效果好,能夠準確測定含量,如圖2所示。
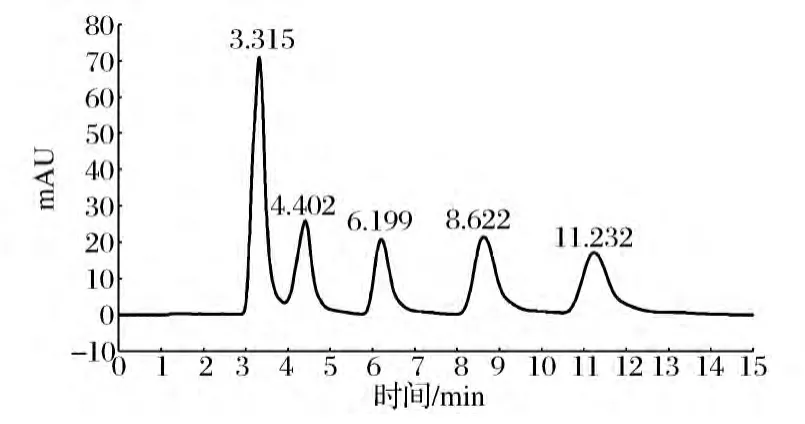
圖2 核苷標樣圖譜Fig.2 Chromatogram of standard nucleosides samples
2.4 樣品中核苷類物質含量測定
蛹蟲草子座甲醇回流提取液經HPLC測定,在260 nm波長下得到的各個化合物的色譜峰分離較好(如圖3所示)。圖3中橫坐標為化合物保留時間,采用相同范圍的縱坐標能夠更清晰的判斷同一位置的色譜峰的峰高及峰面積,也就是提取液中化合物含量的高低,與子座中化合物含量的高低一致。并且可以看出小米子座和大麥子座中蟲草素含量遠遠高于另外兩種子座。
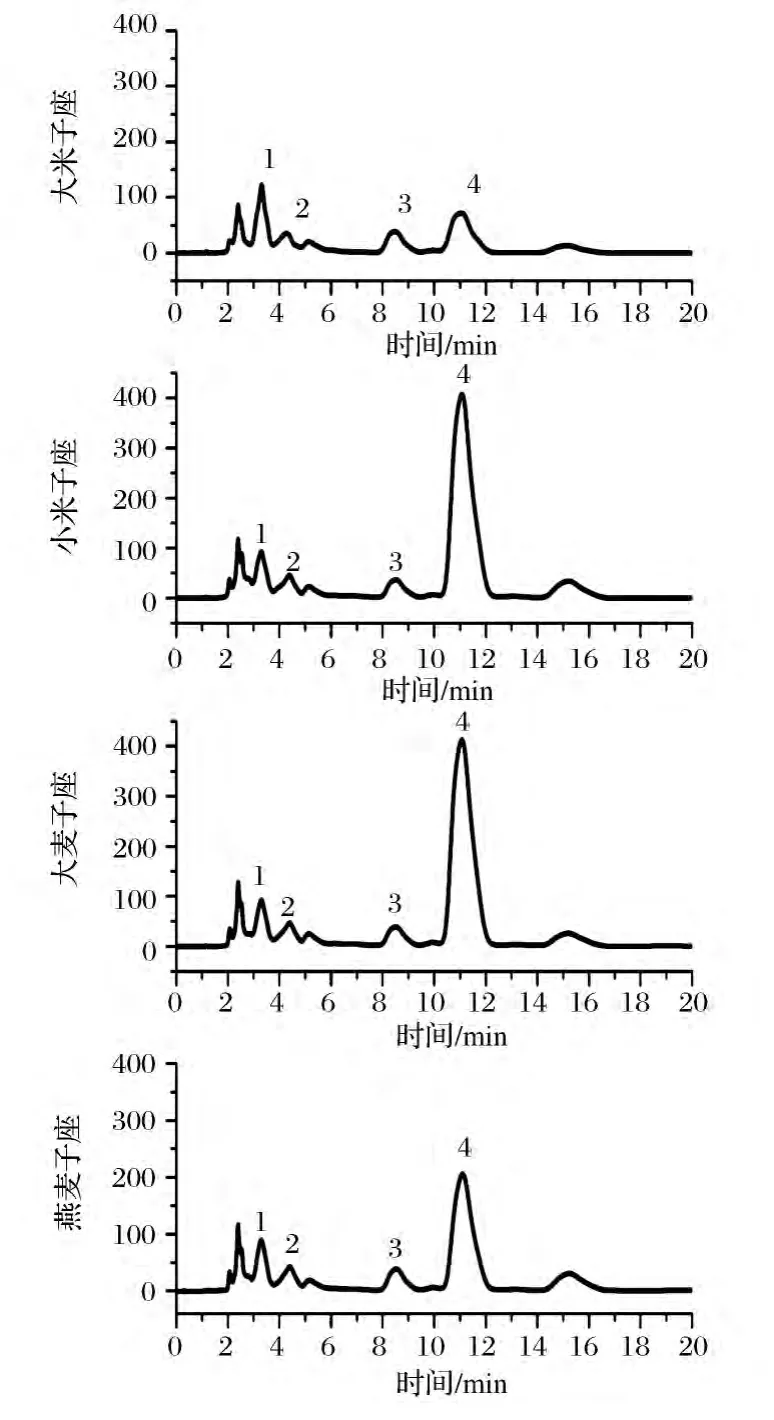
圖3 不同子座中核苷圖譜Fig.3 Chromatogram of nucleosides in different stromata
2.5 不同培養基質獲得的子座中成分含量測定結果
將4種子座提取液樣品測定的蟲草酸、蟲草素、腺苷、尿苷、鳥苷及胸苷的數據分別代入標準曲線方程,計算提取液中蟲草酸及核苷類物質含量,折算后得到每克子座粉末中成分含量,結果如表1所示,數據統計分析采用DPS7.05版軟件,采用Duncar新復極差法比較。
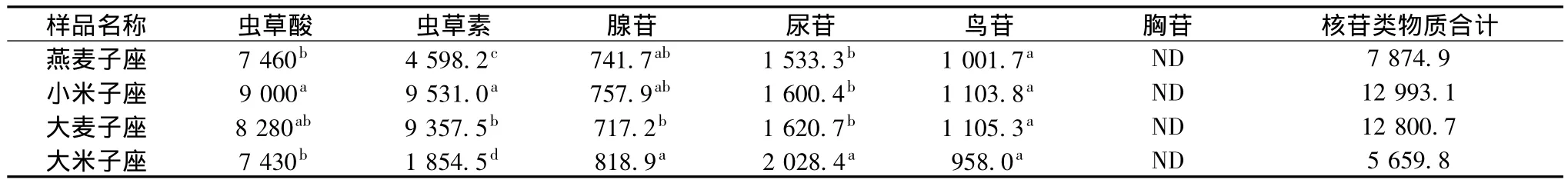
表1 不同培養基質培養蛹蟲草子座中蟲草酸及核苷類物質的含量μg/gTable 1 Content of cordycepic acid and nucleosides in stromata of Cordyceps militaris cultured by different solid culture medium μg/g
表1中數據說明,不同培養基質的子座中核苷類物質含量差別較大,尤其是蟲草素含量差別最大,蟲草素含量最高的為小米子座,最低的為大米子座,兩者相差7 676.5 μg/g,表明培養基質的種類對蟲草素含量的影響很大。小米培養基最利于蟲草素合成,其次為大麥培養基,然后是燕麥培養基和大米培養基。文獻[15]報道高粱米作為培養基蟲草素含量最高,蟲草素含量為2 482 μg/g,小米作為培養基蟲草素含量最低為1 163 μg/g,本研究結果與報道不同,反而得到小米作為培養基蟲草素含量最高為9 531.0 μg/g,遠遠高出文獻[15]報道結果,而腺苷含量大米子座最高為818.9 μg/g,比含量最低的大麥子座高101.7 μg/g,但低于文獻[15]中 1 861 μg/g。分析可能是由于菌株、培養基配方及培養條件的不同引起的。小米子座和大麥子座中尿苷、鳥苷的含量比較接近,差異不顯著,大米子座中尿苷含量最高,鳥苷含量最低。4種子座經甲醇回流所得的提取物中均未檢測到胸苷,可能是由于其含量低于本方法的檢測限值。
3 結論
不同培養基質(燕麥、小米、大麥、大米)對蛹蟲草子座中蟲草酸、蟲草素及其他核苷類物質含量影響各不相同,子座中蟲草酸與蟲草素含量高低順序相同,依次為:小米子座>大麥子座>燕麥子座>大米子座;5種核苷類物質合計與蟲草素含量高低順序一致,依次為:小米子座>大麥子座>燕麥子座>大米子座。核苷物質合計與蟲草素含量高低順序之所以一致主要是由于蟲草素是核苷類物質中主要成分,故其含量決定核苷類物質含量的總和。
小米子座和大麥子座中蟲草酸和蟲草素等核苷類物質含量最高,因此,小米和大麥適合于人工培養高產蟲草素、蟲草酸的蛹蟲草子座,采集子座后的培養基質還可以作為食品或保健食品的原料開發利用,不足之處是與大米相比價格高導致培養成本較高,生產中可以根據需求選擇適合的培養基質。
[1] 戴玉成,李玉.中國六種重要藥用真菌名稱的說明[J].菌物學報,2011,30(4):515-518.
[2] 梁宗琦.中國真菌志第32卷-蟲草屬[M].北京:科學出版社,2007:10-47.
[3] 蔡仲軍,尹定華,秦松云.水提取法測定冬蟲夏草甘露醇含量[J].重慶教育學院學報,2002,15(6):42-44.
[4] 張曉卿,李媚,藍麗紅,等.比色法測定發酵液中甘露醇的含量[J].化工技術與開發,2004,33(2):33-35.
[5] Cunningham K G,Manson W,Spring F S,et al.Cordycepin,a metabolic product isolated from cultures of Cordyceps militaris(Linn.)Link[J].Nature,1950,166(4 231):949.
[6] Cunningham K G,Hutchinson S A,Manson W,et al.Cordycepin,a metabolic product from cultures of Cordyceps militaris Link.Part I.Isolation and characterization [J].Journal of Chemical Society,1951,2:2 299-3 000.
[7] 蔡友華,劉學銘.蟲草素的研究與開發進展[J].中草藥,2007,38(8):1 269-1 272.
[8] Fan B Y,Zhang H B.Cordycepin:pharmacological properties and their relevant mechanisms[J].TANG,2012,2(2):e14,1-7.
[9] 康冀川,康超,文庭池,等.蟲草菌素藥理學研究進展[J].菌物學報,2011,30(2):191-197.
[10] REN Z H,CUI J H,HUO Z R,et al.Cordycepin suppresses TNF-α-induced NF-κB activation by reducing p65 transcriptional activity,inhibiting IκBα phosphorylation,and blocking IKKγ ubiquitination[J].International Immunopharmacology,2012,14(4):698-703.
[11] 吳勇,陳衛東.蛹蟲草藥理作用研究概述[J].中國藥師,2011,14(5):732-734.
[12] 顧冬艷,尹永祺,楊潤強,等.北蟲草固態發酵產蟲草素培養基優化[J].食品科學,2013,34(21):254-258.
[13] 張紅霞,黃開華,陳偉,等.蛹蟲草不同栽培菌株產蟲草素及腺苷差異性研究[J].食用菌,2011,(5):63-64.
[14] 李辰,閆愛國,蔡春燕,等.蛹蟲草及其培養殘基中腺苷和蟲草素含量的快速測定[J].色譜,2012,30(7):711-715.
[15] 樂昕,袁蜜,支月娥,等.栽培基質及碳源對蛹蟲草子實體中主要有效成分的影響[J].食品科技,2014,39(2):2-7.
[16] 郭濤,張龍,王兵,等.不同培養基培育蛹蟲草中的蟲草素和腺苷含量測定[J].蠶業科學,2011,37(6):1117-1122.
[17] 溫魯,夏敏,宋虎衛,等.固體培養蛹蟲草核苷類次生代謝物的產率[J].食品科學,2005,26(11):65-68.
[18] 史敏,趙宇,溫學森.人工培養北蟲草子座和培養基中多糖和核苷類成分的含量分析[J].食品與藥品,2009,11(1):45-47.
[19] 雷寧,杜樹山,倪雪梅,等.RP-HPLC測定天然蟲草與人工蟲草中核苷類成分的含量[J].中國藥學雜志,2006,41(12):948-951.
[20] 劉桂君,尚宏忠,李賽飛,等.細腳擬青霉甘露醇含量的測定[J].食品科學,2011,32(22):226-229.

