無創產前基因檢測在產科門診的應用研究
徐 彬余元勛章小琳李建平劉 萍
◇生育與婦幼衛生◇
無創產前基因檢測在產科門診的應用研究
徐 彬1余元勛1章小琳2李建平1劉 萍1
目的:應用新的基因DNA測序方法研究其對孕中期孕母血漿中胎兒游離DNA(cffDNA)進行染色體非整倍體檢測的靈敏度和特異性,并與羊水核型分析結果比較。方法:收集2013年1月~2014年7月在安徽省立醫院產科門診2596例孕婦的血樣本,進行唐氏綜合癥血清學篩查、12-plex高通量Hiseq2000平臺檢查;對血清學篩査中的cffDNA檢測陽性者,進行羊水細胞遺傳學診斷。結果:孕中期血清學篩查共2596例,發現高危孕婦197例,占7.59%;對高危孕婦176例進行cffDNA檢測發現43例陽性,陽性率為24.43%;同時進行羊水染色體核型分析發現42例核型異常,陽性率為23.86%;兩種方法結果基本一致。結論:孕婦血的胎兒cffDNA檢測,是無創產前診斷方法;檢測靈敏度較高。
無創性產前診斷 唐氏綜合癥 胎兒游離DNA 核型
唐氏綜合征(Down syndrome,DS)又稱21-三體(Trisomy 21,T21)綜合征、先天愚型,是最常見的染色體非整倍體疾病,新生兒發病率在1/700~1/800,占新生兒染色體病的70%~80%[1],其他比較常見的還包括18-三體(Trisomy18,T18)、13-三體(Trisomy13,T13)、Turner綜合癥等。目前簡便、經濟、無創的孕中期血清學標志物篩查,是檢測胎兒染色體非整倍體疾病的重要篩查手段。研究表明,血清學標志物篩查的假陽性率較高(5%~7.5%)[2]。因此應用更好的方法產前發現這些染色體疾病胎兒,能有效減少患兒的出生,是當前圍產優生學的重要任務之一。
1997年Lo等報道,母血中存在胎兒游離DNA(cffDNA),可進行無創診斷胎兒染色體異常,即僅抽取母血,對血中cffDNA進行測序,即可診斷胎兒是否為染色體異常[3];2008年Lo等先后報道,使用對血中cffDNA測序、進行無創產前檢測(NIPT)時,T21的檢測準確度為100%[4]。隨后多項臨床研究證實,使用對血中cffDNA測序,檢測T21、T18、T13的靈敏度、特異度及陰性預測值(NPV)均較高[5~6],適用于產前診斷,目前已成為常用方法。本文通過血清學篩查、cffDNA測序檢測,診斷染色體異常,能為該方法在安徽大規模臨床研究和應用,提供循證醫學證據。
1 資料與方法
1.1 研究對象 選擇2013年1月~2014年7月安徽省立醫院產科門診孕期產檢的2596例孕婦,年齡22~44歲,孕11~24周,采取血樣本者均有知情同意書,本研究經過該醫院的倫理委員會審批通過。入組條件:>孕11周;單胎妊娠;體重在100kg以下。排除條件:多胎妊娠;孕婦是染色體異常患者;孕婦在抽血當天有侵入性手術經歷;孕婦接受過異體輸血、移植手術、干細胞治療等;拒絕行cffDNA檢測者。
1.2 方法 常規抽取靜脈血3~5ml,血液凝固后分離血清,將血清裝入血清保存管,4℃保存,注明標本編號。血清于1周內在安徽省立醫院檢驗科完成TRAFIA法檢測AFP、Free-βHCG、uE3的血清濃度;剩余血清-20℃保存。實驗過程嚴格按照說明書操作,并有質控。研究中保證孕婦臨床資料信息準確,孕周正確估計。孕早期超聲孕周核對應以頭臀長作為標準,孕中期核對時應以雙頂徑作為標準。
1.2.1 按文獻[6]進行cffDNA檢測標本采集 應用孕婦血漿樣本采集標準作業程序(SOP),采集孕婦外周血10ml,一般置于數個標準真空采血管內(EDTA抗凝),充分混勻,在抽血后6小時內進行以下處理:在4℃下兩次離心10min,將上清血漿轉入新的1.5ml離心管中,-80℃保存。
1.2.2 按文獻[6]進行DNA標本的SOP 血漿樣本DNA抽提(磁珠分離法)時,先用1ml血漿,加2ml binding buffer;70μl(20μg/μl)蛋白酶K;120μl(1μg/μl)carrier RNA;15μl(10μg/μl) 糖原; 30μlBEADS;室溫下混勻 15~20min;分裝到1.5mlEP管中,靜置1~2min,吸去廢液;加入40μl EB液,55℃水浴10min(每30s混勻一次);靜置1~2min,收集液體至新的EP管中。Qubit定量樣品DNA濃度。按文獻[6]進行DNA末端修整、末端加A、連接。
1.2.3 PCR與測序、羊水細胞培養染色體核型分析 配制如下反應體系,含DNA液22 μl、PhusionDNA polymerase25μl、PCR primer1.0μl、PCR primer2.0μl;總體積50μl。反應條件:98℃30 s熱變性;再98℃10 s,65℃30 s,72℃30 s,15個循環;延長72℃10 min。按照QIAquick PCR purification kit說明,柱純化DNA。Qubit定量DNA濃度。使用12-plex高通量Hiseq2000平臺進行高通量測序。運用序列比對軟件BWA map,將DNA測序所得的cffDNA序列,比對于人類基因組參考序列。計算每條染色體所占比例(%),并利用公式計算各個染色體Z值。利用Z值來評估樣本的實際患病情況(cut off:Z=3)。按文獻[6]進行羊水細胞培養染色體核型分析。
1.3 統計學方法 本研究所有的研究數據均使用Microsoft Office Excel 2007進行錄入和統計。用SPSS13.0統計軟件進行統計學處理。計量資料用平均數±標準差表示,用方差分析檢驗,計數資料用卡方檢驗。P<0.05為差異存在統計學意義。
2 結果
2.1 孕婦一般情況分析 本次共收入2596例單胎妊娠孕婦進行研究分析,年齡22~44歲,平均年齡32.28±3.72歲。2509例(96.45%)為低齡組(≤35歲),平均年齡(28.83±2.407)歲。87例(3.35%)為高齡組(>35歲),平均年齡(38.13±2.02)歲。采血樣孕周為11~24周,平均(16±3)周;1768例(68.10%)為首次妊娠;2171例(83.63%)為首次生育;208例(8.01%)有流產史。
2.2 血清學篩查結果 血清學篩査2596例后,發現高危患者共197例,陽性率7.59%,不同年齡孕婦血清學篩查的DS高風險率分布情況見表1;C、D年齡組與A、B年齡組間DS高風險發生率差異有統計學意義(P<0.05)。隨著高齡孕婦的增加,唐氏綜合癥篩查的陽性率也增加,高齡組DS風險更高。
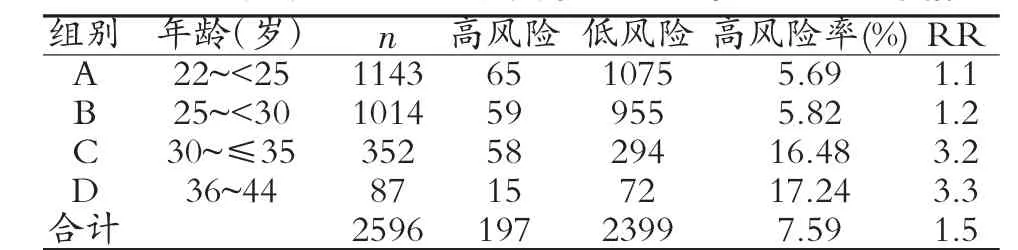
表1 不同年齡組孕婦血清學篩查DS高風險率分布情況
2.3 cffDNA檢測結果 共收集高危孕婦樣本176例,cffDNA檢測43例陽性:28例T21;5例T18;1例T13;4例45,XO;3例45,X;2例47,XXY,總體陽性率為24.43%(43/176)。
2.4 羊水染色體核型分析結果 血清學篩查后共收集高危孕婦經腹羊膜腔穿刺羊水樣本176例,進行細胞培養染色體核型分析;其中染色體核型異常陽性共42例,陽性率23.86%(42/176),包括 27例 T21;5例 T18;1例 T13;4例 45,XO;3例45,X;2例47,XXY,胎兒染色體核型分析結果與cffDNA檢測結果基本一致;無創產前基因檢測與染色體核型分析準確率的比較見表2。
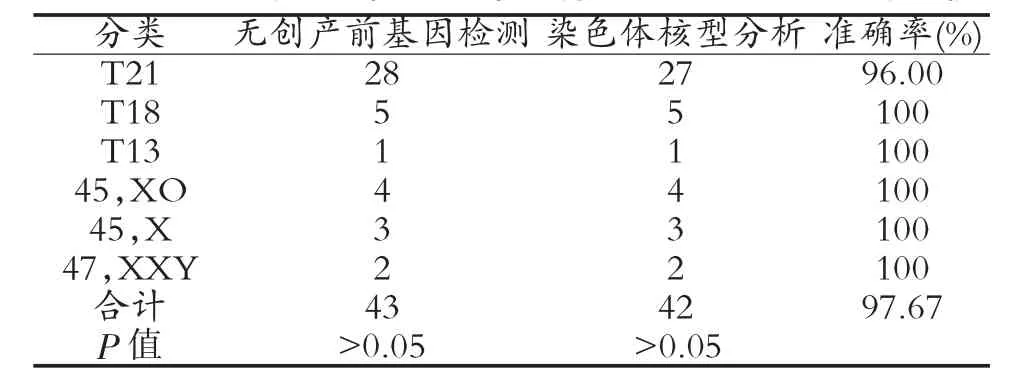
表2 無創產前基因檢測與染色體核型分析準確率的比較
3 討 論
過去診斷胎兒染色體非整倍體疾病,常通過侵入性產前診斷操作,如絨毛活檢、羊膜腔穿刺而獲得樣本。由于侵入性操作可帶來流產風險,而利用血清學生物標記物、超聲等對普通妊娠人群進行篩查,篩選出高危人群進行產前染色體確診,顯得尤為重要;但是篩查后,約3%~5%的人群仍需進行侵入性操作取樣[7]。許多研究表明,血漿cffDNA檢測不受孕周與年齡的限制,為無創產前診斷的較優方法。用孕母血漿cffDNA檢測胎兒非整倍體,尤其是T21時,有較高的敏感性和特異性[6]。本研究選擇普通孕婦作為研究人群,應用第二代DNA測序技術對孕母血漿中cffDNA進行無創胎兒染色體非整倍體檢測,同時平行進行羊水染色體核型分析。
2011年有人發表了一系列研究cffDNA檢測的結果,發現用cffDNA法對胎兒非整倍體產前檢測的效率較高。Ehrich M等[8]對孕母血漿cffDNA進行無創胎兒T21檢測,共檢測480例高危者,結果顯示,對T21檢測的靈敏度為100%,特異性為99.7%。Chiu RW等[9]發現,對胎兒T21高風險孕婦血漿進行cffDNA檢測時較有效、可行。2012年Palomaki GE等[6]對DNA GC含量進行校正后,采用第二代DNA測序方法,對孕母血漿檢測cffDNA,對 T18和 T13檢出率分別為 100%和91.7%,假陽性率分別為0.28%和0.97%;這一方法可使侵入性產前診斷操作率降低95%。ACOG在美國進行了一項多中心研究,前瞻性研究評價cffDNA法對孕母血漿胎兒非整倍體診斷的準確性[10],結果較好。
本研究在安徽省立醫院產科門診采集2596例孕婦的血樣本,血清學篩查高危者共197例,結果陽性率為7.59%。高/低齡組間DS高風險發生率差異有統計學意義,隨著高齡孕婦的增加,唐氏綜合癥篩查陽性率也增加,高齡組DS高風險發生率較高。研究中共收集高危者樣本176例,檢測cffDNA后檢出43例陽性:28例T21;5例T18;1例T13;4例45,XO;3例45,X;2例47,XXY,總陽性率為24.43%;經羊水細胞染色體核型分析證實的染色體非整倍體異常共42例,總陽性率為23.86%;兩種方法結果基本一致,P>0.05。
本研究應用第二代DNA測序技術對孕母血漿中cffDNA進行無創胎兒染色體非整倍體檢測,顯示了較高的靈敏度和特異性,初步證明cffDNA產前檢測技術可以檢測常染色體與性染色體等,產前檢測效率較高,質量控制較簡單,無年齡依賴性和孕周依賴性,可避免大量不必要的侵入性產前診斷操作;應用于孕中期產前篩查時方法可行,但仍需進一步大樣本研究。
1 中華人民共和國衛生行業標準:胎兒常見染色體異常與開放性神經管缺陷的產前篩查與診斷技術標準,第1部分:孕中期母血清產前篩查[S].北京,中國標準出版社,2010:1~9.
2 楊燦鋒,王峻峰,朱云霞,等.15230例孕中期唐氏篩查產前診斷的臨床應用價值[J].實用婦產科雜志,2011,27(2):142~145.
3 Dennis LY.Prenatal diagnosis:progress through plasmanucleicacids[J].NatRevGenet,2007,8(1):71~77.
4 Lo YMD,Chiu RWK.Genomic analysis offetal nucleic acids in maternal blood[J].Annual Review of Genomics and Human Genetics,2012,13:308~316.
5 Sparks AB,Wang ET,Struble CA.Selective analysis of cell-free DNA in maternal blood forevaluation of fetal trisomy[J].Prenat Diagn,2012,32(1):3~9.
6 Palomaki GE,Deciu C,Kloza EM.DNA sequencing of maternal plasma reliably identifies trisomy 18 and trisomy 13 as well as Down syndrome:an international collaborativestudy[J].GenetMed,2012,14(3):296~305.
7 Kagan KO,Cicero S,Staboulidou I.Fetal nasal bone in screening fortrisomies 21,18 and 13and Turner syndrome at 11-13 weeks of gestation[J].Ultrasound Obstet Gynecol,2009,33(3):259~264.
8 Ehrich M,Deciu C,Zwiefelhofer T.Noninvasive detection of fetal trisomy 21 by sequencing of DNA in maternal blood:a study in a clinical setting[J].Am J Obstet Gynecol,2011,204(3):201~205.
9 Chiu RW,Akolekar R,Zheng YW.Non-invasive prenatalassessmentoftrisomy 21 bymultiplexed maternal plasma DNA sequencing:large scale validity study[J].BMJ,2011,342:7401~7409.
10 Bianchi DW,Piatt LD,Goldberg JD.Genome-wide fetal aneuploidy detection by maternal plasma DNA sequencing[J].Obstet Gynecol,2012,119(5):890~899.
Applicativeresearchofnoninvasiveprenatalgenecheckingintheobstetricalclinics
1.Anhui Medical College,Anhui Provice Medical Genetics Center,Hefei 230061,Anhui 2.Anhui Provincial Hospital,Hefei 230001,Anhui XU Bin1,YU Yuan-xun1,ZHANG Xiao-lin2,et al
Objective:To study the sensitivity and specificity of using new gene DNA sequencing method to check the cffDNA in their mother's plasma for the chromosome abnormality,and to compare the results with the results of amniotic fluids karyotyping.Methods:The bloods of 2596 pregnant women from the clinic of the Anhui Province Hospital from January 2013 to July 2014 were screened applying DS serelogical screening method,12-plex high rate Hiseq 2000 checking,we found the cffDNA positive samples that were analyzed by amniotic fluids karyotyping again.Results:From the 2596 pregnant women,we found 197 high riskers(7.59%),from 176 high riskers were cffDNA positive(24.43%),from 176 high riskers,we found that 42 high riskers were abnormal karyotype(23.86%),The two methods can get nearly same result.Conclusion:Checking the cffDNA from their mother's plasmas is the noninvasive prenatal diagnostic method with high sensitivity.
Noninvasive prenatal diagnosis;Down's syndrome;cffDNA;Kryotype
R473.71
A
1671-8054(2015)06-0089-03
/(編審:吳大保 施仲賦)
1.安徽醫學高等專科學校安徽省遺傳醫學中心 合肥 230061 2.安徽省立醫院產科 合肥 230001
安徽高校省級自然科學研究項目(編號:KJ2014A128)
徐彬,男,副研究員
2015-10-07收稿,2015-11-13修回

