基于[FeFe]-氫化酶模型化合物的聚合材料的合成及其催化性能*
鄭禮迪,葉 萍,王宏丹,沈 杰,樊 露,梁紹威,戴強強,周沈超,張靖鑫,張 浩,鐘 偉(嘉興學院生物與化學工程學院,浙江嘉興 314001)
?
基于[FeFe]-氫化酶模型化合物的聚合材料的合成及其催化性能*
鄭禮迪,葉萍,王宏丹,沈杰,樊露,
梁紹威,戴強強,周沈超,張靖鑫,張浩,鐘偉
(嘉興學院生物與化學工程學院,浙江嘉興314001)
摘要:以聚乙烯亞胺(PEI),N-羥基琥珀酰亞胺(NHS)和溴丙酸(BPA)為原料,按不同質量比r[m(Fe-NHS)∶m(PEI-CO2H)]合成了三種基于[FeFe]-氫化酶模型化合物的聚合材料Mr(r=5.5,9.0,12.0),其結構和性能經IR和CV表征。用循環伏安法考察了醋酸存在下,M5.5,M9.0和M12.0的催化制氫性能。結果表明:M12.0的催化性能最好,其催化電流為2.0 μA。
關鍵詞:[FeFe]-氫化酶;聚合材料;合成;循環伏安法;催化性能

Scheme 1

Chart 1
氫化酶廣泛存在于自然界中,可高效催化質子還原和氫氣氧化這一可逆反應。根據催化活性中心,氫化酶可分為三類[1]:[FeFe]-氫化酶、[NiFe]-氫化酶和[Fe]-氫化酶。其中,[FeFe]-氫化酶由于催化活性較高而備受關注。[FeFe]-氫化酶的活性中心(Chart 1)的結構亞單元[2Fe2S]是發生催化質子還原制氫和氫氣氧化反應的主要位點[2-3]。近年來,科研工作者針對[2Fe2S]展開了大量研究,合成了大量類似模型化合物[4-7]。雖然氫化酶催化劑的研究取得了諸多成果,但也仍然面臨許多挑戰:(1)模擬體系催化膜電極超電位高、穩定性較差、使用條件苛刻;(2)[FeFe]-氫化酶的金屬活性中心處于生物高分子蛋白鏈的包圍中,限制了質子傳輸效率[8]。
聚乙烯亞胺(PEI)富含亞胺和伯胺基團,水溶性較好,只需經簡單的親核取代反應即可官能團化。因此,考慮將PEI引入[FeFe]-氫化酶結構中,可有效提高其綜合性能。
本課題組長期從事[FeFe]-氫化酶模型化合物與聚合物拼接的研究,取得了較好效果,如含有炔基的二鐵模型化合物聚合得到功能聚合物[9];含炔基的模型化合物與有機疊氮化合物之間的成環聚合[10];聚氯乙烯自組裝或旋轉涂膜技術制備的聚合物催化電極[11]等。
基于此,本文以聚乙烯亞胺(PEI),N-羥基琥珀酰亞胺(NHS)和溴丙酸(BPA)為原料,按不同質量比r[m(Fe-NHS)∶m(PEI-CO2H)]合成了三種基于[FeFe]-氫化酶模型化合物的聚合材料[Mr(r=5.5,9.0,12.0),Scheme 1],其結構和性能經IR和CV表征。用循環伏安法考察了醋酸存在下,M5.5,M9.0和M12.0的催化制氫性能。結果表明:M12.0的催化性能最好,其催化電流為2.0 μA。
1 實驗部分
1.1儀器與試劑
Varian Scimitar 2000型紅外光譜儀(KBr壓片); Autolab Potentiostat 30型電化學工作站(掃描速率0.1 V·s-1)。
所用試劑均為分析純;溶劑使用前經脫水除氧處理。
1.2合成
(1)2Fe-NHS的合成
在反應瓶中加入α-硫辛酸0.62 g(3 mmol)和Fe3(CO)121.51 g(3 mmol),氮氣保護下加入新蒸THF 40 mL,攪拌下回流(76℃)反應1.5 h(溶液變為紅棕色,無氣泡產生)。冷卻至室溫,依次加入N,N'-二環己基碳二亞胺(DCC)0.74 g(3 mmol),N-羥基琥珀酰亞胺(NHS)0.41 g(3 mmol)和4-二甲氨基吡啶(DMAP)20 mg(0.16 mmol),避光反應過夜。過濾,濾液濃縮后經硅膠柱層析[洗脫劑:V(石油醚)∶V(乙酸乙酯)=1∶1]純化得紅棕色液體2Fe-NHS 0.84 g,產率48.0%; IR ν:2 072,2 033,1 998,1 743,1 648 cm-1。
(2)PEI-CO2H的合成
在反應瓶中加入PEI 2.70 g(62.7 mmol)和溴丙酸4.80 g(31.4 mmol),氮氣保護下加入新蒸甲醇30 mL和三乙胺4.5 mL,攪拌下回流(60 ℃)反應過夜。抽濾,濾餅依次用甲醇(3×40 mL)和乙醚(3×50 mL)逐級沉降,抽濾得淡黃色晶體PEI-CO2H 5.83 g; IR ν:1 724 cm-1。
(3)2Fe-PEI的合成
在Schlenk flask瓶中加入2Fe-CO2H 0.55 g(0.30 mol),氮氣保護下依次加入新蒸甲醇30 mL和2Fe-NHS 0.10 g(0.20 mol),攪拌下于常溫反應過夜。抽濾,濾餅用二氯甲烷(3×20 mL)沉降,抽濾得黃色油狀液體2Fe-PEI; IR ν:2 072,2 032,1 998 cm-1。
(4)M5.5,M9.0和M12.0的合成(以M5.5的合成為例)
在反應瓶中加入PEI-CO2H 0.55 g(0.29 mol),氮氣保護下依次加入新蒸甲醇30 mL和2Fe-NHS 0.10 g(0.20 mol),攪拌下于常溫反應過夜。抽濾,濾餅用二氯甲烷(3×20 mL)沉降,抽濾得紅棕色粉末M5.5; IR ν:2 073,2 031,1 996,1 712,1 680 cm-1。
僅改變質量比r[m(Fe-NHS)∶m(PEICO2H)]為9.0和12.0,用類似的方法合成黃色粉末M9.0和淡黃色粉末M12.0。
1.3催化性能
在干燥的反應管中加入[NnBu4]BF40.40 g,氮氣保護下加入新蒸乙腈9 mL,攪拌使其溶解;搭建三電極體系,加入2Fe-NHS 15 mg和冰醋酸1.5 μL冰醋酸,掃描并繪制循環伏安曲線。
以0.1 mol·L-1KCl溶液替代[NnBu4]BF4的乙腈溶液,用類似的方法測得PEI-CO2H,2Fe-PEI 和Mr的循環伏安曲線(均相對于Ag/AgCl電極)。
2 結果與討論
2.1合成
合成2Fe-NHS時,由于Fe3(CO)12和α-硫辛酸見光易分解,制備過程必須嚴格避光并經氮氣保護;此外,中間產物2Fe-CO2H對空氣和光均較敏感,故在合成后不經分離純化直接投入下一步反應。
2.2表征
(1)IR
圖1為2Fe-NHS,2Fe-PEI和Mr的IR譜圖。由圖1可見,三者均在2 073 cm-1,2 033 cm-1和1 998 cm-1附近出現很強的C=O吸收峰,這與六羰基二鐵的IR譜圖非常吻合[12-15]。由圖1還可見,1 743 cm-1處特征峰為2Fe-NHS中酯基的特征吸收峰; 1 710 cm-1處弱特征峰為Mr中羧基的特征吸收峰;僅有Mr在1 680 cm-1處出現了較明顯的酰胺鍵特征吸收峰。
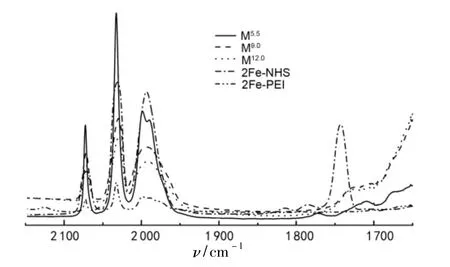
圖1 2Fe-NHS,2Fe-PEI和Mr的IR譜圖Figure 1 FT-IR spectra of 2Fe-NHS,2Fe-PEI and Mr
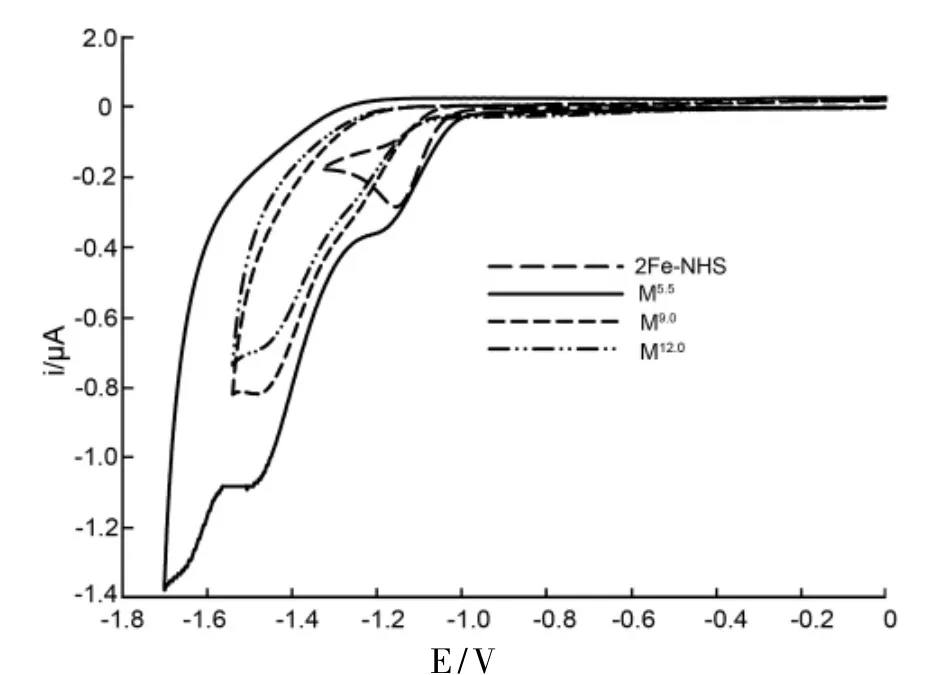
圖2 2Fe-NHS和Mr的CV曲線Figure 2 CV curves of 2Fe-NHS and Mr
(2)CV
圖2為2Fe-NHS與Mr的循環伏安曲線。由圖2可見,2Fe-NHS僅在-1.17 V處有一個還原峰,而Mr在-1.17 V和-1.47 V處均有還原峰。據文獻報道[16-18],-1.17 V處為二鐵六羰基的還原峰,-1.47 V處弱峰為二鐵五羰基的還原峰。-1.47 V處還原峰強度較弱的原因可能在于:PEI-CO2H與2Fe-NHS在反應過程中只有少部分伯胺或腫胺發生了鐵羰基取代反應。因此,由于五羰基鐵化合物含量較少,其特征峰在IR譜圖中也無對應顯示。

圖3 2Fe-NHS,M5.5,M9.0和M12.0的催化性能Figure 3 Catalytic activities of2Fe-NHS,M5.5,M9.0and M12.0
2.3催化性能
圖3為醋酸存在下,2Fe-NHS,M5.5,M9.0和M12.0的催化制氫性能。由圖3可見,2Fe-NHS,M5.5,M9.0和M12.0均在-1.2 V附近出現明顯的質子還原催化電流,說明它們均有催化制氫性能。理論上講,隨著醋酸量增加,金屬活性中心[2Fe2S]亞單元比例最大的M5.5催化效果應最好,但在醋酸加量為6 μL時,M12.0催化電流最大(2.0 μA)。
為進一步準確比較2Fe-NHS,M5.5,M9.0和M12.0的催化制氫性能,繪制了歸一化的催化電流強度,結果見圖4。
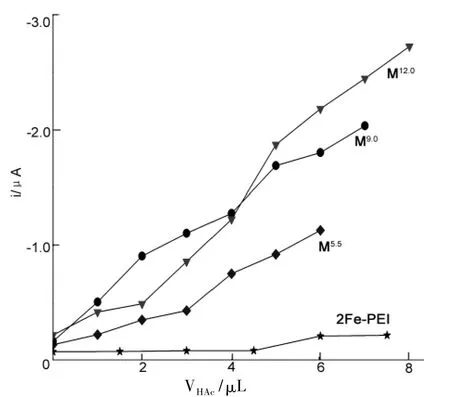
圖4 2Fe-NHS,M5.5,M9.0和M12.0的歸一化i-VHAc曲線Figure 4 Normalized i-VHAccurves of 2Fe-NHS,M5.5,M9.0and M12.0
由圖4可見,增大HAc加量,Mr的催化電流強度增幅更明顯,其可能原因在于:(1)分支狀PEI對[FeFe]-氫化酶模型化合物有包裹保護作用,相同酸濃度下,并非所有[2Fe2S]都能有效催化質子還原,二鐵單元與PEI的鍵合比例對此有重要影響;(2)PEI中含有大量伯胺、仲胺和叔胺基團,在催化質子還原過程中可以結合并傳遞質子,加速催化過程。
參考文獻
[1]Cedric T,Christopher J P.Structural and functional ana
logues of the active sites of the Fe-,NiFe- and FeFe
hydrogenases[J].Chem Rev,2009,109(6):2245-2274.[2]Yvain N,Claudine P,Pierre L,et al.Desulfovibrio
desulfuricans iron hydrogenase:The structure showsunusual coordination to an active site Fe binuclear center[J].Structure,1999,7(1):13-23.
[3]張磊,劉金庭.含單蝶狀[2Fe2S]骨架的新型[FeFe]氫化酶模型物{(μ-FcS)(μ-SMe)Fe2(CO)6}的合成及其晶體結構[J].合成化學,2011,19(6):727-729.
[4]張磊,劉金庭.含雙蝶狀[2Fe2S]骨架的新型[FeFe]氫化酶模型物{(μ-FcS2)[Fe2(CO)6]2(μ-SMe)2}的合成及其晶體結構[J].合成化學,2012,20(1):86-89.
[5]Xiao M L,Saad K L,Cedric T,et al.Iron-only hydrogenase:Synthetic,structural and reactivity studies of model compounds[J].Coord Chem Rev,2005,249(15-16):1641-1652.
[6]Jean F C,Frederic G,Philippe S,et al.Catalysis of the electrochemical H2evolution by di-iron sub-site models[J].Coord Chem Rev,2005,249(15-16):1664-1676.
[7]Stephen P B.Spectroelectrochemistry of hydrogenase enzymes and related compounds[J].Coord Chem Rev,2005,249(15-16):1536-1554.
[8]Eric P,Yvain N,Carole M,et al.The role of the maturase HydG in[FeFe]-hydrogenase active site synthesis and assembly[J].FEBS Lett,2009,583(3):506-511.
[9]Xiang R,Xiang H Z,Zhi M L,et al.Bioinspired polymer functionalized with a diiron carbonyl model complex and its assembly onto the surface of a gold electrode via“Click”chemistry[J].J Polym Sci Part A:Polym Chem,2010,48(11):2410-2417.
[10]Cai X Z,Xiu F W,Zhen H W,et al.Synthesis and characterisation of polymeric materials consisting of { Fe2(CO)5}-unit and their relevance to the diiron sub-unit of FeFe-hydrogenase[J].Dalton Trans,2010,39(46):11255-11262.
[11]Lian J W,Zhi Y X,Xiang R,et al.Enable PVC plastic for a novel role:Its functionalisation with diiron models of the sub-unit of FeFe-hydrogenase,assembly of film electrodes and electrochemical investigations[J].RSC Adv,2011,1(7):1211-1219.
[12]Zhi Y X,Fen F X,Li L,et al.Influence of the basicity of internal bases in diiron model complexes on hydrides formation and their transformation into protonated diiron hexacarbonyl[J].J Organomet Chem,2010,695(5):721-729.
[13]Fen F X,Cedric T,Xiu F W,et al.Controlling carbon monoxide binding at di-iron units related to the iron-only hydrogenase sub-site[J].Chem Commun,2008,5:606-608.
[14]Jean F C,Sa?d E H,Frederic G,et al.N-heterocyclic carbene ligands as cyanide mimics in diiron models of the all-iron hydrogenase active site[J].Organometallics,2005,24(9):2020-2022.
[15]Frederic G,Joshua D L,Michael S,et al.Synthetic and structural studies on Fe2(SR)2(CN)x(CO)x-6-xas active site models for Fe-only hydrogenases[J].J Am Chem Soc,2001,123(50):12518-12527.
[16]Ying T,Zhen H W,Wei Z,et al.Diiron complexes with pendant phenol group(s)as mimics of the diiron subunit of FeFe-hydrogenase:Synthesis,characterisation and electrochemical investigation[J].Eur J Inorg Chem,2011,7:1112-1120.
[17]Xiang H Z,Zhi M L,Zhi Y X,et al.Using pendant ferrocenyl group(s)as an intramolecular standard to probe the reduction of diiron hexacarbonyl model complexes for the sub-unit of FeFe-hydrogenase[J].Electrochem Commun,2010,12(3):342-345.
[18]Yan W W,Zhi M L,Xiang H Z,et al.Synthesis and characterisation of three diiron tetracarbonyl complexes related to the diiron centre of[FeFe]-hydrogenase and their protonating electrochemical investigations[J].New J Chem,2009,33(8):
·快遞論文·
Synthesis and Catalytic Activities of Polymeric
Materials Based on[FeFe]-Hydrogenase Model Complex
ZHENG Li-Di,YE Ping,WANG Hong-Dan,
SHEN Jie,FAN Lu,LIANG Shao-Wei,DAI Qiang-Qiang,ZHOU Shen-Chao,ZHANG Jing-Xin,ZHANG Hao,ZHONG Wei
(College of Biological,Chemical Sciences and Engineering,Jiaxing University,Jiaxing 314001,China)
Abstract:Three polymeric materials[Mr(r=5.5,9.0,12.0)],based on[FeFe]-hydrogenase model complex,were synthesized according to different mass ratio(r)[m(Fe-NHS)∶m(PEICO2H)],using PEI,NHS and BPA as materials.The structures and performance were characterized by IR and CV.The catalytic activities of M5.5,M9.0and M12.0in AcOH were investigated by cyclic voltammetry method.The results showed that M12.0exhibited better catalytic activities.The catalytic current of M12.0was 2.0 μA.
Keywords:[FeFe]-hydrogenase; polymeric material; synthesis; cyclic voltammetry method; catalytic activity
通訊作者:鐘偉,博士,講師,E-mail:weizhong@ mail.zjxu.edu.cn
作者簡介:鄭禮迪(1993-),男,漢族,廣東珠海人,本科生,主要從事金屬配合物催化體系的合成研究。E-mail:zhenglidi17@163.com
基金項目:嘉興學院大學生科學研究訓練計劃重點項目(851713014)
收稿日期:2014-08-26;
修訂日期:2015-04-29
DOI:10.15952/j.cnki.cjsc.1005-1511.2015.06.0490 *
文獻標識碼:A
中圖分類號:O614.8; O633.2

