含硼替佐米的BDT、BCD、BAD化療方案治療初診性多發性骨髓瘤
董月華,徐風華,趙麗君
含硼替佐米的BDT、BCD、BAD化療方案治療初診性多發性骨髓瘤
董月華,徐風華,趙麗君
目的研究分析硼替佐米為主的聯合化療方案BDT、BCD、BAD治療初診性多發性骨髓瘤的整體臨床效果及不良反應。方法回顧性分析筆者所在醫院2011年1月—2015年6月收治的初診性多發性骨髓瘤患者210例,分別行BDT方案化療(B1組)92例,BCD方案化療(B2組)89例,BAD方案化療(B3組)29例。結果聯合化療方案中,B1組治療后有效率為80.43%,B2組治療后有效率為86.52%,B3組治療后有效率為93.11%,三組比較,B3組治療后有效率略高于B2組和B1組的治療后有效率 (P=0.0145);B2組治療后有效率略高于B1組 (P=0.0386);化療后各組的不良反應發生情況比較,粒細胞降低中B1組發生率小于B2組(P=0.0392),B2組小于B3組(P=0.117);血小板降低中,B2組發生率明顯高于B3組(P=0.046),B3組發生率明顯高于B1組(P=0.029);疲乏患者中,B3組發生率明顯高于B2組(P=0.028),而B2組與B1組間無顯著差異(P=0.938);病毒皰疹中,B1組發生率明顯高于B2組(P=0.006)和B3組(P=0.018),而B3組發生率明顯高于B2組(P=0.033),比較差異具有統計學意義;貧血、感染、腹瀉、腹水并發癥發生情況中,三組間無顯著差異,比較無統計學意義(P>0.05)。結論以硼替佐米(萬珂)為主的聯合化療方案BDT、BCD、BAD治療初診多發性骨髓瘤均可取得較好的臨床療效,尤其以BAD的聯合用藥有效率最高。但是由于該研究的病例尚數量不足,何種方案最優還需進一步研究,對于臨床醫師的選擇應用還需其根據患者的具體情況進行制定。
多發性骨髓瘤;硼替佐米;聯合化療方案
目前多發性骨髓瘤 (multiple myeloma,MM)在血液系統腫瘤的發生率可達12%,其為單克隆漿細胞增生性腫瘤[1]。隨著醫學研究的不斷深入,以往化療方案無法滿足臨床醫師的要求及患者的期望。硼替佐米的作用主要是將細胞內控制細胞凋亡和傳導信號的蛋白質阻斷降解,最終是腫瘤細胞凋亡,臨床應用已取得較好的療效[2]。該研究參照以往臨床研究,通過對筆者所在醫院2011年1月—2015年6月初診性多發性骨髓瘤患者210例MM患者進行研究,回顧性分析三種硼替佐米為主的聯合化療方案治療初診性多發性骨髓瘤的綜合治療效果,現報告如下。
1 資料與方法
1.1 一般資料納入標準:(1)所有患者均為初診性多發性骨髓瘤;(2)以往未行相關化療治療;(3)均需行及時的化療治療,且具有有效的血、尿從蛋白標本已進行相關指標評估;(4)化療方案均為硼替佐米為基礎;(5)多發性骨髓瘤根據WHO標準進行診斷;(6)所有患者均行D-S(Durie-Salmon)和ISS(International Staging System)分期;(7)均無腎功能不全者。回顧性分析筆者所在醫院2011年1月—2015年6月收治的初診性多發性骨髓瘤患者210例;其中男134例,女76例;年齡41~76歲,平均(62.17±5.06)歲;Lg分型中,LgA 61例,LgG 124例,LgD 25例;初診時D-S分期中,Ⅰ期36例,Ⅱ其69例,Ⅲ期105例;ISS分期中,Ⅰ期40例,Ⅱ其79例,Ⅲ期91例。210例患者中,行BDT方案化療(B1組)92例,BCD方案化療(B2組)89例,BAD方案化療(B3組)29例。所有患者及家屬均自愿參加該次研究并已簽署知情同意書,該院醫學倫理委員會已批準該研究內容并對全程進行監督。
1.2 治療方法BDT方案化療中,于治療的1、4、8、11 d靜脈注射1.2 mg/m2的硼替佐米,于治療的1、2、3、4 d靜脈滴注20 mg/d地塞米松,化療間口服應用80 mg/d沙利度胺;BCD方案化療中,于治療的1、4、8、11 d靜脈注射1.2 mg/m2的硼替佐米,于治療的1、2、3、4 d靜脈滴注140 mg/m2環磷酰胺,于治療的1、2、3、4 d靜脈滴注20 mg/d地塞米松;BAD方案化療中,于治療的1、4、8、11 d靜脈注射1.2 mg/m2的硼替佐米,于治療的1、2、3、4 d靜脈滴注20 mg/d地塞米松,于治療的1、2、3、4 d靜脈滴注阿霉素15 mg/m2,所有患者均行2~4個療程治療。
1.3 觀察指標根據國際MNI工作組的腫瘤治療后臨床效果評估標準[3],分為完全緩解(complete remission,CR),很好的部分緩解(very good partial response,VGPR),部分緩解(partial response,PR),疾病穩定(stable disease,SD),疾病進展(progressive disease,PD)。有效率為完全緩解例數+很好的部分緩解例數+部分緩解例數/整體例數×100%。無進展生存期(PFS)為患者從起始治療至病情進一步發展的時間;總體生存期(OS)為患者從起始治療至死亡或隨訪停止時間[4]。
1.4 統計學分析采用SPSS 20.0軟件進行分析。患者臨床特征、臨床效果的組間比較采用Pearson χ2檢驗進行比較,采用Kaplan Meie生存函數對患者生存資料進行分析,采用log-rank法行組間生存數據比較。
2 結果
2.1 三組多發性骨髓瘤一般資料見表1。
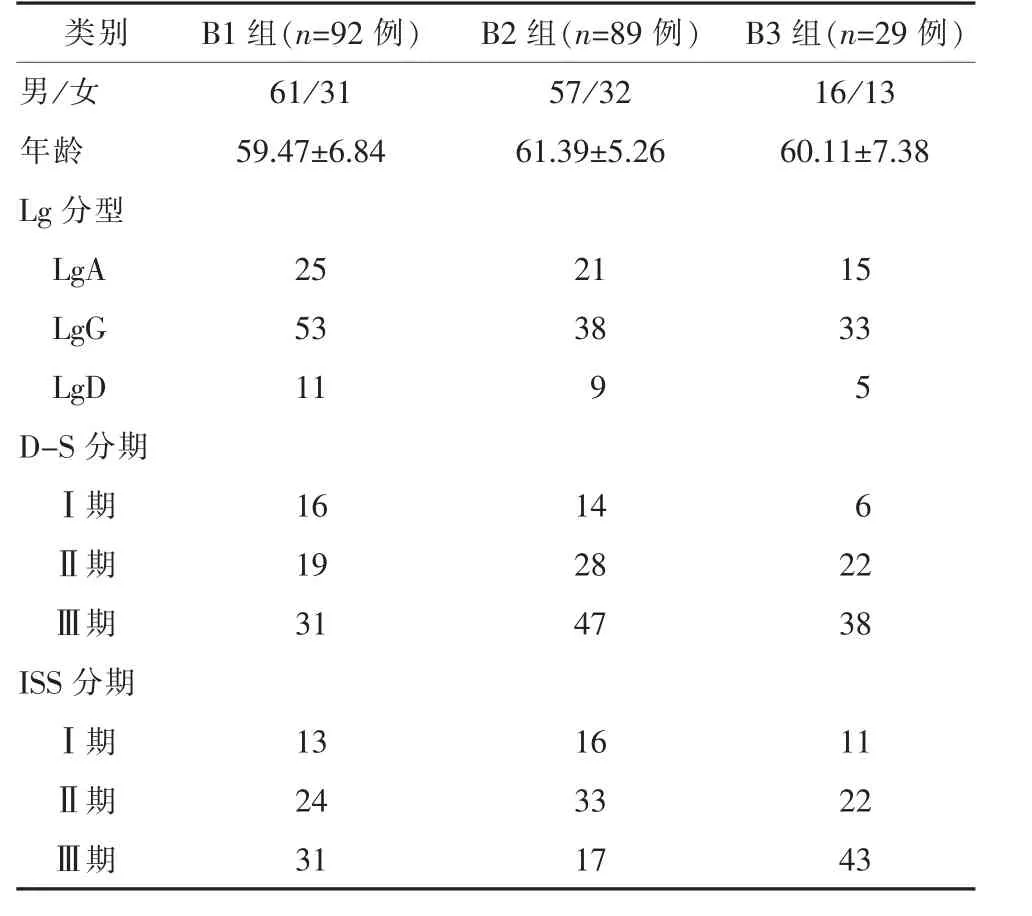
表1 三組多發性骨髓瘤一般資料
2.2 三組患者治療后臨床療效評估比較研究表明,聯合化療方案中,B1組治療后有效率為80.43%,B2組治療后有效率為86.52%,B3組治療后有效率為93.11%,三組比較,B3組治療后有效率略高于B2組和B1組的治療后有效率(P=0.0145);B2組治療后有效率略高于B1組(P=0.0386),見表2。
2.3 三組患者各臨床指標及基數資料與PFS、OS的相關性210例患者中,≥60歲患者的PFS明顯低于<60歲患者 (P=0.0295),≥60歲患者的OS明顯低于<60歲患者(P=0.0017),證明了低年齡患者的PFS、OS明顯優于高年齡患者;血清白蛋白指標比較,≥35 g/L患者的PFS顯著多于<35 g/L患者(P=0.0384);β2微球蛋白比較中,<3500 μg/L患者PFS明顯高于3500~5000 μg/L患者(P=0.0096),而3500~5000 μg/L的患者PFS略高于>5000 μg/L的患者(P=0.0228),比較具有統計學意義;在不同D-S分期和ISS分期情況下,PFS也有所不同,D-S分期中,Ⅰ期患者的PFS顯著小于Ⅱ期患者 (P=0.0176),而Ⅱ期患者的PFS顯著大于Ⅲ期患者(P=0.0426),Ⅰ期、Ⅲ期患者的PFS無顯著差異,比較無統計學意義(P>0.05);ISS分期中,Ⅰ期患者的PFS顯著高于Ⅱ期患者(P=0.0205),而Ⅱ期患者的PFS明顯小于Ⅲ期患者(P=0.0329),Ⅰ期、Ⅲ期患者的PFS無顯著差異,比較無統計學意義(P>0.05);骨髓原始漿細胞比率比較,≥10%患者的PFS顯著低于<10%患者(P=0.0191);血紅蛋白比較,≥90 g/L患者的PFS顯著高于<90 g/L患者(P=0.0314);乳酸脫氫酶水平比較,≥250 U/L患者的PFS明顯低于<250 U/L的患者(P=0.0097)。見表3。
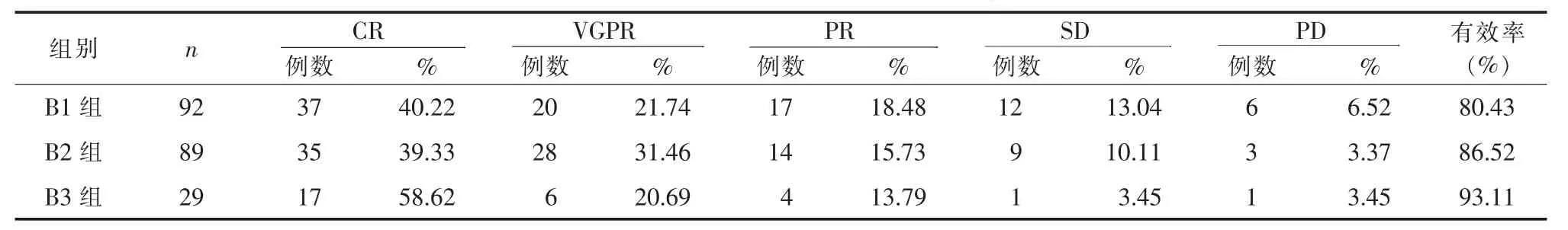
表2 三組患者治療后臨床療效評估比較

表3 三組患者各臨床指標及基數資料與PFS、OS的相關性
2.4 化療后各組的不良反應發生情況比較粒細胞降低中B1組發生率小于B2組 (P=0.0392),B2組小于B3組(P=0.117);血小板降低情況中,B2組發生率明顯高于B3組(P=0.046),B3組發生率明顯高于B1組(P=0.029);疲乏患者中,B3組發生率明顯高于B2組(P=0.028),而B2組與B1組間無顯著差異(P=0.938);病毒皰疹中,B1組發生率明顯高于B2組(P=0.006)和B3組(P=0.018),而B3組發生率明顯高于B2組(P=0.033),比較差異具有統計學意義;貧血、感染、腹瀉、腹水并發癥發生情況中,三組間無顯著差異,比較無統計學意義(P>0.05),見表4。

表4 三組患者治療后不良反應情況比較
3 討論
多發性骨髓瘤是臨床上較為常見的惡性腫瘤,其治療后的癥狀緩解程度與患者的生活質量、生存時間之間緊密相連[5]。硼替佐米(萬珂)的作用主要是將細胞內控制細胞凋亡和傳導信號的蛋白質阻斷降解,最終是腫瘤細胞凋亡,降低或抑制血管新生細胞因子表達,阻礙腫瘤細胞和其基質互相附著,療效顯著,不良反應較其他同類藥物更少[6]。
沙利度胺作為谷氨酸衍生物的鎮靜藥和止痛藥,可用于抗腫瘤、血液系統疾病的治療。可以刺激血管生成的主要為血管內皮生長和成纖維細胞因子,其特異性受體可以和刺激信號結合轉化傳導,導致內皮細胞增多[7]。沙利度胺可以減少成纖維細胞和血管內皮生長因子分泌,導致血管生成收到抑制。有研究表明[8],沙利度胺除了對血管生成具有抑制作用外,還可使整合素亞基減少合成,也是此藥比較重要的抗腫瘤機制。
環磷酰胺對惡性淋巴瘤、多發性骨髓瘤具有較好的臨床效果。藥物在人體內通過肝、腫瘤內的磷酰胺酶或磷酸酶水解,使之成為活化型磷酰胺氮芥,其作用和氮芥相似,可以達到DNA的合成抑制作用,屬細胞周期非特異性藥物。阿霉素是抗腫瘤抗生素藥物,其可對DNA、RNA的合成起到抑制,對RNA抑制作用最強,對臨床較多腫瘤均有一定的作用,同樣也屬于周期非特異性藥物[9]。
以上藥物在臨床上治療腫瘤已得到廣泛使用,其作用機制與硼替佐米并不相同,因此該研究在硼替佐米和地塞米松聯合應用的基礎上,加入環磷酰胺和阿霉素,分別組成BDT(硼替佐米、地塞米松、沙利度胺)、BCD(硼替佐米、地塞米松、環磷酰胺)、BAD(硼替佐米、地塞米松、阿霉素)化療方案,本研究采用三種化療方案對210例初診行多發性骨髓瘤患者進行治療,其中BDT組治療后有效率為80.43%,BCD組治療后有效率為86.52%,BAD組治療后有效率為93.11%,三組比較,BAD組治療后有效率略高于BCD組和BDT組的治療后有效率 (P=0.0145);而BCD組治療后有效率略高于BDT組(P=0.0386)。
該研究認為,多發性骨髓瘤患者治療后恢復期情況主要與年齡、血清白蛋白、β2微球蛋白、D-S分期、ISS分期、骨髓原始漿細胞比率等有關。210例患者中,≥60歲患者的PFS明顯低于<60歲患者 (P=0.0295),≥60歲患者的 OS明顯低于<60歲患者(P=0.0017),證明了低年齡患者的PFS、OS明顯優于高年齡患者;血清白蛋白≥35 g/L、β2微球蛋白<3500 μg/L、骨髓原始漿細胞比率<10%、血紅蛋白≥90 g/L、乳酸脫氫酶<250 U/L患者均具有較長的PFS。D-S分期中,Ⅱ期患者的PFS最長,Ⅰ期、Ⅲ期患者PFS無顯著差異,比較無統計學意義 (P>0.05);ISS分期中,Ⅰ期、Ⅲ期患者的PFS相對較長,Ⅱ期PFS有所縮短。
不良反應是化療后經常出現的問題,該研究結果顯示不同聯合藥物所出現的不良反應發生率也有所不同,粒細胞降低發生率中,BDT組<BCD組<BAD組;血小板降低發生率中,BCD組>BAD組>BDT組;疲乏患者中,BAD組>BCD組,BDT組與BCD組間無顯著差異(P=0.938);病毒皰疹發生率中,BDT組>BAD組>BCD組,比較差異具有統計學意義;而貧血、感染、腹瀉、腹水并發癥發生情況中,三組間無顯著差異。值得注意的是,各種聯合治療方案治療后的周圍神經病變均較高,有研究表明[10,11]硼替佐米(萬珂)的主要不良反應為周圍神經病,在使用此藥物時,需監測患者神經病表現,如感覺過敏、減退、異常、不適感或神經痛。如果患者出現新的周圍神經病或其癥狀加重,則需對治療方案進行調整。
綜上所述,以硼替佐米為主的聯合化療方案BDT、BCD、BAD治療初診多發性骨髓瘤均可取得較好的臨床療效,尤其以BAD的聯合用藥有效率最高。但是由于該研究的病例尚數量不足,何種方案最優還需進一步研究,對于臨床醫師的選擇應用還需其根據患者的具體情況進行制定。對不良反應方面,該研究認為應盡量避免與其他具有神經毒性藥物同階段應用。
[1]徐 源.DC-CIK治療難治性多發性骨髓瘤的臨床研究[J].實用癌癥雜志,2015,30(3):454-456.
[2]莊 韻,沈 群.多發性骨髓瘤維持治療的最新進展[J].中國實驗血液學雜志,2015,23(1):250-254.
[3]中國多發性骨髓瘤工作組.中國多發性骨髓瘤診治指南2011年修訂[J].中華內科雜志,2011,50(10):892-896.
[4]鐘國成,顏 斌,孫 薏,等.DC-CIK過繼免疫聯合化療治療多發性骨髓瘤的療效分析[J].中華血液學雜志,2012,33(12):1000-1003.
[5]周仲昊,王 智.蛋白酶體抑制劑治療多發性骨髓瘤臨床觀察[J].中華全科醫學,2012,11(3):1739-1740.
[6]梁賾隱,任漢云,岑溪南,等.硼替佐米為基礎的化療方案治療多發性骨髓瘤患者的療效及預后因素分析[J].中華血液學雜志,2014,35(3):225-230.
[7]Attal M,Lauwers-Cances V,Marit G,et al.Lenalidomide maintenance after stem-cell transplantation for multiple myeloma[J].N Engl J Med,2012,366(19):1782-1791.
[8]陳 飛,王玉娟,張克儉,等.硼替佐米聯合地塞米松及沙利度胺治療多發性骨髓瘤臨床觀察[J].臨床血液學雜志,2011,24(3):176-177.
[9]徐淑芬,白 海,王存邦,等.硼替佐米為主方案與常規化療方案治療多發性骨髓瘤療效比較[J].現代腫瘤醫學,2015,23(11):1585-1588.
[10]徐麗麗,邱慧穎,胡曉霞,等.含硼替佐米的聯合化療方案治療初診多發性骨髓瘤患者的療效比較[J].中華血液學雜志,2014,35(5):448-450.
[11]黃曉暉.硼替佐米及沙利度胺聯合VAD方案治療難治復發性多發性骨髓瘤療效觀察[J].臨床血液學雜志,2010,23(1):36-37.
[2015-10-16收稿,2015-11-14修回]
[本文編輯:董冰媛]
Contained-bortezomib BDT,BCD or BAD chemotherapy for newly diagnosed multiple myeloma
DONG Yue-hua,XV Feng-hua,ZHAO Li-jun.
The First Internal Medicine Dept.of Beijing General Troop's Hospital of Armed Police,Beijing 100027,China
ObjectiveTo investigate the overall clinical efficacy and adverse reaction of BDT,BCD or BAD combination chemotherapy based on bortezomib for patients with newly diagnosed multiple myeloma.Methods The 210 patients with newly diagnosed multiple myeloma treated in author's hospital from January 2011 to June 2015 were retrospectively analyzed.Among them,92 cases received BDT chemotherapy(B1 group),89 cases received BCD chemotherapy(B2 group)and 20 cases received BAD chemotherapy(B3 group).Results In combination chemotherapy,the effective rate after treatment was 80.43%in B1 group,86.52%in B2 group and 93.11%in B3 group respectively.Among these three groups,the effective rate after treatment was slightly higher in B3 group than that of B2 and B1 group(P=0.0145);In addition,the effective rate after treatment was slightly higher in B2 group than that of B1 group(P=0.0392);Through comparing incidences of adverse effects in different groups,the incidence of reducing granulocyte in B1 group was lower than that of B2 group(P=0.0392)and B2 group was lower than B3 group(P=0.117);There was significantly higher incidence of reducing platelet in B2 group than that of B3 group(P=0.046),and B3 group was significantly higher than B1 group(P=0.029);B3 group had higher incidence of fatigue than that of B2 group(P=0.028),however,there was no significant difference between B2 and B1 group(P=0.938);The incidence of herpes was significantly higher in B1 group than that of B2 group(P=0.006)and B3 group(P=0.018),and B3 group was significantly higher than B2 group(P=0.033),with a statistically significant difference.There were no significant differences in the incidence of complications such as anemia,infection,diarrhea and ascites between three groups,without a statistically significant difference(P>0.05).ConclusionsAll the BDT,BCD or BAD combination chemotherapy based on bortezomib for patients with newly diagnosed multiple myeloma can achieve good clinical efficacy,among them,BAD is especially the most effective therapy.However,as for the limited number of cases included in this study,further studies are needed to decide which therapy is the best.Thus,for practical choice in clinic,it should be based on specific conditions.
Multiple myeloma;Bortezomib;Combination chemotherapy
R733.3
A
10.14172/j.issn1671-4008.2016.04.005
100027北京,武警北京總隊醫院內一科(董月華,徐風華,趙麗君)

