植物法改性類Fenton反應催化劑降解甲基橙
秦聰麗,傅吉全
(北京服裝學院 材料科學與工程學院,北京 100029)
植物法改性類Fenton反應催化劑降解甲基橙
秦聰麗,傅吉全
(北京服裝學院 材料科學與工程學院,北京 100029)
采用銀杏葉和桑葉提取液制備了改性類Fenton反應催化劑并進行了表征分析,研究了溶液初始pH、反應溫度、催化劑加入量、甲基橙初始質量濃度等因素對甲基橙降解率的影響,同時考察了催化劑的重復使用效果。表征結果表明:制備出的催化劑為Fe2O3和FeOOH的混合物;桑葉改性催化劑的粒徑分布較銀杏葉改性催化劑均勻,粒徑較小,比表面積較大。實驗結果表明:在初始pH為6.23、反應溫度60 ℃、催化劑用量1 g/L、甲基橙初始質量濃度100 mg/L的條件下,銀杏葉改性催化劑的甲基橙降解率為99.40%,桑葉改性催化劑的甲基橙降解率為99.96%;堿性條件下,甲基橙降解率仍接近100%,擴寬了反應的pH適用范圍,為堿性條件下處理偶氮染料提供了新思路;催化劑重復使用6次之后,甲基橙降解率仍可達到99%。根據反應前后溶液的紫外-可見吸收光譜,初步探討了降解機理。
銀杏葉;桑葉;改性;類Fenton試劑;催化劑;降解;甲基橙
染料廢水是水污染控制領域中的有害廢水之一,而其中占主要部分的為偶氮染料廢水[1]。偶氮染料在日常生活中被廣泛應用,但有些偶氮染料會產生致癌物,從而嚴重危害人體健康[2-4]。因此,偶氮染料的處理一直受到人們的關注。利用Fenton試劑氧化法降解廢水中的偶氮染料,是研究者關注的熱門話題。但該方法存在許多不足,如催化劑的分離和重復利用問題以及反應過程中產生的鐵泥對環境造成二次污染的問題[5-9]。植物改性法是利用植物中的某些基團與鐵離子進行反應制備鐵氧化物[10]。相對于化學法,該方法具有反應條件溫和、對環境危害小、植物來源廣等優點,是納米材料的一種新型綠色合成方法,現已引起學者的廣泛關注。Mahnaz等[11]以FeCl3為鐵源,與褐藻提取液反應,成功制備出了粒徑為(18±4) nm的立方體形Fe3O4磁性納米顆粒。
本工作以甲基橙溶液模擬印染廢水,采用植物法對類Fenton反應催化劑(改性催化劑)進行改性,并考察其對溶液中甲基橙的降解效果。該法拓展了非均相類Fenton體系的應用,解決了催化劑的分離以及重復使用問題,并從源頭上減少了化學試劑的使用,為印染廢水提供了一種新的處理方法,具有工業應用價值。
1 實驗部分
1.1 試劑和儀器
硫酸亞鐵、H2O2、去離子水、無水乙醇、甲基橙:均為分析純;銀杏葉和桑葉:九月采自北京服裝學院。
Lambda 750型紫外-可見分光光度計:美國珀金埃爾默公司;PHS-3B型pH計:上海雷磁儀器廠;Sigma Probe型X射線光電子能譜(XPS)儀:英國ThermoVG公司;JSM-6360LV型掃描電子顯微鏡(SEM):JOEL公司;Thermo型傅里葉變換紅外光譜(FTIR)儀:天津瑞岸科技有限公司;TCL-16C Anke型離心機:上海安亭科學儀器制造廠;FW80型高速萬能粉碎機:天津泰斯特儀器有限公司。
1.2 實驗方法
植物提取液的制備:將采集的銀杏葉(桑葉)洗凈、曬干,用高速萬能粉碎機粉碎至粒徑約為150 μm。稱取5 g銀杏葉(桑葉)干粉于錐形瓶中,加入100 mL去離子水和150 mL無水乙醇,于60 ℃水浴加熱24 h,自然冷卻,過濾得到質量濃度為20 g/L的銀杏葉(桑葉)提取液。
改性催化劑的制備:量取一定體積的銀杏葉(桑葉)提取液,與濃度為0.1 mol/L的FeSO4溶液等體積混合,50 ℃水浴加熱4 h。離心,將所得沉淀水洗后在真空干燥箱中干燥。
甲基橙的降解:取一定體積一定濃度的甲基橙溶液,加入濃度為0.1 mmol/L的H2O2溶液及一定量的改性催化劑,調節pH,在恒溫振蕩器中反應30 min至達到反應平衡,離心后測定溶液的吸光度,計算甲基橙質量濃度及甲基橙降解率。
催化劑的重復使用:以銀杏葉改性催化劑為例,考察催化劑的重復使用情況。每次反應結束后離心收集催化劑,用蒸餾水反復洗滌,干燥后用于下次實驗。
1.3 分析方法
采用紫外-可見分光光度計在464 nm處測定溶液的吸光度,比色皿規格為1 cm×1 cm,以去離子水為參比。采用 XPS譜圖表征催化劑的化學狀態及表面化學元素組成,雙陽極(Mg靶和Al靶),能量分辨率0.47 eV,最小分辨區域15 μm。采用 SEM觀察改性催化劑的形貌,掃描電壓5 kV。采用FTIR譜圖表征改性前后以及反應前后的催化劑。
2 結果與討論
2.1 改性催化劑的表征
2.1.1 XPS分析
改性催化劑的XPS譜圖見圖1。由圖1可見,經過植物改性后的催化劑分別在725 eV和711 eV附近出現譜峰,分別對應Fe2O3和FeOOH的標準峰位置,說明制備出的催化劑為Fe2O3和FeOOH的混合物。
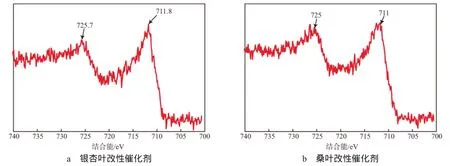
圖1 改性催化劑的XPS譜圖
2.1.2 SEM分析
改性催化劑的SEM照片見圖2。由圖2可見,制備的催化劑為球形,形貌大小分布都很均勻,這可能是由于植物體中的基團對催化劑進行了保護,抑制了顆粒的團聚。從圖2中還可看出,桑葉改性催化劑的粒徑分布較銀杏葉改性催化劑均勻,粒徑較小,比表面積較大。

圖2 改性催化劑的SEM照片
2.1.3 FTIR分析
銀杏葉改性催化劑的FTIR譜圖見圖3。由圖3可見:3 330 cm-1處為N—H鍵和O—H鍵的振動吸收峰,2 924,2 851 cm-1處為飽和長碳鏈C—H鍵的伸縮振動吸收峰,1 605 cm-1處為N—H鍵的振動吸收峰,1 040 cm-1處為—OCH2的振動吸收峰;對比a,b,d譜線,發現改性催化劑出現了銀杏葉提取液干粉的特征峰(2 924,2 851,1 605 cm-1處),說明銀杏葉起到了改性作用,銀杏葉和催化劑之間的作用可能是鐵原子與銀杏葉中的氨基氮原子或甲氧基中的氧原子之間的配位作用;對比b,c譜線,發現降解反應前后催化劑的出峰位置和峰的強度基本沒有變化,說明植物還原法改性的催化劑比較穩定,具有較好的重復利用性。
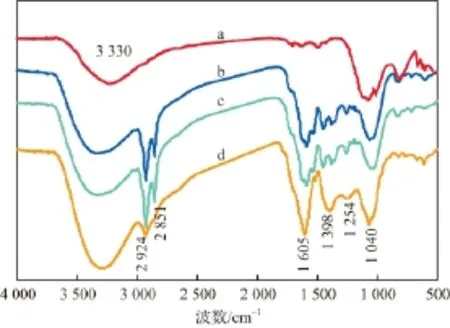
圖3 銀杏葉改性催化劑的FTIR譜圖
2.2 甲基橙降解的影響因素
2.2.1 初始pH的影響
在反應溫度為60 ℃、催化劑加入量為1 g/L、甲基橙初始質量濃度為100 mg/L的條件下,初始pH對甲基橙降解率的影響見圖4。由圖4可見,經植物改性后的催化劑對甲基橙的降解效果明顯增強,且植物改性后的催化劑對甲基橙無論是在酸性還是在堿性條件下都有很好的降解效果,甲基橙降解率都在98%以上。其原因為:H2O2在催化劑的催化作用下產生·OH,H+有助于·OH的產生,因此在酸性條件下,有很好的降解效果;隨著pH升高,·OH產率降低,但本工作制備出的催化劑含有FeOOH,彌補了·OH的不足,因此在堿性條件下仍可達到98.61%的甲基橙降解率,為堿性條件下偶氮染料的降解提供了一種新思路。
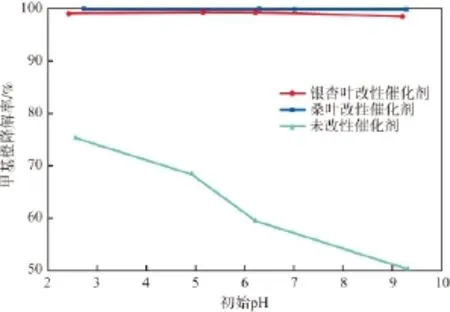
圖4 初始pH對甲基橙降解率的影響
2.2.2 反應溫度的影響
在初始pH為6.23、催化劑加入量為1 g/L、甲基橙初始質量濃度為100 mg/L的條件下,反應溫度對甲基橙降解率的影響見圖5。由圖5可見:銀杏葉改性催化劑的甲基橙降解率隨反應溫度的升高而增大,60 ℃時達99.4%;而桑葉改性催化劑的甲基橙降解率受反應溫度影響不大,在30~60 ℃范圍內均可達99%以上。分析其原因可能是由于提高反應溫度,反應體系中甲基橙分子的擴散速度增加,且H2O2產生·OH的速率也變快,從而促進了反應的進行。對比兩種改性催化劑發現,桑葉改性催化劑的降解效果比銀杏葉改性催化劑好,參照圖2 SEM照片分析其原因為:桑葉改性催化劑粒徑分布更加均勻,顆粒較小,比表面積較大,因此降解效果更好。
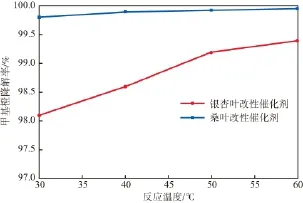
圖5 反應溫度對甲基橙降解率的影響
2.2.3 催化劑加入量的影響
在初始pH為6.23、反應溫度為60 ℃、甲基橙初始質量濃度為100 mg/L的條件下,催化劑加入量對甲基橙降解率的影響見圖6。由圖6可見:當改性催化劑的加入量從0.01 g/L增加至0.25 g/L時,甲基橙降解率增加較快,再繼續增大催化劑加入量,甲基橙降解率增加較慢,桑葉改性催化劑當催化劑加入量為0.50 g/L時,甲基橙降解率已接近100%。這是因為隨著催化劑加入量的增加,催化劑總表面積增大,活性位點增加,吸附和還原的甲基橙分子數量增大,因而使甲基橙降解率增大。
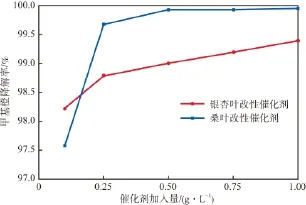
圖6 催化劑加入量對甲基橙降解率的影響
2.2.4 甲基橙初始質量濃度的影響
在初始pH為6.23、反應溫度為60 ℃、催化劑加入量為1 g/L的條件下,甲基橙初始濃度對甲基橙降解率的影響見圖7。由圖7可見:甲基橙降解率均隨初始質量濃度的增大而減小;銀杏葉改性催化劑受初始質量濃度影響較大;桑葉改性催化劑隨著初始濃度的增加變化較小。分析其原因:1)可能由于甲基橙初始濃度較小時,催化劑表面的活性位點相對甲基橙分子數是過量的,因此有較高的降解率;而隨著甲基橙濃度的增大,甲基橙對固定數目的活性位點競爭增強,接觸活性位點的可能性減少,從而降低了降解率。2)桑葉改性催化劑比銀杏葉改性催化劑分布更均勻,因此催化活性較好。
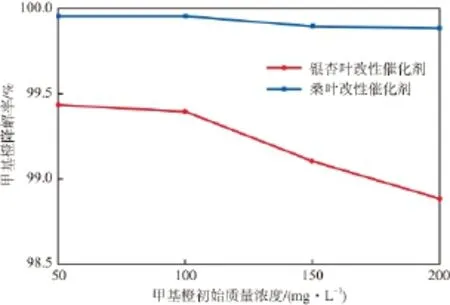
圖7 甲基橙初始質量濃度對甲基橙降解率的影響
2.3 催化劑的重復使用效果
在初始pH為6.23、反應溫度為60 ℃、催化劑加入量為1 g/L、甲基橙初始質量濃度為100 mg/L的條件下,銀杏葉改性催化劑的重復使用效果見表1。由表1可見,重復使用6次后銀杏葉改性催化劑仍保持著良好的催化活性,甲基橙降解率仍可達99.51%。表明銀杏葉改性催化劑重復使用效果好,同時具有很好的穩定性。
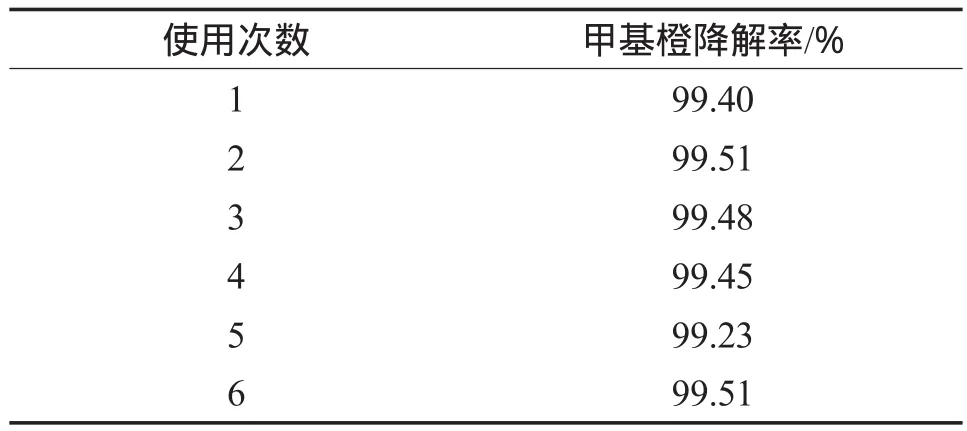
表1 銀杏葉改性催化劑的重復使用效果
2.4 降解機理的探討
在初始pH為6.25、反應溫度為60 ℃、催化劑加入量為1 g/L、甲基橙初始質量濃度為100 mg/L的條件下,以銀杏葉改性催化劑處理甲基橙溶液。反應前后甲基橙溶液的紫外-可見吸收光譜譜圖見圖8。由圖8可見:甲基橙在270 nm和464 nm附近各有一個吸收峰,其中270 nm處為甲基橙分子結構中苯環π-π共軛鍵的吸收峰,464 nm處為甲基橙分子中偶氮基團的吸收峰;反應后,270 nm處的吸收峰強度減弱,464 nm處的吸收峰基本消失。分析其原因可能是:1)苯環分子中的共軛結構和偶氮基團被破壞;2)催化劑對甲基橙的吸收作用;3)二者共同作用的結果。
結合本工作的實驗結果和相關文獻,推測植物改性類芬頓法降解甲基橙的機理可能有兩個方面:1)催化劑對甲基橙的吸收和吸附作用;2)催化劑催化H2O2產生具有強氧化性的·OH與甲基橙分子發生化學反應,即破壞甲基橙分子結構中的苯環的π-π共軛鍵以及偶氮基團。具體的過程可能為:H2O2吸附至催化劑表面,使Fe3+轉變為Fe2+;催化劑表面形成的Fe2+與H2O2反應生成具有強氧化性的·OH;·OH擴散到溶液中,與甲基橙分子發生氧化還原反應,從而降解甲基橙。
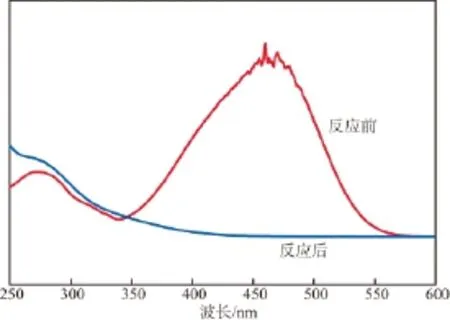
圖8 反應前后甲基橙溶液的紫外-可見吸收光譜圖
3 結論
a)采用銀杏葉和桑葉提取液制備改性類Fenton反應催化劑,對溶液中的甲基橙有很好的降解效果。在初始pH為6.23、催化劑加入量為1 g/L、甲基橙初始質量濃度為100 mg/L的條件下,銀杏葉和桑葉改性的類Fenton反應催化劑的甲基橙降解率分別為99.4%和99.96%。
b)考察了初始pH、反應溫度、催化劑加入量、甲基橙初始濃度對甲基橙降解率的影響,發現隨著pH增加,兩種植物改性催化劑對甲基橙降解率都有所下降,但在堿性條件下降解率仍可達到98%以上;隨著溫度的升高銀杏葉改性催化劑對甲基橙降解率逐漸增大,而桑葉改性催化劑的甲基橙降解率受反應溫度影響不大;隨著兩種植物改性催化劑用量的增加,甲基橙降解率均逐漸增大;隨著甲基橙初始濃度增加,兩種植物改性催化劑的甲基橙降解率均有所下降。
c)銀杏葉改性催化劑重復利用6次后,甲基橙降解率仍可達99.51%。
[1] 張林生,蔣嵐嵐. 染料廢水的脫色方法[J]. 化工環保,2000,20(1):14 - 18.
[2] 何新風. 多相類芬頓法對甲基橙染料廢水的降解研究[D]. 西安:陜西師范大學,2011
[3] 溫沁雪,王進,鄭明明,等. 印染廢水深度處理技術的研究進展及發展趨勢[J]. 化工環保,2015,35 (4):363 - 369.
[4] 梁志榮. 染料廢水物理化學處理技術的現狀與進展[J]. 四川環境,2003,22(6):25 - 29.
[5] 武智,石晶晶,陳旭東,等. Fenton試劑氧化法在工業廢水處理中的研究及應用進展[J]. 河北化工,2009(1):61 - 63.
[6] 鄭展望,雷樂成,張珍. 非均相UV/Fe-Cu-Mn-Y/ H2O2反應催化降解4BS染料廢水[J]. 環境科學學報,2004,24(6):1032 - 1038.
[7] 唐明明,劉葵,梁敏,等. 均相催化與多相催化降解甲基橙廢水[J]. 山東化工,2005,34(2):7 - 10.
[8] 倪可,王利平,李祥梅,等. 負載型金屬催化劑的制備及印染廢水的催化氧化處理[J]. 化工環保,2014,34(2):176 - 180.
[9] 何熾,趙景聯,夏敏強,等. 分子篩固載Fe2+-Fenton法降解水中甲基橙的研究[J]. 環境科學與技術,2006,12(29):1 - 3.
[10] Cezar C,Carmen T,Matei M,et al. Catalytic wet peroxide oxidation of phenol over Fe-exchanged pillared beidellite[J]. Water Res,2003,37:1154 - 1160 .
[11] Mahnaz Mahdavi,Farideh Namvar,Mansor Bin Ahmad,et al. Green biosynthesis and characterization of magnetic iron oxide (Fe3O4) nanoparticles using seaweed (sargassum muticum) aqueous extract [J]. Molecules,2013,18(5): 5954 - 5964.
(編輯 葉晶菁)
Degradation of methyl orange using plant modified catalyst for Fenton-like reaction
Qin Congli,Fu Jiquan
(School of Materials Science and Engineering,Beijing Institute of Fashion Technology,Beijing 100029,China)
The modifi ed catalysts for Fenton-like reaction were prepared using extracts of ginkgo leaf and mulberry leaf,and were characterized. The factors affecting the degradation rate of methyl orange were studied,and the reusability of the catalysts was researched. The characterization results show that:The prepared catalysts are mixtures of Fe2O3and FeOOH;Comparing with the catalyst modifi ed using ginkgo leaf,the particles of the catalyst modifi ed using mulberry leaf are more uniform with smaller size and larger specifi c surface area. The experimental results show that:Under the conditions of initial pH 6.23,reaction temperature 60 ℃,catalyst dosage 1 g/L and initial mass concentration of methyl orange 100 mg/L,the degradation rates of methyl orange on the catalysts modifi ed using ginkgo leaf and mulberry leaf are 99.40% and 99.96% respectively;The degradation rates of methyl orange keep nearly 100% under alkaline condition,which indicate that the pH range for reaction is enlarged and this provides a new way for degradation of azo dye under alkaline condition;After the catalyst has reused for 6 times,the degradation rates of methyl orange can still reach 99%. According to the UV-Vis absorption spectrum of the solutions before and after reaction,the degradation mechanism was discussed.
ginkgo leaf;mulberry leaf;modifi cation;Fenton-like reagent;catalyst;degradation;methyl orange
X703
A
1006-1878(2016)03-0312-05
10.3969/j.issn.1006-1878.2016.03.015
2015 - 11 - 29;
2015 - 11 - 26。
秦聰麗(1989—),女,河北省石家莊市人,碩士生,電話 13161085369,電郵 qincongli@126.com。聯系人:傅吉全,電話13601394362, 電郵 fujq010@sina.com。

