以頑固性胸腔出血為表現的肺上皮樣血管肉瘤1例
冀磊 張月琴
[摘要] 肺上皮樣血管肉瘤(PEA)非常罕見,僅見個案報道。目前病因不明確,尚無統一的治療標準,化療及放療都不敏感,臨床表現多樣,診斷困難。本文介紹1例以頑固性胸腔出血為表現的PEA病例的臨床表現、病理、治療經過及病情進展,進一步加深對該疾病的認識。PEA病理提示廣泛出血,發病時有咯血及多發轉移者預后極差。
[關鍵詞] 上皮樣血管肉瘤;上皮樣血管內皮細胞瘤;肺;胸腔出血
[中圖分類號] R735.7 [文獻標識碼] A [文章編號] 1674-4721(2016)02(c)-0148-03
[Abstract] Pulmonary epithelioid angiosarcoma is a kind of malignant tumor which is derived from blood vessel and very rare in clinic ,only case reports.The etiology is not clear,it has no unified standard treatment and is not sensitive to chemotherapy and radiotherapy.Because of the variety of clinical symptoms,it is difficult to diagnosis.1 case of pulmonary epithelioid angiosarcoma with refractory pleural hemorrhage was reported in this paper,in order to provide more clinical information and improve the understanding of the disease.Once pathological prompt extensive hemorrhage,hemoptysis,multiple transfer and the prognosis would be very poor.
[Key words] Epithelioid angiosarcoma;Epithelioid hemangioendothelioma;Lung;Pleural hemorrhage
肺上皮樣血管肉瘤(pulmonary epithelioid angiosarcoma,PEA)是一種極為少見的血管源性惡性腫瘤,國內外罕見報道[1-5]。目前病因不明確,治療困難,預后差,尤其對于病理提示廣泛出血,發病即有咯血及多發轉移的患者預后更差[5]。診斷主要依據病理,vimentin和CD31敏感性高。由于PEA大多是轉移而來,且原發和轉移病灶病理學形態類似[6-7],故在診斷原發性PEA時需首先排除是否存在可疑原發病灶。常見臨床表現有持續性咳嗽、血痰、胸痛等,但也可無明顯臨床癥狀[8],因其臨床表現多樣且無特異性,故容易導致誤診及漏診,從而延誤治療。本文報道1例以頑固性胸腔出血為表現的PEA病例的臨床診療經過以及病情發展過程,以期提供更多臨床資料,提高對該疾病的認識。我們相信,隨著病例報道的增多,可以掌握更多不同的臨床表現,及早診斷,同時更多的病例也可以提供更多的臨床資料,以便進一步探討治療方法,提高該疾病的預后。
1 病例資料
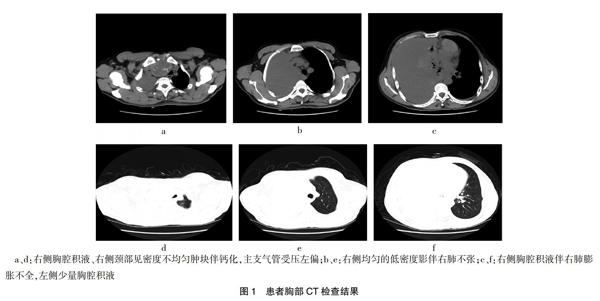
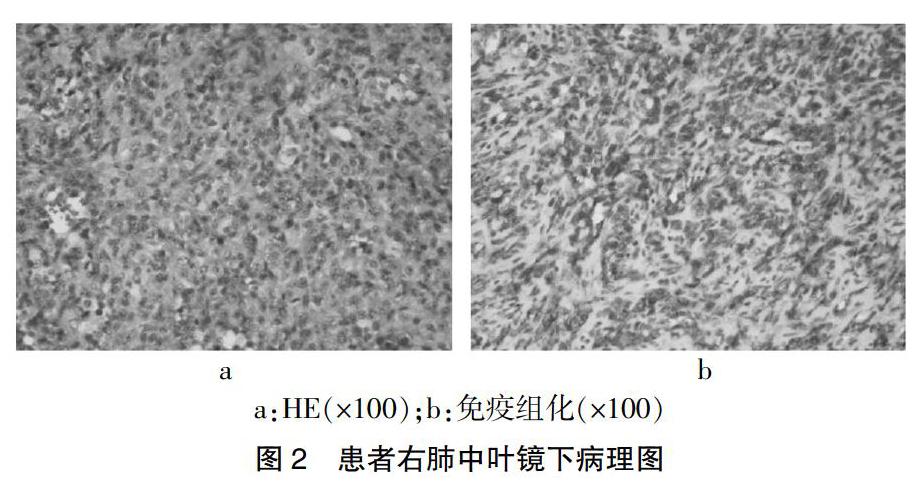
患者,男性,39歲,以“咳嗽、咯血伴胸悶20 d”入院。患者20 d前勞累后出現咳嗽、痰中帶血,24 h咯血量約50 ml,在家自服阿莫西林,癥狀未見明顯緩解,故來本院就診;既往有無特殊病史。入院查體:體溫36.2℃,脈搏85/min,呼吸頻率18/min,血壓120/80 mmHg(1 mmHg=0.133 kPa),瞼結膜輕度蒼白,右側甲狀腺Ⅱ度腫大,質中,活動度好,無壓痛,未觸及震顫,未聞及血管雜音,右側肩胛線第9后肋以下叩診呈濁音,右肺呼吸音低,余未見陽性體征。入院查甲狀腺功能:促甲狀腺激素(TSH)7.308 μIU/ml;腫瘤標志物、凝血、血清結核抗體及結核菌素試驗均未見異常;血常規:紅細胞4.08×1012/L,血紅蛋白116 g/L,白細胞9.33×109/L,血小板204×109/L。3 d后復查紅細胞及血紅蛋白明顯下降(紅細胞 2.09×1012/L,血紅蛋白53 g/L),予以止血(卡絡磺鈉)、輸血(懸浮紅細胞4 U)等積極治療后血色素無明顯提升,行右側胸腔閉式引流,可見暗紅色血性胸腔積液,不凝,胸腔積液常規:細胞計數1520×106/L,單核細胞60%,多核細胞40%,胸腔積液生化:蛋白17.238 g/L,提示胸腔積液介于滲出液及漏出液之間,胸腔積液病理細胞示大量增生的間皮細胞,個別細胞輕度異形。患者右側胸腔2 d共引流出血性不凝液體約1700 ml,血色素下降明顯。胸部CT(圖1)示右側大量胸腔積液并右肺不張,左側少量胸腔積液,右側頸部上縱隔腫塊,考慮甲狀腺腺瘤;甲狀腺彩超提示:右側甲狀腺囊實性結節。請我院胸外科會診建議行急診剖胸探查,術中可見右側胸腔大量陳舊性血液,共吸出約4200 ml,探查見右肺中葉外側段局部病變,約1.5 cm×1.5 cm,質中,邊界不清,表面有活動性出血,壁層胸膜廣泛滲血,縱隔胸膜完整,前上縱隔腫塊與胸膜無粘連,予以行右肺中葉病變楔形切除。病理:肉眼可見灰褐色組織5 cm×2 cm×1.5 cm,切開見一個0.8 cm×0.5 cm大小的灰白色區,質中,鏡下所見(圖2):腫瘤組織瘤細胞彌散排列,胞質較豐富,核大,淡然,核仁明顯,有異形性,見幼稚的小血管腔隙,局部有壞死,核分裂象>15個/10HPF(圖2a);免疫組化:AE1/AE3(+),Vinmentin(+),CD34(-),bcl-2(-),Calretinin(-),TTF-1(-),EMA(-),Mesothelial cell(-),CD31(+),FⅧ(+)(圖2b),診斷PEA。術后第1天胸腔引流出血性不凝液體量約600 ml,第2天約2200 ml,第3天約1750 ml,行胸腔積液化驗性質基本同前。患者胸腔出血仍明顯,時隔3 d第2次行右側剖胸探查,術中右側胸腔吸出少量陳舊性血液,量約100 ml,壁層胸膜仍有廣泛滲血,余未見活動性出血,術后3天共引流血性不凝液體量約5300 ml(胸腔積液性質基本同前),患者胸腔出血未得到有效控制,家屬要求自動出院,2 d后于家中病故。
2 討論
PEA發病年齡為10~73歲,平均51歲,青少年發病少,臨床可有持續性咳嗽、血痰、胸痛等表現,亦可無明顯臨床癥狀[8]。影像學主要表現為結節影,常伴衛星病灶,胸膜受累常見,可有胸腔積液,病理學表現為腫瘤細胞可排列成片狀、巢狀及不規則形,并可在幼稚血管腔內形成乳頭,血管腔可由單細胞組成或3~4個細胞圍成,管腔形成不易被發現,網織纖維染色可見大而無管腔的血管,其主要由兩種形態的細胞組成,一種為梭形細胞,另一種為上皮樣細胞,以后者多見,具有嗜酸性或嗜雙色胞質,細胞核大且異形性明顯、常見空泡[9]。免疫組化表現為幾乎所有病例vimentin表達強陽性,約90%病例CD31表達陽性[10],30%左右的病例CK呈陽性表達[11],Ⅷ因子特異性相對較高,但敏感度不夠[12]。
PEA主要應與肺上皮樣血管內皮細胞瘤(pulmonary epithelioid hemangioendothelioma,PEH)相鑒別。兩者均是來源于血管內皮源性的腫瘤,但從上皮樣血管內皮細胞瘤(epithelioid hemangioendothelioma,EH)到上皮樣血管肉瘤(epithelioid angiosarcoma,EA) 是由良性到惡性發展的過程,鑒于兩者在良惡性上及生物學行為上的差別,對兩者鑒別及明確診斷具有重要臨床意義。PEH是一種低度惡性的血管源性腫瘤,手術后易局部復發,但轉移少見,鑒別主要依靠病理學。淋巴結及遠處轉移不是區別PEH和PEA的標準[13]。PEH腫瘤常與血管壁相連,瘤細胞成巢或角狀排列,管腔樣結構多見,細胞異形性不明顯,核分裂少(1~2個/10HPF),出血及壞死少見。而PEA瘤細胞異形性顯著,核分裂多(>3個/10HPF),細胞核更大更圓,核仁更加明顯,細胞壞死和出血廣泛,淋巴管內可見癌栓,容易淋巴結轉移,Ki-67增殖指數>20%[8-12],梭形細胞增多,Kitaichi等[14]研究認為梭形細胞所占比例增多是PEA預后不良的因素。PEH和PEA病因尚不明確,大多數患者無吸煙史,可能與肺胸膜慢性炎癥及肺炎病史有關[15]。目前無統一推薦的治療方案,臨床研究發現其對化療及放療均不敏感,大多數PEH術后近期效果良好,在缺乏其他輔助治療情況下70%的患者生存期達2~20年[14],而PEA病理提示廣泛出血,發病時有咯血及多發轉移者預后極差[5]。
本病例來院時表現為胸悶、咯血、咳嗽,入院后主要以反復胸腔出血為突出表現,患者兩次剖胸探查均提示壁層胸膜廣泛滲血,雖經積極治療,但終因出血而死亡。患者出血未得到有效控制,考慮與上皮樣血管肉瘤本身性質有關,其來源于血管且不規則幼稚血管多,易導致出血,此外肺本身血供豐富,上皮樣血管肉瘤作為惡性腫瘤侵襲性生長破壞血管,造成反復出血而不易控制。
由于EA原發性和轉移性病灶在病理學上形態類似,且肺內此類腫瘤大多是轉移而來[6-7],故在診斷原發性PEA時首先需排除是否存在可疑原發病灶。該患者右側甲狀腺Ⅱ度腫大,因住院時間短,且入院后病情迅速惡化,故未行甲狀腺針吸活檢,因此目前該病例是原發于肺組織還是轉移鑒別困難,較為遺憾。
綜上,對于臨床上出現咯血、血性胸腔積液的患者,尤其是應用多種方法治療效果欠佳者,在排除常見疾病的情況下應考慮少見病如PEA,及時手術,依據病理進行診斷。雖然目前尚無有效治療方法,但早診斷可以避免一些對患者不必要的傷害,對于醫患溝通而言也非常重要,可以降低醫患之間的矛盾。隨著醫療技術的發展,像PEA這些惡性程度高、治療棘手、預后差的疾病可能會得到改善。
[參考文獻]
[1] Ozcelik C,Onat S,Yaldiz M,et al.Primary epithelioid angiosarcoma of the lung presenting as pulmonary hemorrhage[J].Asian Cardiovasc Thorac Ann,2006,14(1):69-71.
[2] Carillo GA,Carretero MA,Vazquez JE,et al.Epithelioid angiosarcoma of the lung with pleural metastases:a rare cause of haemoptysis clinicopathological conference[J].Heart Lung Circ,2010,19(10):624-628.
[3] Tochigi N,Tsuta K,Maeshima AM,et al.Malignant pulmonary epithelioid haemangioendothelioma with hilar lymph node metastasis[J].Ann Diagn Pathol,2011,15(3):207-212.
[4] 韋萍,陸鳴,周小鴿,等.肺上皮樣血管肉瘤臨床病理觀察[J].診斷病理學雜志,2006,13(4):291-293.
[5] 陳國勤,劉桂紅,莫明聰,等.肺上皮樣血管肉瘤臨床病理觀察[J].診斷病理學雜志,2013,20(3):81-84.
[6] Lund L,Anwe R.Epithelioid angiosarcoma involving the lungs[J].Arch Pathol Lab Med,2005,129(1):e7-10.
[7] Adem C,Aubry MC,Tazelaar HD,et al.Metastatic angiosarcoma masquerading as diffuse pulmonary hemorrhage:clinicopathologic analysis of 7 new patients[J].Arch Patholtab Med,2001,125(12):1562-1565.
[8] 陳灝珠,林為果.實用內科學[M].13版.北京:人民衛生出版社,2009:1810.
[9] Fletcher CD,Unni KK,Mertens F.Pathology and genetics tumours of soft tissue and bone[M].Lyon:IARC Press,2002:176-177.
[10] Travis WD,Brambilla E,Muller-Hermelink HK,et al.Pathology and genetics of tumours of the lung,plema,thymus and heart[M].Lyon:IARC Press,2004:97-98.
[11] Miettinen M,Fetsch JF.Distribution of keratins in normal endothelial cells and a spectrumof vasallar tumors:imlications in tumour diagnosis[J].Hum Pathol,2000,31(9):1062-1067.
[12] Lin BT,Colby T,Gown AM,et al.Malignant vascular tumors of the serous membranes mimicking mesothelioma:a report of 14 cases[J].Am J Surg Pathol,1996,20(1):1431-1439.
[13] Amin RM,Hiroshima K,Kokubo T,et al.Risk factors and independent predictosof surviva in patients with pulmonary epithelioid haemangioendothelioma——review of the literature and a case report[J].Respiology,2006,11(6):818-825.
[14] Kitaichi M,Nagai S,Nishimura K,et al.Pulmonary epithelioid hemangioendothelioma in 21 patients,including three partial spontaneous regression[J].Eur Respir J,1998, 12(1):89-96.
[15] Aozasa K,Naka N,Tomite Y,et al.Angiosarcoma developing from chronic pyothorax[J].Modern Pathol,1994,7(9):906-911.
(收稿日期:2015-11-05 本文編輯:衛 軻)

