從終端評價要求談“元素周期律與化學鍵”的教學策略
楊曉曼經(jīng)志俊
(南京市第三高級中學 江蘇南京 210001)
?
從終端評價要求談“元素周期律與化學鍵”的教學策略
楊曉曼經(jīng)志俊
(南京市第三高級中學江蘇南京210001)
摘要:以“元素周期律與化學鍵”為例,依據(jù)終端評價要求確定教學重點和難點;依據(jù)內(nèi)容特點通過“問題引導(dǎo)閱讀”、“情境引導(dǎo)歸納”、“活動引導(dǎo)探究”、“故事引導(dǎo)感悟”、“案例引導(dǎo)對比”等手段落實教學重點;依據(jù)難點成因,運用“整合知識,建構(gòu)聯(lián)系”、“整理素材,指導(dǎo)方法”、“精選練習,訓練思維”等策略突破教學難點。
關(guān)鍵詞:元素周期律;化學鍵;終端評價
“落實重點”、“突破難點”是課堂教學的兩項重要任務(wù)。教學實踐中,如何確定教學重點和難點,如何落實重點、突破難點是教師必須解決的現(xiàn)實問題。
一、教學重點與難點的確定
教師通常依據(jù)課程標準和教學經(jīng)驗確定教學重點和難點,但課程標準的表述過于簡潔(見表1),教學經(jīng)驗又因人而異,導(dǎo)致不少教師教學重點和難點的確定帶有很大的主觀性和隨意性。

表1課程標準要求
怎樣才能準確把握教學的重點和難點?教學實踐表明:剖析“終端評價”要求,可以幫助教師直觀地感知教學重點,深刻地感悟教學難點。
分析近三年江蘇省普通高中學業(yè)水平測試化學卷,無論是必修科目還是選修科目的必考內(nèi)容,終端評價的知識范圍與能力要求基本相同(見表2)。

表2終端評價的統(tǒng)計分析

原子半徑比較 √ √ √ √ √ √最高價氧化物的水化物的酸堿性比較 √ √ √ √離子電子層結(jié)構(gòu) √氫化物穩(wěn)定性比較 √ √ √ √單質(zhì)氧化性比較 √化學鍵或化合物類別判斷 √ √ √化合價判斷 √元素類型判斷√物質(zhì)間相互反應(yīng)情況判斷 √ √命題思路熱點選項統(tǒng)計以元素推斷的形式,圍繞元素周期律及其應(yīng)用設(shè)計而成的選擇題,主要考查學生對元素性質(zhì)(原子半徑、金屬性和非金屬性、氣態(tài)氫化物的穩(wěn)定性、最高價氧化物對應(yīng)水化物的酸堿性等)周期性變化規(guī)律的掌握程度和對元素周期律本質(zhì)的理解程度。考查學生應(yīng)用化學知識分析、比較、歸納和判斷等能力。解題關(guān)鍵根據(jù)元素的原子結(jié)構(gòu)、元素在周期表中的位置、元素的特殊性質(zhì)或特征用途等信息,推斷出相關(guān)元素。根據(jù)元素所在周期表的位置,結(jié)合元素周期律知識正確地進行元素有關(guān)性質(zhì)的比較。
依據(jù)“元素推斷依據(jù)”和“熱點選項統(tǒng)計”,“元素周期律與化學鍵”的教學重點應(yīng)確定為:
①認識元素周期表的結(jié)構(gòu),周期與族的分類依據(jù)與結(jié)果。
②掌握1~18號元素原子核外電子排布規(guī)律。
③認識原子結(jié)構(gòu)與元素在周期表中位置及元素性質(zhì)的關(guān)系。
④掌握元素周期律(原子半徑、主要化合價、金屬性與非金屬性、氣態(tài)氫化物的穩(wěn)定性、最高價氧化物對應(yīng)水化物的酸堿性等周期性變化規(guī)律)。
⑤掌握同周期元素及其化合物性質(zhì)的遞變規(guī)律,同主族元素及其化合物性質(zhì)的相似性與遞變性。
⑥掌握離子鍵和共價鍵、離子化合物與共價化合物的識別方法。
依據(jù)“命題思路”和“解題關(guān)鍵”,不難感知“元素周期律與化學鍵”的教學難點主要包括:
①理解元素“位、構(gòu)、性”的關(guān)系,依據(jù)某種元素“位、構(gòu)、性”的信息對元素進行推斷。
②依據(jù)多種元素原子序數(shù)、最外層電子數(shù)、周期表位置的相互關(guān)系,結(jié)合數(shù)學方法和邏輯分析對元素進行推斷。
二、教學重點的落實策略
教學重點的落實必須依據(jù)重點的知識內(nèi)容,靈活選擇教學手段和呈現(xiàn)方式,積極引導(dǎo)學生自主建構(gòu)核心知識、形成基本觀念。
1.問題引導(dǎo)閱讀,自主認識元素周期表的結(jié)構(gòu)
設(shè)計問題鏈,引導(dǎo)學生通過閱讀教材尋找問題答案,清晰掌握周期、族、短周期、主族等核心概念,全面認識元素周期表的結(jié)構(gòu)。
[問題1]什么叫原子序數(shù)?原子序數(shù)與元素的原子結(jié)構(gòu)有什么內(nèi)在聯(lián)系?
[問題2]在元素周期表中,排列元素的原則是什么?
[問題3]元素周期表中有幾個橫行?構(gòu)成幾個周期?周期分為幾類?分類依據(jù)是什么?
[問題4]元素周期表中有幾個縱行,構(gòu)成幾個族?族分為幾類?分類依據(jù)是什么?
[問題5]畫出元素周期表的輪廓,標出周期序數(shù)和族序數(shù),標明“堿金屬元素”、“鹵族元素”、“稀有氣體元素”所處的區(qū)域。
2.情境引導(dǎo)歸納,自主總結(jié)結(jié)構(gòu)與位置的關(guān)系
創(chuàng)設(shè)問題情境,引導(dǎo)學生運用歸納的方法自主發(fā)現(xiàn)“周期序數(shù)=原子核外電子層數(shù)”、“主族序數(shù)=原子最外層電子數(shù)”的規(guī)律,自主建構(gòu)“結(jié)構(gòu)決定位置,位置反映結(jié)構(gòu)”的觀念。
[問題情境1]短周期元素原子結(jié)構(gòu)示意圖

圖1短周期元素原子結(jié)構(gòu)示意圖
[問題情境2]主族元素結(jié)構(gòu)與位置的相互轉(zhuǎn)換

元素 原子結(jié)構(gòu) 周期表位置 原子序數(shù)A B 2周期IVA族C 13
3.活動引導(dǎo)探究,自主建構(gòu)并理解元素周期律
設(shè)計教學活動,組織學生合作探究、討論交流,自主建構(gòu)元素周期律,領(lǐng)悟元素周期律內(nèi)部蘊藏的因果關(guān)系。
[活動設(shè)計1]結(jié)合短周期元素原子結(jié)構(gòu)示意圖(圖1),討論短周期元素原子核外電子排布的變化規(guī)律。
[活動設(shè)計2]借助原子半徑示意圖(圖2),討論同周期、同主族元素原子半徑的變化規(guī)律。

圖2原子半徑示意圖
[活動設(shè)計3]閱讀短周期元素主要化合價曲線圖(圖3),討論短周期元素主要化合價的變化規(guī)律。

圖3短周期元素主要化合價曲線圖
[活動設(shè)計4]閱讀判斷元素金屬性、非金屬性強弱的實驗標準,組織學生設(shè)計實驗探究同周期元素金屬性的變化規(guī)律,查閱資料論證元素非金屬性的變化規(guī)律。
[活動設(shè)計5]從原子結(jié)構(gòu)的角度解釋同周期元素金屬性、非金屬性的遞變規(guī)律。
[活動設(shè)計6]分析同主族元素原子結(jié)構(gòu)的異同,預(yù)測同主族元素金屬性、非金屬性的變化,并通過實驗探究或事實材料加以驗證。
[設(shè)計活動7]歸納出元素周期律,討論元素周期律形成的原因,揭示元素周期律中蘊藏著的因果關(guān)系。
5.故事引導(dǎo)感悟,自主體驗元素周期律的價值
講述元素周期律的發(fā)現(xiàn)簡史(表3),介紹元素周期律在學習、生產(chǎn)、生活中的運用,引導(dǎo)學生體驗科學發(fā)現(xiàn)的艱辛,科學方法的力量,創(chuàng)新思維的魅力。

表3元素周期律發(fā)現(xiàn)簡史
6.案例引導(dǎo)對比,自主識別化學鍵的類型
以NaC1和HC1的形成過程為案例,引導(dǎo)學生從原子結(jié)構(gòu)特點及其對穩(wěn)定結(jié)構(gòu)的追求,分析NaC1和HC1形成過程中的電子轉(zhuǎn)移情況,并運用電子式加以表達,建構(gòu)離子鍵和共價鍵、離子化合物和共價化合物的概念,掌握“電子式”的書寫規(guī)則。

表4離子鍵與共價鍵的比較
三、教學難點的突破藝術(shù)
教學難點的突破必須依據(jù)難點的形成原因,針對性地選擇突破方法和化解策略,積極引導(dǎo)學生深化對難點的認識,掌握問題解決的思路和方法。
1.整合知識,建構(gòu)聯(lián)系
龐雜、抽象的內(nèi)容特點是“元素周期律與化學鍵”難點形成的原因之一。據(jù)此,依據(jù)核心知識間的內(nèi)在聯(lián)系,將其進行有效整合,幫助學生全面認識、系統(tǒng)掌握、深刻領(lǐng)悟核心知識,為靈活運用核心知識奠定基礎(chǔ)。
(1)凸顯“位、構(gòu)、性”關(guān)系,深化觀念領(lǐng)悟
引導(dǎo)學生自主整合“位、構(gòu)、性”關(guān)系(圖4),深刻領(lǐng)會“結(jié)構(gòu)決定性質(zhì)”、“結(jié)構(gòu)決定位置”的化學觀念,為依據(jù)元素的原子結(jié)構(gòu)、元素在周期表中的位置、元素的特殊性質(zhì)和特征用途進行元素的推斷奠定基礎(chǔ)。

圖4元素“位、構(gòu)、性”關(guān)系圖
(2)整合周期律重要信息,強化直觀認識
引導(dǎo)學生依托元素周期表,高度整合短周期元素的重要信息(圖5)[4],幫助學生直觀把握元素周期律,為依據(jù)元素周期律進行元素有關(guān)性質(zhì)的比較奠定基礎(chǔ)。
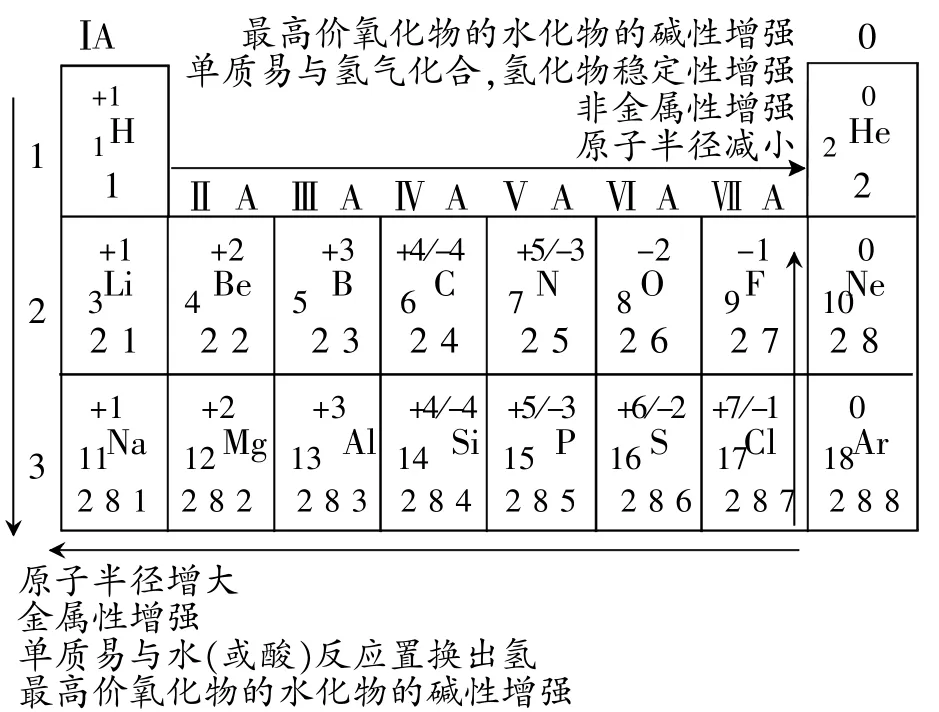
圖5短周期元素知識體系
(3)建構(gòu)思維導(dǎo)圖,訓練有序思維
引導(dǎo)學生依據(jù)核心概念間內(nèi)在的邏輯聯(lián)系,建構(gòu)思維導(dǎo)圖(圖6),幫助學生形成有序思維品質(zhì),提高學生邏輯思維能力。

圖6“元素周期律與化學鍵”思維導(dǎo)圖
2.整理素材,指導(dǎo)方法
遷移、推理的能力要求是“元素周期律與化學鍵”難點形成的另一原因。據(jù)此,依據(jù)終端評價的要求,整理推斷素材,熟悉元素推斷的常用視角、依據(jù)和方法,幫助學生掌握推斷規(guī)律。
(1)從原子結(jié)構(gòu)特征推斷元素
依據(jù)原子結(jié)構(gòu)特征對元素進行推斷,關(guān)鍵在于依據(jù)短周期元素核外電子排布模型對元素的原子結(jié)構(gòu)進行分析與推理。

表4部分元素的原子結(jié)構(gòu)特征
(2)從元素性質(zhì)特征推斷元素
依據(jù)元素特征性質(zhì)或用途(表5)進行元素推斷,關(guān)鍵在于對關(guān)鍵知識的全面了解和準確把握。

表5部分短周期主族元素的特征性質(zhì)
(3)從元素的相互關(guān)系推斷元素
依據(jù)元素的相互關(guān)系推斷元素,關(guān)鍵在于依據(jù)元素在周期表中的相對位置,分析彼此間原子序數(shù)(最外層電子數(shù))的關(guān)系,同時具備良好的數(shù)學推演和邏輯推理的能力(表6)。

表6運用邏輯分析推理元素的案例
3.精選試題,訓練思維
高度綜合、能力立意的命題特點是“元素周期律與化學鍵”難點形成的再一個原因。據(jù)此,精選學業(yè)水平測試真題,結(jié)合問題的深度解析(表7),指導(dǎo)學生敏銳地抓住問題的突破口,依據(jù)彼此聯(lián)系進行邏輯推理,結(jié)合典型錯誤的歸因分析,幫助學生查堵知識與方法的漏洞,有效訓練學生思維。

表7測試真題的深度剖析
教學實踐表明:深入研究終端評價,可以讓教學重點和難點的確定更加準確,教學重點的落實將更為扎實,教學難點的突破將更為有效。
參考文獻
[1]中華人民共和國教育部制訂.普通高中化學課程標準(實驗)[M].北京:人民教育出版社,2003:9
[2]江蘇省教育考試院試題分析編寫組.2013年高考(江蘇卷)試題分析[M].南京:東南大學出版社,2013:153-155
[3]江蘇省教育考試院. 2012年高考(江蘇卷)試題分析[M].南京:東南大學出版社,2012:142-144
[4]經(jīng)志俊.基于等級評價的備考策略:知識點精減與整合[J].化學教學,2015,(10):28-31
doi:10.3969/j.issn.1008-0546.2016.02.004
文章編號:1008-0546(2016)02-0016-05
中圖分類號:G632.41
文獻標識碼:B

