IL對NK細胞殺傷人骨髓瘤RPMI 8226細胞活性的影響及其機制
韓露,高全立,宋永平,周健(鄭州大學附屬腫瘤醫院 河南省腫瘤醫院,鄭州450008)
?
·論著·
IL對NK細胞殺傷人骨髓瘤RPMI 8226細胞活性的影響及其機制
韓露,高全立,宋永平,周健(鄭州大學附屬腫瘤醫院 河南省腫瘤醫院,鄭州450008)
摘要:目的探討IL對NK細胞殺傷人骨髓瘤RPMI 8226細胞活性的影響,并探討其機制。方法取正常人外周血單個核細胞,隨機分為6 組,對照組以單純培養基培養,IL-2組加入1 000 U/mL IL-2,IL-7組加入40 ng/mL IL-7,IL-21組加入20 ng/mL IL-21,IL-2+IL-7組分別加入1 000 U/mL IL-2和40 ng/mL IL-7,IL-2+IL-7+IL-21組分別加入1 000 U/mL IL-2、40 ng/mL IL-7和20 ng/mL IL-21,均培養5天。采用流式細胞術檢測各組NK細胞比例及其表面激活性受體NKG2D、NKp46、NNKp30陽性表達細胞比例,RT-PCR法檢測各組NK細胞NKG2D mRNA、NKP46 mRNA和NKP30 mRNA,CFSE/PI雙染法檢測各組NK細胞對RPMI 8226細胞的細胞毒效應(殺傷率)。結果除IL-7組外,其余各組NK細胞比例和細胞表面NKG2D陽性表達細胞比例均較對照組升高(P均<0.05)。各組NK細胞NKG2D mRNA、NKP46 mRNA和NKP30 mRNA表達量比較差異均無統計學意義(P均>0.05)。對照組NK細胞對RPMI 8226細胞的殺傷率為2.13%±0.42%、IL-2組為58.73%±1.80%、IL-7組為1.90%±0.60%、IL-21組為14.43%±1.22%、IL-2+IL-7組為34.27%±2.35%、IL-2+IL-7+IL-21組為37.47%±0.60%,各組與對照組比較P均<0.05。結論單因子IL-2、IL-21,雙因子IL-2+IL-7和多因子IL-2+IL-7+IL-21均能提高NK細胞對人骨髓瘤RPMI 8226細胞的殺傷活性,以單因子IL-2作用效果最好;其作用機制可能為IL增加NK細胞數量和其表面活化性受體NKG2D的表達量。
關鍵詞:多發性骨髓瘤;自然殺傷細胞;白細胞介素;天然細胞毒受體;NKG2D
多發性骨髓瘤(MM)是一種漿細胞惡性增殖性疾病,發病率占血液系統腫瘤的10%[1]。多藥聯合化療對MM的完全緩解率低于5%。造血干細胞移植聯合高劑量化療方案能夠延長MM患者生存期,但移植相關疾病病死率高、缺乏人類白細胞抗原(HLA)相合供者使造血干細胞移植難以實施。近年來,細胞免疫治療成為化療和造血干細胞移植后清除殘留腫瘤細胞的重要手段[2]。NK細胞是一類具有直接殺傷靶細胞效應的淋巴細胞。IL-2可增強外周血NK細胞的體外殺傷活性,目前已經廣泛應用于惡性腫瘤的治療,有效率為15%~20%[3]。但IL-2對MM及其他IL對MM的影響及其作用機制研究較少。2010年1月~2011年3月,本研究觀察了IL-2、IL-7、IL-21對NK細胞殺傷人骨髓瘤RPMI 8226細胞活性的影響,現分析結果并探討其機制。
1材料與方法
1.1材料①主要試劑:RPMI 1640培養液(Hyclone公司),GT-T551培養液(TaKaRa公司),胎牛血清(FBS,Gibco公司),重組人IL-2(山東泉港藥業有限公司)、IL-7(Peprotech公司)、IL-21(Peprotech公司),NKG2D-APC、NKP46-APC、NKP30-APC、CD3-FITC/CD16+CD56+-PE流式細胞熒光標記抗體(Biolegend公司),碘化丙啶(PI,Sigma公司)。逆轉錄試劑盒、Reagent試劑盒、PCR Marker(Invitrogen公司),RT-PCR反應試劑盒(大連寶生物工程公司)。活細胞熒光染料羧基(CFSE,Invitrogen公司)。②細胞株:人骨髓瘤細胞株RPMI 8226由鄭州大學中心實驗室提供。③人外周血樣品:取自鄭州大學身體健康的大學生志愿捐獻者。
1.2人骨髓瘤RPMI 8226細胞培養人骨髓瘤RPMI 8226細胞置于含100 mL/L FBS的RPMI 1640培養基,37 ℃、5% CO2、充分濕度的培養箱中培養。取對數生長期細胞用于實驗。
1.3NK細胞收集、分離與培養采用Ficoll密度梯度離心法分離人外周血單個核細胞(PBMC)(獻血2 h內完成),PBS洗滌兩次,細胞計數后以5×106/mL分別接種于6個25 cm2培養瓶置于含100 μg/mL鏈霉素、100 U/mL青霉素、5%自體血漿的10 mL GT-T551培養基培養。隨機分為6 組,對照組以單純培養基培養,IL-2組加入1 000 U/mL IL-2,IL-7組加入40 ng/mL IL-7,IL-21組加入20 ng/mL IL-21,IL-2+IL-7組分別加入1 000 U/mL IL-2和40 ng/mL IL-7,IL-2+IL-7+IL-21組分別加入1 000 U/mL IL-2、40 ng/mL IL-7和20 ng/mL IL-21,作用3天后離心換液并全量補充以上細胞因子,5天后收獲細胞。
1.4相關指標觀察
1.4.1NK細胞比例及其表面激活性受體NKG2D、NKP46、NKP30表達采用直接免疫熒光標記法標記各組細胞NK細胞比例,即CD3-/CD16+CD56+細胞百分比;FACS Calibur流式細胞儀(B-D公司)檢測NK細胞表面激活性受體NKG2D、NKP46、NKP30陽性表達細胞百分比。
1.4.2NK細胞NKG2D mRNA、NKP46 mRNA和NKP30 mRNA表達采用RT-PCR法。采用TRIzol一步法提取各組細胞總RNA,按逆轉錄試劑盒說明書步驟進行逆轉錄合成cDNA。NKG2D、NKP46和NKP30引物序列均由上海生工生物工程技術服務有限公司合成(見表1)。按照說明書步驟采用ABI7300實時定量PCR儀上樣擴增,ABI7300系統分析熒光值,采用2-ΔΔCt法對結果進行相對定量分析。

表1 NKG2D、NKP46、NKP30、β-actin引物序列及產物
1.4.3NK細胞對人骨髓瘤RPMI 8226細胞的殺傷率收集靶細胞RPMI 8226,細胞計數后用預溫好的CFSE-PBS液重懸,37 ℃放置5 min,加入含10% FBS的RPMI 1640培養基終止反應,離心棄上清,用GTT-551培養基調整細胞終濃度為5×105/mL;分別將各組NK細胞密度調整為5×106/mL;將上述兩種細胞按20∶1(660 mL∶330 mL)比例混合,培養箱中放置4 h;每管加終濃度為1.5 mg/mL的PI,上機檢測,CellQuest軟件分析結果,計算靶細胞殺傷率[3]。
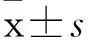
2結果
2.1各組NK細胞比例及其表面激活性受體NKG2D、NKP46、NKP30陽性表達細胞百分比比較除IL-7組,各組NK細胞比例及其表面NKG2D陽性表達細胞百分比均較對照組升高(P均<0.05)。見表2。
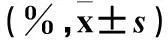
表2 各組CD3-/CD16+CD56+細胞及其表面受體NKG2D、
注:與對照組比較,*P<0.05。
2.2各組NK細胞NKG2D mRNA、NKP46 mRNA和NKP30 mRNA相對表達量比較各組NK細胞NKG2D mRNA、NKP46 mRNA和NKP30 mRNA相對表達量比較差異均無統計學意義(P均>0.05)。見表3。

表3 各組NK細胞NKG2D mRNA、NKP46 mRNA
2.3各組NK細胞對RPMI 8226細胞的殺傷率對照組NK細胞對RPMI 8226細胞的殺傷率為2.13%±0.42%、IL-2組為58.73%±1.80%、IL-7組為1.90%±0.60%、IL-21組為14.43%±1.22%、IL-2+IL-7組為34.27%±2.35%、IL-2+IL-7+IL-21組為37.47%±0.60%,IL-7組較對照組降低,其余組均較對照組升高,組間比較P均<0.05。
3討論
NK細胞是一類具有直接殺傷靶細胞效應的淋巴細胞,在機體的免疫系統中發揮關鍵作用。研究發現,NK細胞表面有活化性受體和抑制性受體,這些受體與靶細胞表面相應的配體結合,形成兩種不同的信號傳遞系統,對NK細胞的殺傷功能起激活或抑制作用[3]。NK細胞表面的活化性受體包括NKG2D、天然細胞毒受體(NCRs)、KIR2DS及其輔助刺激活化性受體CD244、NTB2A、CD59等[4]。NKG2D為NK細胞表面重要的活化性受體[5],NKG2D與其配體結合后,能直接或輔助激活一系列的免疫細胞,在機體抗腫瘤免疫中發揮重要作用。NCRs家族包含三種免疫球蛋白樣分子,即NKP46、NKP44和NKP30[6,7]。NCRs在細胞表面的表達程度與NK細胞功能的發揮密切相關,但NCRs的配體至今尚未明確[8]。NK細胞抑制性受體包括免疫球蛋白超家族、C型凝集素家族。抑制性受體和其相應配體結合,傳導抑制信號,從而阻止NK細胞對靶細胞的細胞毒作用。因此,如要提高NK細胞對靶細胞的殺傷活性,除降低抑制性信號外,激發NK細胞的活化性信號更為重要[9,10]。
本研究結果顯示,除了IL-7組NK細胞比例(CD3-/CD16+CD56+)較對照組降低外,其余各組NK細胞比例均較對照組升高,表明單因子IL-2或IL-21、雙因子IL-2+IL-7和三因子IL-2+IL-7+IL-21培養均能促進NK細胞擴增;NK細胞被IL-2或IL-21單獨刺激后殺傷活性較未被刺激時明顯增強,NK細胞比例較未被刺激時明顯增多,NKG2D陽性表達細胞百分比明顯上調;表明IL-2或IL-21對NK細胞的細胞毒活性影響可能一方面是增加NK細胞數量,另一方面通過上調NKG2D增強NK細胞的殺傷能力。但RT-PCR結果顯示,IL-2或IL-21活化的NK細胞NKG2D mRNA相對表達量與對照組比較并無明顯差異。推測IL-2或IL-21雖然可以上調細胞表面NKG2D表達,但并不能影響其基因水平,IL-2或IL-21對于NKG2D的調節作用可能主要是通過影響其mRNA的翻譯水平實現的,這與以往的研究相吻合[11,12]。IL-7組誘導培養NK細胞比例及活化性受體的相對表達量與對照組比較差異均無統計學意義,可能是本研究中IL-7的工作濃度過低,也可能是單一的IL-7并不能誘導NK細胞的產生。IL-2+IL-7組和IL-2+IL-7+IL-21組NK細胞比例及激活性受體的相對表達量并未較單獨的IL-2作用增強,表明IL-2、IL-7和IL-21聯合并無協同作用,其機制有待進一步探討。
研究發現,IL-2可上調NK細胞表面受體NKG2D、KIR2DL1、KIR2DL2表達[13]。Lu等[14]研究表明,IL-2、OKT-3和IFN-γ刺激培養的CIK,可使其細胞表面高表達NKG2D受體,且可阻斷MM細胞的NKG2D配體,CIK對MM細胞的細胞毒效應明顯降低,NKG2D和其配體相互作用是介導CIK殺傷MM細胞的重要機制。Denman等[15]研究發現,膜型IL-21可促進NK細胞活化并增強NK細胞的殺傷活性,膜型IL-21刺激NK細胞表面高表達NCRs、CD16和NKG2D,并可分泌大量細胞因子。本研究結果顯示,單因子IL-2或IL-21、雙因子IL-2+IL-7和多因子IL-2+IL-7+IL-21均能提高NK細胞對人骨髓瘤RPMI 8226細胞的殺傷活性,其中以單因子IL-2作用效果最好;其機制可能與細胞因子誘導NK細胞數量及其細胞表面活化性受體NKG2D表達增加有關,但其確切機制還需進一步探討。
參考文獻:
[1] Costello RT, Boehrer A, Sanchez C, et al. Differential expression of natural killer cell activat marrow in patients with monoclonal gammopathy[J]. Immunology, 2013,139(3):338-341.
[2] Ryosei N, Jeanette B, Andreas B, et al. In vivo trafficking and survival of cytokine-induced killer cells resulting in minimal GVHD with retention of antitumor activity[J]. Blood, 2008,112 (8):2563-2574.
[3] De Saint Basile G, Menasche G, Fischer A. Molecular mechanisms of biogenesis and exocytosis of cytotoxic granules[J]. Nat Rev Immunol, 2010(10):568-579.
[4] 劉丹.NK細胞表面活化性受體的研究進展[J].國際免疫學雜志,2006,29(5):302-305.
[5] Zafirova B, Wensveen FM, Gulin M, et al. Regulation of immune cell function and differentiation by the NKG2D receptor[J]. Cell Mol Life Sci, 2011(68):3519-3529.
[6] Roland KS. A symmetric ligand recognition by theactivating natural killer cell receptor NKG2D, asymmetric homodimer [J]. Molecular Jmmunology, 2001,38(14):1029-1037.
[7] Li Y, Wang Q, Mariuzza RA. Structure of the human activating natural cytotoxicity receptor NKp30 bound to its tumor cell ligand B7-H6[J]. J Exp Med, 2011,208(4):703-714.
[8] Pende D, Cantoni C, Rivera P, et al. Role of NKG2D in tumor cell lysis mediated by human NK cells: cooperation with natural cytotoxicity receptors and capability of recognizing tumors of nonepithelial origin[J]. Eur J Immunol, 2001,31(4):1076-1086.
[9] Coudert JD, Zimmer J, Tomasello E, et al. Altered NKG2D function in NK cells induced by chronic exposure to NKG2D ligand-expressing tumor cells[J]. Blood, 2005,106(15):1711-1717.
[10] Vankayalapati R, Garg A, Porgador A, et al. Role of NK cell-activating receptors and their ligands in the lysis of mononuclear phagocytes infected with an intracellular bacterium[J]. J Immunol, 2005,175 (7):4611-4617.
[11] Dhanji S, Teh HS. IL-2-activated CD8+CD44high cells express both adaptive and innate immune system receptors and demonstrate specificity for syngeneic tumor cells[J]. J Immunol, 2003,171(7):3442-3450.
[12] Decot V, Voillard L, Latger-Cannard V, et al. Natural-killer cell amplification for adoptive leukemia relapse immunotherapy: comparison of three cytokines, IL-2, IL-15, or IL-7 and impact on NKG2D, KIR2DL1, and KIR2DL2 expression[J]. Experimental Hematology, 2010,38(5):351-362.
[13] Peest D, Leo R, Deicher H. Tumor-directed cytotoxicity in multiple myeloma-the basis for an experimental treatment pproach with interleukin-2[J]. Stem Cells, 1995,13(2):72-76.
[14] Lu XZ, Zhu AS, Cai XH, et al. Role of NKG2D in cytokine-induced killer cells against multiple myeloma cells [J]. Cancer Biol & Ther, 2012,13(8):623-629.
[15] Denman CJ, Senyukov VV, Somanchi SS, et al. Membrane-bound IL-21 promotes sustained ex vivo proliferation of human natural killer cells[J]. PLoS One, 2012,7(1):e30264.
Influence of interleukin in inducing the cytotoxicity of NK cells against human multiple myeloma RPMI 8226 cells and its mechanism
HANLu,GAOQuanli,SONGYongping,ZHOUJian
(TheAffiliatedTumorHospitalofZhengzhouUniversity,Zhengzhou450008,China)
Abstract:ObjectiveTo investigate the influence of interleukin (IL) in inducing the cytotoxicity of natural killer (NK) cells against the activity of human multiple myeloma RPMI 8226 and the correlated molecular mechanisms. MethodsThe human peripheral blood mononuclear cells (PBMC) were randomly divided into 6 groups: the control group (simple culture medium), IL-2 group (added with 1 000 U/mL IL-2), IL-7 group (40 ng/mL IL-7), IL-21 group (20 ng/mL IL-21), IL-2+IL-7 group (1 000 U/mL IL-2+40 ng/mL IL-7) and IL-2+IL-7+IL-21 group (1 000 U/mL IL-2, 40 ng/mL IL-7+20 ng/mL IL-21). They were all cultured for 5 days. The proportion of NK cells and the expression of activated receptors (NKG2D, NKp46, NKp44 and NNKp30) were measured by flow cytometry. The expression of NKG2D mRNA, NKP46 mRNA and NKP30 mRNA was measured by RT-PCR. Cytotoxicity of NK cells against RPMI8226 cells was analyzed by CFSE/PI double staining. ResultsExcept the IL-7 group, the proportion of NK cells and the expression of NKG2D in the other groups were increased as compared with those of the control group (all P<0.05). No significant difference in the gene expression of NKG2D, NNKp46 and NKp30 was found among these groups (all P>0.05). The cell-killing rate of NK cells on RPMI8226 cells in the control group was 2.13%±0.42%, and that in the IL-2 group was 58.73%±1.80%, the IL-7 group was 1.90%±0.60%, the IL-21 group was 14.43%±1.22%, the IL-2+IL-7 group was 34.27%±2.35%, and the IL-2+IL-7+ IL-21 group was 37.47%±0.60%. Significant difference was found in the cell-killing rate between the control group and the other groups (all P<0.05). ConclusionsThe single factor IL-2, IL-21, double-factor IL-2+ IL-7 and multi-factor IL-2+ IL-7+IL-21 can enhance the cytotoxic effect of NK cells against RPMI 8226 cells, and the single factor IL-2 is the best. The increased number of NK cells and the expression of cell surface activation acceptor (NKG2D) may be the possible mechanism.
Key words:multiple myeloma; natural killer cell; interleukin; natural cytotoxicity receptor; NKG2D
(收稿日期:2015-12-02)
中圖分類號:R733.3
文獻標志碼:A
文章編號:1002-266X(2016)12-0001-04
doi:10.3969/j.issn.1002-266X.2016.12.001
通信作者簡介:周健(1975-),男,副主任醫師,主要研究方向為血液病的免疫治療。E-mail: zhoujiandoctor@163.com
第一作者簡介:韓露(1979-),女,住院醫師,主要研究方向為血液病的免疫治療。E-mail: luhan0377@163.com
基金項目:國家自然科學基金資助項目(81000921)。

