找準最近發展區 打造探究性課堂
梁書

摘要:基于“最近發展區”理論,以溶液的質量分數的概念和一定質量分數溶液的配制為起點,幫助學生在探究性學習中對于溶液濃度表示方法的認識上升到一個新的高度。
關鍵詞:最近發展區;配制及分析;質量分數
文章編號:1008-0546(2016)08-0061-04 中圖分類號:G633.8 文獻標識碼:B
doi:10.3969/j.issn.1008-0546.2016.08.021
20世紀30年代,前蘇聯著名心理學家N.C.維果茨基提出了“最近發展區”理論。“最近發展區”常被譯為“潛在發展區”,是指“兒童獨立解決問題的實際發展水平與在成人指導下或在有能力的同伴合作中解決問題的潛在發展水平之間的差距”。即兒童有兩種發展水平:一是兒童的現有水平,二是可能達到的發展水平。這兩種水平之間的差異就是“最近發展區”。該理論要求我們要重視學生的原有水平,讓教學處于“最近發展區”之中,這樣才能促進學生的發展。
基于以上理解,筆者就以找準學生的最近發展區為突破口,對“溶液的配制及分析”進行了設計。
一、教學目標
1. 知識與技能
(1)從廣義角度理解濃度的含義,初步理解物質的量濃度的含義和使用價值。
(2)掌握實驗室準確配制一定物質的量濃度的溶液的一般步驟、方法和技能。
2. 過程與方法
(1)通過分析表示溶液組成的各類標簽、醫院生化報告,歸納濃度的含義,復習質量分數,理解物質的量濃度。
(2)通過對比實驗探索掌握實驗室準確配制一定物質的量濃度的溶液的方法和技能。
(3)通過動畫模擬儀器間的變換,展示“創新”與“需求”的關系,加深學生對容量瓶的特點的認識。
3. 情感、態度與價值觀
(1)培養學生嚴謹求實的科學態度。
(2)使學生感受到創新的源動力來自于解決實際問題。
(3)體會定量研究方法對化學學習和科學研究的重要作用。
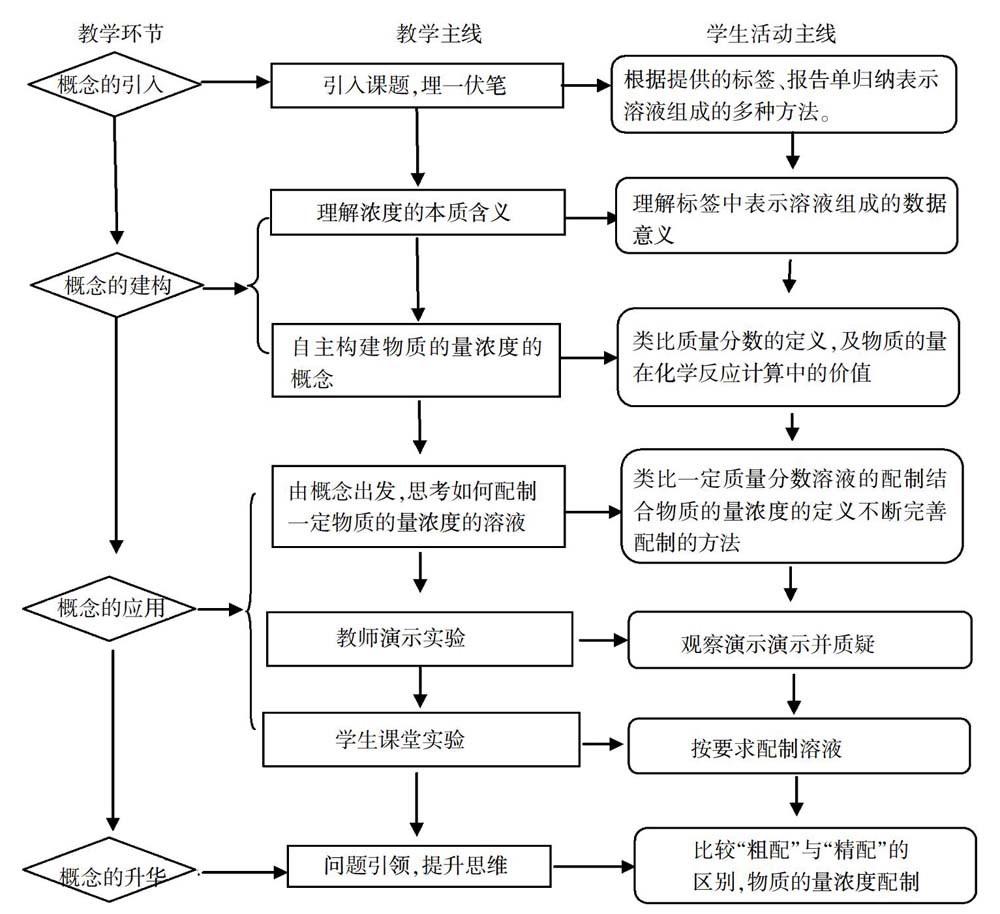
二、設計思路
“溶液的配制及分析”這部分內容位于《化學1》的第一章,主要包括三個內容:一是物質的量濃度概念的理解;二是如何配制一定物質的量濃度的溶液;三是學會配制溶液過程中一些不規范操作引起的實驗誤差。高一學生對于溶液的濃度并不是一無所知,他們在初中已經學過了溶質的質量分數、一定質量分數溶液的配制。同時本章又剛學習了物質的量、摩爾質量和氣體摩爾體積。通過本部分內容的學習是要讓學生對于溶液濃度表示方法的認識上升到一個新的高度,體會定量研究方法對化學學習和科學研究的重要作用。由此可以確定學生的最近發展區:一、為什么要引入物質的量濃度來表示溶液的濃度,它與溶液的質量分數有什么聯系,能相互轉化嗎?表示溶液組成的方法還有哪些?二、配制一定物質的量濃度溶液的方法能從配制一定質量分數溶液的方法遷移而來嗎?它們之間有哪些異同點。針對學生的最近發展區開展充分的討論和實驗,最后讓學生的能力發展到新的水平。
三、教學過程
環節一:設置懸念,將學生思維引入“最近發展區”
【展示】氯化鈉注射液、五糧液、礦泉水的標簽、醫院生化體檢報告單。
【問題1】請根據標簽、報告單歸納表示溶液組成的多種方法,并說一說對標簽中表示溶液組成的數據意義的理解。
【問題2】請聯系溶液質量分數的定義給物質的量濃度下一個定義,并寫出其表達式,指出單位是什么?
【設計意圖】通過生活中的實例,讓學生體會到表示溶液濃度的方法是多樣的,可以是m/m、V/V、m/V、 n/V,得出各種濃度表示方法的共性。
同時意識到各種方法在不同的領域的使用都有其優勢。在領會了物質之間發生化學反應的本質是構成物質微粒之間的相互轉化,化學反應方程式前面的系數可以代表反應物與生成物的物質的量之比,我們在科學實驗和實際應用中需要清楚溶液中含有溶質的微粒數,所以引入了衡量溶液組成的新方法——物質的量濃度。
為了實現從“質量分數”定量表示溶液的組成向用“物質的量濃度”定量表示溶液的組成的轉化,利用學生現有水平——知道利用質量分數可以表示溶液的組成,通過展示表示溶液組成的多種方法,引起學生認知沖突,師生之間圍繞濃度的本質意義開展討論,從而使學生將知識內化,形成自己的理解,體驗到物質的量濃度的核心價值,最后使認知達到了新的水平。
環節二:多層設疑,引導學生突破思維的“最近發展區”
【展示】裝有0.100mol·L-1 Na2CO3溶液的試劑瓶
【問題3】請大家參考配制一定溶質質量分數溶液的方法,思考如何利用Na2CO3固體配制100mL 0.100mol·L-1 Na2CO3溶液?
學生可能提供的方案:
方案一:(1)通過計算,需要Na2CO3固體1.06g。(2)用托盤天平稱量1.1g Na2CO3固體,倒入燒杯中。(3)用量筒量取100mL水,倒入燒杯中,用玻璃棒攪拌,促進溶解。
方案二:前兩步驟同上,第三步改成在燒杯中加水至100mL,用玻璃棒攪拌,促進溶解。
方案三:第一步同方案一,第二步改成用電子天平稱量1.06g Na2CO3固體,倒入量筒中,最后在量筒中加入水至100 mL,用玻璃棒攪拌,促進溶解。
【問題4】大家覺得要準確配制100mL 0.100mol·L-1 Na2CO3溶液關鍵需要解決什么問題?
【問題5】大家覺得以上提供的方案能達到這個要求嗎?怎樣改進?
【展示】電子天平、容量瓶、酸式滴定管、堿式滴定管。
【投影】利用三維動畫模擬玻璃片→表面皿→燒杯→錐形瓶→容量瓶的變形。
【總結與歸納】容量瓶的特點:細頸、梨形瓶,有一刻度線,有磨口玻璃塞,標有容積和溫度。
【設計意圖】遵循由具體到抽象、由感性到理性的思維發展順序,先讓學生通過熟悉的一定溶質質量分數溶液的配制,遷移到如何配制一定物質的量濃度的溶液。再回過頭通過對物質的量濃度概念的深入解讀,發現精確配制需要做到兩個關鍵點:一、稱量的固體質量要準確;二、溶液的體積要準確。最后檢查發現方案一用托盤天平稱量固體、量筒量取液體達不到要求的準確度,同時將100mL水與碳酸鈉固體混合后溶液體積一定會發生變化,所以最終不妥。方案二中托盤天平稱量達不到要求的準確度,利用燒杯測量最終溶液的體積誤差會很大。方案三中量筒量取液體達不到要求的準確度,同時在量筒中配制溶液是不規范的。量筒上標有溫度,溶液在溶解過程中會出現放熱、吸熱現象,所以最終量取的溶液體積也是不準確的。怎么辦?此時學生處于注意、好奇、質疑、憤悱等急于解決問題的心理狀態,展示模擬儀器之間的變形關系的動畫,生動形象。有需要就有創新。
【思考】 現在請大家對比此前的實驗設計進行修正。并結合下面老師進行的演示實驗,指出你對哪些操作步驟有疑問或操作目的不明確,甚至還需補充一些什么操作。
【演示實驗】教師演示配制實驗的全過程。
學生可能提出的以下幾個問題:
1、容量瓶為什么要檢漏?
2、為什么不在容量瓶中溶解固體?
3、為什么要洗滌燒杯和玻璃棒?
4、為什么需要用玻璃棒引流,而且需要將玻璃棒放到容量瓶刻度線以下位置?
5、為什么要初步搖勻?
6、如果不小心使液面超過了刻度線,怎么辦?
7、定容搖勻后,液面下降,怎么辦?
8、容量瓶需要干燥的嗎?
9、需要在溶解的時候增加一步操作,利用量筒量取一定體積的水再加入到燒杯中嗎?
10、容量瓶能長時間儲存液體嗎?
11、 由1.50 mol·L-1 Na2CO3濃溶液配制100mL 0.100mol·L-1 Na2CO3溶液怎樣操作?
針對1-6這六個問題可以采用如下的對比實驗,針對7-11這5個問題可以采用交流與討論的方法。
【演示對比實驗】 針對1-6這六個問題可以采用如下的對比實驗。
1、教師將一容量瓶中加水,塞好瓶塞,倒立。故意讓學生看到瓶塞周圍有大量水滴逸出。
2、將碳酸鈉和碳酸氫鈉固體分別溶解在燒杯中,讓學生觸摸燒杯外部感受固體溶于水中的能量變化。
3、將高錳酸鉀溶液從燒杯中轉移到相應的試劑瓶。讓學生觀察燒杯和玻璃棒的表面,看看是否有殘留的液體。
4、將燒杯中的高錳酸鉀溶液直接加入到容量瓶中,讓學生看到液體從瓶口流到桌面并部分殘留在容量瓶刻度線以上。
5、首先將10mL 1.00mol·L-1 Na2CO3溶液與80mL水按順序注入容量瓶振蕩搖勻后靜置,記下液面標記線1。洗凈該容量瓶將50mL 0.200mol·L-1 Na2CO3溶液與50mL水按順序注入容量瓶振蕩搖勻后靜置,記下液面標記線2,讓學生觀察兩條標記線的差距。
6、故意“不小心”在事先配制好放置高錳酸鉀溶液的試劑瓶中再加入水,使其液面超過刻度線,觀察加水前后溶液的顏色,讓學生感覺到即使將多余液體吸出,溶質也會損失掉一部分。
【歸納與總結】1、由固體配制一定物質的量濃度溶液的實驗步驟:計算→稱量→溶解→恢復到室溫→轉移→洗滌→定容→搖勻→裝瓶貼簽(為了保證實驗精度,在稱量固體時,應用分析天平或電子天平。若條件限制,可用托盤天平代替進行練習)。
2、由濃溶液稀釋配制稀溶液的實驗步驟:計算→量取→溶解→恢復到室溫→轉移→洗滌→定容→搖勻→裝瓶貼簽(為了保證實驗精度,在量取濃溶液時,應用滴定管。若條件限制,可用量筒代替進行練習)。
【課堂學生實驗】 請同學們根據所給的儀器和藥品配制90mL 0.200mol·L-1 Na2CO3溶液。并思考在操作過程中的哪些不當操作會造成你所配溶液的濃度偏大或偏小。
【設計意圖】通過師生對話,實驗對比操作,配制過程中的難點、重點,一一映射在學生的大腦中。如果覺得當場演示對比實驗課堂會造成課堂時間不夠,可以將對比實驗錄成微課,課堂播放。對課堂演示環節中每一個步驟的認同,其實就是對物質的量濃度概念的準確理解,所以我們不能讓學生含糊過關。比如問同學還有沒有不同意見時,大家面面相覷,沒人主動回答。再叫一位同學個別回答時,它可能會說與其他同學的想法一樣。此時可以讓他再用自己的語言說一說,結果可能相去甚遠,暴露出了大問題。這樣的教學效果將會很好。
讓學生自主配制90 mL的溶液的目的是讓學生學會挑選最合適的儀器,而且更符合實際需要,平常我們需要的液體體積往往與容量瓶的規格是不符合的。
環節三:創設嶄新“最近發展區”,把學生思維推向更高發展層次。
【問題6】 要配制濃度約為2mol·L-1 NaOH溶液100mL,你覺得該怎樣配?
讓同學交流討論后再提供以下操作請同學們判斷是否正確。
A. 稱取8g NaOH固體,放入250mL燒杯中,用100mL量筒量取100mL蒸餾水,加入燒杯中,同時不斷攪拌至固體溶解
B. 稱取8g NaOH固體,放入100mL量筒中,邊攪拌,邊慢慢加入蒸餾水,待固體完全溶解后用蒸餾水稀釋至100mL
C. 稱取8g NaOH固體,放入100mL容量瓶中,加入適量蒸餾水,振蕩容量瓶使固體溶解,再加水到刻度,蓋好瓶塞,反復搖勻
D. 用100mL量筒量取40mL 5mol·L-1 NaOH溶液,倒入250mL燒杯中,再用同一量筒取60mL蒸餾水,不斷攪拌下,慢慢倒入燒杯中
【設計意圖】 配制一定物質的量濃度的溶液是為了科學研究的需要,我們在配制前一定要明確配制的要求與目標,而不應將溶液的配制一味地“精確化”。確定溶液體積的儀器并非僅有容量瓶一種,讓學生從本質理解容量瓶使用的范圍。
【問題7】能否通過精密儀器配制得到2.000mol·L-1 NaOH溶液?為什么?
【設計意圖】 通過討論使同學們意識到并不是所有的物質都能精確配制的。比如NaOH由于其在空氣中易于吸收CO2和水分等,不可能精配。類似的物質還有濃硫酸、鹽酸等。而NaCl、Na2CO3等在空氣中穩定、純度高、實際組成與化學式完全符合、具有較大的摩爾質量的物質往往可以精配,并以它們為基準物質。在實際生產與研究中,像NaOH等不能精配的物質一般均采用先粗略配制,再用基準物質進行滴定標定的方法獲得其準確濃度。這樣也為以后滴定的學習埋下了伏筆。
四、教學反思
對于“一定物質的量濃度溶液的配制”這節課,浙江省普通高中學科教學指導意見給出的要求是:1.知道物質的量濃度的含義;2.初步學會溶液配制的實驗技能;3.體會定量研究方法對化學學習和科學研究的重要作用。平常試題中也非常強調對配制一定物質的量濃度的溶液操作步驟、細節的考查。基于以上認識,部分教師過于注重實驗過程中的準確配制細節,忽視物質的量濃度概念的形成,將課堂變成了純粹的實驗技能的傳授。這樣勢必無法發揮學生的主體能動性,增加了學生記憶的負擔,體會不到學習的價值。同時如果教學遵循先概念教學再實驗演示,最后進行誤差分析,在一堂課內完成往往時間很緊迫。但是最近發展區理論提醒我們,每個學生都不是一張白紙,找準學生的最近發展區將起到事半功倍的效果。
參考文獻
[1] 王祖浩.普通高中課程標準實驗教科書·化學必修1[M].南京:江蘇教育出版社,2009
[2] 王偉,趙春輝. 維果茨基“最近發展區”理論對化學教學的啟示[J].通化師范學院學報,2011,(10)
[3] 張書云. “一定物質的量濃度溶液的配制”的教學策略[J].化學教與學,2012,(7)

