關于“碳酸鈣性質”的探究及教學思考
田長明


摘要:文章從質疑碳酸鈣飽和溶液能否使酚酞試液變色入手,就變色的本質進行了探討,對碳酸鈣的溶解性和穩定性進行了適當的拓展和延伸,并對課堂教學提出了自己的看法。
關鍵詞:問題質疑;本質探討;知識拓展;教學反思
文章編號:1008-0546(2016)08-0009-02 中圖分類號:G632.41 文獻標識碼:B
doi:10.3969/j.issn.1008-0546.2016.08.003
在提倡培養學生核心素養的今天,培養學生的批判性思維是其中重要的一環,要培養學生的批判性思維,教師首先必須具有批判性思維。而教師批判性思維的立足點應該是課堂教學,有教師就關于“碳酸鈣性質”提出了如下質疑。
一、問題的質疑
有質疑,才會有創新思維。質疑是創新思維的首要條件,是獲得創見的第一步。小疑則小進,大疑則大進。愛因斯坦說過:“提出一個問題往注比解決一個問題更重要。”
為了證明大理石高溫下分解產生氧化鈣,很多老師會做如下實驗:
實驗1:將大理石在酒精噴燈上煅燒一段時間,然后將煅燒后的石灰石投入盛有水的燒杯中,在燒杯中滴加2滴酚酞,發現溶液變紅,因此得出結論:大理石高溫煅燒分解產生氧化鈣。理由:CaCO3CaO+CO2↑, CaO+H2OCa(OH)2。反應后溶液呈堿性。
有些老師對上述實驗證明過程提出了質疑,他們的理由如下:
實驗2:在試管中加入少量碳酸鈣粉末,并加入2mL水,振蕩搖勻,制成碳酸鈣的懸濁液,在試管中滴加2滴酚酞,結果發現濁液變紅。
沒有高溫煅燒的碳酸鈣,加水制成飽和溶液后,滴入酚酞,溶液也會變紅,因此上述證明過程存在缺陷。
筆者對照上述兩個實驗,發現了兩個問題,其一是物質的狀態不同,一個是塊狀,一個是粉末狀,其二是兩者純度不同,石灰石含有雜質,而碳酸鈣是分析純。為了弄清上述問題,筆者又做了如下兩個實驗:
實驗3:在試管中加入幾塊石灰石,并加入2mL水,振蕩,在試管中滴加2滴酚酞,長時間放置,結果溶液不變紅。
實驗4: 在試管中加入研磨細的大理石,并加入2mL水,振蕩,在試管中滴加2滴酚酞,結果濁液變紅。
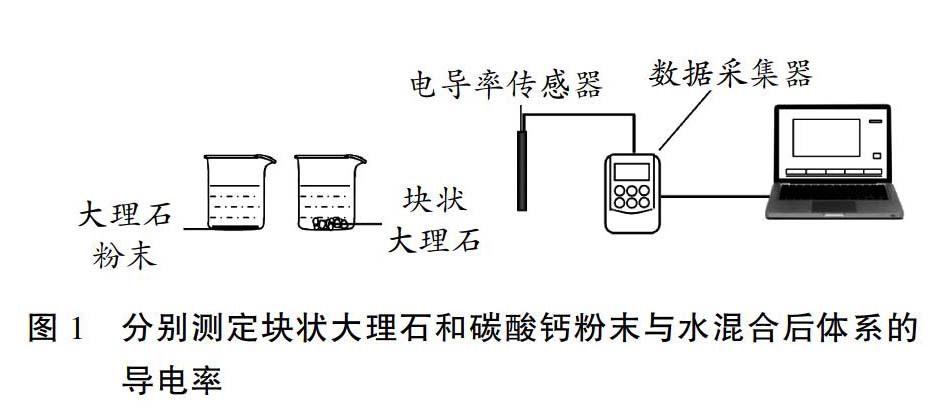
為了定量地說明上述問題,有教師利用傳感技術來分別測定上述兩溶液的電導率。裝置如圖1:
測得的數據如下:
由此可見,石灰石加入水后,滴加酚酞,濁液是否變紅,溶液導電能力的大小跟大理石的聚集狀態有著很大的關系。
二、本質的探討
碳酸鈣懸濁液滴加酚酞后為什么會變紅?筆者查閱了相關資料并進行了相關計算。
碳酸鈣的Ksp=8.7×10-9,根據Ksp=c(Ca2+) c (CO32-)[1],則溶液中c(Ca2+)=c(CO32-)=9.33×10-5mol·L-1。
碳酸的Ka1=4.30×10-7;Ka2=5.61×10-11[1]。
CaCO3的水解常數為:Kh=Kw/Ka2=10-14/5.61×10-11=1.78×10-4。飽和碳酸鈣溶液中氫氧根離子濃度為c (OH-)==1.29×10-4 mol·L-1,pOH=3.89,pH=10.11。
酚酞的變色范圍如下:
所以飽和碳酸鈣溶液能使酚酞變紅。
三、知識的拓展
拓展延伸是課堂教學當中很重要的一個組成部分。我們要在尊重學生學好教材、立足課堂的基礎上有效地拓寬,以實現學生學習上質的飛躍——超越教材、超越課堂,真正達到學為我用的目的。
拓展1:碳酸鈣懸濁液滴加酚酞后加熱,紅色會變深嗎?
對于上述問題很多老師認為紅色會加深,理由如下:
(1) 隨著溫度的升高,碳酸鈣的溶解度會增大,溶液中碳酸根離子濃度增大。
(2) 隨著溫度的升高,碳酸根離子的水解度會增大,溶液中氫氧根離子濃度增大,從而導致濁液的堿性增加,因此紅色會加深。
實驗5:在試管中加入少量碳酸鈣,并加入2mL水,振蕩搖勻,制成碳酸鈣的懸濁液,在試管中滴加2滴酚酞,濁液變紅,如果將溶液加熱,紅色逐漸變淡。
這是什么原因造成的呢?根據文獻知碳酸鈣溶解度數據如下:
通過表3可知,碳酸鈣的溶解度是隨著溫度的升高而降低的。影響溶液堿性強弱的因素有兩個,一是碳酸根離子的濃度,二是碳酸根離子的水解度,當溫度變化時,這兩個因素中碳酸根離子濃度的影響是主要因素,因此碳酸鈣懸濁液滴加酚酞后加熱,會出現紅色變淡的情況。
拓展:2:為什么碳酸鈣高溫會分解,而碳酸鈉卻很難分解
一般堿金屬碳酸鹽具有較高的熱穩定性,堿土金屬碳酸鹽不穩定,按下式分解:MCO3MO(s)+CO2(g)↑。這是什么原因呢?碳酸鹽的熱穩定性我們可用離子極化觀點來說明:在MCO3中,既存在中心C原子對周圍O2-的作用,也存在M2+對O2-的作用。
陽離子半徑愈小,極化力愈強,愈容易從CO32-中奪取O2-,成為MO。同時放出CO2,表現為MCO3的熱穩定性愈低,最易發生分解。部分碳酸鹽的分解溫度如下:
另一方面,陽離子所帶的電荷數越高,極化力愈強,離子+2價的堿土金屬離子,電荷較高,極化力強于同周期的堿金屬離子。碳酸鈉高于1000℃時會分解,當溫度高于1200℃時也只是部分分解。可見碳酸鈉的熱穩定性非常高。
四、教學的反思
現在很多年輕教師對教材的研究很膚淺,筆者認為教師對教材知識的研究分四個層次,第一層次是“是什么”,第二層次是“為什么”,第三層次是“怎么辦”,第四層次是“還有什么”。筆者以苯酚的化學性質為例:第一層次是“苯酚有哪些物理和化學性質”,第二層次是“苯酚和苯化學性質相比,為什么容易發生取代,為什么具有弱酸性,為什么不能使紫色石蕊試劑變色等”,第三層次是“如何利用苯酚的性質分離苯和苯酚”,第四層次是“苯酚具有還原性,是否可以發生銀鏡反應,過量的濃溴水能不能將苯酚氧化等”。不少年輕教師對教材知識點的研究僅限于“是什么”和“怎么辦”。課堂教學時只注重外在的形式,有精美的課件,有生動的表情,有師生的互動,但研究討論的知識只是蜻蜓點水,這樣的課堂教學感覺缺乏內涵,沒有深度。有些課堂教學則太功利,純粹的講和練,一切都是為了提高分數。
筆者希望我們教學不要太浮躁、太功利,教師應該加強對教材的研究,敢于質疑,勤于探究,讓課堂教學充滿好奇和理性的光輝。
參考文獻
[1] Handbook of Chemistry and Physics[M]. 1982-1983:B-242,D-173

