改進教材實驗,構(gòu)建學(xué)生學(xué)科觀念
劉堅

摘要:以化學(xué)實驗為載體,從建構(gòu)化學(xué)觀念角度入手,在硝酸的氧化性課堂教學(xué)中深入探討真實化學(xué)問題 ,其中包括實驗觀、 微粒觀和元素觀等化學(xué)觀念,在問題解決和活動探究中,使學(xué)生達到技能與智能的融合統(tǒng)一。
關(guān)鍵詞:實驗;硝酸的氧化性;學(xué)科觀念
文章編號:1008-0546(2016)08-0079-04 中圖分類號:G633.8 文獻標識碼:B
doi:10.3969/j.issn.1008-0546.2016.08.026
化學(xué)是一門以實驗為基礎(chǔ)的學(xué)科,而現(xiàn)行教材中,濃、稀硝酸與銅的反應(yīng),涉及到反應(yīng)物的危險性,產(chǎn)物的污染性,面臨著無法將實驗搬進教室的窘境。筆者在進行“硝酸的氧化性”的教學(xué)時,在教材原有的實驗基礎(chǔ)上,進行了深入的挖掘和改進,采用注射器和輸液袋的實驗裝置,有效地排除空氣中O2對實驗現(xiàn)象的干擾。此外,產(chǎn)生的污染氣體,也可以儲存在輸液袋中,減少了污染物的排放,最大程度的保護了學(xué)生。在教學(xué)過程中,根據(jù)教學(xué)的需求增補了一些實驗,鼓勵學(xué)生發(fā)揮主動性和創(chuàng)造性,讓學(xué)生積極參與實驗方案的設(shè)計和操作,在解決實際問題中達到了技能與智能的融合統(tǒng)一,建構(gòu)了基本化學(xué)學(xué)科觀念。
實驗觀:本節(jié)課師生共同合作設(shè)計了“測硝酸的pH”,“濃、稀硝酸與銅反應(yīng)”,“銅與NaNO3溶液反應(yīng)的條件”,“附有銅的鐵條的鈍化”等一系列實驗,通過對實驗儀器的改進和方案的優(yōu)化,引導(dǎo)學(xué)生以實驗事實為依據(jù),構(gòu)建了硝酸的強氧化性知識體系。
微粒觀:硝酸的強氧化性體現(xiàn)哪種微粒上呢?是HNO3分子,NO3-,還是H+和NO3-協(xié)同作用?通過對比銅與濃、稀硝酸的實驗現(xiàn)象,銅與NaNO3溶液反應(yīng)的條件的探究,加深了學(xué)生對微粒觀的理解,深化認識氧化還原反應(yīng)發(fā)生的條件。
元素觀:硝酸具有強氧化性是學(xué)生基于硝酸中+5價氮元素的氧化性的認識,以及其它含有+5價氮元素氧化性的探究,發(fā)展了學(xué)生的元素觀。
此外,分類觀、守恒觀、變化觀,分析比較和化學(xué)價值觀在教學(xué)中也有體現(xiàn),合理建構(gòu)了學(xué)生的基本學(xué)科觀念,提高了教學(xué)效率。
一、教學(xué)設(shè)計思路
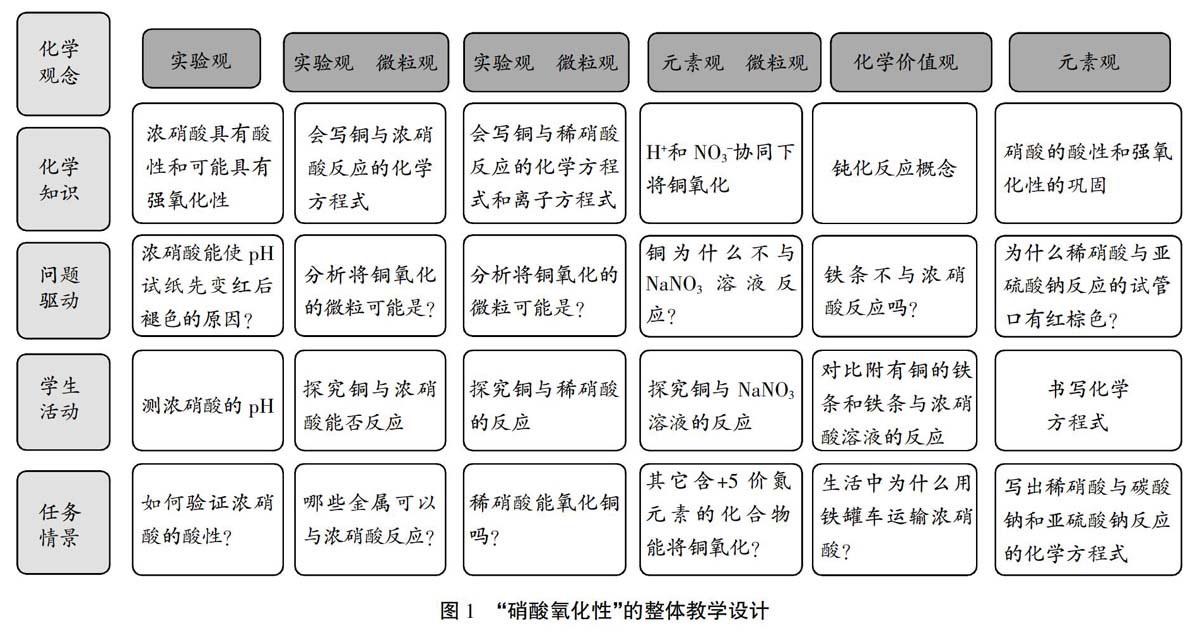
通過初中化學(xué)知識的學(xué)習(xí),學(xué)生已經(jīng)掌握酸的通性,而前一節(jié)課,學(xué)習(xí)了濃硫酸的性質(zhì),知道了濃度不同物質(zhì)的氧化性不同,產(chǎn)物也不同,這些都為硝酸的學(xué)習(xí)鋪墊了堅實的知識基礎(chǔ)。硝酸的主干知識就是強氧化性,它能與大部分金屬反應(yīng),能氧化一些非金屬,生成氮氧化物,這是與初中知識區(qū)別最大之處,本節(jié)課以化學(xué)實驗為載體,通過學(xué)生實驗,突破硝酸的強氧化性的知識難點,深化氧化還原反應(yīng)知識理論,符合“通過以化學(xué)實驗為主的多種探究活動,使學(xué)生體驗科學(xué)研究的過程,激發(fā)學(xué)習(xí)化學(xué)的興趣,強化科學(xué)探究的意識,促進學(xué)習(xí)方式的轉(zhuǎn)變,培養(yǎng)學(xué)生的創(chuàng)新精神和實踐能力”的課程理念。本節(jié)課的整體設(shè)計思路如圖1所示。
二、教學(xué)過程
1. 問題探究,初建實驗觀
[問題情景] 硝酸是強酸,如何驗證濃硝酸的酸性?
[學(xué)生活動]能與堿或某些鹽反應(yīng),與酸堿指示劑反應(yīng),與某些金屬氧化物反應(yīng),測pH等。
[學(xué)生實驗1]用pH試紙測濃硝酸的pH。
[問題情景] 我們所學(xué)的知識中,哪種物質(zhì)滴在pH試紙的現(xiàn)象和濃硝酸滴在pH試紙的現(xiàn)象變化相同?為什么pH試紙會先變紅后褪色?(追問1)說明濃硝酸可能具有什么性質(zhì)?(追問2)
[學(xué)生]新制的氯水,新制的氯水具有酸性使pH試紙變紅,具有強氧化性而使紅色褪去。說明濃硝酸可能具有強氧化性。
設(shè)計意圖:將濃硝酸滴在pH試紙上,出現(xiàn)紅色,在學(xué)生的“意料之中”,很快紅色褪去,學(xué)生驚訝不已。新的實驗現(xiàn)象與舊的知識產(chǎn)生沖突,激發(fā)了學(xué)生學(xué)習(xí)硝酸性質(zhì)的欲望。
2.實驗探究,構(gòu)建微粒觀
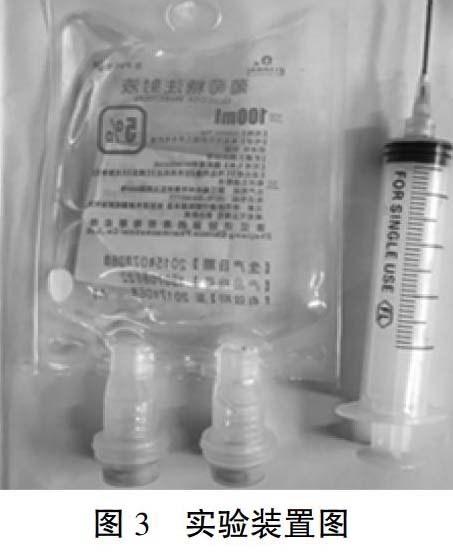
[問題情景]如果讓你選擇一種藥品來研究硝酸的氧化性,你會選什么樣的物質(zhì)呢?選什么樣的金屬呢(追問)?今天實驗室為我們提供了一種不活潑金屬單質(zhì)銅來驗證硫酸和硝酸的強氧化性,實驗裝置如圖3。
[引導(dǎo)討論](1)實驗方案。(2) 預(yù)測實驗現(xiàn)象。
(3)如何證明反應(yīng)發(fā)生?
(4) 注射器和輸液袋在實驗中有什么特殊的用途?
選取學(xué)生提出的實驗方案,進行優(yōu)化,分小組進行實驗。
[學(xué)生實驗2]
設(shè)計意圖:將教材中的“觀察與思考”改為“活動與探究”,讓學(xué)生在親身體驗中獲得了新的知識。采用輸液袋和注射器裝置,學(xué)生既可以觀察到明顯的實驗現(xiàn)象,又可以避免實驗過程中產(chǎn)生有毒害的氣體逸出,輸液袋中事先放入濃硝酸可以避免學(xué)生在吸取濃硝酸的過程中的意外發(fā)生。
[學(xué)生活動]小組匯報實驗現(xiàn)象,書寫并根據(jù)化合價升降法配平銅與濃硝酸反應(yīng)的化學(xué)方程式。
[問題情景]濃硝酸中存在哪些主要微粒?濃硝酸將銅氧化,可能是什么微粒的作用?(通過分析硝酸中氮元素的價態(tài)進行說明(追問1)?如何排除HNO3分子的影響?(追問2)。
[學(xué)生]HNO3分子、H+和NO3-還有H2O (集體回答)。
[學(xué)生1]HNO3分子(學(xué)習(xí)濃硫酸后的啟發(fā))。
[學(xué)生2]NO3-。
[學(xué)生3]加水稀釋,可以使硝酸完全電離。
[學(xué)生實驗3]完成稀硝酸與銅反應(yīng)的實驗。
設(shè)計意圖: 由于受到銅與濃硫酸反應(yīng)的影響,在討論濃硝酸與銅的反應(yīng)時,很多同學(xué)會想到濃硝酸之中存在HNO3分子,是HNO3分子與銅發(fā)生了氧化還原反應(yīng),向濃硝酸中加入水,使得HNO3在水中完全電離而排除HNO3分子的影響(高中階段),在實驗的過程中發(fā)現(xiàn)的稀硝酸和銅也可以反應(yīng),只是產(chǎn)物有所不同,說明將銅氧化的不是HNO3分子。
[學(xué)生活動]小組匯報實驗現(xiàn)象,書寫并配平銅與稀硝酸反應(yīng)的化學(xué)方程式,并將化學(xué)方程式改寫成離子方程式。
[問題情景]將銅片氧化的微粒不是HNO3,是什么呢?NaNO3溶液中也存在+5價氮元素的NO3-,銅能被NaNO3氧化嗎?(追問)
[學(xué)生]NO3-(集體回答,信心滿滿),能 (集體回答,信心滿滿)。
[學(xué)生實驗4] 將銅置于Y型試管中NaNO3溶液內(nèi)觀察,結(jié)果無明顯現(xiàn)象。
[問題情景]銅為什么不與NaNO3溶液反應(yīng)?請大家分析NaNO3溶液中存在的微粒,并結(jié)合銅與稀硝酸反應(yīng)的離子方程式進行說明。
[學(xué)生活動]小組交流討論,確定新的實驗方案:向NaNO3溶液加入稀硫酸溶液。待有明顯現(xiàn)象后,將Y型管傾斜使銅片與溶液分離。
設(shè)計意圖:通過對NaNO3溶液和稀硝酸溶液中微粒成分的比較和離子方程式的書寫和觀察,引導(dǎo)學(xué)生發(fā)現(xiàn)NO3-的氧化性依賴溶液中H+,配合后續(xù)實驗補充稀硫酸,幫助學(xué)生形成正確的“微粒觀”。使學(xué)生對硝酸的氧化性的認識上升到一個新的臺階。
3. 運用實驗,體會化學(xué)價值
[生活情景]鐵比銅活潑,為什么在生活中用鐵罐車運輸濃硝酸?
[學(xué)生實驗5]將附有Cu的鐵條和打磨后的鐵條分別插入到濃硝酸溶液中。
設(shè)計意圖:由于在鋁及其化合物的學(xué)習(xí)時,學(xué)生已經(jīng)接觸到鋁條在濃硝酸中發(fā)生鈍化,通過圖片情景,學(xué)生的舊知識很快在腦海中重現(xiàn)。通過對強調(diào)的銅與濃硝酸的反應(yīng)現(xiàn)象再次出現(xiàn),當(dāng)銅反應(yīng)完后,反應(yīng)停止,再一次視覺沖擊使學(xué)生牢固地形成鈍化的概念。學(xué)習(xí)了知識,有了收獲,更重要的是能服務(wù)于生活,讓生活變得更美好!
4. 問題解決,實現(xiàn)知識建構(gòu)
[問題情景]寫出稀硝酸分別與Na2CO3和Na2SO3反應(yīng)的化學(xué)方程式。
[學(xué)生活動]書寫化學(xué)方程式。
[引導(dǎo)討論]分析學(xué)生書寫的方程式的正誤,并引導(dǎo)學(xué)生討論稀硝酸與Na2CO3和Na2SO3反應(yīng)的化學(xué)方程式書寫為什么不同?
[演示實驗]將Y型試管中稀硝酸加入到Na2CO3固體和Na2SO3固體中。
[學(xué)生]觀察實驗現(xiàn)象,體會化學(xué)方程式的表達。
設(shè)計意圖:通過觀察實驗現(xiàn)象的不同,讓學(xué)生正確理解稀硝酸的酸性和氧化性,為學(xué)生創(chuàng)設(shè)合理的實驗情境,讓學(xué)生在實驗情境中運用知識,既是知識的遷移又是知識的升華,讓學(xué)生學(xué)有所用,體驗學(xué)習(xí)的快樂,享受問題解決的樂趣,實現(xiàn)新舊知識的建構(gòu)。
三、教學(xué)后記
“硝酸的氧化性”是元素化合物的重要組成部分,硝酸的氧化性是高中化學(xué)的重點,也是學(xué)生學(xué)習(xí)的難點。在本節(jié)課的教學(xué)中以實驗為載體通過實驗引導(dǎo)學(xué)生發(fā)現(xiàn)問題,通過實驗的方式引導(dǎo)學(xué)生認識銅與濃硝酸、稀硝酸反應(yīng)時的不同現(xiàn)象,加深對硝酸氧化性的認識及對反應(yīng)產(chǎn)物的記憶。同時在學(xué)生活動中較多地關(guān)注了學(xué)科基本技能的訓(xùn)練,通過銅與濃、稀硝酸反應(yīng)方程式的配平,學(xué)生自覺地體會硝酸在反應(yīng)中既體現(xiàn)酸性又體現(xiàn)氧化性。通過離子方程式的改寫,有利于學(xué)生客觀地認識在硝酸溶液中體現(xiàn)氧化性的微粒及H+所起的作用,從反應(yīng)中氮元素電子的得失和化合價的變化,分析了硝酸與金屬反應(yīng)的實質(zhì)。
在教材中有許多值得我們挖掘的素材,作為教師需要認真理解和充分利用資源,發(fā)揮教材的最大能效為教學(xué)服務(wù)。本節(jié)課的教學(xué)設(shè)計中,對教材中的實驗進行了改進,利用注射器和輸液袋連接成一個密閉體系,有效地排除了O2對實驗現(xiàn)象的干擾。利用注射器抽取置于輸液袋中的濃硝酸,與預(yù)先放入注射器的薄銅片反應(yīng),可以清晰地觀察銅與濃硝酸反應(yīng)的現(xiàn)象以及NO2氣體的顏色。稀硝酸與銅反應(yīng)時,針筒中產(chǎn)生的氣體為無色,當(dāng)向輸液袋中注入空氣后,氣體變化為紅棕色,由此可以證實銅與稀硝酸反應(yīng)產(chǎn)生的氣體為NO。在整個實驗中產(chǎn)生的氣體都收集在注射器封閉體系中排除了NO、 NO2有毒氣體對環(huán)境的污染,綠色環(huán)保更符合現(xiàn)代化學(xué)實驗設(shè)計的理念。
參考文獻
[1] 梁卉.中學(xué)化學(xué)學(xué)科觀念的初步研究 [D].南京:南京師范大學(xué),2008
[2] 倪娟.論基于學(xué)科觀念的化學(xué)概念教學(xué) [J].化學(xué)教育,2014,(1): 1-3
[3] 胡愛彬.實驗探究中滲透多元化學(xué)觀念的教學(xué)實踐與思考[J].中學(xué)化學(xué)教學(xué)參考,2015,(9):36-38

