運用數字化實驗測定阿司匹林腸溶片中有效成分的含量?鄢
胡蓓 劉紅葉

摘要:建立運用pH傳感器和滴數器測定阿司匹林腸溶片中阿司匹林含量的方法。利用pH傳感器的實時檢測功能和滴數器精確記錄反應液體積的功能,并借助數據采集器和計算機直接生成數據曲線,可便捷、直觀地反應中和反應過程中pH的變化,根據突變點對應的體積計算阿司匹林腸溶片中阿司匹林的含量。激發學生學習興趣,培養學生運用定量研究思維進行化學實驗的科學探究能力。
關鍵詞:pH傳感器;滴數器;阿司匹林腸溶片;含量測定
文章編號:1008-0546(2016)08-0088-03 中圖分類號:G632.41 文獻標識碼:B
doi:10.3969/j.issn.1008-0546.2016.08.029
一、問題的提出
化學是一門以實驗為基礎的自然科學,以實驗為基礎是化學教學的最基本特征。隨著現代科技的迅速發展,數字化技術作為一種現代化的新型教育手段,具有實時性、準確性、便攜性、直觀性和綜合性的特點,已成為當今科學實驗探究與課堂教學最有力的教學工具。
在人教版選修1《化學與生活》教材里[1],第二章第二節“正確使用藥物”中介紹的解熱鎮痛藥——阿司匹林,是人們熟知的治感冒藥,其化學名為乙酰水楊酸,是一種有機酸。阿司匹林作為第一個重要的人工合成藥物,其應用開辟了醫藥化工的全新領域,投入市場一百多年來,迄今仍然是銷量最大的藥物,人們還不斷發現它的新作用,如防止心臟病發作、減緩老年人視力衰退和提高免疫功能等。通過本節內容學習,學生關注健康的同時也知道生病時該如何正確用藥,進一步樹立健康新觀念、促進身心健康,體會到化學如何改善生活品質、提高生活質量,也真正體現了“化學從生活中來,到生活中去”的理念。
滴定分析法是化學分析法的基本內容之一,酸堿中和滴定作為一種重要的滴定分析法,由于該方法所涉及原理、藥品、操作都相對簡單,使其成為中學階段介紹的唯一的滴定分析法,同時也是中學化學為數不多的定量實驗之一,具有重要的方法教育作用。根據阿司匹林顯酸性的羧基與氫氧化鈉進行酸堿中和滴定反應,數字化實驗系統可以記錄實驗過程并繪制反應曲線,運用計算機進行數據分析得到pH突變點,即完全反應點,由消耗溶液的體積和濃度計算出待測品的量[2]。
本文在中學可能提供的儀器條件下,通過課本上的化學知識與數字化實驗的結合,激發學生學習化學的興趣,有利于提高課堂教學效果;加強學生使用數字化實驗進行課外拓展科學探究活動的意識,讓學生積極參與精密定量分析的實驗,培養嚴謹求實的科學態度。
二、實驗過程
1. 實驗用品和裝置
(1)儀器:pH傳感器、滴數器、數據采集器、計算機、磁力攪拌器、燒杯、容量瓶、量筒、移液管、膠頭滴管、玻璃棒、漏斗等;
(2) 試劑:阿司匹林腸溶片(規格:25mg/片)、NaOH溶液(0.2mol/L)、HCl溶液(0.1mol/L)、無水乙醇等。
(3)裝置圖。
2. 實驗目的
把數字化實驗系統引進課堂,讓學生熟悉數字化實驗系統的操作,學會酸堿中和反應曲線的數據分析,培養定量科學探究的思維;同時讓學生在課堂上更好地理解阿司匹林的結構和性質,也加深對必修二中有機化學的基礎知識的掌握。
3. 實驗原理
阿司匹林,化學名為乙酰水楊酸,其結構式(如下)中,含有—COOH,顯酸性,可以與氫氧化鈉進行酸堿中和反應;—OCOCH3,可在堿性條件下加熱水解。
(乙酰水楊酸)
阿司匹林腸溶片中的羧酸主要包含阿司匹林的羧基、少量殘留水楊酸的羧基、穩定劑酒石酸或檸檬酸的羧基等。在低溫條件下,這些羧酸都能與NaOH直接反應,統稱為總羧酸,終點1反應后都生成羧酸鈉,反應計量比為1:1[3]。
方程式如下:
根據阿司匹林鈉鹽在過量NaOH加熱條件下,酯基水解消耗NaOH的量測定阿司匹林的含量,剩余NaOH用HCl返滴定。
方程式如下:
4. 實驗方法
(1)取數片阿司匹林(25mg/片規格,取約0.3g,10片)腸溶片研磨后放于燒杯中,量取25mL60%的乙醇溶液溶解阿司匹林。按照圖1連接裝置,將pH傳感器、滴數器與數據采集器連接,再與計算機相連,打開軟件。
(2)用0.2mol/L NaOH溶液滴定,自動記錄pH-VNaOH曲線,根據曲線突變點記下消耗NaOH為V1mL,該點記錄為終點1;終點1后繼續加入NaOH溶液直到V0mL(V0≈2V1~3V1)。
(3) 將上述溶液放于磁力攪拌器上加微熱攪拌10min,再迅速冷卻至室溫,用0.1mol/L HCl溶液滴定,記錄pH-VHCl曲線,根據曲線突變點記下消耗HCl為V2mL,該點記錄為終點2。根據V1、V0、V2 計算阿司匹林腸溶片中阿司匹林的含量。
5. 數據處理
阿司匹林w% =
式中:w為標示量的百分含量;c(NaOH)為NaOH溶液的濃度;V1為終點1消耗NaOH溶液的體積;V0為加入NaOH溶液的總體積;V2為終點2消耗HCl溶液的體積;180.2為阿司匹林的摩爾質量;m為阿司匹林腸溶片中阿司匹林的標示量;n為直接取阿司匹林腸溶片的片數。
三、實驗結果
1. 實驗1
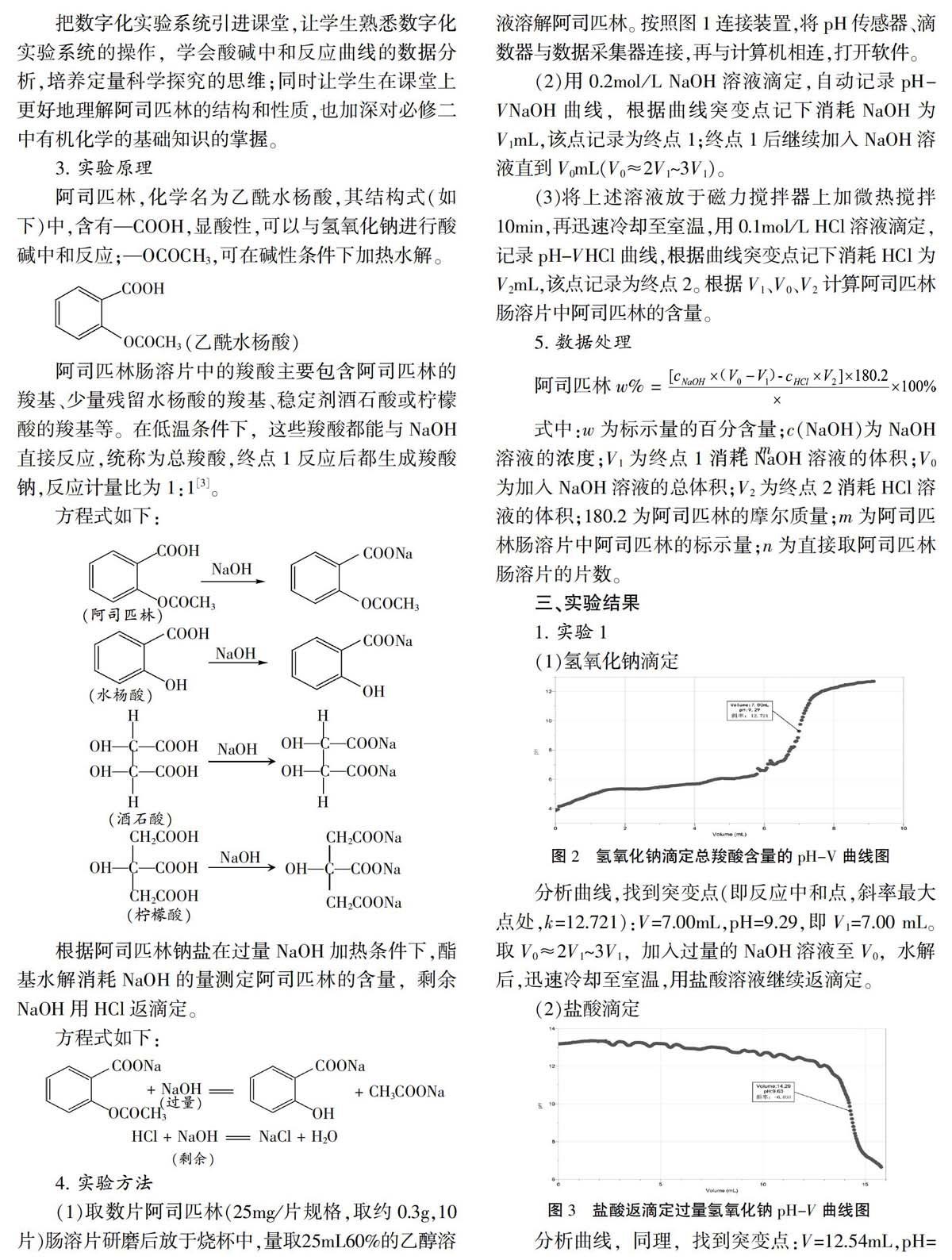
(1)氫氧化鈉滴定
分析曲線,找到突變點(即反應中和點,斜率最大點處,k=12.721):V=7.00mL,pH=9.29,即V1=7.00 mL。取V0≈2V1~3V1,加入過量的NaOH溶液至V0,水解后,迅速冷卻至室溫,用鹽酸溶液繼續返滴定。
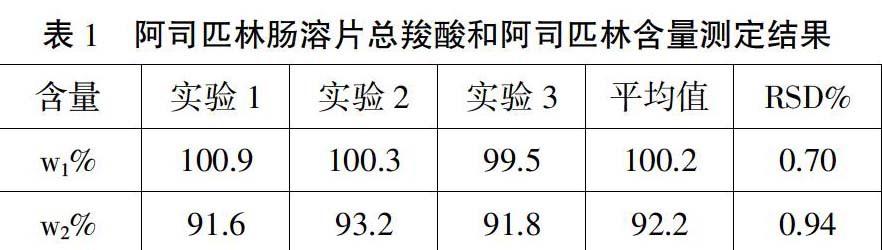
(2)鹽酸滴定
分析曲線,同理,找到突變點:V=12.54mL,pH=9.38,即V2=12.54mL。
(3)含量
根據計算公式,得阿司匹林含量w% =91.6%。
說明:在上述滴定實驗中,突變點(即滴定終點)的pH分別為9.29和9.38,而水楊酸鈉中的酚羥基在pH<12時是穩定的,pH>12時會形成酚鈉[5],且酯水解常溫下反應很慢,需要一定的加熱條件,故上述實驗中的V1只是羧基消耗的氫氧化鈉體積;第二步加氫氧化鈉并加熱10min時消耗的氫氧化鈉是用于酯基水解的。
以上述方式重復做實驗2、實驗3。
4. 結果
四、討論與總結
1. 討論
本實驗中阿司匹林腸溶片的溶解操作,需先研磨成粉末,加入乙醇溶液再微熱(溫度不宜過高,否則乙醇會揮發)攪拌的條件下,可促進阿司匹林充分溶解;若有條件的話可使用超聲波清洗機進行超聲處理加速溶解。若溶解不完全則會導致第一次氫氧化鈉滴定體積偏低。
阿司匹林在過量氫氧化鈉中微熱水解前,考慮到阿司匹林腸溶片中還有淀粉等不溶性輔料也會與氫氧化鈉反應,所以在第一步滴定完成后采取過濾操作;實驗室里用漏斗過濾速度較慢,若能提供減壓抽濾裝置則可加快過濾,提高效率。另外,還需注意,若過濾不完全,阿司匹林水解時間過長,溫度過高,則會導致第二次鹽酸滴定體積偏低,即氫氧化鈉消耗偏多,阿司匹林含量偏高。
最后,滴定時滴定速度不宜過快;一方面要使反應充分進行,另一方面滴定曲線也會更平滑美觀,滴定的突躍更明顯,對于體積的讀數會更準確。
2. 總結
在采用數字結合酸堿中和反應滴定阿司匹林腸溶片中總羧酸和阿司匹林的含量,終點突躍明顯(終點出現pH>7,那是因為反應生成的羧酸鈉顯堿性,所以符合要求);而且利用傳感器檢測中和反應過程中的pH的變化,經數據采集器和計算機的處理可以直接轉化為曲線呈現,大大簡化了繪制中和反應曲線的過程,使學生能夠更加直觀地認識這一過程pH變化的趨勢,從而幫助學生理解酸堿中和滴定方法的原理。
在現今中學階段的實驗中,學生多依賴于直覺觀察,所以若能將傳感器技術應用于含量測定的定量實驗中,把數字化手持技術實驗和化學課堂教學整合,探究定量化學實驗,使教學過程更加生動、便于理解,提高教學效率;同時學生可以得出直觀、準確的實驗結論,掌握科學探究的方法,提高創新思維和實踐能力,從而充分落實化學學科的知識與技能、過程與方法和情感態度價值觀三維目標。
參考文獻
[1] 人民教育出版社課程教材研究所化學課程研發中心.普通高中課程標準實驗教科書·化學 選修1[M].北京:人民教育出版社,2012
[2] 魏銳,包明等.利用pH傳感器研究中和反應過程中pH的突變[J].化學教育,2007,28(4):59-61
[3] 楊孝容,向清祥等.自動電位滴定法測定阿司匹林腸溶片中總羧酸和阿司匹林的含量[J].化學研究與應用,2015,27(12):1891-1895
[4] 王鋼.新課程標準下數字化實驗在化學教學中的探索與實踐[J].科學教育家,2008,(4):400-401
[5] 熊曉丹,孫丹,吳雪亭,伍曉春.阿司匹林中乙酰水楊酸含量測定的問題探討[J]. 化學教學,2015,10:91-93

