益生菌對非酒精性脂肪性肝病的干預(yù)作用
趙慶衛(wèi) 呂道仙

[摘要] 目的 觀察口服益生菌對非酒精性脂肪性肝病(NAFLD)干預(yù)的效果。 方法 采用隨機(jī)、對照、雙盲研究方法,選取2012年5月~2014年10月對符合NAFLD入選標(biāo)準(zhǔn)的63例患者隨機(jī)分為兩組(隨機(jī)比例為1∶1),在予改變生活方式和中等量有氧運(yùn)動的基礎(chǔ)治療同時,試驗組予口服培菲康(雙歧桿菌三聯(lián)活菌膠囊)0.84 g/次,2次/ d,對照組予淀粉膠囊,每次4粒,2次/d,治療6個月。觀察治療前后體質(zhì)量指數(shù)(BMI)、腰圍(WC)、ALT、AST、GGT、TG、TC變化,采用脂肪肝指數(shù)(FLI)作療效評價。 結(jié)果 除對照組GGT(t=1.731,P=0.089)與治療前比較無統(tǒng)計學(xué)的顯著差異外,兩組患者分別與治療前比較,體質(zhì)量指數(shù)(BMI)、腰圍(WC)、ALT、AST、TG、TC、脂肪肝指數(shù)(FLI)的差異均有統(tǒng)計學(xué)意義(P<0.05)。治療后益生菌干預(yù)組與對照組間BMI(t=1.407,P=0.165)以及WC(t=1.223,P=0.226)比較差異無統(tǒng)計學(xué)意義(P>0.05);ALT(t=2.125,P=0.038)、AST(t=2.058,P=0.044)、GGT(t=2.045,P=0.045)、TG(t=2.091,P=0.041)、TC(t=2.047,P=0.045)比較差異均有統(tǒng)計學(xué)意義(P<0.05)。FLI(t=4.257,P=0.000)比較有顯著統(tǒng)計學(xué)意義(P<0.01)。治療前兩組患者FLI均>60,治療后益生菌干預(yù)組30≤FLI<60患者例數(shù)為10例(30.3%),F(xiàn)LI<30患者例數(shù)為23例(69.7%),無FLI>60患者。對照組30≤FLI<60患者例數(shù)為17例(56.7%),F(xiàn)LI<30患者例數(shù)為13例(43.3%),也無FLI>60患者。兩組間比較差異有統(tǒng)計學(xué)意義(χ2=4.460,P=0.0347)。 結(jié)論 口服益生菌對非酒精性脂肪性肝病干預(yù)效果確切。但各項觀察指標(biāo)未能完全恢復(fù),對NAFLD的療效仍有待進(jìn)一步探索。
[關(guān)鍵詞] 益生菌; 非酒精性脂肪性肝病; 雙歧桿菌三聯(lián)活菌膠囊; 脂肪肝指數(shù); 腸道微生態(tài)
[中圖分類號] R575 [文獻(xiàn)標(biāo)識碼] B [文章編號] 1673-9701(2016)08-0029-05
隨著人們生活習(xí)慣和飲食結(jié)構(gòu)的改變,非酒精性脂肪性肝病(non-alcoholic fatty liver disease,NAFLD)的患病率日益增高,已構(gòu)成日益嚴(yán)重的社會公共衛(wèi)生問題。非酒精性脂肪性肝病是一種與胰島素抵抗和遺傳易感性密切相關(guān)的代謝應(yīng)激性肝損傷,是一種無過量飲酒史、以肝實質(zhì)細(xì)胞大泡性脂肪變和脂肪貯積為主要特征的臨床病理綜合征。疾病譜包括非酒精性單純性脂肪肝(non-alcoholic simple fatty liver,NAFL),非酒精性脂肪性肝炎(non-alcoholic steatohepatitis,NASH)及其相關(guān)肝硬化和肝細(xì)胞癌。NAFLD的發(fā)病機(jī)制未明確。目前認(rèn)為,NAFLD的發(fā)生、進(jìn)展與腸道菌群改變密切相關(guān),腸道微生態(tài)作為人體的一個代謝器官,有望成為藥物治療的靶點。本研究探討益生菌培菲康治療NAFLD的療效,現(xiàn)報道如下。
1 資料與方法
1.1 一般資料
所有受試者來源于我院內(nèi)科門診,全部獲得知情同意,并簽署知情同意書。選取2012年5月~2014年10月共63例符合入選標(biāo)準(zhǔn)的NAFLD患者納入臨床試驗。
1.2 診斷標(biāo)準(zhǔn)
根據(jù)中華醫(yī)學(xué)會肝臟病學(xué)分會脂肪肝和酒精肝病學(xué)組2010年1月修訂的《非酒精性脂肪性肝病的診療指南》[1],符合以下3項條件:(1)無飲酒史或飲酒折合乙醇量小于140 g/周(女性<70 g/周);(2)除外病毒性肝炎、藥物性肝病、全胃腸外營養(yǎng)、肝豆?fàn)詈俗冃浴⒆陨砻庖咝愿尾〉瓤蓪?dǎo)致脂肪肝的特定疾病;(3)鑒于肝組織學(xué)診斷難以獲得,采用肝臟影像學(xué)標(biāo)準(zhǔn):腹部超聲檢查符合以下3項表現(xiàn)中的兩項:①肝臟近場回聲彌漫性增強(qiáng)(“明亮肝”),回聲強(qiáng)于腎臟;②肝內(nèi)管道結(jié)構(gòu)顯示不清;③肝臟遠(yuǎn)場回聲逐漸衰減或CT診斷為肝臟密度普遍減低,肝/脾CT值之比小于1.0。
1.3 排除標(biāo)準(zhǔn)
(1)酒精性脂肪肝、各種病毒性肝炎;(2)肝硬化失代償期、肝癌患者;(3)合并心腦血管、肝、肺、腎、內(nèi)分泌等原發(fā)性疾病以及精神病患者;(4)妊娠或哺乳期婦女;(5)近4周內(nèi)使用過抗生素、乳果糖、制酸劑、微生態(tài)制劑及其他影響胃腸動力的藥物,近1周患急性腸炎者;(6)用藥依從性差,2 d以上未按要求服藥者;(7)觀察期內(nèi)合并使用其他治療如降脂藥保肝藥;不按時復(fù)診或失訪者不進(jìn)入療效分析;(8)轉(zhuǎn)氨酶(包括ALT、AST)超過4 ULN的患者。
1.4 方法
本研究采用隨機(jī)、雙盲對照研究,入選患者在進(jìn)行健康宣教、飲食控制、改變飲食組分,中等量有氧運(yùn)動(每周4次以上,累計鍛煉時間大于150 min/周,運(yùn)動后靶心率>170-年齡)的治療基礎(chǔ)上,隨機(jī)分為兩組:試驗組予培菲康(雙歧桿菌三聯(lián)活菌膠囊,上海信誼藥廠有限公司,批準(zhǔn)文號:國藥準(zhǔn)字S10950032,規(guī)格:0.21 g/片,含活菌數(shù)分別不低于0.5×107 CFU)0.84 g/次,2次/d干預(yù)治療,對照組予淀粉膠囊,每次4粒,2次/d。由專門人員對符合標(biāo)準(zhǔn)的受試者按照門診就診號由計算機(jī)隨機(jī)分組(隨機(jī)比例為1∶1)。建立電子檔案及門診隨訪卡,但對治療方案作隱匿。療程共6月。
1.5 觀察指標(biāo)
入組后:(1)詳細(xì)詢問病史,包括體質(zhì)量變化、煙酒嗜好、既往病史、家族史和相關(guān)藥物史,記錄飲食和運(yùn)動情況;(2)測量身高(精確到1 cm)、體重(精確到0.1 kg)、腰圍(WC,以臍水平為測量部位),計算體質(zhì)量指數(shù)[BMI=體質(zhì)量(kg)/身高2(m2)],測量靜息血壓。(3)血液檢查:全血細(xì)胞分析;隔夜空腹12 h,抽取靜脈血檢測空腹血糖、糖化血紅蛋白,肝功能生化指標(biāo)(ALT、AST、GGT)、血脂(總膽固醇TC、三酰甘油TG、高密度脂蛋白膽固醇、低密度脂蛋白膽固醇);(4)腹部超聲檢查及CT檢查。3、6個月復(fù)查BMI、肝功能、血脂、空腹血糖及腹部超聲檢查。
1.6 療效評價
觀察治療前后BMI、WC、ALT、AST、GGT、TG、TC變化,采用脂肪肝指數(shù)(fatty liver index,F(xiàn)LI)[2]作療效評價。FLI計算公式
FLI=■×100
其中l(wèi)n代表取自然對數(shù),е為自然對數(shù)的底數(shù)。TG單位為mg/dL(1 mmol/L = 88.5 mg/dL),BMI單位為kg/m2,GGT單位為U/L,WC單位為cm。FLI<30為NAFLD消退,30≤FLI<60為可疑NAFLD,F(xiàn)LI>60為NAFLD可能性極大。
1.7 統(tǒng)計學(xué)方法
應(yīng)用Excel2003及SPSS 19.0統(tǒng)計學(xué)軟件處理,計量資料以(x±s)表示,計數(shù)資料以率或構(gòu)成比表示。兩組間比較、治療前后比較,計量資料采用t檢驗,計數(shù)資料采用χ2檢驗,P<0.05為差異有統(tǒng)計學(xué)意義。
2 結(jié)果
2.1 基線資料
選取2012年5月~2014年10月在我院內(nèi)科門診就診診斷為非酒精性脂肪性肝病符合入選標(biāo)準(zhǔn)的患者63例,其中男38例,女25例,男∶女1.52∶1,年齡26~67歲,平均(44.27±9.50)歲。隨機(jī)分為兩組,試驗組33例,男20例,女13例,年齡29~67歲,平均(44.05±11.60)歲,對照組30例,男18例,女12例,年齡26~63歲,平均(43.13±9.57)歲。兩組患者性別(χ2=0.002,P=0.96)、年齡(t=0.341,P=0.734)比較無差異性。兩組患者治療前體質(zhì)量指數(shù)(BMI)、腰圍(WC)、ALT、AST、GGT、TG、TC、脂肪肝指數(shù)(FLI)比較見表1,t/P值分別為1.086/0.282、0.675/0.502、1.116/0.269、1.442/0.154、0.453/ 0.652、0.817/0.417、0.259/0.797、1.274/0.208,差異均無統(tǒng)計學(xué)意義(P>0.05)。
2.2 治療前后兩組組內(nèi)BMI、WC、肝功能、血脂及脂肪肝指數(shù)(FLI)比較
經(jīng)治療6個月,各項指標(biāo)治療前后對比,除對照組GGT(t=1.731,P=0.089)與治療前比較差異無統(tǒng)計學(xué)意義外,兩組患者體質(zhì)量指數(shù)(BMI)、腰圍(WC)、ALT、AST、TG、TC、脂肪肝指數(shù)(FLI)分別與治療前比較,差異具有統(tǒng)計學(xué)意義(P<0.05)(表1)。
2.3 治療后兩組BMI、WC、肝功能、血脂及FLI比較
治療后,試驗組與對照組BMI(t=1.407,P=0.165)以及WC(t=1.223,P=0.226)比較差異無統(tǒng)計學(xué)意義(P>0.05)。ALT(t=2.125,P=0.038)、AST(t=2.058,P=0.044)、GGT(t=2.045,P=0.045)、TG(t=2.091,P=0.041)、TC(t=2.047,P=0.045)比較差異均有統(tǒng)計學(xué)意義(P<0.05)。兩組FLI比較有極顯著差異(t=4.257,P<0.01)(表1)。
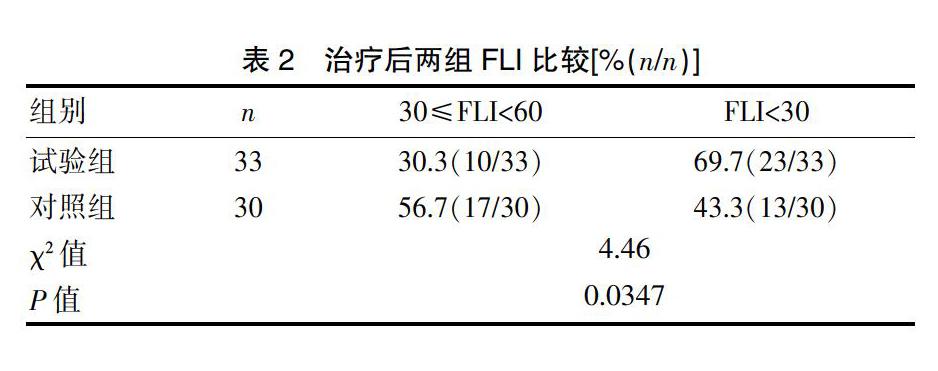
2.4 兩組治療后脂肪肝指數(shù)(FLI)比較
治療前兩組患者FLI均>60,治療后兩組均無FLI>60患者。兩組間FLI比較差異有高度統(tǒng)計學(xué)意義(P<0.01)(表2)。
3 討論
NAFLD發(fā)病機(jī)制中,肥胖、高脂血癥、糖尿病是NAFLD發(fā)病的主要危險因素。在氧化應(yīng)激、胰島素抵抗、炎性反應(yīng)等多因素的“二次打擊”,甚至是多重打擊[3]的結(jié)果導(dǎo)致了NAFLD。肝臟與胃腸道作為消化系統(tǒng)的重要組成部分,二者在解剖上、功能上有著密切聯(lián)系。作為門靜脈的首過器官,肝臟易受腸源性微生物及其代謝產(chǎn)物的影響,進(jìn)而影響腸道菌群,導(dǎo)致菌群失調(diào)。腸道微生態(tài)失衡,生物屏障功能受損后大量內(nèi)毒素進(jìn)入門脈系統(tǒng),促發(fā)炎癥介質(zhì)釋放,導(dǎo)致肝臟的氧化應(yīng)激反應(yīng)及炎癥損傷,又加重NAFLD的炎癥。近年的研究表明,小腸細(xì)菌過度生長[4](small intestinal bacterial overgrowth,SIBO)、細(xì)菌易位、腸黏膜通透性改變等所致腸源性內(nèi)毒素(intestinal endotoxemia,IETM)可促進(jìn)NAFLD向非酒精性脂肪性肝炎(NASH)進(jìn)展,而NASH患者腸道IETM如脂多糖(lipopolysaccharide,LPS)等生成增多可進(jìn)一步加劇肝損傷,兩者形成惡性循環(huán),加速NASH的進(jìn)展[5,6]。
NAFLD患者腸道菌群在數(shù)量、構(gòu)成,以及定位上發(fā)生改變。沈峰、范建高等[7]采用454焦磷酸測序技術(shù)對47例經(jīng)肝活檢確診的NAFLD患者新鮮糞便進(jìn)行測序,結(jié)果顯示NAFLD患者厚壁菌門所占比例顯著升高,而擬桿菌門顯著降低,乳球菌和普氏菌顯著減少,而鏈球菌占比顯著增高。另一研究[8]也證實NAFLD患者存在小腸細(xì)菌過度生長(small intestinal bacterial overgrowth,SIBO),發(fā)生率為57.8%(59/102),與健康人群發(fā)生率8.0%(4/50)比較,差異有統(tǒng)計學(xué)意義(P<0.05)。較多的研究顯示[9-12],腸道菌群失調(diào),突出表現(xiàn)為腸道原有的益生菌如雙歧桿菌、類桿菌等明顯減少,而大腸埃希菌、產(chǎn)氣桿菌等革蘭陰性菌大量繁殖,腸球菌和真菌比例也明顯增加。腸道革蘭陰性桿菌產(chǎn)生的脂多糖(LPS)作為一種細(xì)菌毒性因子誘發(fā)產(chǎn)生氧自由基,造成肝細(xì)胞脂質(zhì)過氧化,使肝細(xì)胞線粒體內(nèi)K+通透性增高,通過一系列改變,造成肝細(xì)胞損害、自溶。LPS還通過Toll樣受體4(Toll-like receptor 4,TLR4)信號途徑激活胰島細(xì)胞、肝臟的Kupffer細(xì)胞,釋放大量炎癥因子如TNF-α、NF-κB等,阻斷胰島素受體從而導(dǎo)致胰島素抵抗(insulin resistance,IR),介導(dǎo)肝臟的炎癥和病理損傷[5,13]。LPS參與了NAFLD發(fā)病的“二次打擊”過程中IR和炎性反應(yīng)的多個環(huán)節(jié)。
肥胖是NAFLD發(fā)病的主要危險因素,肥胖人群腸道中擬桿菌數(shù)量明顯高于消瘦人群,隨著BMI增加,大腸桿菌、乳酸桿菌、雙歧桿菌數(shù)量呈下降趨勢。動物實驗證實,擬桿菌可發(fā)酵和降解機(jī)體無法消化、吸收的植物多糖,增加15%的能量吸收,可使機(jī)體脂肪量增加,血三酰甘油水平明顯增加。擬桿菌還可以抑制腸黏膜上皮中禁食誘導(dǎo)脂肪因子(fasting-induced adipose factor,F(xiàn)iaf)的表達(dá),從而導(dǎo)致脂肪積累,促進(jìn)肥胖形成[14,15]。
口服益生菌,補(bǔ)充腸道有益菌,在腸道中對致病菌產(chǎn)生營養(yǎng)競爭、粘附競爭以及生物化學(xué)競爭作用,其代謝產(chǎn)物能阻止致病微生物的定植和入侵,調(diào)節(jié)腸道微生態(tài)平衡,抑制小腸細(xì)菌過度生長(SIBO),改善小腸動力阻力,改善NAFLD患者的腸道屏障功能,降低血循環(huán)中代謝性內(nèi)毒素水平,減輕肝臟損傷及脂肪沉積[16]。還能減輕脂肪組織的炎癥反應(yīng)及氧化應(yīng)激,提高胰島素的敏感性,從而控制及治療NAFLD,或延緩NAFLD進(jìn)展,并能使體質(zhì)量降低。趙嚴(yán)等[17]報道應(yīng)用培菲康治療后,可減輕NAFLD患者的TNF-α、IR,降低腸源性內(nèi)毒素血癥(IETM),改善脂聯(lián)素(adiponection,APN)及肝功能。另一報道顯示[18],經(jīng)益生菌治療后NAFLD患者ALT、AST、GGT、TG、TC、TNF-α水平均顯著降低,CT肝/脾比值顯著增高、超聲積分顯著降低(P<0.05)。
在益生菌治療NAFLD的臨床試驗研究中,大規(guī)模隨機(jī)對照試驗(randomized controlled trial,RCTs)研究不多。一項系統(tǒng)評價研究[19]結(jié)果顯示,益生菌類制劑可減低NAFLD患者ALT、AST、GGT、TG、TC水平,恢復(fù)肝功能。本研究采用隨機(jī)、雙盲、空白對照試驗,比較以改變生活方式和增加運(yùn)動的基礎(chǔ)治療同時口服益生菌培菲康與基礎(chǔ)治療在治療前后肝功能、血脂及脂肪肝指數(shù)上的差異,結(jié)果顯示益生菌能顯著降低NAFLD患者的肝功能、血脂等各項指標(biāo),降低患者FLI,從而減輕、消退NAFLD。
在NAFLD的診斷和療效評估方面,肝活檢這一“金標(biāo)準(zhǔn)”因其創(chuàng)傷性,受試者依從性差,且費用昂貴,難以在臨床日常工作中開展及進(jìn)行重復(fù)運(yùn)用。而CT檢查放射性強(qiáng),對人體也有傷害,也應(yīng)盡量減少檢查,常規(guī)超聲檢查靈敏度不高,而且CT及常規(guī)超聲檢查無法對脂肪變的程度進(jìn)行定量。瞬時彈性成像系統(tǒng)Fibro Scan等[20]新技術(shù)臨床應(yīng)用尚未普及,在此背景下血清學(xué)方法仍為臨床試驗評估NAFLD的常用手段,但單純BMI、肝功能或血脂譜等的評估價值較低。西方國家及韓國等應(yīng)用FLI對NAFLD進(jìn)行評估,準(zhǔn)確性為0.785~0.84(95%CI:0.81~0.87)。國內(nèi)上海交通大學(xué)醫(yī)學(xué)院瑞金醫(yī)院[2,21]開展FLI與NAFLD相關(guān)性研究,其準(zhǔn)確性為0.721~0.84(95%CI:0.678~0.86)。我們借用這一方法來對培菲康干預(yù)NAFLD進(jìn)行療效評估,作定量分析。研究顯示兩組患者FLI治療前和治療后分別對比,均有明顯降低,治療前后差異具有統(tǒng)計學(xué)意義。兩組間治療后對比有極顯著差異(t=4.257,P<0.01),兩組間NAFLD消退(FLI<30)例數(shù)比較差異也具有統(tǒng)計學(xué)意義。本研究中GGT在對照組治療前后無統(tǒng)計學(xué)意義,猜測可能與GGT的變化反應(yīng)相對要慢些有關(guān),也說明單純指標(biāo)的評估價值很有限,而應(yīng)用FLI綜合判斷相對較好。
本研究中發(fā)現(xiàn)兩組患者BMI和WC在治療前和治療后分別對比,治療前后具有顯著差異,而兩組間治療后對比無顯著差異,其原因分析可能因抗肥胖與補(bǔ)充腸道有益菌種種類等有關(guān)。羅佳等[22]對文獻(xiàn)綜述顯示人體腸道高水平干酪乳桿菌、副干酪乳桿菌以及植物乳桿菌與肥胖的發(fā)生呈負(fù)相關(guān),高水平羅伊乳桿菌與肥胖發(fā)生呈正相關(guān)。
總之,本文研究表明口服益生菌對非酒精性脂肪性肝病干預(yù)具有確切療效。但本研究顯示其對BMI、WC、肝功能、血脂的各項指標(biāo)仍未降至正常水平內(nèi),仍未能完全治愈NAFLD。另外,本研究樣本數(shù)較少,對益生菌干預(yù)NAFLD作用的評價有限。對益生菌干預(yù)治療NAFLD,在菌種選擇、劑量、療程等方面仍有較大的探索空間。
[參考文獻(xiàn)]
[1] 中華醫(yī)學(xué)會肝病學(xué)分會脂肪肝和酒精性肝病學(xué)組. 非酒精性脂肪性肝病診療指南(2010年1月修訂)[J]. 中華內(nèi)科雜志,2010,49(3):275-278.
[2] 張迪,孫侃,劉宇,等. 脂肪肝指數(shù)在非酒精性脂肪性肝病診斷中的應(yīng)用價值[J]. 內(nèi)科理論與實踐,2012,7(3):201-204.
[3] 巫協(xié)寧. 非酒精性脂肪性肝炎的發(fā)病機(jī)制新說:多重打擊論和治療[J]. 中華消化雜志,2014,34(3):206-209.
[4] 鄭霞,戴寧. 小腸細(xì)菌過度生長的發(fā)病機(jī)制和診斷進(jìn)展[J].胃腸病學(xué),2012,17(8):499-502.
[5] 馬光斌,陸倫根. 腸源性內(nèi)毒素血癥:非酒精性脂肪性肝病的重要危險因素[J]. 胃腸病學(xué),2010,15(9):562-564.
[6] 吳文明,李帆,楊云生. 腸道菌群與肝病關(guān)系的研究進(jìn)展[J]. 中華消化雜志,2013,33(7): 500-502.
[7] 沈峰,陳建能,鄭瑞丹,等. 應(yīng)用454測序技術(shù)評價非酒精性脂肪性肝病患者腸道菌群結(jié)構(gòu)差異[J]. 實用肝臟病雜志,2015,18(2):145-149.
[8] 張愛青,楊雪敏,李韋,等. NAFLD患者小腸細(xì)菌過度生長情況及雙歧三聯(lián)活菌膠囊的療效[J]. 山東醫(yī)藥,2014, 54(15):69-71.
[9] 楊云生,王子愷. 腸道微生態(tài)的重要作用與研究展望[J].中華消化雜志,2013,33(12):803-805.
[10] 李蘭娟. 進(jìn)一步深入對腸道微生態(tài)失衡與肝病重癥化關(guān)系的研究[J]. 中華內(nèi)科雜志,2015,54(5):393-395.
[11] 楊云生. 消化道微生態(tài)研究聚焦與展望[J]. 中華內(nèi)科雜志,2015,54(5):396-398.
[12] 王斯南,曹海龍,鄢芳,等. 基于腸道菌群的代謝性疾病防治新策略[J]. 中華內(nèi)科雜志,2015,54(5):458-460.
[13] 李帆,楊云生. 非酒精性脂肪性肝病與腸道菌群關(guān)系的研究進(jìn)展[J]. 中華消化雜志,2013,33(1):67-68.
[14] 蔣彩鳳,陳岳祥,謝謂芬. 腸道微生態(tài)在慢性肝病發(fā)生發(fā)展中的作用[J]. 中華消化雜志,2013,33(12):814-816.
[15] 郝一鳴,余鵬飛,白檳,等. 腸道菌群、肥胖、飲食和能量吸收關(guān)系的研究進(jìn)展[J]. 中華消化雜志,2014,34(12):867-869.
[16] 姚惠香,陳維雄,陳瑋,等. 益生菌治療非酒精性脂肪性肝病的臨床研究[J]. 胃腸病學(xué)與肝病學(xué)雜志,2013, 22(3):221-223.
[17] 趙嚴(yán),湯茂春,程禮,等. 培菲康治療非酒精性脂肪性肝病的臨床觀察[J]. 胃腸病學(xué)與肝病學(xué)雜志,2009,18(7):612-614.
[18] 羅靈和,陳軍賢,劉海燕,等. 枯草桿菌腸球菌二聯(lián)活菌對非酒精性脂肪性肝炎患者的干預(yù)作用[J]. 中華消化雜志,2014,34(12):852-853.
[19] 劉潔,李嘉. 益生菌類制劑治療非酒精性脂肪性肝病療效評價[J]. 山東醫(yī)藥,2015,55(7):82-84.
[20] 曾祥華,石代蓉,王宇明. FibroScan用于慢性肝病臨床診治新進(jìn)展[J]. 中國實用內(nèi)科雜志,2014,34(12):1185-1188.
[21] 常顯星,蔣兆彥,徐琛瑩,等. 脂肪肝指數(shù)與非酒精性脂肪性肝病和冠狀動脈粥樣硬化性心臟病的相關(guān)性研究[J]. 胃腸病學(xué),2013,18(1):6-10.
[22] 羅佳,姜春燕. 腸道微生態(tài)與代謝性疾病關(guān)系的研究進(jìn)展[J]. 胃腸病學(xué),2013,18(9):569-571.
(收稿日期:2015-11-30)

