基于學生為主體的“協進課堂”教學設計
徐新峰

摘要:以“課題3溶液的濃度(第1課時)”為例,呈現“協進課堂”的設計理念,即基于學生為主體,調動各類積極教學因素相互協作,通過學生的主動參與進行解惑,在師生互動、生生合作探究中完成知識體系的構建。
關鍵詞:學生主體;協進課堂;學習方式
文章編號:1008—0546(2016)07—0076-03
中圖分類號:G633.8
文獻標識碼:B
doi:lO.3969/j.issn.1008—0546.2016.07.027
一、背景
“協進”即協作共進,和諧成長。“協進課堂”是師生和諧成長的課堂教學模式,既突出了學生的主體地位,同時也強調了教師的主導角色,理順教學關系,讓各類教學因素協作起來,為學生的可持續發展和教師的專業成長提供保障的課堂。
筆者應南通市教科研中心之邀,參加了江蘇省海門市能仁中學教育集團“百花獎”教學活動,并執教了人教版初中化學下冊九單元“課題3溶液的濃度(第1課時)”的示范課,起到了很好的教學效果,同時也受到了南通化學教育同行的一致好評。本節課的設計著力體現了“協進課堂”理念,基于學生為主體,調動各類積極教學因素相互協作,通過學生的主動參與進行解惑,在師生互動、生生合作探究中完成知識體系的構建。在設計中,我運用下列策略突出了以學生為主體的教學理念,即:問題(設疑與激疑)、交流(理解與溝通)、協作(互助與競爭)、展示(表達與思考)、傾聽(尊重與信任)、構建(體驗與歸納)。
二、教學片斷及意圖
1.片斷一:探究有色溶液的顏色深淺與
有關
師:請同學們觀察老師手上的三支試管中的紅糖溶液顏色有何不同,并作出猜想,這與什么有關?(在試管架上事先放有三支試管,分別裝有顏色深淺的紅糖溶液)
生:紅色有深有淺,這與溶液的濃度有關。
師:看來“濃度”一詞,對大家并不陌生。請同學們查閱課本,看看溶液濃度的表達方式如何?(停頓,學生閱讀)
生:可用溶質的質量分數表示。(同理,這位同學到黑板上書寫溶質的質量分數計算公式,其他同學在筆記上書寫,整理出的公式如下。)
師:請各位同學先自主設計實驗方案,來證明你的猜想:有色溶液的顏色深淺與溶液的濃度有關,然后在小組內交流。(巡視,并參與多個合作小組的交流)
生1:取等質量的3種溶液,蒸干水分后,比較得到3份紅糖的質量大小。
生2:另取等質量的水,加入不同質量的紅糖,溶解后比較顏色的深淺。
生3:對試管3中的溶液繼續加入紅糖,觀察顏色的變化。(試管3是紅色最淺的溶液)
師:從實驗的簡單易做角度思考,同學們選擇哪種方案?請一位同學到前面來完成實驗。
生(齊聲):第3個。(一名同學在講臺上完成演示實驗)
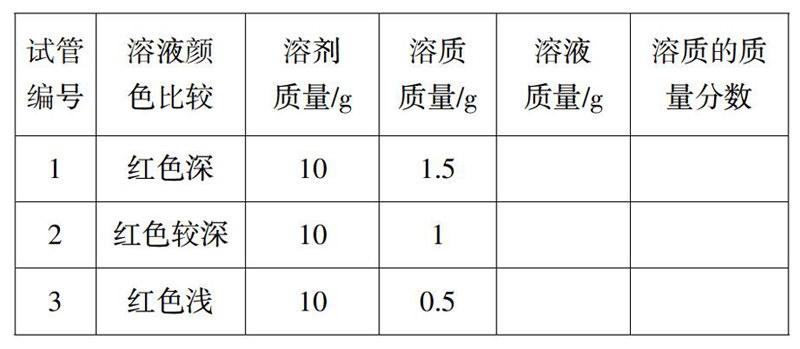
師:剛才上述3支試管中紅糖溶液的濃度是多少呢?請同學們查看老師配制這3種溶液時的數據,并計算其溶質的質量分數。
學生完成計算過程,老師選擇幾個代表性的作業進行投影,采用生生互評的方式組織教學,得出結論:對有色溶液來講,濃度越大,其顏色越深。
設計意圖:溶質的質量分數定義及計算公式是本節課的核心知識。學習形式設計成以學生為主體的探究式,而沒有采用“講授一練習鞏固”的傳統形式,且從生活中的紅糖溶液入手,沒有選擇教材中的硫酸銅溶液作為實驗資源,這樣的設計貼近學生的生活,激發學習興趣,很快將學生帶入探究情境。溶質的質量分數的定義與計算式采用學生自主學習的形式,閱讀文本而獲取(學生自己能看懂)。學生獲取計算式之后,沒有采用例題鞏固應用的“俗套”方式組織教學,而是將公式的解讀與實驗設計、方案比較、完成實驗進行多元融合,加深了學生對溶質質量分數定義和計算式的主動意義建構,這成為本節課的亮點之一。表格設計的計算并非“孤獨”,將對比和驗證的思想蘊含于其中并滲透給學生,為結論的得出提供了數據論證。
2.片斷二:深度認識溶質質量分數的表達式
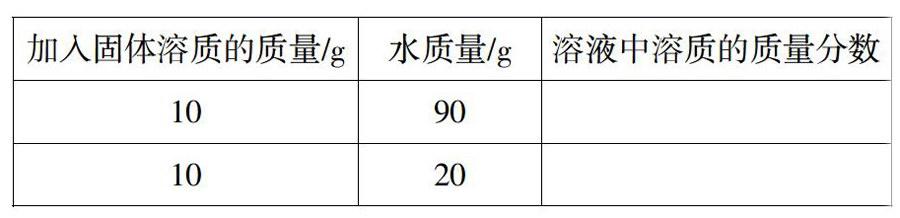
師:現在室內的水溫為10℃,已知10℃時,氯化鈉的溶解度為35.8g。在10℃時,根據下表規定的質量進行配制氯化鈉溶液,并計算溶液中溶質的質量分數(水的密度可看做lg/cm3)。
兩位學生主動上黑板板演計算過程。第1題的計算過程所有學生一致贊同,但有少數同學對第2位同學的解題列式(如下)提出了不同見解。
生:根據10℃時,氯化鈉的溶解度為35.8g,可推知,此溫度下,20g水中最多只溶解7.16g氯化鈉,所以溶液中溶質的質量不是lOg。
生:我們可以通過做實驗來檢驗。
師:同桌的兩位同學為一組,動手完成上述表格中兩種溶液的配制,并匯報實驗結果。
學生開始實驗,教師巡視,并及時糾正學生實驗中的不規范操作。
生:第1個實驗中lOg氯化鈉全部溶解,第2個實驗中lOg氯化鈉固體沒有全部溶解,得到了飽和溶液。
生:第2個實驗中所得溶液中溶質的質量應為7.16g,所以第2問的解題過程如下:
師:你對公式中“溶質的質量”如何理解?
生:必須是溶解的溶質質量。
教師板書,并用紅筆標注,“溶質的質量必須溶解的質量”。
師:第2個實驗所得溶液是飽和溶液,老師對剛才這位同學的解題過程作如下變通(在黑板上板演):
師:從上述變通中,你是否可以總結出飽和溶液中溶質質量分數的計算公式?
師:已知20℃時,氯化鈉的溶解度是36g。有人說:“20℃時氯化鈉飽和溶液中溶質的質量分數為36%”。這種說法對嗎?為什么?
學生分析回答,各合作小組進行組內質疑,組內解決。
設計意圖:這一片斷的教學培養了學生的主動發現能力。學生在學習了溶質質量分數的計算公式后,很容易在第2小題走進教者設計的“陷阱”中。“錯誤是寶貴的教學資源”,引導學生相互糾錯,協作共進,進而提出自己的見解:一是從計算推理角度來闡述,根據溶解度定義來推知l0g氯化鈉不能全溶解:二是從實驗的角度來證明并創設每位學生動手的機會,在實驗動手后真實的感悟出“溶質質量必須是溶解的質量”,這樣的設計充分肯定學生是學習主人的前提下展開的,也體現了學科特質和研究問題的真實性,這成了本節課的亮點之二。而飽和溶液的溶質質量分數的推出,是基于例題情境展開的老師引導、學生歸納而總結出來的,體現了讓知識的形成與學生的主體參與相結合的教學思想。
3.片斷三:根據情境和數據進行編題
師:在農業生產上,常用溶質質量分數為16%的氯化鈉溶液進行選種。提供如下數據:①NaCl質量24kg;②水質量126kg;③溶液質量150kg。請同學們自主編題,將上述任一數據設置為未知(即題目的問),通過編制題目來問答。
學生編題,教師巡視,挑選不重復的問題進f=亍展示。
生1的問題:在農業生產上,常用溶質質量分數為16%的氯化鈉溶液進行選種。若用24kg的氯化鈉來配制溶液,需水的質量多少?
生2的問題:用24kg的氯化鈉和126kg的水配制溶液進行農業的選種,求此溶液中的溶質質量分數是多少?
生3的問題:在農業生產上,常用溶質質量分數為16%的氯化鈉溶液進行選種。已配制了150kg的此溶液,問需氯化鈉和水的質量分別是多少?
生4的問題:在農業生產上,用126kg的水配制成了溶質質量分數為16%的氯化鈉溶液去選種,問需氯化鈉質量是多少?
全體學生圍繞這4個問題,分別列式求解,并歸納出相應的變式公式:
設計意圖:這一環節教學將課本中的例題改成學生自編自求題,突破了文本的束縛,改變了傳統的教師拋問題學生思考問答的形式。學生成為問題設計的主人,學習和思考的主體意識增強,萌生了自主展示意識,必然會自主思考此題的求解路徑、公式變通,至此,變式公式自然生成。同時,這一改變調動了不同層次學生的積極思考,學業成績優秀的學生想設計出多種不同類型的習題給其他同學來做,同時證明自己是優秀的。有些基礎較差的學生也能設計出1至2個問題,盡管有些“羞澀”,但也期待著其他同學來求解自己設計的題目,這正是我們所期待的生生之間的“協作共進”,這成了本節課的亮點之三。教學表明,全體學生在這一環節中充分體現了自己是學習的主人,展示與和諧成長成了這一教學片斷的主題。
三、教學反思
1.變通文本資源,與學生走得更近
教學是一種藝術,“教”的服務對象是“學”,“學”是主體。教師在選擇教學資源時,不應墨守成規、束縛于課本資源,“變通”會激活“學的主體”。在本節課中放棄了課本中的硫酸銅溶液,去選擇學生熟悉的生活情景“紅糖水”作為教學資源,拉近了與全體學生的距離,對知識的親切感和探究欲望自然而生。“教材是個例子”,但并非每個例子都是很好的教學資源,評價標準是學生,只有讓學生“走近”教學情景,才能“走進”學科本質,掌握學科內涵。
2.創設多樣化學習方式,讓各層次學生樂于“協進學習”
教學方式的單一,必然會帶來學習方式的單一,勢必引起學生對學習化學的厭倦。新課程標準倡導“多樣化的學習方式”,鼓勵教師從具體的教學目標、教學內容和學生的實際情況出發,靈活創設多樣化學習方式,激發各層次學生學習的興趣,并在互相協作中完成化學的快樂學習,這應是我們化學教師所向往的,追求的教學場景。本節課中創設了自主學習、合作學習、探究學習、發現歸納學習等,生與生之間的實驗方案互補協作、實驗動手協作、相互糾錯協作等合作形式,這些形式最大程度上促進了各層次學生的和諧發展。
3.調動教學多因素“協作”,引領學生主動建構知識
教材內容、教師、學生、教學方式、課堂文化等多因素之間互動的合力所決定了教學效果,學生是關鍵因素,因為評價的最終落腳點是學生的進步與發展。
本節課中,將計算公式的理解寓于一定的生活情景中,引領學生主動建構了溶質質量分數的公式:在實驗情景中,主動理解了公式中“溶質質量”的真正含義,并自主歸納了飽和溶液中溶質質量分數的計算公式:通過自編問題的情境,激發了各層次學生的主動思考,培養了全體學生的問題設計能力。在整個教學過程中,教師起組織者、指導者、幫助者和促進者的作用;利用情境、合作、對話等學習環境要素充分發揮學生的主動性、積極性,最終達到學生有效地實現對當前所學知識的意義建構的目的。

