LiFePO4/C/GO的制備及其電化學性能研究
楊虎侯振清馬育新(昌吉學院物理系 昌吉 831100新疆有色金屬研究所烏魯木齊830000)
?
LiFePO4/C/GO的制備及其電化學性能研究
楊虎①侯振清①馬育新②
(①昌吉學院物理系昌吉831100②新疆有色金屬研究所烏魯木齊830000)
摘要通過靜電紡絲法制備LiFePO4/C/GO正極復合材料。通過X射線衍射圖譜(XRD)、掃描電鏡(SEM)對合成材料進行結構及形貌分析,并采用循環伏安(CV)、恒流充放電等表征手段對合成材料進行電化學性能測試。結果表明:氧化石墨烯的引入沒有改變磷酸鐵鋰橄欖石晶體結構,在形貌上優于普通,表現出更優越的電化學性能,電荷轉移電阻顯著降低,在0.1C倍率時的放電容量為118.4 mAh/g。
關鍵詞靜電紡絲磷酸鐵鋰氧化石墨烯
DOI∶10.16206/j.cnki.65-1136/tg.2016.02.030
1 引言
LiFePO4由于具有較高的理論容量(170 mAh/g)、較高的工作電壓(3.5 V vs.Li/Li+)、良好的循環穩定性、低成本和環境友好等優點而備受關注[1-6]。但是由于LiFePO4的電導率[7]和鋰離子擴散速率較低[8],從而限制了LiFePO4的應用。目前,研究者通常采用包覆導電碳或者摻雜金屬離子來提高LiFePO4的電子導電率。
氧化石墨烯作為一種二維碳材料,由于高比表面積、優良的化學穩定性、良好的力學強度和柔韌性,使得石墨烯復合材料具有較高的導電性[9]。本文將通過溶膠-凝膠法與靜電紡絲技術制備LiFePO4/ GO/C復合納米纖維,再經過預氧化和煅燒工藝獲得納米纖維,并對其進行物理表征和電化學性能測試,探究石墨烯的加入對LiFePO4/C正極材料相貌和電化學性能的影響。
2 實驗
2.1試劑與儀器
乙酸鋰(C2H3LiO2?2H2O,純度≥98.5%,天津市光復精細化工研究所),磷酸(H3PO4,純度≥85%,天津百世化工有限公司),硝酸鐵(Fe(NO3)3?9H2O,純度≥98.5%,天津永晟精細化工有限公司),聚丙烯腈(PAN,Mw=150 000 g/mol,Spectrum公司),N,N-二甲基甲酰胺(DMF,純度≥99.5%,天津市光復科技有限公司),氧化石墨烯(GO,蘇州恒球科技)N-甲基吡絡烷酮(NMP,純度≥99.0%,天津光復精細化工研究所),聚偏二氟乙烯(上海試劑三廠),電解液(張家港市國泰華榮化工)。
GSL-1100X真空管式高溫爐(合肥科晶材料技術有限公司),D8X射線粉末衍射儀(XRD,德國Bruk?er公司),CHI660D電化學工作站(上海辰華儀器公司),掃描電子顯微鏡(SEM,日本Hitachi公司),藍點電池測試系統(武漢市藍電電子有限公司),電化學阻抗測試系統(德國Zahner公司)。
2.2材料的制備及電池組裝
(1)材料的制備
稱取0.01 g氧化石墨烯溶于DMF中超聲4 h,再將PAN加入上述溶液中,并持續攪拌直至PAN完全溶解且形成均勻溶液。PAN使用前先在真空干燥箱40℃保溫24 h。按化學計量比稱取乙酸鋰、磷酸和硝酸鐵加入到上述溶液中,攪拌形成透明且具有一定粘度的電紡原液A。為了作對比,B樣品不加氧化石墨烯。將配好的電紡原液裝入21號針頭注射器,使用鋁箔做接收負極,接收距離為15 cm,注射器流速為0.15 mL/h,電壓15 kV。將制備好的前驅體先在馬弗爐中預氧化,升溫速率1℃/min,280℃恒溫4 h,待冷卻至室溫取出,放入氮氫氣氛下的管式爐中進行煅燒,升溫速率2℃/min,700℃燒結12 h。
(2)電極片的制備
稱取活性物質85%、乙炔黑10%和粘結劑PVDF 5%至研缽進行研磨,研磨0.5 h后再加入一定量的NMP制成漿料。將制備好的漿料涂覆在處理過的鋁箔集電極上,放在真空干燥箱中110℃恒溫12 h,冷卻至室溫。
(3)電池的組裝
采用CR2032型號的電池殼,制備材料為正極,金屬鋰為對電極,隔膜為Celgard2004聚丙烯微孔膜,電解液為1 mol/L LiPF6/EC+DEC+DMC(1∶1∶1,V/V/ V)。在充滿氬氣氣氛手套箱中組裝,組裝后在手套箱放置12 h后取出。
2.3表征和測試手段
采用X射線衍射儀對樣品進行物相分析,Cu靶為輻射源,掃描范圍10°~80°;用S-4800場發射掃描電子顯微鏡對樣品進行形貌分析;用藍電測試儀進行恒流充放電測試,充放電電壓范圍2.5~4.2 V;電化學工作站對其進行循環伏安測試,掃描電壓范圍2.5~4.2 V,掃描速率為0.1 mV/s。
3 結果與討論
3.1XRD分析
圖1為樣品LiFePO4/C和LiFePO4/C/GO的XRD圖譜。將樣品的XRD圖譜與LiFePO4的標準卡片進行比較,可以看出兩者均沒有雜相出現,峰形完全一致,說明氧化石墨烯的引入沒有改變LiFePO4/C的物相。另外,LiFePO4/C/GO沒有觀察到碳的衍射峰,可能是因為碳含量較低或者殘余的碳為無定形結構,因而衍射不明顯。

圖1 樣品LiFePO4/C和LiFePO4/C/GO的XRD圖
3.2形貌分析
圖2為樣品LiFePO4/C(a)和LiFePO4/C/GO(b)的SEM圖。從圖2中可以看出,LiFePO4/C纖維直接介于71~100 nm之間,形狀較不規則并且出現輕微的團聚現象。而LiFePO4/C/GO纖維的直徑介于63~85 nm之間,形貌較規則,而且沒有出現團聚。

圖2 LiFePO4/C和LiFePO4/C/GO的SEM圖
3.3材料的電化學性能分析

圖3 LiFePO4/C和LiFePO4/C/GO的循環伏安曲線對比圖
3.3.1循環伏安性能對比圖3是正極材料LiFePO4/C和LiFePO4/C/GO在掃速為0.1 mV/s-1的循環伏安圖,測試窗口為[2.5 V,4.2 V]。與正極材料LiFePO4/C比較發現,LiFePO4/C/GO
在循環伏安曲線中氧化還原峰更加尖銳,表明LiFe?PO4/C/GO的電化學極化程度更低,電荷轉移效率較高。另外,LiFePO4/C的氧化峰電位為3.54 V,還原峰電位為3.31 V,氧化還原電位差為0.23 V;LiFePO4/C/ GO的氧化峰電位為3.54 V,還原峰電位為3.31 V,氧化還原電位差為0.17 V,比LiFePO4/C更小。表明氧化石墨烯在充放電循環過程中能提高的電化學反應可逆性和減小極化作用。
3.3.2首次充放電性能對比

圖4 樣品在0.1C倍率下的首次充放電曲線
圖4是樣品LiFePO4/C和LiFePO4/C/GO在0.1C倍率下的首次充放電容量曲線。從圖4中可以看出,在此倍率下,LiFePO4/C的首次放電容量為94.8 mAh/g,而同種方法制得的LiFePO4/C/GO首次放電容量達到118.4 mAh/g;LiFePO4/C/GO復合材料的充放電平臺比較平穩,且充放電電壓平臺的差值(極化電位)低于LiFePO4/C的充放電電壓平臺之差,結合掃描電鏡和循環伏安測試結果說明石墨烯特殊結構提供了導電網絡結構,改善了LiFePO4/C的電子電導率,降低了材料的極化程度,具有較高的放電容量。
3.3.3交流阻抗性能對比
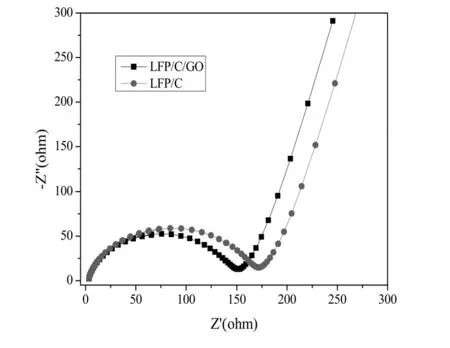
圖5 LFP/C和LFP/C/GO的交流阻抗圖
圖5為LiFePO4/C和LiFePO4/C/GO在頻率范圍為0.01~100 kHz的交流阻抗圖。從圖5中可以看出,曲線由一段半圓(高頻區)和一條直線(低頻區)組成,前者與電荷在電解液和電極表面的轉移(Rct)有關,后者與鋰離子在電池內部的擴散(Warburg阻抗)有關。LiFePO4/C/GO半圓的直徑小于LiFePO4/C的,表明LiFePO4/C/GO的電荷轉移(Rct)小于LiFePO4/C的,這是因為石墨烯自身較大的比表面積和優越的導電性能,對顆粒進行了有效的包覆,提高了材料的電荷轉移能力,從而很好地改善了LiFePO4/C的導電性。
4 結論
采用靜電紡絲法制備LiFePO4/C和LiFePO4/C/GO復合材料。結果發現,氧化石墨烯的引入沒有改變LiFePO4的橄欖石結構,纖維直徑相對較小。在0.1C下首次放電容量達到118.4 mAh/g,比LiFePO4/C的容量有很大的提升,而且的電荷轉移電阻小,有利于提高的導電能力和鋰離子的擴散速率。
參考文獻
[1]Goodenough,J. B.;Kim,Y.,Challenges for Rechargeable Li Batteries. Chemistry of Materials 2010,22(3),587-603.
[2]Aravindan,V.;Gnanaraj,J.;Lee,Y.-S.;Madhavi,S.,LiMn?PO4-A next generation cathode material for lithium-ion batter?ies. Journal of Materials Chemistry A 2013,1(11),3518.
[3]Park,M.;Zhang,.C.;Chung,M. D.;Less,G. B.;Sastry,A. M.,A review of conduction phenomena in Li-ion batteries. Journal of Power Sources 2010,195(24),7904-7929.
[4]Thackeray,M. M.;Wolverton,C.;Isaacs,E. D.,Electrical energy storage for transportation approaching the limits of,and go?ing beyond,lithium-ion batteries. Energy & Environmental Sci?ence 2012,5(7),7854-7863.
[5]Ellis,B. L.;Lee,K. T.;Nazar,L. F.,Positive Electrode Materials for Li-Ion and Li-Batteries?. Chemistry of Materials 2010,22(3),691-714.
[6]Bruce,P. G.;Scrosati,B.;Tarascon,J. M.,Nanomaterials for rechargeable lithium batteries. Angewandte Chemie 2008,47 (16),30-46.
[7]Xu,Y.-N.;Chung,S.-Y.;Bloking,J. T.;Chiang,Y.-M.;Ching,W. Y.,Electronic Structure and Electrical Conductivity of Undoped LiFePO4. Electrochemical and Solid-State Letters 2004,7(6),A131.
[8]Prosini,PP;Lisi,M;Zane,D;Determination of the chemi?cal diffusion coefficient of lithium in LiFePO4.2002,148(2),45-51.
[9]Stankovich,S.;Dikin,D. A.;Dommett,G. H.;Kohlhaas,K. M.;Zimney,E. J.;Stach,E. A.;Piner,R. D.;Nguyen,S. T.;Ruoff,R. S.,Graphene-based composite materials. Nature 2006,442(7100),282-6.
收稿:2016-03-11

