骨折早期調節RANKL表達對骨折愈合影響的實驗研究
沈業彤 張學斌 吳麗紅 劉果彤 王琳 陶敏燕 徐鳳琳
齊齊哈爾醫學院附屬第一醫院骨外科,齊齊哈爾 161041
OPG/RANKL/RANK系統自1997年被發現以來,被認為是骨科研究領域中的一項重大突破,許多細胞因子、激素等影響因素均可通過骨保護素(OPG)的競爭機制來調節核因子-κB受體活化因子配體(RANKL) 的表達, 從而調控OPG、RANKL和核因子-κB受體活化因子(RANK) 之間的比值,直接對破骨細胞的分化和功能產生決定性作用,OPG由成骨細胞及骨髓基質細胞分泌,可與RANKL結合,競爭性抑制其表達, 來調節破骨細胞的活性及凋亡過程,體內有很多激素及調控因子均可通過影響OPG/RANKL 的比值來調節其表達,并影響骨代謝。骨折早期的骨吸收階段,破骨細胞起著重要的作用,OPG在軟骨內成骨過程中也有著重要的影響,既往研究表明,BMP、雌激素、IL-1、 1, 25-( OH)2D3、TGF和TNF等都能通過調節OPG mRNA的表達[1-5],通過競爭性抑制來調節RANKL的表達,使破骨細胞的活性降低,減少骨吸收,減輕固定后廢用性骨質疏松,對縮短骨折的愈合時間,防治骨缺損、骨壞死、骨折不愈合及再骨折均具有重要的臨床意義。本項目通過對鼠的骨折模型進行實驗治療,以探討應用基因技術治療骨折模式的可行性及有效性,同時為進一步研究該系統對骨生成及代謝方向的影響機制奠定實驗基礎。
1 材料和方法
1.1 實驗動物和試劑
重組人骨保護素Fc 融合蛋白(Recombinant Human OPG-Fc)劑型(50 μg/支)、二甲苯溶液、蜂蠟、酒精溶液、蘇木精染液、石蠟溶液、1%鹽酸乙醇、1%伊紅酒精溶液、樹膠等。 TRAP 免疫組化染色試劑盒。健康雌性3個月齡SD大鼠48只,體重270 g~320 g,由齊齊哈爾醫學院動物實驗研究室提供。
1.2 動物分組和模型
48只大鼠隨機分為骨折+OPG組和單純骨折對照組,每組各24只并標記組別。備皮后以10%水合氯醛行腹腔注射麻醉。取右大腿外側切口,鈍性分離至股骨干,經股骨中段(大轉子下1.5 cm處)以直徑1.0 mm牙科鉆鉆過,縱向形成規整的3 mm×1 mm不完全骨折及骨缺損槽,保持骨缺損兩側骨折完好,并有足夠強度不形成完全骨折,縫合后單純骨折組局部注射1 ml生理鹽水,OPG組將重組人骨保護素 Fc 融合蛋白50 μg溶入10 ml注射用水中,即濃度為5 μg/ml,亦以1 ml局部注射[6],術前及術后兩組大鼠均肌注慶大霉素一次預防感染,淘汰失敗模型,并補充,保持數目不變。
1.3 標本采集和處理
兩組動物于術后第7、14、21、28d 4個時間節段分批處死,每組每個節段各6只,在無菌操作下將骨折處骨痂組織截取, 用4%的多聚甲醛在4℃下固定24 h,用20%的乙二胺四乙酸以脫鈣,脫水,透明,包埋。將標本均沿縱軸中線切片,連續3張,厚度5 μm,將一張行HE染色,而另兩張行免疫組化染色。
1.4 觀察指標
1.4.1HE染色:制好的切片經脫蠟、水化、蘇木素染核、鹽酸及酒精分化、伊紅染漿、再脫水透明,最后以中性樹膠封片,在光鏡下觀察其骨痂生長情況及其組織形態。
1.4.2免疫組化染色:將切片脫蠟復水, 首先孵育液 A 液:0.2 mol/L 醋酸緩沖液8 ml;再孵育液 B 液:取六偶氮副品紅 1 ml;再孵育液C液:在1 ml N,N-二甲基甲酰胺中溶解20 mg萘酚AS-BI 磷酸酯。然后將 A、B 液按比例混和,并將pH值調到5.0,加入C液,最后將141 mg酒石酸鉀鈉加入。破骨細胞固定后,切片浸入孵育液內,封片。鏡下觀察破骨細胞數量。
1.5 數據收集與處理
將染色后的切片在光學顯微鏡 400 倍鏡頭下觀察,并計數TRAP 陽性染色的破骨細胞。在顯微鏡下,染色陽性的破骨細胞胞漿呈酒紅色,將這兩張切片中的破骨細胞數量分別計數。選擇染色明、分布均的部位進行破骨細胞計數,計數10 個高倍視野下的破骨細胞細胞總數為值,即該張切片的破骨細胞數。樣本的數值為兩張切片的破骨細胞總數的平均數。然后采用SPSS11. 0軟件分析, 對各時間點兩組數值行t檢驗,最后比較,如P<0. 05為有統計學意義。
2 結果
2.1 骨痂組織形態觀察
HE染色切片低倍鏡下觀察發現每時間點骨折+OPG組,骨痂直徑平均值均大于單純骨折組,骨痂生成速度快及生成量增多。具體情形如下:7d時,骨折+OPG組骨折處可見大量的軟骨細胞在形成的纖維肉芽組織中,并有明顯的成骨出現,軟骨基質形成,軟骨明顯膜內化骨及軟骨內化骨現象,骨折間隙的纖維肉芽組織中有大片軟骨細胞骨膜增生變厚,其下出現新生骨組織,有大量成骨細胞聚集;單純骨折組骨痂中纖維組織成分多,出現散在少量軟骨細胞及成骨細胞,骨膜有增厚,但新生骨組織明顯較少。第14天時,骨折+OPG組纖維性骨痂減少,軟骨性骨痂增多并向編織骨轉化;單純骨折組軟骨性骨痂少。21天時,骨折+OPG組骨折間隙編織骨逐漸聚集,呈連續性骨痂,骨小梁逐漸形成并增多;單純骨折組骨折有大量軟骨細胞,骨小梁形成少。28天時,骨折+OPG組骨折處進一步融合、連接,出現板層骨,骨量增多;單純骨折組仍有軟骨組織,骨組織成熟慢、量較少,見圖1、圖2。
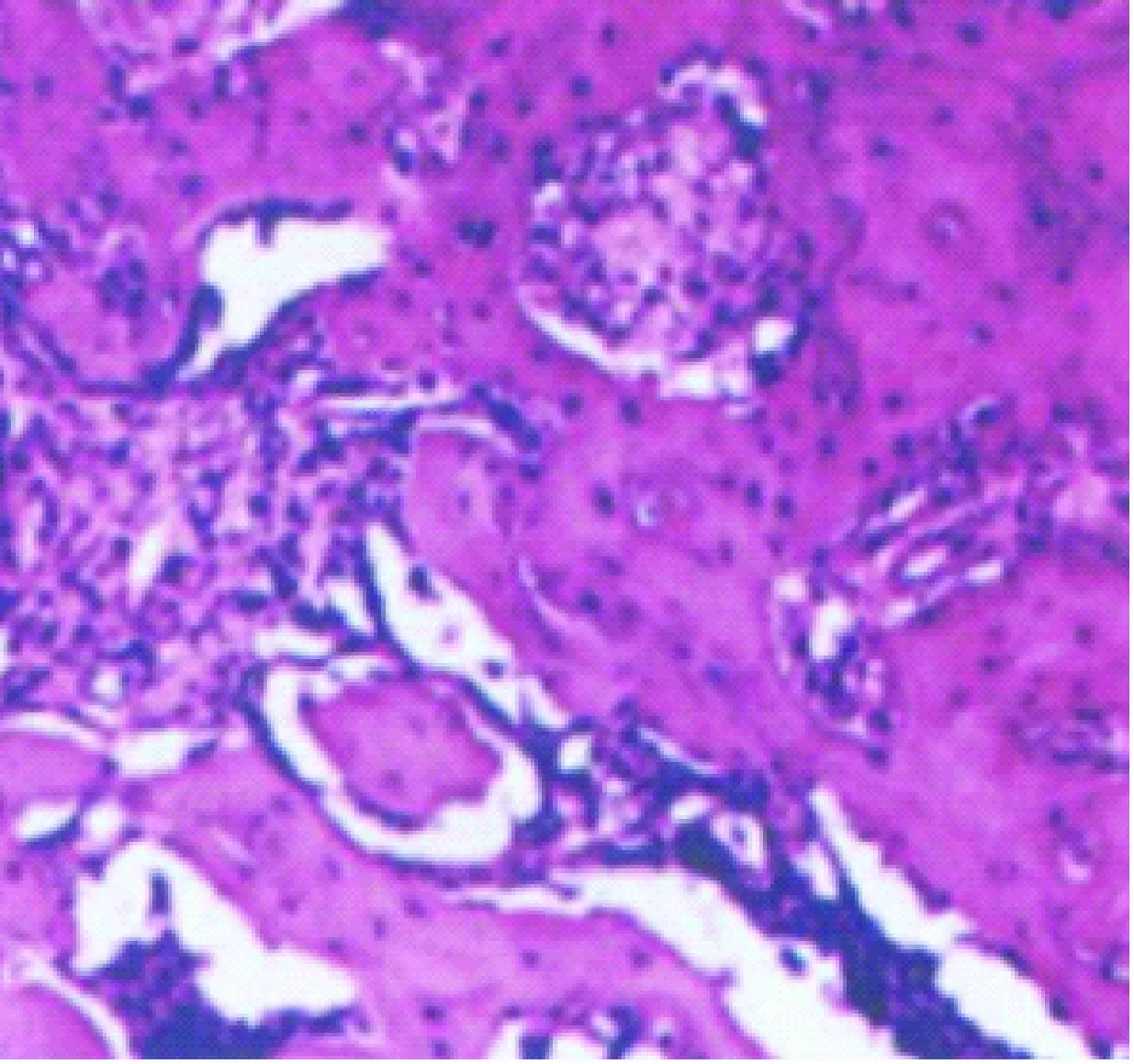
圖1 單純骨折組28天時低倍鏡下見軟骨組織多,骨組織少Fig.1 The simple fracture group was lower than that in the 28 days of the fracture group, and there were more cartilage tissues and less bone tissue

圖2 骨折+OPG組28天時低倍鏡下見骨量多,多為板層骨,骨成熟度高Fig.2 The fracture +OPG group was lower than that in 28 days, and the number of bone was much more than that of lamellar bone, and the height of bone was high
2.2 光學顯微鏡下對破骨細胞觀察并計數
將骨折+OPG組、生理鹽水組所計數的破骨細胞個數取平均值,得出7d、14d、21d、28d的兩組中每個樣本的破骨細胞個數的平均數,OPG 組分別為3.153±0.057,2.964±0.162,1.831±0.068,5.462±0.073, 對照組分別為5.536±0.035,8.859±0.041,5.464±0.027,7.427±0.052再對兩組破骨細胞數進行統計學分析。見圖3。

圖3 OPG組與對照組在不同時間節段破骨細胞數量對比圖Fig.3 OPG group and control group at different time of the number of broken bone cells
3 討論
在實驗研究及臨床治療中觀察發現,骨折早期即有破骨細胞參與骨吸收及骨生成的動態平衡,并為其重要調節因素之一。RANKL為破骨細胞生長及分化所必需的細胞因子[7],它通過與RNAK結合使破骨細胞活性增強,達到骨吸收加強的效果,OPG是RANKL的誘騙受體,通過競爭性抑制作用,可以減少RANKL與RNAK結合,從而抑制破骨細胞分化、成熟,并且成熟破骨細胞活性也受到抑制[8-9]。OPG還可以激發成骨活性,通過促進成骨細胞樣細胞分化成熟為成骨細胞來完成,進而促進新骨組織形成[10]。AyaShiotani等[11]也通過研究證實了OPG/RANKL/RANK系統對破骨細胞的分化和重吸收的作用。體內諸多激素、細胞因子也是通過RANKL/RANK/OPG環路來實現調控破骨細胞的活化和功能的[12]。破骨細胞表面的RANK是RANKL的唯一受體,成骨細胞分泌OPG,競爭性地抑制了RANKL與RANK結合,從而抑制了破骨細胞的生物活性及其成熟[13]。骨形態發生蛋白BMPs、PGE2、甲狀旁腺激素PTH、轉化生長因子TGFβ、雌激素、糖皮質激素等對破骨細胞的抑制作用均是通過調節該通路,改變成骨細胞系的OPG和RANKL的表達而完成的。本實驗應用OPG-Fc可排除其他因素,達到直接下調RANKL表達的目的,與應用腺病毒改變基因表達效果相同,使OPG/RANKL比值增大,為基因治療奠定實驗基礎,以往實驗顯示該蛋白藥效為局部作用,半衰期約 6-7 天,藥物性能持續約30天,可完全滿足本實驗要求,也是28天后OPG組破骨細胞數量開始回升的原因之一。
Kon等[14]發現OPG表達高峰在骨折后24小時內和骨折后第7天;而RANKL表達高峰在骨折后第3天和第14天。在我們實驗研究中,術后即應用OPG-Fc,觀察到第7天、第14天、第21天時間點明顯下調了RANKL的表達,破骨細胞數量遞減,28天時破骨細胞數量回升,考慮為隨著藥物代謝,性能下降導致,也可能與骨折后期骨改造增強,破骨細胞活性增強有關,對照組破骨細胞數量也回升,也說明了這個問題。對照組顯示破骨細胞活性最活躍是在第14天和第28天以后,與RANKL表達高峰相符,對比其臨床意義,考慮第一個高峰可促進骨折斷端及壞死骨的吸收,第二個高峰有利于骨痂的塑形改造,結合低倍鏡下觀察骨痂愈合情況,充分說明骨折早期下調RANKL表達,能明顯抑制破骨細胞活性,抑制早期骨折端骨質的吸收,打破骨生成與骨吸收的動態平衡,使骨痂明顯增多,并可促進骨成熟加速,減少骨吸收,提高骨密度,28天后隨著藥效的減低,對骨折后期骨痂的塑形改造并不會產生嚴重影響,本實驗通過研究骨折愈合不同階段骨痂OPG/RANKL的表達變化,提示OPG/RANKL比值決定骨代謝方向和骨折愈合進程。骨組織中OPG/RANKL的相對比值升高則骨形成作用大于骨吸收作用,骨折愈合加速;反之則骨折愈合減慢,但本實驗并未對成骨細胞表達進行觀察比較,有待于進一步研究探討。
過度抑制RANKL的表達,將使破骨細胞的活性極度下降,嚴重影響骨吸收及改造,當敲除小鼠OPG基因后會患嚴重的骨質疏松癥;而小鼠OPG基因過度表達時,將出現嚴重的石骨癥。所以,在骨折早期適度下調RANKL表達對骨折愈合具有積極的促進作用,但過度抑制其表達將會過猶不及。

