葛根素對成骨細胞中miRNA-204的調控及其與Runx2基因表達的關系
張瑩瑩 周建斌 趙鳳鳴 詹秀琴
南京中醫藥大學基礎醫學院生物教研室,江蘇 南京 210023
骨質疏松癥(osteoporosis,OP)是一種因骨量低下、骨微結構破壞,導致骨脆性增加、易發生骨折為特征的全身性骨病(世界衛生組織,WHO)[1],是由于成骨細胞(OB)形成的新骨量少于被破骨細胞(OC)吸收的舊骨量,骨代謝從而發生負平衡,導致骨總量丟失所致。Runx2是骨發育過程中激活與啟動骨髓基質干細胞(BMSCs)向OB分化并調節OB成熟的重要轉錄因子,上調多種成骨相關基因的表達,對膜內和軟骨內骨化成骨均有控制作用,因此,其表達、活性下降與OP發病密切相關。miRNA是一類機體內源性表達的、長度在18到25個核苷酸的非編碼小分子RNA,這些僅占人類基因1%的miRNA分子,卻可控制人類三分之一以上基因的表達、修飾、轉錄和翻譯過程。它能夠在轉錄后調節基因表達,從而影響多種生物學過程,包括細胞的增殖[2]、分化[3]、凋亡[4]、發育[5]。miRNA的發現可能成為極有應用價值的分子標志物,為骨質疏松癥的治療提供新的靶標。我們以前的研究發現,葛根素可促進成骨細胞增殖和分化,但其機制是否與細胞內的Runx2和miRNA分子有關,且二者之間是否有關聯,是本文要研究的問題。
1 材料和方法
1.1 實驗材料
1.1.1細胞:MC3T3-E1細胞購自中國科學研究院上海細胞庫。
1.1.2藥物:葛根素標準品:購自中國藥品生物制品檢定所,20 mg/支,純度為96.0%,性狀:白色粉末,干燥密封保存。
1.1.3試劑:α-MEM培養基(維森特生物技術有限公司,貨號:310010008);含EDTA的25%胰蛋白酶(GIBCO,USA);胎牛血清(GIBCO,USA);miRNA逆轉試劑盒(Takara 036A);Trizol(Invitrogen,USA);Realtime PCR SYBR premix 2×(Takara RR420A,Japan);目的基因一抗(rabbit Runx2)(Cell Signaling Technology);內參一抗(rabbit β-actin)(Cell Signaling Technology);二抗(Anti-Rabbit IgG HRP)(Cell Signaling Technology);Trizol(RNAiso for Small RNA)(Takara);miRNA反轉錄試劑盒(VaZyMe 公司);LipofectamineTM2000(Invitrogen,USA);miRNA所有相關引物由上海生物工程有限公司合成;野生型Runx2 3’UTR/突變型Runx2 3’UTR重組質粒、miRNA-204 mimics 及陰性對照由上海吉馬公司合成;miRNA-204擴增采用莖環引物;Runx2和β-actinPCR擴增引物由南京金斯瑞公司合成。
1.1.4主要儀器:二氧化碳細胞培養箱(SANYO,Japan);相差倒置顯微鏡(Olympus,Japan);光鏡(Motic);低溫高速冷凍離心機(Eppendorf, USA);熒光實時定量PCR儀(Agilent Technologies Mx3000P);紫外分光光度計(BioDrop,USA);凝膠成像儀(Bio-Rad,USA型號:GelDoc2000);酶標儀(BioTek,USA);常溫mini 離心機(Eppendorf, USA);6孔、24孔、96孔細胞培養板(Corning,USA)。
1.2 實驗方法
1.2.1熒光實時定量PCR檢測Runx2轉錄水平:按1×105密度在六孔板里接種MC3T3-E1細胞,用含胎牛血清的α-MEM培養液進行培養,設置葛根素處理組和空白對照組, 在葛根素組細胞中加入終濃度為0.01 mg/mL的葛根素,將兩組細胞置于37℃、5% CO2培養箱培養72 h。使用Trizol法對細胞進行總RNA的提取,用核酸蛋白分析儀測其濃度和純度。使用mRNA逆轉試劑盒(Takara 036A)逆轉錄,反應體系參考說明書。熒光實時定量PCR反應體系為:cDNA樣品2 μL, Realtime PCR SYBR premix 2× 12.5 μL,上、下游引物(10 μmol/L)各0.5 μL,Runx2 Forward:CGGACGAGGCAAGAGTTT CA,Reverse:GGATGAGGAATGCGCCCTAA,擴增片段長度為192bp;β-actin Forward:GTGCTATGTTGC TCTAGACTTCG,Reverse:ATGCCACAGGATTCCATA CC,擴增片段長度為174bp。 加蒸餾水補充至 25 μL。每組設置三個復孔。PCR的反應采用二步法:95℃、30 s預變性,(95℃,5 s; 60℃ 34 s,)×40個循環,做熔解曲線分析。
1.2.2Western blot檢測蛋白表達水平:按全蛋白抽提試劑盒說明書提取處理72h后的各組細胞總蛋白,并用BCA法進行蛋白定量,-20℃凍存。取各組樣本25 μg進行SDS-PAGE聚丙烯胺凝膠電泳,將分離后的蛋白質電轉移到PDVF膜上,放入少量封閉液,室溫下,搖床上封閉1 h。TBST漂洗濾膜3次,每次5 min。按約0.1 mL/cm2的量加入一抗抗體和封閉液(1∶1000),4℃過夜后,TBST漂洗濾膜3次,每次5 min。將膜與HRP結合的二抗(二抗用封閉液稀釋1∶3000),室溫下搖蕩孵育1 h,TBST漂洗濾膜3次,每次5 min。配制顯色液: 按0.1 mL/cm2顯影液計算用量,在正面加混勻的顯色液,放入凝膠成像儀中顯影,調整曝光時間,直至出現最佳條帶。
1.2.3microRNA表達譜檢測:利用microRNA表達譜檢測葛根素作用于成骨細胞72h后發生變化的可能靶向Runx2的miRNA(實驗過程由康成生物公司完成)。
1.2.4軟件預測靶向Runx2的miRNA:采用miRNA靶基因預測軟件TargetScan、PicTar、miRBase和miRDB進行預測,找出可能靶向Runx2的miRNA。同時,將軟件預測的miRNA與表達譜測定結果進行比對,確定靶向Runx2的miRNA。
1.2.5PCR驗證葛根素作用后靶向Runx2的miRNA變化:細胞培養方法及葛根素作用時間同前、miRNA用Trizol(RNAiso for Small RNA)提取,方法同普通RNA提取。逆轉錄反應體系: 5×Reverse Transcription Mix 10.0 μL、Stem-loop 反轉錄引物1.0 μL、miRNA 500 ng、hiscript Enzyme Mix 2.0 μL、加 RNA free H2O至總體積 20 μL。反應條件為:25℃,5 min;45℃,50 min;85℃,5 min;4℃,反應結束后,將其放入-20℃保存。
引物序列:miRNA-204 RT Primer:
GTCGTATCCAGTGCAGGGTCCGAGGTATTCGCACTGGATACGACAGGCAT,Reverse:ATCCAGTGCAGGGTCCGAGG;U6 RT Primer:AACGCTTCACGAATTTGCGT,Forward:CTCGCTTCGGCAGCACA,Reverse:AACGCTTCACGAATTTGCGT。
Real-time PCR 檢測反應體系條件方法同前。
1.2.6構建重組質粒:先合成不含有Runx2基因的空載體(載體序列結構見圖),將空載體(圖1)進行單酶切,酶切位點是Xbal,酶切后分別插入野生型Runx2 3‘UTR和突變型Runx2 3’UTR,組合成重組質粒。Runx2 WT 3’UTR序列為:ttctatgcacgtattgtacaaattgtgctttgtgccacaggtcatgatcgtggatgag tttactctgaacttcaaagggactatttgtattgtatgttgcaactgtaaattgaatt atttggcatttccccctctcatgattgtaatatt;Runx2 MT 3’UTR: ttctatgcacgtattgtacaaattgtgctttgtgccacaggtcatgatcgtggatga gtttactctgaacttcaaatccactatttgtattgtatgttgcaactgtaaattgaat tatttggcatttccccctctcatgattgtaatatt。
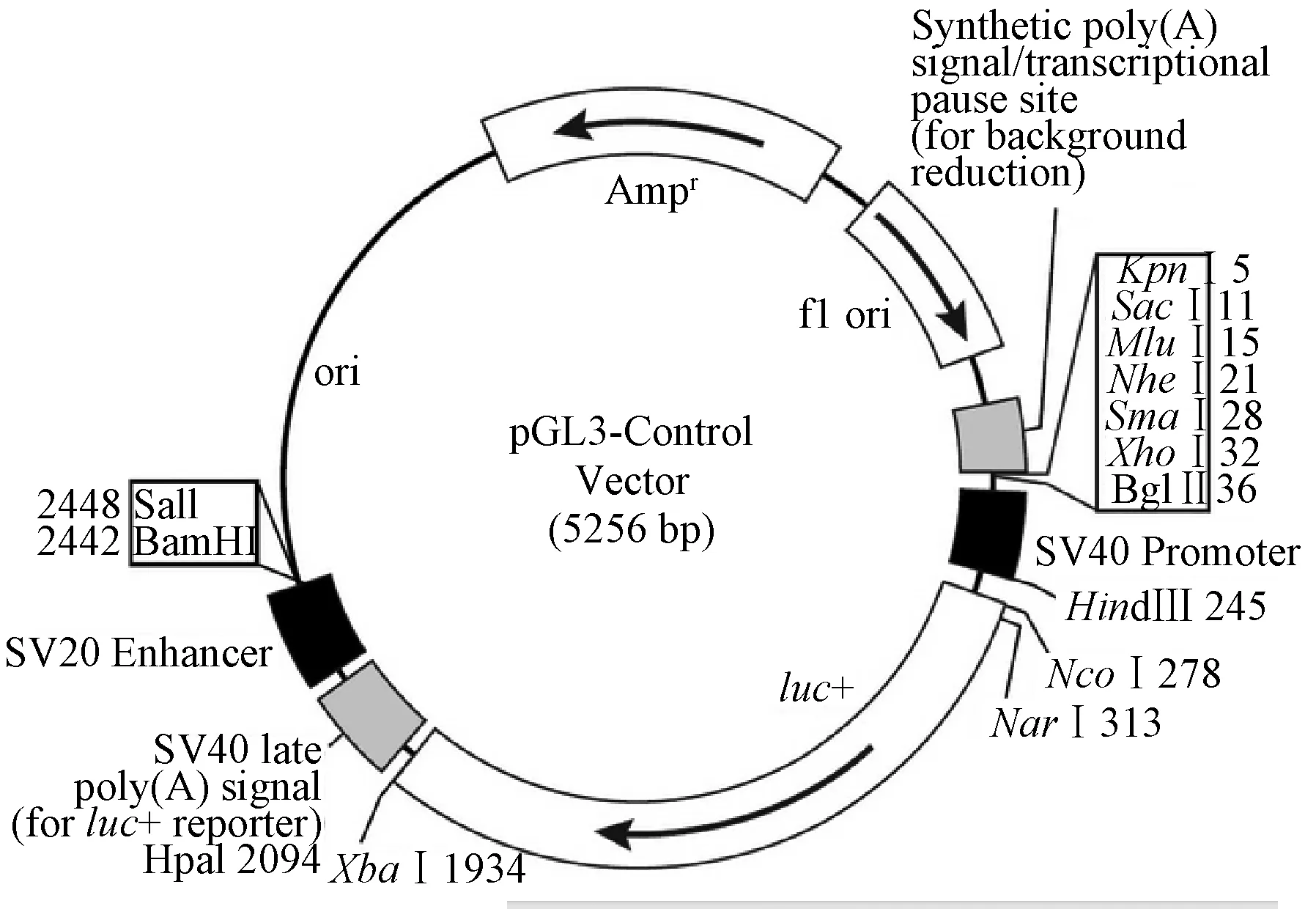
圖1 空載體結構Fig.1 Structure of empty vector
1.2.7雙熒光素酶報告基因法驗證靶基因:取對數生長期細胞MC3T3-E1,以每孔2×104細胞種于24孔培養板中,充分混勻,置于 37℃培養箱培養 24 h。當融合度接近90%時進行轉染。取1.5 mL EP管4個,均加入無血清雙抗的α-MEM培養液(按50 μL/孔)和Lipofectamine 2000脂質體(按1 μL/孔),使其充分混勻,靜置5 min。向新的EP管中加入無血清雙抗的α-MEM培養液(按50 μL/孔)和Runx2 3’UTR/突變型Runx2 3’UTR重組質粒(100 ng/孔)、miRNA mimics/陰性對照NC(2 μM/孔),并充分混勻,共分成四組,即Runx2 3’UTR+miRNA mimics、Runx2 3’UTR+miRNA NC、Runx2mut3’UTR+miRNA mimics、Runx2mut3’UTR+miRNA NC。將混有脂質體的α-MEM培養液和上述四組α-MEM培養液分別相混合(100 μL/孔),并充分混勻,室溫下靜置20 min,分別加到24孔培養板相應的實驗組中(每組設定三個復孔),混勻放置于37℃ CO2培養箱中培養48 h。
每孔用1×PBS輕柔洗滌1次,每孔加1×PLB(裂解液),反復吹打,凍融3次,以充分裂解細胞。13000×g,4℃離心15 s,取上清。用熒光檢測儀中進行測定,設置2 s的預測延遲和10 s的測定用時,在測量管中加入5 μL樣本充分混勻10 s,再加入100 μL Luciferase Reporter Assay Reagent II(LAR II,螢火蟲熒光素酶底物)測定螢火蟲熒光1,而后加入100 μLStop&Glo?substrate(海腎熒光素酶底物)測定海腎熒光2。以熒光1/熒光2的值作為相對熒光素酶活性。
1.2.8miRNA-204基因的過表達和干擾:在6孔培養板中每孔接種1×105細胞,充分混勻,置于 37℃培養箱培養 24 h,當融合度接近90%時進行轉染。取1.5 mL EP管4個,均加入無血清雙抗的α-MEM培養液(按200 μL/孔)和Lipofectamine 2000脂質體(按4μL/孔),使其充分混勻,靜置5 min。向新的EP管中加入無血清雙抗的α-MEM培養液(按200 μL/孔)和miRNA mimics或miRNA inhibitor 或陰性對照NC(8 μM/孔),并充分混勻,共分成3組,將混有脂質體的α-MEM培養液和上述兩組α-MEM培養液分別相混合(400μL/孔),并充分混勻,室溫下靜置20 min,分別加到6孔培養板相應的實驗組中,分別為加等量Lipofectamine 2000脂質體孔,加入miRNA mimics組、miRNA inhibitor和陰性對照NC組,混勻放置于37℃ CO2培養箱中培養48 h。
1.3 統計學處理
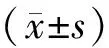
2 結果
2.1 葛根素對成骨細胞MC3T3-E1 Runx2 mRNA表達水平的影響
葛根素作用72h后,Runx2 mRNA表達量與空白對照組比較具有顯著性差異,上升了1.47倍。見圖2。
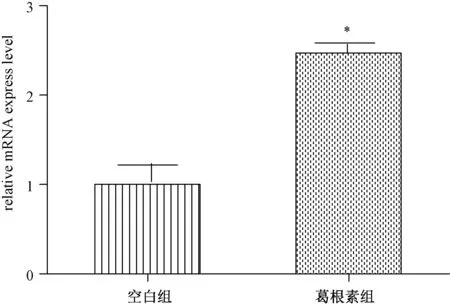
圖2 葛根素作用前后Runx2 mRNA表達水平(*P<0.05)Fig.2 The mRNA expression level of Runx2 before and after the addition of puerarin
2.2 葛根素對成骨細胞MC3T3-E1 Runx2蛋白表達水平的影響
同空白組相比,葛根素作用后Runx2的蛋白水平上升。見圖3。
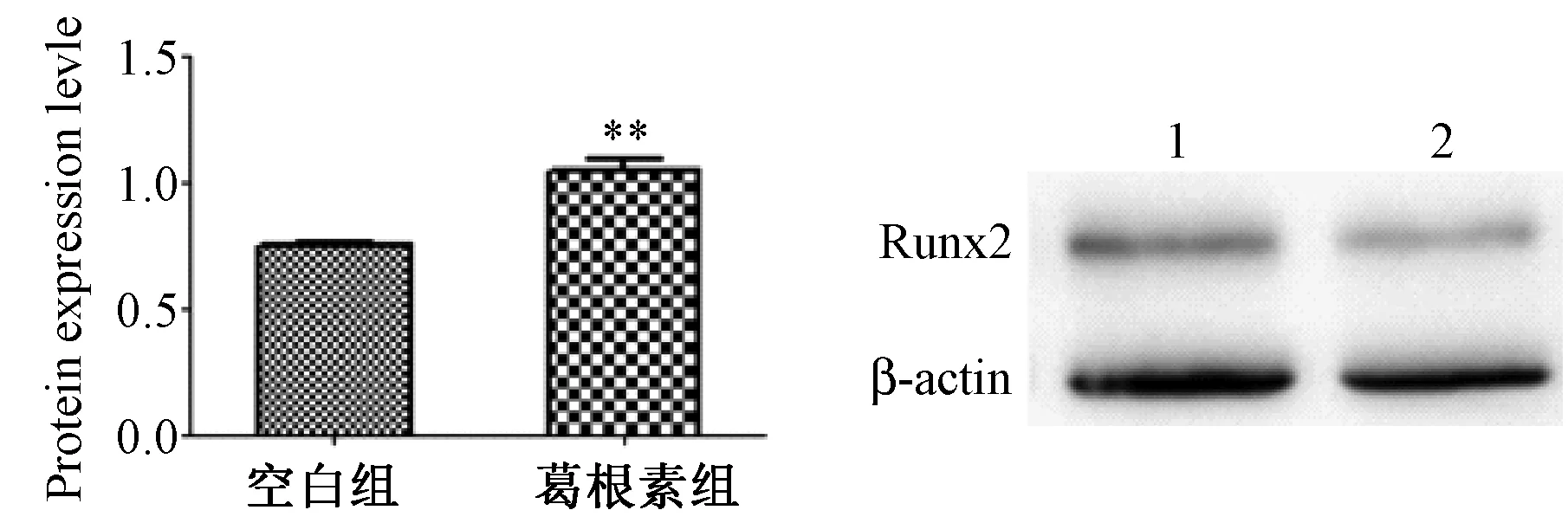
圖3 葛根素作用前后Runx2 蛋白的比值Fig.3 The protein ratio of Runx2 before and after the addition of puerarin1. Puerarin group 2. Blank control group
2.3 靶向Runx2的miRNA預測結果
綜合利用TargetScan、PicTar、miRBase和miRDB這四個軟件預測結果顯示靶向Runx2的miRNA有miR-204、miR-128、miR-135b-5p、miR-3072-3p、miR-2861、miR-770-5p。microRNA表達譜檢測結果顯示miR-204、miR-3072-3p、miR-2861等119個microRNA葛根素作用前后發生變化。其中共同交集有miR-204、miR-3072-3p等4個,我們選擇miR-204作為研究對象驗證靶基因預測的正確性。
序列(5’ TO 3’)mmu-miR-204 mimics:UUCCCUUUGUCAUCCUAUGCCU;mmu-miR-204 Inhibitor:AGGCAUAGGAUGACAAAGGGAA;mmu-miR-204NC:GCGACGAUCUGCCUAAGAU。
2.4 葛根素作用后miRNA-204表達量的變化
熒光實時定量PCR結果顯示(圖4),葛根素作用后miRNA-204 在成骨細胞中的表達顯著低于空白對照組,表達差異有顯著的統計學意義(P<0.05)。初步說明了Runx2可能為miRNA-204的靶基因。
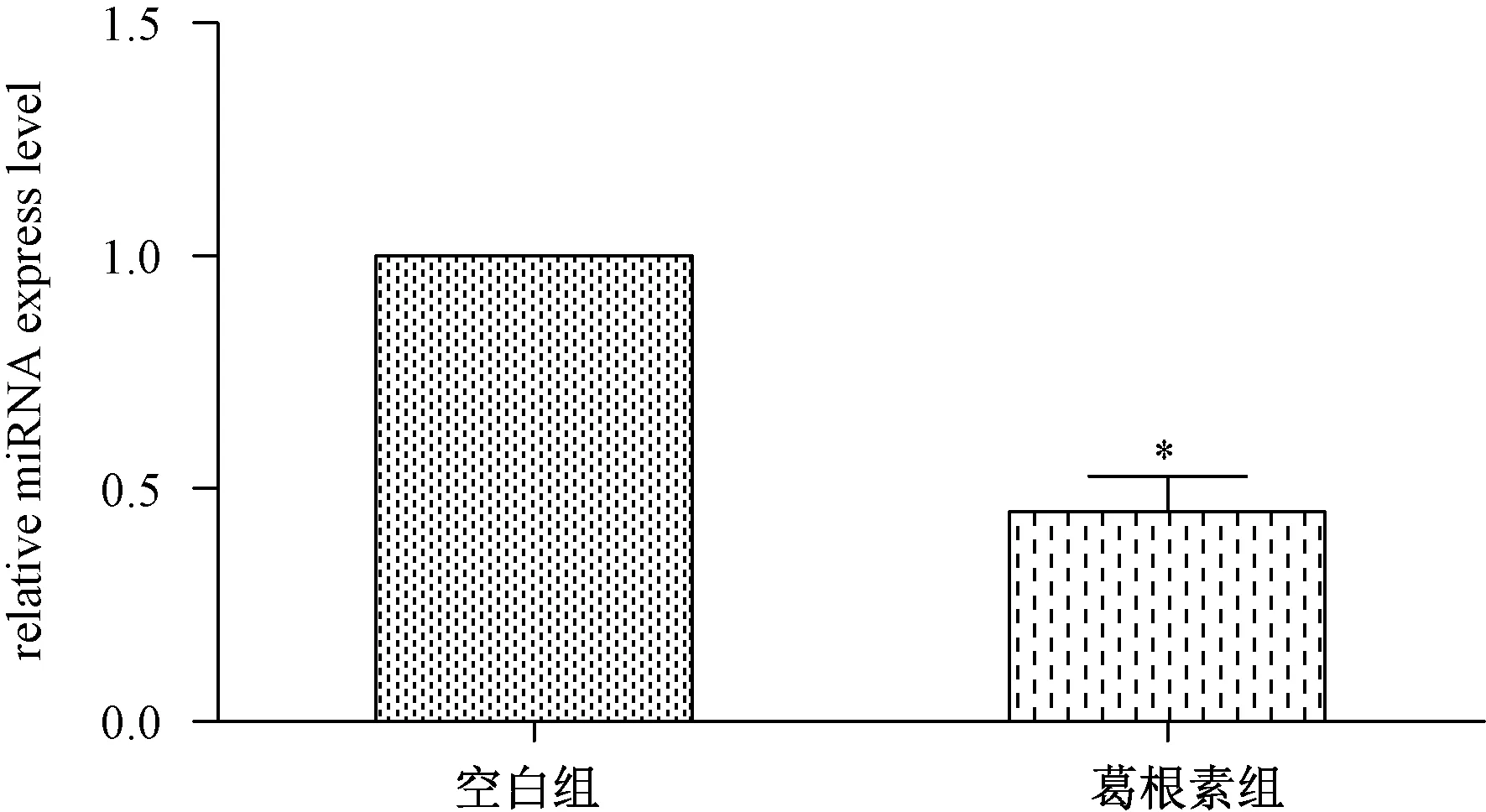
圖4 miRNA-204表達水平(*P<0.05)Fig.4 The expression level of miRNA-204
2.5 雙熒光素酶報告基因法結果
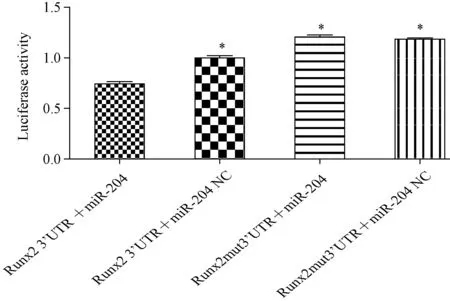
圖5 miRNA-204對Runx2 3’UTR表達的影響(*P<0.05) Fig.5 Effect of miRNA-204 on expression of Runx2 3’UTR
雙熒光素酶報告基因法結果顯示(圖5),細胞轉染48 h后,只有Runx2 3’UTR+miRNA-204 mimics組熒光素蛋白的表達水平顯著降低(P<0.05),說明只有miRNA-204可抑制Runx2 3’UTR報告基因的表達,miRNA-204+Runx2mut3’UTR組、miRNA-204NC+Runx2 3’UTR組和miRNA-204NC+Runx2mut3’UTR組熒光素蛋白的表達水平均變化不顯著(P>0.05),表明了Runx2 為miRNA-204的靶基因。
2.6 過表達或干擾miRNA-204對Runx2蛋白表達的影響
與空白對照組相比,轉染試劑組Runx2蛋白表達水平有一定程度的下降(圖6),說明轉染試劑對細胞蛋白表達有一定的抑制作用。因此,miRNA-204對Runx2蛋白表達的影響,應以轉染試劑組為比較對象。結果顯示:同轉染試劑組相比,miRNA-204過表達后Runx2的蛋白水平下降, miRNA-204干擾表達后Runx2的蛋白水平上升,且都有統計學意義。進一步驗證了Runx2 為miRNA-204的靶基因。
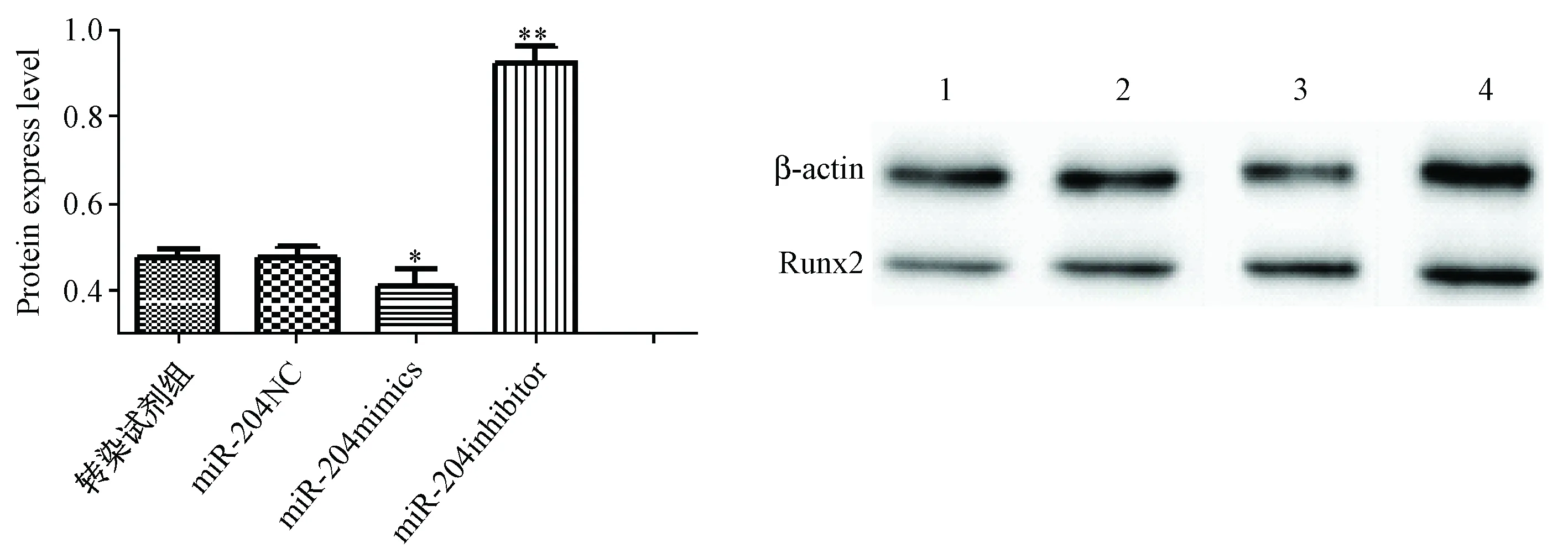
圖6 過表達或干擾miRNA-204后Runx2蛋白表達的水平(*P<0.5,**P<0.01)1轉染試劑組 2 NC對照組 3 miR-204mimics組 4 miR-204inhibitor組Fig.6 The protein level of Runx2 after overexpression or interference of miRNA-2041, Transfection reagent group; 2, NC control group; 3, miR-204mimics group; 4, miR-204inhibitor group
2.7 過表達或干擾miRNA-204對Runx2 mRNA表達的影響
與轉染試劑組相比,miRNA-204過表達以及干擾表達后Runx2 mRNA表達水平均沒有明顯差異,說明miRNA-204對Runx2 mRNA表達沒有明顯作用,不參與Runx2的轉錄過程,而參與翻譯調節。
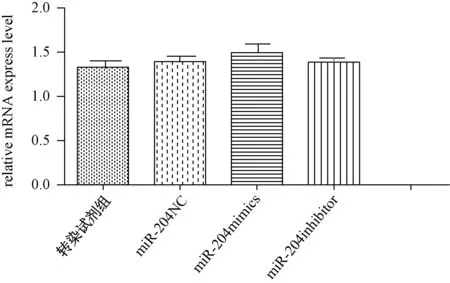
圖7 過表達或干擾miRNA-204后Runx2 mRNA表達的水平Fig.7 The mRNA level of Runx2 after overexpression or interference of miRNA-204
3 討論
Runx2 的表達是成骨細胞分化的開始,它使骨髓基質干細胞只發育成成骨細胞或軟骨細胞[6],因此是骨形成過程中最早和最具特征性的標志[7],Runx2亦是骨發育過程中激活與啟動骨髓基質干細胞向成骨細胞分化并調節成骨細胞成熟的重要轉錄因子,它能上調多種成骨相關基因的表達,對膜內和軟骨內骨化成骨均有控制作用,參與正常骨骼發育的全過程,對防治骨質疏松癥具有重要意義。
miRNA是細胞內的一類小分子RNA,能夠在轉錄后調節基因表達,從而影響多種生物學過程,包括細胞的增殖、分化、凋亡、發育。它的發現可能成為極有應用價值的分子標志物,為骨質疏松癥的治療提供新的靶標。
前期研究發現葛根素能促進成骨細胞增殖與分化,對骨量保持具有正向意義從而達到防治骨質疏松的目的[8,9]。本實驗表明,葛根素作用于成骨細胞后,能上調成骨細胞Runx2的表達,同時,miRNA表達譜也有很大的改變,推測葛根素對Runx2蛋白表達的影響可能與miRNA有關。
Wang等[10]體外實驗表明,miR-204負調節Runx2抑制成骨分化,從而抑制成骨細胞相關基因的表達,包括堿性磷酸酶(ALP)、骨鈣素,這些都是由BMP-2誘導產生的。Huang等[11]也發現,miR-204作為重要的內源性衰減器負調控Runx2,抑制間充質祖細胞系和骨髓間充質干細胞中骨生成和促進脂肪生成。說明Runx2可作為MiR-204的直接靶標[12]。
我們的實驗表明,miRNA表達譜和PCR結果都發現葛根素作用后miRNA-204表達下降,說明了Runx2和MiR-204的表達呈負相關。我們采用生物信息學分析發現,miR-204能與Runx2的3 '非翻譯區特異性結合從而抑制其翻譯。
為進一步驗證miR-204和Runx2之間的關系,我們構建了Runx2 3‘UTR和突變型Runx2 3’UTR的表達載體,采用熒光素酶報告基因法證實了Runx2是miRNA-204的靶基因,而且,過表達miRNA-204可使Runx2蛋白表達下降,干擾miRNA-204則使Runx2蛋白表達上升,這些結果都說明在成骨細胞中,miRNA-204直接抑制Runx2表達,Runx2可作為miRNA-204的直接靶標。葛根素可通過下調miRNA-204來促進Runx2表達、促進成骨細胞增殖和分化,實現預防和治療骨質疏松癥的作用。

